初三化学下册《炼铁的原理》精品课时练
- 格式:docx
- 大小:460.47 KB
- 文档页数:4

炼铁的原理同步练习(有解析新人教版九年级化学下册)题3 金属资的利用和保护
第1时炼铁的原理
知能演练提升
能力提升
1碳在高温下可以与氧化铁反应,化学方程式可表示为3C+2Fe2O3 4Fe+3CO2↑,下列说法中正确的是( )
A该反应属于分解反应
B反应中碳元素的化合价降低,铁元素的化合价升高
C碳是还原剂
D氧化铁是还原剂
2(10%)=63 t×96%,解得x=142 g=16 g,故生成物中铁、氧两元素的质量比=42 g∶16 g=21∶8,四氧化三铁中铁、氧元素质量比也是21∶8,故该黑色固体粉末是四氧化三铁。
仔细观察虚线框内的装置可知,洗气瓶内进气管、出气管都伸入了瓶底,可推测出其作用是吸收二氧化碳并收集一氧化碳。
答案 (1)3CO+Fe2O3 2Fe+3CO2
C+O2 CO2、C+CO2 2CO
(2)[实验与猜想]①氧化亚铁(FeO) ②铁和四氧化三铁的混合物全部是四氧化三铁(二者可互换,化学式也可)
[得出结论]四氧化三铁
[反思与评价]②AB。



第1课时铁的冶炼知识点1常见的金属矿物1.地球上的金属资源广泛地存在于地壳和浩瀚的海洋中。
下列金属在自然界中能以单质形式存在的是()A.钾B.钠C.镁D.金2.下列矿石的主要成分的化学式书写错误的是()A. 赤铁矿(Fe2O3) B.磁铁矿(FeO)C.菱铁矿(FeCO3) D.铝土矿(Al2O3)3.用下列矿石冶炼金属的时候,排放的废气不容易引起酸雨的是()A. 辉铜矿(Cu2S) B.方铅矿(PbS)C.黄铁矿(FeS2) D.铝土矿(Al2O3)知识点2铁的冶炼4.下列对教材中模拟炼铁的实验装置的说法不正确的是()A.实验中需要高温的条件B.实验开始时应先通一会儿一氧化碳再加热C.实验中可观察到玻璃管中的固体由黑色变为红棕色D.该实验需要处理尾气一氧化碳5.高炉炼铁的原料是()①焦炭②铁矿石③石灰石④一氧化碳⑤空气A.②③④⑤B.①②③⑤C.①②③D.②③④6.下列关于高炉炼铁的说法错误的是()A .高炉中焦炭的作用是供热并产生一氧化碳B .高炉中石灰石的作用是将矿石中的二氧化硅转变为炉渣C .高炉中把铁矿石炼成铁的主要反应原理是2Fe 2O 3+3C=====高温4Fe +3CO 2↑D .高炉炼铁得到的产品是生铁,不是纯铁7.炼铁的原理是利用一氧化碳与氧化铁反应。
某同学利用该原理设计了一个实验,实验装置如图8-3-1所示。
图8-3-1对实验进行分析并回答:(1)给玻璃管加热的仪器叫作酒精喷灯,要用其________(填“外焰”“内焰”或“焰心”)进行加热。
(2)实验中玻璃管里氧化铁粉末的颜色变化是________________________,观察到澄清石灰水的现象是__________________。
反应的化学方程式分别为_______________________________________、_____________________________。
(3)实验前“通入CO ”与“开始加热”的顺序是_________________;实验后“停止通入CO ”与“停止加热”的顺序是_________________________________________。

课题3 金属资源的利用和保护第1课时铁的冶炼知识点1常见的金属矿物1.下列金属在自然界中有单质形式存在的是()A.钾B.钠C.镁D.金2.写出下列金属矿石的主要成分的化学式。
知识点2铁的冶炼3.下列关于工业炼铁的叙述中错误的是()A.使用的设备是高炉B.主要原料为铁矿石、石灰石、焦炭和热空气等C.主要原理是2Fe2O3+3C4Fe+3CO2↑D.主要产物为生铁4.小明的笔记中有一处错误,你认为是下列中的哪一处()A.a处B.b处C.c处D.d处5.煤加工得到的焦炭广泛用于炼铁,如图高炉炼铁的示意图,回答下列问题。
(1)焦炭在炼铁过程中的主要作用是。
(2)原料中石灰石的主要作用是。
(3)铁矿石进入高炉前要粉碎的目的是,高炉内生成铁的化学方程式为。
(4)高炉炼出的是(填“生铁”或“纯铁”)。
(5)出铁口低于出渣口的原因是。
6.炼铁的原理是利用一氧化碳与氧化铁反应。
某同学利用该原理设计了一个实验,实验装置如图示。
对实验进行分析并回答问题。
(1)玻璃管中观察到的现象是,反应的化学方程式为,试管内石灰水变浑浊说明生成了,该反应的化学方程式为。
(2)实验时“通入一会儿一氧化碳”与“开始加热”的顺序是; 实验结束后“停止通入一氧化碳”与“停止加热”的顺序是。
(3)实验时要在装置末端a处放一只燃着的酒精灯,其作用是。
知识点3含杂质物质的计算7.工业上用480 t含氧化铁80%的赤铁矿石为原料炼铁,得到含杂质4%的生铁,据此填写有关物质的质量。
8.某钢铁厂若日产含铁1.4×104 t的生铁,至少需要含Fe2O3 80%的赤铁矿的质量是多少?(写出计算过程)9.某钢铁厂高炉炼铁的主要原料是焦炭、赤铁矿石(主要含Fe2O3)、空气等,主要反应过程如图所示,请回答问题。
(1)A的化学式:。
(2)写出反应②的化学方程式:。
(3)写出反应③的化学方程式: 。
10.《天工开物》中介绍了锌的冶炼方法:把炉甘石(ZnCO3)和煤炭饼装入炼锌罐(如图示),泥封,“其底铺薪,发火煅红”“冷定毁罐取出”。
人教版化学九年级下册 第八单元 课题3 金属资源的利用和保护课时1 铁的冶炼一、金属资源的存在方式地球上的金属资源广泛存在于地壳和海洋中,大多数金属化学性质较活泼,所以它们以__化合物__的形式存在;只有少数金属化学性质很不活泼,如金、银等以__单质__形式存在。
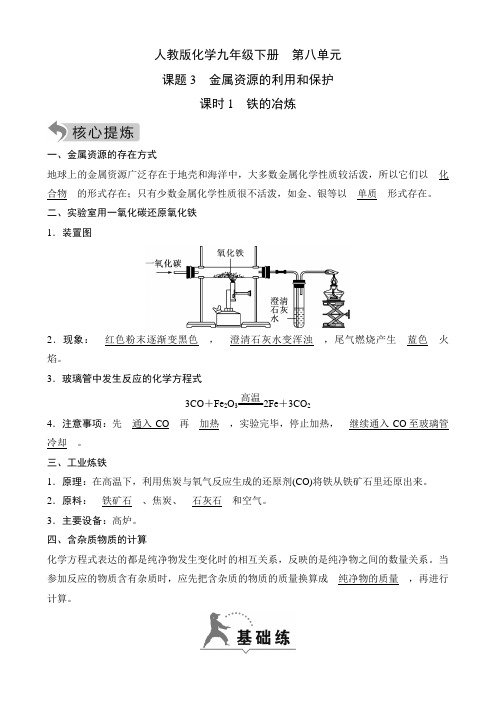
二、实验室用一氧化碳还原氧化铁 1.装置图2.现象:__红色粉末逐渐变黑色__,__澄清石灰水变浑浊__,尾气燃烧产生__蓝色__火焰。
3.玻璃管中发生反应的化学方程式3CO +Fe 2O 3=====高温2Fe +3CO 24.注意事项:先__通入CO__再__加热__,实验完毕,停止加热,__继续通入CO 至玻璃管冷却__。
三、工业炼铁1.原理:在高温下,利用焦炭与氧气反应生成的还原剂(CO)将铁从铁矿石里还原出来。
2.原料:__铁矿石__、焦炭、__石灰石__和空气。
3.主要设备:高炉。
四、含杂质物质的计算化学方程式表达的都是纯净物发生变化时的相互关系,反映的是纯净物之间的数量关系。
当参加反应的物质含有杂质时,应先把含杂质的物质的质量换算成__纯净物的质量__,再进行计算。
1.元素在自然界里分布不均匀,如智利富藏铜矿、澳大利亚多铁矿、我国山东富含黄金,但从整个地壳中元素的含量来看,最丰富的金属元素是( C ) A .O B .Si C .AlD .Fe2.下列金属矿物的主要成分错误的是( D ) A .赤铁矿(Fe 2O 3) B .磁铁矿(Fe 3O 4) C .菱铁矿(FeCO 3) D .辉铜矿(CuS)3.下列说法不符合事实的是( B ) A .地壳中大多数金属含量是很少的 B .硫黄属于金属矿物C .自然界中绝大多数金属以化合物的形式存在D .目前,人类从大自然提取量最大的金属是铁4.现有①赤铁矿(主要成分是Fe 2O 3);②磁铁矿(主要成分是Fe 3O 4);③黄铁矿(主要成分是FeS 2),请你从经济效益和环境保护的角度分析三种矿石哪种不适合用来炼铁:__③__(填序号),理由是__黄铁矿中铁的含量最低,且会生成SO 2等有害气体,污染环境。
课题3 金属资源的利用和保护第1课时 铁的冶炼核心·易错判断正误:(在括号内打“√”或“×”)(1)磁铁矿的主要成分是Fe 3O 4( )(2)高炉炼铁的原理是:2Fe 2O 3+3C=====高温4Fe +3CO 2↑( )(3)在高炉中炼铁时,焦炭的作用只是提高炉内温度( )(4)一氧化碳还原氧化铁的实验中,要先通一会儿一氧化碳再点燃酒精喷灯( )(5)Fe 2O 3+3CO=====高温2Fe +3CO 2↑( )(6)赤铁矿石是纯净物,可将其质量直接代入化学方程式进行计算( )[核心知识] 炼铁原理:在高温下,利用还原剂一氧化碳把铁从铁矿石里还原出来。
[易错点拨] 不要把杂质的质量分数当作纯物质的质量分数代入化学方程式计算。
纯物质的质量分数=1-杂质的质量分数。
1.下列金属在地壳中能以单质形式存在的是( )A .钠B .铝C .铁D .金2.如图8-3-1所示的金属矿石的主要成分不属于氧化物的是( )图8-3-13.炼铁高炉中发生了下列反应( )①高温下一氧化碳将铁矿石还原为铁②高温煅烧石灰石③灼热的焦炭和二氧化碳反应④焦炭充分燃烧其中属于化合反应的是A .①和④B .②和③C .③和④D .只有④4.炼铁时加入石灰石的主要作用是( )A .作还原剂B .提供CO 2C .降低铁矿石的熔点D .将矿石中的SiO 2转化为炉渣5.如图8-3-2是“一氧化碳与氧化铁反应”的部分实验装置,关于该实验说法正确的是( )图8-3-2A .充分反应后,向固体中加稀盐酸会产生气泡B .在实验过程中,黑色的粉末会逐渐变成红色C .该实验的反应原理为FeO +CO=====高温Fe +CO 2D .在实验过程中,产生的尾气可以直接排放到空气中6.2019·重庆 A 工业炼铁中会发生一氧化碳与氧化铁的反应,该反应中发生还原反应的物质是( )A .COB .Fe 2O 3C .CO 2D .Fe7.2019·巴中 用“W”形管进行微型实验,如图8-3-3所示,下列说法错误的是( )图8-3-3A.a处红棕色粉末变为黑色B.a处实验结束时先停止通入CO,后停止加热C.b处澄清石灰水变浑浊证明有CO2生成D.可利用点燃的方法进行尾气处理8.2019·山西科学精神与社会责任,是化学学科素养更高层面的价值追求。
6.3金属矿物与冶炼1、我国古代的主要化学成就有:①制造青铜器 ②湿法冶铜 ③冶炼钢铁,按历史年代先后顺序应用于生产排列的是( )A.①②③B.①③②C.③②①D.②①③2、下列变化过程不属于金属冶炼的是( )A .电解氧化铝B .铁在氧气中燃烧C .金属氧化物与焦炭在高温下反应D .高温下CO 还原CuO3、X 、Y 、Z 三种金属中,只有Z 能和稀硫酸反应;将Y 放人X 的盐溶液中,Y 表面有X 析出。
则X 、Y 、Z 三种金属的活动性顺序为 ( )A .X > Z > YB .Y > X > ZC .Y > Z > XD .Z > Y > X4、在氧化铁(Fe 2O 3)、氧化亚铁(FeO)和四氧化三铁(Fe 3O 4)这三种铁的氧化物中,铁的质量分数按由大到小顺序排列的是A .Fe 3O 4、Fe 2O 3、FeOB .FeO 、Fe 2O 3、Fe 3O 4C .FeO 、Fe 3O 4、Fe 2O 3D .Fe 2O 3、Fe 3O 4、FeO5、1989年世界卫生组织把铝确定为食品污染源之一加以控制使用。
下列对铝应控制使用的是( )①制铝合金 ②制电线 ③制餐饮具 ④制银色漆的原料 ⑤制装饮料的易拉罐 ⑥包装糖果和小食品A .①③④ B.③⑤⑥ C.②⑤⑥ D.全部控制6、化学的研究目的就是帮助人们认识、改造和应用物质,把金属矿物冶炼成金属就是人们利用化学方法实现物质改造的典型范例。
下表中不同的金属被开发和利用的年代不同,从化学反应的角度看,决定这一年代先后顺序的关键因素是( )A .金属的活动性B .金属的导电性C .金属的延展性D .地壳中金属元素的含量7、工业生产中常将两种金属在同一容器里加热使其熔合,冷凝后得到合金。
试根据下表所列的有关数据(其它条件均已满足),判断不能制得合金的是( )Na A .Na —Al 合金 B .Na —K 合金C .Fe —Cu 合金D .K —Fe 合金8、下列叙述中,不符合右图实验设计意图的是( )A .说明一氧化碳具有还原性B .说明生成物二氧化碳的密度比空气大C .说明一氧化碳和氧化铜的反应需要加热D .可以防止有毒的一氧化碳气体对空气的污染。
课时作业(五)[范围:第八单元 课题3 第1课时 炼铁的原理 含杂质物质的有关计算 建议用时:15分钟]一、选择题1.下列金属在自然界中有单质形式存在的是( )A.MgB.FeC.ZnD.Ag2.下列有关高炉炼铁的说法正确的一组是( )①高炉中焦炭的作用是产生一氧化碳①高炉中焦炭的作用是供热[来源:]①高炉中把铁矿石冶炼成铁的主要反应原理是2Fe 2O 3+3C=====高温4Fe +3CO 2↑ ①高炉炼铁得到的产品是生铁,不是纯铁A.①①①B.①①①C.①①①D.①①①3.2019·北京用“W”形玻璃管进行微型实验,如图K -5-1所示。
下列说法不正确的是( )图K -5-1A.a 处红棕色粉末变为黑色B.a 处的反应为CO +Fe 2O 3===2Fe +CO 2C.b 处澄清石灰水变浑浊证明有CO 2生成D.可利用点燃的方法进行尾气处理二、填空题4.写出下列矿石的主要成分的化学式:①赤铁矿 ,①磁铁矿 ,①菱铁矿 ,①铝土矿 。
其中主要成分是氧化物的是 (填序号)。
5.图K -5-2是课堂中模拟炼铁的实验装置。
图K -5-2(1)写出图中标有序号的仪器名称:(2)实验过程中,先要进行的是 (填“①”或“①”)。
①.加热 ①.通一氧化碳(3)B 中盛放的是 ,B 中发生反应的化学方程式是________________________________________________________________________,其作用是检验 。
(4)该装置的不足之处是________________________________________________________________________。
链接听/6例1方法点拨6.某钢铁厂高炉炼铁的主要原料是焦炭、赤铁矿石(主要含Fe 2O 3)、空气等,主要反应过程如下:焦炭――→过量空气、高温①生成物 A ――→过量焦炭、高温①生成物 B ――→赤铁矿、高温①铁 图K -5-3请回答:(1)A 的化学式: 。
第1课时铁的冶炼知识点1常见的金属矿物1.地球上的金属资源广泛地存在于地壳和浩瀚的海洋中。
下列金属在自然界中能以单质形式存在的是()A.钾B.钠C.镁D.金2.下列矿石的主要成分的化学式书写错误的是()A. 赤铁矿(Fe2O3) B.磁铁矿(FeO)C.菱铁矿(FeCO3) D.铝土矿(Al2O3)3.用下列矿石冶炼金属的时候,排放的废气不容易引起酸雨的是()A. 辉铜矿(Cu2S) B.方铅矿(PbS)C.黄铁矿(FeS2) D.铝土矿(Al2O3)知识点2铁的冶炼4.下列对教材中模拟炼铁的实验装置的说法不正确的是()A.实验中需要高温的条件B.实验开始时应先通一会儿一氧化碳再加热C.实验中可观察到玻璃管中的固体由黑色变为红棕色D.该实验需要处理尾气一氧化碳5.高炉炼铁的原料是()①焦炭②铁矿石③石灰石④一氧化碳⑤空气A.②③④⑤B.①②③⑤C.①②③D.②③④6.下列关于高炉炼铁的说法错误的是()A.高炉中焦炭的作用是供热并产生一氧化碳B .高炉中石灰石的作用是将矿石中的二氧化硅转变为炉渣C .高炉中把铁矿石炼成铁的主要反应原理是2Fe 2O 3+3C=====高温4Fe +3CO 2↑D .高炉炼铁得到的产品是生铁,不是纯铁7.炼铁的原理是利用一氧化碳与氧化铁反应。
某同学利用该原理设计了一个实验,实验装置如图8-3-1所示。
图8-3-1对实验进行分析并回答:(1)给玻璃管加热的仪器叫作酒精喷灯,要用其________(填“外焰”“内焰”或“焰心”)进行加热。
(2)实验中玻璃管里氧化铁粉末的颜色变化是________________________,观察到澄清石灰水的现象是__________________。
反应的化学方程式分别为_______________________________________、_____________________________。
(3)实验前“通入CO ”与“开始加热”的顺序是_________________;实验后“停止通入CO ”与“停止加热”的顺序是_________________________________________。
课题3金属资源的利用和保护第1课时炼铁的原理
一氧化碳还原氧化铁的实验操作顺序及解释
3
(1)CO 具有可燃性,因此,实验前一定要验纯;
(2)因尾气中含有 CO ,而 CO 有毒,因此,操作中一定不能忽视尾气的处理,一般采用 燃烧法或收集集中处理法。
【例题】 (2011·四川南充中考改编)CO 是一种无色、无味、有毒的可燃性气体污染物, 具有还原性,可用于冶金工业。
某兴趣小组为探究其具有还原性,设计了如下实验装置。
请 回答以下有关问题:
(1)写出图中标有序号的仪器名称①______________,②_____________。
(2)实验过程中,先要进行的是________。
(填Ⅰ或Ⅱ) Ⅰ.加热 Ⅱ. 通一氧化碳
(3)B 中反应的化学方程式是_____________________________________,B 中观察到的 现象是______________________________________。
(4)该装置的不足之处是_________________________________________________。
解析:由于一氧化碳具有可燃性,若混有空气,点燃或加热时易发生爆炸,所以实验过 程中要先通一氧化碳,把管内空气排干净后再加热;一氧化碳有毒,不能直接排放到空气中, 要进行尾 气处理。
答案 :(1)铁架台 试管
(2)Ⅱ (3)Ca(OH)2+CO 2===CaCO ↓+H 2O 澄清的石灰水变浑浊
(4)没有尾气处理装置(或没有用燃着的酒精灯处理尾气等)
1.下列不属于金属矿物的是( )。
A .赤铁矿 B .黄铜矿 C .铝土矿 D .汉白玉矿 答案:D
2.金属钛(Ti)是重要的航空航天材料。
Ti 可以用 TiO 2 与 Si 共熔制取,反应的化学方
高温
程式为 TiO 2+Si=====SiO 2+Ti 。
该反应中的还原剂是( )。
A .TiO 2
B .Si
C .SiO 2
D .Ti 答案:B
3.工业上将赤铁矿冶炼成铁是一个复杂的过程,炼铁高炉中主要发生了下列反应:
点燃 高温 高温 高温
①C+ O 2=====CO 2 ②CO 2+C=====2CO ③CaCO 3=====CaO +CO 2↑ ④3CO+ Fe 2O 3=====2Fe +3CO 2
其中属于化合反应的是( )。
A .①② B .②③ C .③④ D .①④ 答案:A
4.炼铁的过程是( )。
A .含铁的化合物在高温下分解而得到铁
B .含有铁的化合物与碳发生置换反应
C .在高温下用还原剂一氧化碳从铁的氧化物中将铁还原出来
D .在高温下用一氧化碳从铁的化合物中将铁氧化出来 答案:C
5.(2012·福建福州中考)竖炉冶铁工艺流程如图所示。
回答下列问题:
(1)该工艺流程中,甲烷的作用是________,冶炼出的铁水属于________(填“纯净物” 或“混合物”)。
(2)用化学方程式表示还原反应室内炼铁的原理________________。
( 写一个) (3)该工艺流程中,可循环利用的物质是______。
答案:(1)燃烧产生热量、做生产合成气的原料 混合物
高温 高温
(2)3CO +Fe 2O 3 =====2Fe +3CO 2 或 3H 2+Fe 2O 3=====2Fe +3H 2O(合理答案均可) (3)CO 2 和 H 2O(高温尾气)
6.在下图中,甲图是一氧化碳与氧化铁反应装置的示意图,乙图是高炉炼铁示意图。
请回答下列问题。
甲
乙
(1)写出甲图中的实验现象:_____________________________________________。
(2)甲图中装置的不足之处是:____________________________________________。
(3)请写出高炉中生成铁的化学方程式:________________________________________。
答案:(1)红色粉末变黑,澄清石灰水变浑浊(只需回答一种现象即可) (2)没有尾气处理装置
高温
(3)Fe 2O 3+3CO=====2Fe +3CO 2。