化学周练(8)元素周期表
- 格式:docx
- 大小:55.28 KB
- 文档页数:2

元素周期表原子的构成:如果用 A Z X 的形式表示一个质量数为A 、质子数为Z 的原子,那么组成原子的粒子间的关系可以表达为:原子 A Z X质量数:将原子核内所有的质子和中子的相对质量取近似整数值加起来所得的数值,叫质量数。
注意:原子的质量数近似等于其相对原子质量,不能说原子的质量数就是其相对原子质量(3)构成原子或离子的微粒间的数量关系:①原子中:原子序数=核内质子数=核电荷数=核外电子数②原子的质量数(A )= 质子数(Z )+ 中子数(N )③阴、阳离子所带电荷数=质子数-核外电子数④阳离子中:质子数(Z )=阳离子的核外电子数+阳离子所带电荷数⑤阴离子中:质子数(Z )=阴离子的核外电子数-阴离子所带电荷数⑷ 核外电子的电子排布电子层:在多个电子的原子里,根据电子能量的差异和通常运动的区域离核远近不同,把电子分成不同的能级,每一层电子数最多不超过2n 2 ;最外层电子数最多不超过8个,次外层电子数最多不超过18个,倒数第三层不超过32个;核外电子总是先占有能量最低的电子层,当能量最低的电子层排满后,电子才依次进入能量较高的电子层。
电子的排布是先排K 层,K 层排满再排L 层,L 层排满再排M 层,M 层不一定排满了再排N 层,后面的也一样不一定排满了再排下一层。
(只有前3层)当电子层数≥4,最外层为1~2个电子,则次外层电子数为: 8 ;最外层为3~8个电子,则次外层电子数为: 18 。
元素周期表元素周期表的发现:1869年,俄国化学家门捷列夫指出第一张元素周期表。
编制原则:将元素按照相对原子质量由小到大的顺序排列,将化学性质的元素放在一个纵行。
原子序数与原子结构的关系:原子序数=核内质子数=核电荷数=核外电子数⑴编排原则① 按照 核电荷数 由小到大的顺序排列。
②将电子层数相同......的各元素从左到右排成一横行..。
(周期序数=原子的电子层数) ③ 把最外层电子数相同........的元素按电子层数递增的顺序从上到下排成一纵行..。

九年级化学元素周期表专项练习1.元素周期表是学习和研究化学的重要工具。
请根据下表(元素周期表的部分内容)回答有关问题。
(1)请从上表中查出关于碳原子的相对原子质量为 。
(2)铝原子的原子结构示意图有______个电子层,铝离子的符号为___________。
(3)第12号元素与第17号元素组成的物质是 (填化学式),构成该物质的微粒是 (填“分子”、“原子”或“离子”)。
(4)在元素周期表中,同一族(纵行)的元素具有相似的化学性质。
则下列各组元素具有相似化学性质的是 (填标号)。
①. He 和Ne②. B 和Mg③. Al 和Si④. F 和Cl2.元素周期表是学习研究化学的重要工具。
根据下表(元素周期表的部分内容)回答:(1)第3周期(横行)中金属元素有 种;(2)第8号元素与第13号元素组成的化合物的化学式是 。
(3)在元素周期表中,同一族(纵行)的元素具有相似的化学性质。
则下列各组元素具有相似化学性的是 (填标号)。
①. C 和Ne②. O 和S③. Li 和Na(4)观察上表,其中有一种常见元素的“元素名称”书写有误,请写出其正确的元素名称 ,过量排放该元素的一种氧化物到大气中,会引起 效应。
11 H 氢1.0082 He 氦4.00323 Li 锂6.941 4 Be 铍9.012 5 B 硼10.81 6 C 碳12.017 N 氮14.018 O 氧16.009 F 氟19.0010 Ne 氖20.18311 Na 钠22.9912 Mg 镁24.3113 Al 铝26.9814 Si 硅28.0915 P 磷30.9716 S 硫32.0617 Cl 氯35.4518 Ar 氩39.95(5)聚合物锂离子电池被誉为“21世纪的电池”,根据上图元素周期表中锂元素的相关信息,回答下列问题:锂元素在化学反应中容易 (填“得到”或“失去”)电子;锂元素与第17号元素组成的化合物的化学式是 。

初中化学元素周期表题目答案在初中化学的学习中,元素周期表无疑是一个非常重要的知识点。
它就像是一座蕴藏着无数化学奥秘的宝库,为我们揭示了物质世界的基本构成和规律。
接下来,让我们一起通过一些题目来深入了解元素周期表。
首先,看这样一道题目:“元素周期表中,同一周期元素的原子具有相同的()”A 电子层数B 核电荷数C 最外层电子数D 相对原子质量这道题目的答案是 A。
在元素周期表中,同一周期的元素,其原子的电子层数是相同的。
随着原子序数的递增,核电荷数、最外层电子数和相对原子质量都会发生变化。
再来看这道题:“下列元素中,属于金属元素的是()”A 氯B 氧C 钠D 氮答案是 C。
钠元素是金属元素,而氯、氧、氮都属于非金属元素。
判断元素是金属元素还是非金属元素,通常可以通过元素名称的偏旁来初步判断。
带有“钅”字旁的元素一般是金属元素(汞除外)。
还有这样一道题:“元素周期表中,原子序数等于()”A 质子数B 中子数C 核外电子数D 质子数与中子数之和这道题的答案是 A 和 C。
在原子中,原子序数等于质子数等于核外电子数。
而中子数则不一定与原子序数相等。
接下来这道题:“元素周期表中,同一族元素的化学性质相似,这是因为它们的()相同。
”A 电子层数B 核电荷数C 最外层电子数D 相对原子质量答案是 C。
同一族元素的最外层电子数相同,这决定了它们的化学性质相似。
再看这个题目:“在元素周期表中,位于第二周期第ⅥA 族的元素是()”A 氮B 氧C 碳D 氟答案是 B。
氧元素位于第二周期第ⅥA 族。
还有这样的题目:“下列关于元素周期表的说法中,错误的是()”A 共有 7 个周期B 共有 18 个族C 金属元素和非金属元素分区排列D 是学习和研究化学的重要工具答案是 B。
元素周期表共有 16 个族,而不是 18 个族。
元素周期表是我们学习和研究化学的重要工具,它清晰地展示了元素的性质规律和周期性变化。
通过以上这些题目,我们可以更深入地理解元素周期表的相关知识。

201 年中化学九年级专属讲义课题:元素周期表和元素周期律学生姓名:授课教师:201 年月日考点一元素周期表1.世界上第一张元素周期表是在1869年由俄国化学家门捷列夫绘制完成的,随着科学的不断发展,已逐渐演变为现在的常用形式。
2.原子序数:按照元素在周期表中的顺序给元素编号,称之为原子序数,原子序数=核电荷数=质子数=核外电子数。
3.编排原则(1)周期:把电子层数相同的元素,按原子序数递增的顺序,从左至右排成的横行。
(2)族:把最外层电子数相同的元素,按电子层数递增的顺序,从上至下排成的纵行。
4.元素周期表的结构5.元素周期表中的特殊位置(1)分区①分界线:沿着元素周期表中铝、锗、锑、钋与硼、硅、砷、碲、砹的交界处画一条斜线,即为金属元素区和非金属元素区分界线(氢元素除外)。
②各区位置:分界线左面为金属元素区,分界线右面为非金属元素区。
③分界线附近元素的性质:既表现金属元素的性质,又表现非金属元素的性质。
(2)过渡元素:元素周期表中部从ⅢB族到ⅡB族10个纵列共六十多种元素,这些元素都是金属元素。
(3)镧系:元素周期表第六周期中,57号元素镧到71号元素镥共15种元素。
(4)锕系:元素周期表第七周期中,89号元素锕到103号元素铹共15种元素。
(5)超铀元素:在锕系元素中92号元素铀(U)以后的各种元素。
结构巧记口诀横行叫周期,现有一至七,四长三个短,第七尚不满。
纵列称为族,共有十六族,一八依次现①,一零再一遍②。
一纵一个族,Ⅷ族搞特殊,三纵算一族,占去8、9、10。
镧系与锕系,蜗居不如意,十五挤着住,都属ⅢB族。
说明①指ⅠA、ⅡA、ⅢB、ⅣB、ⅤB、ⅥB、ⅦB、Ⅷ;②指ⅠB、ⅡB、ⅢA、ⅣA、ⅤA、ⅥA、ⅦA、0。
深度思考1.请在下表中画出元素周期表的轮廓,并在表中按要求完成下列问题:(1)标出族序数。
(2)画出金属与非金属的分界线,并用阴影表示出过渡元素的位置。
(3)标出镧系、锕系的位置。

初三化学元素周期表(完整版) 初三化学元素周期表原子序数元素符号元素名称相对原子质量元素名称读音1 H 氢 1.0079 (qīng)2 He 氦 4.0026 (hài)3 Li 锂 6.941 (lǐ)4 Be 铍 9.0122 (pí)5 B 硼 10.811 (péng)6 C 碳 12.011 (tàn)7 N 氮 14.007 (dàn)8 O 氧 15.999 (yǎng)9 F 氟 18.998 (fú)10 Ne 氖 20.17 (nǎi) 11 Na 钠 22.9898 (nà)12 Mg 镁 24.305 (měi)13 Al 铝 26.982 (lǚ)14 Si 硅 28.085 (guī)15 P 磷 30.974 (lín)16 S 硫 32.06 (liú)17 Cl 氯 35.453 (lǜ)18 Ar 氩 39.94 (yà)19 K 钾 39.098 (jiǎ)20 Ca 钙 40.08 (gài)21 Sc 钪 44.956 (kàng)22 Ti 钛 47.9 (tài)23 V 钒 50.94 (fán)24 Cr 铬 51.996 (gè)25 Mn 锰 54.938 (měng)26 Fe 铁 55.84 (tiě)27 Co 钴 58.9332 (gǔ)28 Ni 镍 58.69 (niè)29 Cu 铜 63.54 (tóng)30 Zn 锌 65.38 (xīn)31 Ga 镓 69.72 (jiā)32 Ge 锗 72.5 (zhě)33 As 砷 74.922 (shēn)34 Se 硒 78.9 (xī)35 Br 溴 79.904 (xiù)36 Kr 氪 83.8 (kè)37 Rb 铷 85.467 (rú)38 Sr 锶 87.62 (sī) 39 Y 钇 88.906 (yǐ)40 Zr 锆 91.22 (gào)41 Nb 铌 92.9064 (ní)42 Mo 钼 95.94 (mù)43 Tc 锝 (99) (dé)44 Ru 钌 161.0 (liǎo)45 Rh 铑 102.906 (lǎo)46 Pd 钯 106.42 (bǎ)47 Ag 银 107.868 (yín)48 Cd 镉 112.41 (gé)49 In 铟 114.82 (yīn)50 Sn 锡 118.6 (xī)51 Sb 锑 121.7 (tī)52 Te 碲 127.6 (dì)53 I 碘 126.905 (diǎn)54 Xe 氙 131.3 (xiān)55 Cs 铯 132.905 (sè)56 Ba 钡 137.33 (bèi) 57-71 La-Lu 镧系57 La 镧 138.9 (lán)58 Ce 铈 140.1 (shì)59 Pr 镨 140.9 (pǔ)60 Nd 钕 144.2 (nǚ)61 Pm 钷 (147) (pǒ)62 Sm 钐 150.3 (shān)63 Eu 铕 151.96 (yǒu)64 Gd 钆 157.25 (gá)65 Tb 铽 158.9 (tè) 66 Dy 镝 162.5 (dī)67 Ho 钬 164.9 (huǒ)68 Er 铒 167.2 (ěr)69 Tm 铥 168.9 (diū)70 Yb 镱 173.04 (yì)71 Lu 镥 174.967 (lǔ)72 Hf 铪 178.4 (hā)73 Ta 钽 180.947 (tǎn)74 W 钨 183.8 (wū)75 Re 铼 186.207 (lái)76 Os 锇 190.2 (é)77 Ir 铱 192.2 (yī)78 Pt 铂 195.08 (bó)79 Au 金 196.967 (jīn)80 Hg 汞 200.5 (gǒng)81 Tl 铊 204.3 (tā)82 Pb 铅 207.2 (qiān)83 Bi 铋 208.98 (bì)84 Po 钋 (209) (pō)85 At 砹 (201) (ài)86 Rn 氡 (222) (dōng)87 Fr 钫 (223) (fāng)88 Ra 镭 226.03 (léi) 89-103 Ac-Lr 锕系89 Ac 锕 (227) (ā)90 Th 钍 232.0 (tǔ)91 Pa 镤 231.0 (pú)92 U 铀 238.0 (yóu) 93 Np 镎 (237) (ná)94 Pu 钚 (244) (bù)95 Am 镅 (243) (méi)96 Cm 锔 (247) (jú)97 Bk 锫 (247) (péi)98 Cf 锎 (251) (kāi)99 Es 锿 (252) (āi) 100 Fm 镄 (257) (fèi) 101 Md 钔 (258) (mén) 102 No 锘 (259) (nuò) 103 Lr 铹 (262) (láo) 104 Rf 钅卢 (257) (lú) 105 Db 钅杜 (261) (dù) 106 Sg 钅喜 (262) (xǐ)107 Bh 钅波 (263) (bō)108 Hs 钅黑 (262) (hēi)109 Mt 钅麦 (265) (mài)110 Uun (281)111 Uuu (272)112 Uub (285)114 Uuq (289)(加括号的数据为该放射性元素半衰期最长同位素的质量数。

初中化学元素周期表练习题及答案1. 以下不属于主族元素的是:a) 碳b) 铜c) 锌d) 铝答案: b) 铜2. 下列元素中,原子序数最小的是:a) 氧b) 氢c) 氮d) 锂答案: b) 氢3. 元素周期表中,横行被称为:a) 周期b) 纵行c) 族d) 分组答案: a) 周期4. 下列元素中,能形成正离子的是:a) 氯b) 溴c) 氧d) 氖答案: a) 氯5. 元素周期表中第一周期有几个元素?a) 4b) 6c) 8d) 2答案: d) 26. 下列元素中,化学性质相似的是:a) 镁、铝、硅b) 碳、氧、氮c) 钾、钙、铷d) 锌、铁、铜答案: b) 碳、氧、氮7. 具有类似电子结构的元素在元素周期表中位于同一:a) 周期b) 族c) 分组d) 列答案: a) 周期8. 具有相同周期的元素,其原子核中的电子层数:a) 相等b) 不相等c) 无法确定d) 取决于元素种类答案: a) 相等9. 在元素周期表中,第一周期元素是:a) 碱金属b) 碱土金属c) 非金属d) 惰性气体答案: a) 碱金属10. 具有不完全填满外层电子层的元素,其化学性质更倾向于成为:a) 阴离子b) 阳离子c) 氧化剂d) 物质答案: b) 阳离子总结:元素周期表是化学中重要的工具,帮助我们理解和组织化学元素。
通过掌握元素周期表的基本知识,我们可以更好地理解元素的性质和周期规律。
希望以上练习题能够帮助您巩固对元素周期表的了解。

元素周期表及元素周期律1.元素X、Y、Z原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构。
下列推测不正确的是()。
A.同周期元素中X的金属性最强B.原子半径X>Y,离子半径X+>Z2-C.同族元素中Z的氢化物稳定性最高D.同周期元素中Y的最高价含氧酸的酸性最强【点评】在周期表中,元素的原子序数差因周期表结构出现以下两种情况:(1)同主族,相邻周期元素原子序数之差的判断。
①第ⅠA、ⅡA族元素,相差上一周期元素所在周期所含元素的种数。
②第ⅢA~ⅦA族元素,相差下一周期元素所在周期含有的元素的种数。
(2)同周期相邻主族元素原子序数之差的判断。
①ⅠA、ⅡA元素或ⅢA~ⅦA相邻元素相差1。
②ⅡA、ⅢA元素:若为第二或第三周期则相差1,若为第四或第五周期相差11,若为第六或第七周期则相差25。
2.A、B、C为三种短周期元素,A、B在同周期,A、C的最低价离子分别为A2-和C-,B2+和C-具有相同的电子层结构。
下列说法正确的是()。
A.原子序数:A<B<CB.原子半径:A>B>CC.离子半径:A2->C->B2+D.原子核外最外层电子数:A>C>B3.在以离子键为主的化学键中常含有共价键的成分。
下列各对原子形成化学键时共价键成分最少的是()A.Li,F B.Na,F C.Na,Cl D.Mg,O4.下列说法正确的是()。
①非金属元素不可能组成离子化合物②构成分子的粒子一定含有共价键③共价化合物中可能含有离子键④离子化合物中可能含有共价键⑤非极性键只存在于双原子单质分子里⑥不同元素组成的多原子分子里的化学键一定都是极性键A.①②④⑥ B.②④⑤⑥C.①③⑤⑥ D.只有④5.W、X、Y、Z均是短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-离子具有相同的电子层结构。
下列说法正确的是( )A.原子最外层电子数:X>Y>Z B.单质沸点:X>Y>ZC.离子半径:X2->Y+>Z-D.原子序数:X>Y>Z6.根据原子结构及元素周期律的知识,下列推断正确的是A.同主族元素含氧酸的酸性随核电荷数的增加而减弱B.核外电子排布相同的微粒化学性质也相同C.Cl‾、S2‾、Ca2+、K+半径逐渐减小D.3517Cl与3717Cl得电子能力相同7.下列各组中两种微粒所含电子数不相等的是A.H3O+和OH-B.CO和N2 C.HNO2和NO2-D.CH3+和NH4+8.短周期主族元素X、Y、Z、W的原子序数依次增大。

第一周期元素:1 氢(qīng) 2 氦(hài)元素周期表正确金属汉字写法第二周期元素:3 锂(lǐ) 4 铍(pí) 5 硼(péng) 6 碳(tàn) 7 氮(dàn) 8 氧(yǎng) 9 氟(fú) 10 氖(nǎi) 第三周期元素:11 钠(nà) 12 镁(měi) 13 铝(lǚ) 14 硅(guī) 15 磷(lín) 16 硫(liú) 17 氯(lǜ) 18 氩(yà) 第四周期元素:19 钾(jiǎ) 20 钙(gài) 21 钪(kàng) 22 钛(tài) 23 钒(fán) 24 铬(gè) 25 锰(měng) 26 铁(tiě) 27 钴(gǔ) 28 镍(niè) 29 铜(tóng) 30 锌(xīn) 31 镓(jiā) 32 锗(zhě) 33 砷(shēn) 34 硒(xī) 35 溴(xiù) 36 氪(kè) 第五周期元素:37 铷(rú) 38 锶(sī) 39 钇(yǐ) 40 锆(gào) 41 铌(ní) 42 钼(mù) 43 锝(dé) 44 钌(liǎo) 45 铑(lǎo) 46 钯(bǎ) 47 银(yín) 48 镉(gé) 49 铟(yīn) 50 锡(xī) 51 锑(tī) 52 碲(dì) 53 碘(diǎn) 54 氙(xiān) 第六周期元素:55 铯(sè) 56 钡(bèi) 57 镧(lán) 58 铈(shì) 59 镨(pǔ) 60 钕(nǚ) 61 钷(pǒ) 62 钐(shān) 63 铕(yǒu) 64 钆(gá) 65 铽(tè) 66 镝(dī) 67 钬(huǒ) 68 铒(ěr) 69 铥(diū) 70 镱(yì) 71 镥(lǔ) 72 铪(hā) 73 钽(tǎn) 74 钨(wū) 75 铼(lái) 76 锇(é) 77 铱(yī) 78 铂(bó) 79 金(jīn) 80 汞(gǒng) 81 铊(tā) 82 铅(qiān) 83 铋(bì) 84 钋(pō) 85 砹(ài) 86 氡(dōng) 第七周期元素:87 钫(fāng) 88 镭(léi) 89 锕(ā) 90 钍(tǔ) 91 镤(pú) 92 铀(yóu) 93 镎(ná) 94 钚(bù) 95 镅(méi) 96 锔(jú) 97 锫(péi) 98 锎(kāi) 99 锿(āi) 100 镄(fèi) 101 钔(mén) 102 锘(nuò) 103 铹(láo) 104 鈩(lú) 105 (dù) 106 (xǐ) 107 (bō) 108 (hēi) 109 䥑(mài) 110 鐽(dá) 111 錀(lún) 112 鎶(gē)[暂定] 注:新元素汉字请使用Win7系统浏览,XP系统下无法显示。

高中化学必修二元素周期表专题练习(带答案)work Information Technology Company.2020YEAR第一章 物质结构 元素周期律第一节 元素周期表一、元素周期表的结构:元素周期表有7个横行,每一个横行叫做一个周期。
其中第一、二、三周期叫做短周期,四至六周期叫做长周期,第七周期由于没有排满叫做不完全周期。
1.周期序数=电子层数 主族序数=最外层电子数2.除第1周期只包括氢和氦,第7周期尚未填满外,每一周期的元素都是从最外层电子数为1的碱金属开始,逐步过渡到最外层电子数为7的卤素,最后以最外层电子数为8的稀有气体结束。
短周期(第1、2、3周期)周期:7个(共七个横行) 长周期(第4、5、6周期)周期表 不完全周期(第7周期)主族7个:ⅠA-ⅦA族:16个(共18个纵行)副族7个:IB-ⅦB第Ⅷ族1个(3个纵行)零族(1个)稀有气体元素口诀:三长、三短、一不完全;七主七副一零一Ⅷ二.元素的性质和原子结构:(一)碱金属元素:相似性:最外层电子数相同,都为1个1. 原子结构 递变性:从上到下,随着核电核数增大,电子层数增多2.碱金属化学性质的相似性: 4Li + O 2 2Li 2O 2Na + O 2 Na 2O 2点燃 点燃2 Na + 2H2O =2NaOH + H2↑ 2K + 2H2O =2KOH + H2↑通式:2R + 2 H2O = 2 ROH + H2 ↑产物中,碱金属元素的化合价都为+1价。
结论:碱金属元素原子的最外层上都只有1个电子,因此,它们的化学性质相似。
3.碱金属化学性质的递变性:递变性:从上到下(从Li到Cs),随着核电核数的增加,碱金属原子的电子层数逐渐增多,原子核对最外层电子的引力逐渐减弱,原子失去电子的能力增强,即金属性逐渐增强。
所以从Li到Cs的金属性逐渐增强。
结论:1)原子结构的递变性导致化学性质的递变性。
2)金属性强弱的判断依据:与水或酸反应越容易,金属性越强;最高价氧化物对应的水化物(氢氧化物)碱性越强,金属性越强。

初中化学专题练习-元素周期表专题(含答
案)
以下是一些初中化学的元素周期表专题练题,每题都附带了答案。
这些练题涵盖了元素的基本概念、周期表的结构和元素周期表的运用等知识点。
希望这些练题能够帮助你更好地理解和掌握元素周期表的相关内容。
1. 何为元素周期表?它又包含了哪些信息?
答案:元素周期表是按照原子序数从小到大排列的化学元素表格。
它包含了每个化学元素的原子序数、元素符号、相对原子质量和元素名称等信息。
2. 元素周期表是按照什么原则进行排列的?
答案:元素周期表是按照化学元素的原子序数(即元素的质子数)从小到大排列的。
3. 元素周期表中的横行称为什么?纵列称为什么?
答案:元素周期表中的横行称为周期,纵列称为族或者组。
4. 元素周期表中的第一周期有多少个元素?它们是哪些元素?
答案:第一周期有两个元素,它们是氢(H)和氦(He)。
5. 元素周期表中最外层电子数相同的元素属于同一什么?
答案:最外层电子数相同的元素属于同一族或者组。
6. 元素周期表中的元素符号有什么作用?
答案:元素符号是表示化学元素的缩写形式,用来简化元素名称。
以上是基于元素周期表的专题练习题,希望能够帮助你加深对元素周期表的理解。
做题过程中,可以参考相关的学习资料进行复习和巩固,以提升自己的化学知识水平。
祝你学习进步!。

27个化学元素周期表元素读音第一周期元素:1 氢(qīng)2 氦(hài)元素周期表正确金属汉字写法第二周期元素:3 锂(lǐ)4 铍(pí)5 硼(péng)6 碳(tàn)7 氮(dàn)8 氧(yǎng)9 氟(fú) 10 氖(nǎi)第三周期元素:11 钠(nà) 12 镁(měi) 13 铝(lǚ) 14 硅(guī) 15 磷(lín) 16 硫(liú) 17 氯(lǜ) 18 氩(yà)第四周期元素:19 钾(jiǎ) 20 钙(gài) 21 钪(kàng) 22 钛(tài) 23 钒(fán) 24 铬(gè) 25锰(měng) 26 铁(tiě) 27 钴(gǔ) 28 镍(niè) 29 铜(tóng) 30 锌(xīn) 31 镓(jiā) 32锗(zhě) 33 砷(shēn) 34 硒(xī) 35 溴(xiù) 36 氪(kè)第五周期元素:37 铷(rú) 38锶(sī) 39 钇(yǐ) 40 锆(gào) 41 铌(ní) 42 钼(mù) 43 锝(dé) 44 钌(liǎo) 45 铑(lǎo)46 钯(bǎ) 47 银(yín) 48 镉(gé) 49 铟(yīn) 50 锡(xī) 51 锑(tī) 52 碲(dì) 53碘(diǎn) 54 氙(xiān)第六周期元素:55 铯(sè) 56 钡(bèi) 57 镧(lán) 58 铈(shì) 59镨(pǔ) 60 钕(nǚ) 61 钷(pǒ) 62 钐(shān) 63 铕(yǒu) 64 钆(gá) 65 铽(tè) 66 镝(dī)67 钬(huǒ) 68 铒(ěr) 69 铥(diū) 70 镱(yì) 71 镥(lǔ) 72 铪(hā) 73 钽(tǎn) 74钨(wū) 75 铼(lái) 76 锇(é) 77 铱(yī) 78 铂(bó) 79 金(jīn) 80 汞(gǒng) 81 铊(tā)82 铅(qiān) 83 铋(bì) 84 钋(pō) 85 砹(ài) 86 氡(dōng)第七周期元素:87 钫(fāng) 88镭(léi) 89 锕(ā) 90 钍(tǔ) 91 镤(pú) 92 铀(yóu) 93 镎(ná) 94 钚(bù) 95 镅(méi)96 锔(jú) 97 锫(péi) 98 锎(kāi) 99 锿(āi) 100 镄(fèi) 101 钔(mén) 102 锘(nuò)103 铹(láo) 104 炉(lú) 105 (dù) 106 (xǐ) 107 (bō) 108 (hēi) 109䥑(mài) 110 鐽(dá) 111 錀(lún) 112 鎶(gē)其中常用的27个:1氢 H 2氦 He3锂 Li 4 铍 Be 5 硼 b 6 碳 C 7 氮 N 8 氧 O 9 氟 F 10 氖Ne11 钠 Na 12镁 Mg 13铝 Al 14硅Si 15磷P 16硫S 17氯Cl18 氩 Ar19 钾 K 20 钙 Ca 22钛 Ti 25锰Mn 26铁Fe 28镍Ni 29铜Cu 30锌Zn 33砷As35 溴 Br47银Ag 50锡 Sn 53碘I56钡Be 78铂 Pt 79金Au 80汞Hg 82铅Pb相关知识:元素周期表的规律按照电子排布,可把周期表的元素划分为5个区:s区、 p区、d区、ds区、f 区。

随堂模拟测试第二节元素周期律和元素周期表1. “神舟七号”的燃料是氢化锂三兄弟物质的下列说法正确的是 ( )LiH、LiD、LiT。
其中Li的质量数为7,对这三种2.3. A .质子数之比为1 : 2 : 3C .摩尔质量之比为 8 : 9: 10B .中子数之比为D.化学性质不相同解析:A项,质子数之比为(3 + 1):+ 1) : (4+ 2) = 4 : 5 : 6; C 项摩尔质量之比为:(7 + 1) : (7+ 2) : (7 + 3) =8 : 9 : 三种物质的化学性质相同。
(3+ 1) : (3 + 1) = 1 : 1 :1 ; B项,中子数之比为(4+ 0) :(410; D 项,答案:C(2009山东理综,11)元素在周期表中的位置,反映了元素的原子结构和元素的性质。
法正确的是( )A .同一元素不可能既表现金属性,又表现非金属性B .第三周期元素的最高正化合价等于它所处的主族序数C•短周期元素形成离子后,最外层都达到8电子稳定结构D .同一主族的元素的原子,最外层电子数相同,化学性质完全相同解析:Al元素既表现金属性又表现非金属性,故A项错误;氢元素失去 1最外层没有电子,得到 1个电子为H-,为2电子稳定结构,故 C项错误; 与钠元素最外层电子数相同,但化学性质不同。
答案:B(2009 •东单科,11)元素X、Y、Z原子序数之和为 36 , X、Y在同一周期, 相同的核外电子层结构。
下列推测不正确的是( )A•同周期元素中X的金属性最强B .原子半径 X>Y,离子半径 X + >Z2「C •同族元素中Z的氢化物稳定性最高D•同周期元素中丫的最高价含氧酸的酸性最强下列说个电子为H + ,I A族中氢元素X +与Z2-具有解析:分析题给条件可推知:X是钠(Na)、Y是氯(CI)、Z 是氧(O)。
原子半径X>Y,但X +(Na + )与Z2—(02—)电子层结构相同,离子半径X + >Z2—。

元素周期表,元素周期律练习题【知识框架】【基础回顾】一、元素周期表1、元素周期表的编排原则(1)横行:把电子层数相同的元素按原子序数递增的顺序从左至右排成横行。
(2)纵行:把不同横行中最外层电子数相等的元素,按电子层数递增的顺序,由上而下排成纵行。
2、元素周期表的结构(1)周期(七个横行,七个周期)(2)族(18个纵行,16个族)3.元素周期表的分区(★选修)按构造原理最后填入电子的能级的符号可把周期表里的元素划分为5个区,分别为s区、d区、ds、p区、f区,各区分别包括ⅠA、Ⅱ族元素、ⅢB~Ⅷ族元素、ⅠB、ⅡB族元素、ⅢA~ⅦA族和0族元素、镧系和锕系元素,其中s区(H除外)d 区、ds区和f区的元素都为金属。
二、元素周期律1、概念元素的性质随核电荷数递增发生周期性的递变。
2、实质元素周期律的实质是元素原子结构的周期性变化必然引起元素性质的周期性变化。
3、对角线规则在元素周期表中,某些主族元素与右下方的主族元素的某些性质相似,如Li和Mg,Be和Al。
4、元素周期表中同周期、同主族元素性质的递变规律5、电离能(★选修)(1)第一电离能:气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量。
(2)元素第一电离能的意义:元素的第一电离能可以衡量元素的原子失去一个电子的难易程度。
第一电离能数值越小,原子越易失去一个电子,该元素的金属性越强;反之,第一电离能数值越大,原子越难失去一个电子。
(3)变化规律:①同一周期从左到右元素的第一电离能呈增大的趋势,但某些地方出现曲折变化,如Be>B,N>O, Mg>Al,P>S。
②同一族从上到下元素的第一电离能变小。
6.电负性(★选修)(1)键合电子:原子中用于形成化学键的电子。
(2)电负性:用来描述不同元素的原子对键合电子吸引力的大小。
(3)意义:电负性越大的原子,对键合电子的吸引力越大,非金属性越强。
故电负性的大小可用来衡量元素非金属性和金属性的大小。

高中化学组卷元素周期表及周期律练习题答案及解析一.选择题(共6小题)1.地壳中含量最多的元素在周期表中的位置是()A.第二周期VIA族B.第二周期V A族C.第三周期VIA族D.第三周期V A族2.Q、W、X、Y、Z都是短周期元素.X、Y、Q在周期表中的位置关系如图.W、Z的最外层电子数相同,Z的核电荷数是W的2倍.则下列说法不正确的是()ⅠA ⅡA ⅢA ⅣAQX YA.非金属性:W>ZB.原子半径:X>Y>ZC.最高价氧化物对应水化物的碱性:X>YD.氢化物稳定性:Q>W3.下列叙述正确的有()A.第四周期元素中,锰原子价电子层中未成对电子数最多B.第二周期主族元素的原子半径随核电荷数增大依次减小C.卤素氢化物中,HCl的沸点最低的原因是其分子间的范德华力最小D.价层电子对相斥理论中,π键电子对数不计入中心原子的价层电子对数4.四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与Y同族,Z与X形成的离子化合物的水溶液呈中性.下列说法正确的是()A.简单离子半径:W<X<ZB.W与X形成的化合物溶于水后溶液呈碱性C.气态氢化物的热稳定性:W<YD.最高价氧化物的水化物的酸性:Y>Z5.根据元素周期表和元素周期律分析下面的推断,其中错误的是()A.酸性由强到弱的顺序:HClO4>H2SO4>H3PO4B.氢氧化钙比氢氧化镁碱性强C.气态氢化物的稳定性X>Y,说明X的非金属性比Y强D.最外层电子数X>Y,说明X的非金属性比Y强6.已知Cl、S、P为三种原子序数相连的元素,则下列说法正确的是()A.气态氢化物的稳定性:HCl>H2S>PH3B.非金属活泼性:S<Cl<PC.原子半径:Cl>S>PD.原子序数:S<P<Cl二.填空题(共3小题)7.针对下面10种元素,完成以下各小题.回答下列间题.ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅤⅡA 02 C N F Ne3 Na Mg Al Si S Cl(1)非金属性最强的元素是(填名称).化学性质最不活泼的元素是(填元素符号).(2)S 原子结构示意图为;(3)Mg和Al中,原子半径较小的是;(4)N的氢化物的分子式,该物质中N元素与H元素的质量比为,(相对原子质量:N﹣14 H﹣1),其水溶液呈性.(5)元素硅的氧化物常用于制造(填一种高性能的现代通讯材料的名称);(6)元素最高价氧化物对应的水化物中,碱性最强的是(填化学式),呈两性的是(填化学式);两者反应的化学方程式.8.X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大.X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子.请回答下列问题:(1)Y在元素周期表中的位置为.(2)上述元素的最高价氧化物对应的水化物酸性最强的是(写化学式),非金属气态氢化物还原性最强的是(写化学式).(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有(写出其中两种物质的化学式).(4)ZX的电子式为;ZX与水反应放出气体的化学方程式为.9.下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题.族IA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0周期二①②③④三⑤⑥⑦⑧⑨⑩(1)非金属性最强的元素是(填元素符号,下同),形成化合物种类最多的元素是.(2)第三周期元素除⑩外原子半径最小的是(填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是(填化学式,下同),具有两性的是.(3)⑤⑥⑦单质的活泼性顺序为>>(填元素符号),判断的实验依据是(写出一种).三.多选题(共1小题)10.X、Y、Z、W 四种短周期元素在周期表中位于连续的四个主族,相对位置如图所示.Z 元素原子核外K层与M层电子数相等.下列说法正确的是()X YWZA.原子半径由小到大的顺序为Y<X<W<ZB.Y的单质和Z的单质能够发生反应C.X的单质都是熔点高、硬度大的物质D.工业上利用电解Z、W的熔融氯化物的方法制备对应的单质四.推断题(共1小题)11.如表为元素周期表短周期的一部分,请用化学用语(元素符号或化学式)回答相关问题:①②③④⑤⑥⑦⑧⑨(1)⑥元素在周期表中的位置为.(2)表中序号元素中半径最大的常见离子是.(3)表中最高价氧化物对应水化物的碱性最强的物质的电子式为,酸性最强的物质的化学式是,气态氢化物最稳定的物质的化学式是.(4)元素非金属性强弱比较有很多方法,其中③和⑧的非金属性强弱的探究方案中不可行的是(填序号)A.比较两种氢化物的熔沸点高低B.比较氢化物的稳定性C.通过和铁反应,比较得电子能力D.通过置换反应(5)由①和②两种元素组成的化合物,同条件下与氧气密度相当,请写出该分子的电子式.(6)⑦与⑨两元素的单质反应生成1mol⑦的最高价化合物,恢复至室温,放热687kJ,已知该化合物的熔、沸点分别为﹣69℃和58℃,写出该反应的热化学方程式.高中化学组卷参考答案与试题解析一.选择题(共6小题)1.(2017•嘉兴模拟)地壳中含量最多的元素在周期表中的位置是()A.第二周期VIA族B.第二周期V A族C.第三周期VIA族D.第三周期V A族【分析】地壳中含量最多的元素为O元素,其原子序数为8,核外含有2个电子层,最外层含有6个电子,据此判断氧元素在周期表中的位置.【解答】解:地壳中含量最多的元素为O元素,其原子序数为8,核外含有2个电子层,最外层含有6个电子,则氧元素位于周期表中第二周期VIA族,故选A.【点评】本题考查了元素周期表的结构及应用,题目难度不大,明确地壳中元素含量为解答关键,注意掌握原子结构与元素周期表的关系,试题侧重考查学生的灵活应用能力.2.(2017•湛江校级模拟)Q、W、X、Y、Z都是短周期元素.X、Y、Q在周期表中的位置关系如图.W、Z的最外层电子数相同,Z的核电荷数是W的2倍.则下列说法不正确的是()ⅠA ⅡA ⅢA ⅣAQX YA.非金属性:W>ZB.原子半径:X>Y>ZC.最高价氧化物对应水化物的碱性:X>YD.氢化物稳定性:Q>W【分析】Q、W、X、Y、Z都是短周期元素.由X、Y、Q在周期表中的位置关系可知:X 为Na元素、Y为Al元素、Q为碳元素元素.W、Z的最外层电子数相同,二者处于同族,Z的核电荷数是W的2倍,令W的核电荷数为a,则Z的核电荷数为2a,故a+8=2a,解得a=8,故W为O元素、Z为S元素,据此解答.【解答】解:Q、W、X、Y、Z都是短周期元素.由X、Y、Q在周期表中的位置关系可知:X为Na元素、Y为Al元素、Q为碳元素元素.W、Z的最外层电子数相同,二者处于同族,Z的核电荷数是W的2倍,令W的核电荷数为a,则Z的核电荷数为2a,故a+8=2a,解得a=8,故W为O元素、Z为S元素,A.同主族自上而下非金属性减弱,故非金属性O>S,即W>Z,故A正确;B.同周期自左而右原子半径减小,故原子半径Na>Al>S,即X>Y>Z,故B正确;C.同周期自左而右金属性减弱,金属性越弱,最高价氧化物对应水化物的碱性越弱,故碱性:X>Y,故C正确;D.非金属性越强,氢化物越稳定,故稳定性H2O>CH4,故D错误;故选D.【点评】本题考查结构性质位置关系、元素周期律等,难度不大,注意整体把握元素周期表的结构,掌握元素周期律.3.(2016•海南)下列叙述正确的有()A.第四周期元素中,锰原子价电子层中未成对电子数最多B.第二周期主族元素的原子半径随核电荷数增大依次减小C.卤素氢化物中,HCl的沸点最低的原因是其分子间的范德华力最小D.价层电子对相斥理论中,π键电子对数不计入中心原子的价层电子对数【分析】A、第四周期元素中,外围电子排布为nd x ns y,且能级处于半满稳定状态时,含有的未成对电子数最多;B、同周期核电荷数越多半径越小;C、HF分子间存在氢键;D、价层电子对相斥理论中,σ键和孤对电子对计入中心原子的价层电子对数,而π不计入.【解答】解:A、第四周期元素中,外围电子排布为nd x ns y,且能级处于半满稳定状态时,含有的未成对电子数最多,即外围电子排布为3d54s1,此元素为铬,故A错误;B、同周期核电荷数越多半径越小,所以第二周期主族元素的原子半径随核电荷数增大依次减小,故B正确;C、HF分子间存在氢键,HCl分子内没有氢键,故C错误;D、价层电子对相斥理论中,σ键和孤对电子对计入中心原子的价层电子对数,而π不计入,故D正确;故选BD.【点评】本题考查核外电子排布规律、元素周期律、氢键和价层电子对理论等,难度不大,注意选A在理解核外电子排布规律,注意能级处于全满、半满、全空时的稳定状态.4.(2016春•南宁校级期末)四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与Y 同族,Z与X形成的离子化合物的水溶液呈中性.下列说法正确的是()A.简单离子半径:W<X<ZB.W与X形成的化合物溶于水后溶液呈碱性C.气态氢化物的热稳定性:W<YD.最高价氧化物的水化物的酸性:Y>Z【分析】四种短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是短周期主族元素原子中最大的,则X是钠;Z与X形成的离子化合物的水溶液呈中性,说明这种盐不水解,Z只能是第三周期的非金属元素,且Z的氢化物的水溶液属于强酸,则Z是氯;W、X的简单离子具有相同电子层结构,则W在第二周期且是非金属元素,可能是氮和氧;W与Y同族,Y在X与Z之间,位置关系如图:,据此解答.【解答】解:四种短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是短周期主族元素原子中最大的,则X是钠;Z与X形成的离子化合物的水溶液呈中性,说明这种盐不水解,Z只能是第三周期的非金属元素,且Z的氢化物的水溶液属于强酸,则Z是氯;W、X的简单离子具有相同电子层结构,则W在第二周期且是非金属元素,可能是氮和氧;W与Y同族,Y在X与Z之间,位置关系如图:,A.X、W离子的电子层为2层,Z离子即氯离子电子层为3层,电子层多半径大,电子层结构相同时,序小半径反而大,则简单离子半径大小顺序是:X<W<Z,故A错误;B.W在第二周期且是非金属元素,可能是氮和氧,与钠形成的化合物可能是氮化钠,氧化钠,过氧化钠,它们与水反应都能生成氢氧化钠使溶液呈碱性,故B正确;C.W与Y处于同于主族,从上到下,非金属性逐渐减弱,气态氢化物的热稳定性逐渐减弱,则W>Y,故C错误;D.Y与Z处于同同期,从左到右,非金属性逐渐增强,最高价氧化物的水化物的酸性逐渐增强,则Z>Y,故D错误;故选:B.【点评】本题考查了原子结构与元素周期表的关系,正确推断各元素为解答关键,在答题时,画出各元素的位置关系使解题更快也更准确,试题培养了学生的分析能力及灵活应用能力.5.(2016•淄博校级模拟)根据元素周期表和元素周期律分析下面的推断,其中错误的是()A.酸性由强到弱的顺序:HClO4>H2SO4>H3PO4B.氢氧化钙比氢氧化镁碱性强C.气态氢化物的稳定性X>Y,说明X的非金属性比Y强D.最外层电子数X>Y,说明X的非金属性比Y强【分析】A.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;B.同主族元素的金属性越强,对应的最高价氧化物的水化物的碱性越强;C.元素的非金属性越强,对应的氢化物越稳定;D.元素的非金属性的大小取决于得电子能力.【解答】解:A.非金属性Cl>S>P,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,故A正确;B.金属性Ca>Mg,元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,故B 正确;C.元素的非金属性越强,对应的氢化物越稳定,故C正确;D.元素的非金属性的大小取决于得电子能力,与原子最外层电子数的多少无关,故D错误.故选D.【点评】本题考查元素周期律知识,为高考常见题型和高频考点,侧重于学生的分析能力的考查,注意把握元素周期律的递变规律以及对应单质、化合物的性质的相似性和递变性的判断,把握比较角度,难度不大.6.(2016•吴忠校级模拟)已知Cl、S、P为三种原子序数相连的元素,则下列说法正确的是()A.气态氢化物的稳定性:HCl>H2S>PH3B.非金属活泼性:S<Cl<PC.原子半径:Cl>S>PD.原子序数:S<P<Cl【分析】同周期从左向右随原子序数的增大,非金属性增强、原子半径减小,非金属性越强,对应氢化物越稳定,以此来解答.【解答】解:A.非金属性Cl>S>P,气态氢化物的稳定性为HCl>H2S>PH3,故A正确;B.非金属性Cl>S>P,非金属活泼性为Cl>S>P,故B错误;C.同周期从左向右原子半径减小,则原子半径为P>S>Cl,故C错误;D.同周期从左向右原子序数增大,则原子序数为P<S<Cl,故D错误;故选A.【点评】本题考查非金属元素的性质,为高频考点,把握元素在周期表的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.二.填空题(共3小题)7.(2016•晋江市校级模拟)针对下面10种元素,完成以下各小题.回答下列间题.ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅤⅡA 02 C N F Ne3 Na Mg Al Si S Cl(1)非金属性最强的元素是氟(填名称).化学性质最不活泼的元素是Ne(填元素符号).(2)S 原子结构示意图为;(3)Mg和Al中,原子半径较小的是Al;(4)N的氢化物的分子式NH3,该物质中N元素与H元素的质量比为14:3,(相对原子质量:N﹣14 H﹣1),其水溶液呈碱性性.(5)元素硅的氧化物常用于制造光导纤维(填一种高性能的现代通讯材料的名称);(6)元素最高价氧化物对应的水化物中,碱性最强的是NaOH(填化学式),呈两性的是Al(OH)3(填化学式);两者反应的化学方程式NaOH+Al(OH)3=NaAlO2+2H2O.【分析】(1)同周期自左而右非金属性增强,同主族自上而下非金属性减弱;稀有气体原子最外层为稳定结构,化学性质最不活泼;(2)S原子质子数为16,核外电子数为16,有3个电子层,各层电子数为2、8、6;(3)同周期自左而右原子半径减小;(4)N的氢化物的分子式为NH3,其水溶液呈碱性;(5)二氧化硅可以制造光导纤维;(6)同周期自左而右金属性减弱,金属性越强,最高价氧化物对应水化物的碱性越强;氢氧化铝属于两性氢氧化物.【解答】解:(1)同周期自左而右非金属性增强,同主族自上而下非金属性减弱,上述元素中F元素非金属性最强;稀有气体Ne原子最外层为稳定结构,化学性质最不活泼,故答案为:氟;Ne;(2)S原子质子数为16,核外电子数为16,有3个电子层,各层电子数为2、8、6,原子结构示意图为,故答案为:;(3)同周期自左而右原子半径减小,故原子半径Mg>Al,故答案为:Al;(4)N的氢化物的分子式为NH3,分子中N、H元素质量之比为14:3 其水溶液呈碱性,故答案为:NH3;14:3;碱;(6)二氧化硅可以制造光导纤维,故答案为:光导纤维;(6)上述元素中Na的金属性最强,故NaOH的碱性最强,Al(OH)3属于两性氢氧化物,二者反应生成偏铝酸钠与水,反应方程式为:NaOH+Al(OH)3=NaAlO2+2H2O,故答案为:NaOH;Al(OH)3;NaOH+Al(OH)3=NaAlO2+2H2O.【点评】本题考查元素周期表与元素周期律综合应用,侧重对元素周期律的考查,注意掌握元素化合物性质,比较基础.8.(2016春•龙海市校级期末)X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大.X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子.请回答下列问题:(1)Y在元素周期表中的位置为第二周期第ⅥA族.(2)上述元素的最高价氧化物对应的水化物酸性最强的是HClO4(写化学式),非金属气态氢化物还原性最强的是H2S(写化学式).(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有O3、ClO2(写出其中两种物质的化学式).(4)ZX的电子式为;ZX与水反应放出气体的化学方程式为NaH+H2O=NaOH+H2↑.【分析】X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大,所以X是H 元素;X、Z同主族,可形成离子化合物ZX,且Y原子序数大于Y原子序数,所以Z是Na元素;Y、M同主族,可形成MY2、MY3两种分子,所以Y是O元素,M是S元素,G是短周期主族元素,所以G是Cl元素(不考虑稀有气体),据此解答,【解答】解:X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大,所以X是H元素;X、Z同主族,可形成离子化合物ZX,且Y原子序数大于Y原子序数,所以Z 是Na元素;Y、M同主族,可形成MY2、MY3两种分子,所以Y是O元素,M是S元素,G是短周期主族元素,所以G是Cl元素(不考虑稀有气体),(1)Y是O元素,O原子有2个电子层,最外层电子数为6,处于第二周期第ⅥA族,故答案为:第二周期第ⅥA族;(2)非金属元素的非金属性越强,其相应的最高价含氧酸的酸性越强,这几种元素非金属性最强的是Cl元素,所以其最高价含氧酸的酸性最强的是高氯酸HClO4,非金属性越弱,气态氢化物还原性越强,还原性最强的气态氢化物是硫化物H2S,故答案为:HClO4;H2S;(3)Y的单质O3、G的单质Cl2、二者形成的ClO2可作消毒剂,故答案为:O3、ClO2等;(4)ZX为NaH,属于离子化合物,由钠离子与氢负离子构成,电子式为,Na 与水反应是氢氧化钠与氢气,反应化学方程式为为:NaH+H2O=NaOH+H2↑,故答案为:;NaH+H2O=NaOH+H2↑.【点评】本题以元素推断为载体考查了元素化合物的性质,能正确判断元素是解本题的关键,注意(4)中NaH电子式书写氢负离子的电子式2个电子成对,不能分开.9.(2016春•伊犁州校级期末)下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题.IA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0 族周期二①②③④三⑤⑥⑦⑧⑨⑩(1)非金属性最强的元素是F(填元素符号,下同),形成化合物种类最多的元素是C.(2)第三周期元素除⑩外原子半径最小的是Cl(填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是NaOH(填化学式,下同),具有两性的是Al(OH)3.(3)⑤⑥⑦单质的活泼性顺序为Na>Mg>Al(填元素符号),判断的实验依据是单质与水或酸反应的剧烈程度(写出一种).【分析】由元素在周期表中的位置可知,①为C,②为N,③为O,④为F,⑤为Na,⑥为Mg,⑦为Al,⑧为S,⑨为Cl,⑩为Ar,然后利用元素及其单质、化合物的性质来解答.【解答】解:由元素在周期表中的位置可知,①为C,②为N,③为O,④为F,⑤为Na,⑥为Mg,⑦为Al,⑧为S,⑨为Cl,⑩为Ar,(1)以上元素中第二周期中F的非金属性最强,在第ⅦA中F的非金属性最强,则F的非金属性最强,碳元素形成的有机物种类最多,故答案为:F;C;(2)同周期,从左向右原子半径在减小,则Cl的原子半径在第三周期最小,以上元素中Na的金属性最强,则最高价氧化物对应水化物NaOH的碱性最强,Al元素的最高价氧化物对应水化物Al(OH)3的具有两性,故答案为:Cl;NaOH;Al(OH)3;(3)同周期,从左向右金属性在减弱,则Na、Mg、Al单质的活泼性为Na>Mg>Al,可利用单质分别与水(或酸)反应的剧烈程度来验证,故答案为:Na;Mg;Al;单质与水或酸反应的剧烈程度.【点评】本题考查元素周期表和元素周期律,熟悉元素在元素周期表中的位置是解答本题的关键,并利用元素及其单质、化合物的性质来解答即可,难度不大.三.多选题(共1小题)10.(2016•海南校级模拟)X、Y、Z、W 四种短周期元素在周期表中位于连续的四个主族,相对位置如图所示.Z元素原子核外K层与M层电子数相等.下列说法正确的是()X YWZA.原子半径由小到大的顺序为Y<X<W<ZB.Y的单质和Z的单质能够发生反应C.X的单质都是熔点高、硬度大的物质D.工业上利用电解Z、W的熔融氯化物的方法制备对应的单质【分析】X、Y、Z、W为四种短周期主族元素,Z元素原子核外K层与M层电子数相等,则Z原子M层电子数为2,故Z为Mg元素;由元素周期表中的相对位置可知,W为Al元素、X为C元素、Y为N元素,结合对应单质、化合物的性质以及元素周期律知识解答该题.【解答】解:X、Y、Z、W为四种短周期主族元素,Z元素原子核外K层与M层电子数相等,则Z原子M层电子数为2,故Z为Mg元素,由元素周期表中的相对位置可知,W为Al元素、X为C元素、Y为N元素,A.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径大小为:N <C<Al<Mg,即Y<X<W<Z,故A正确;B.Y的单质和Z的单质分别是氮气、镁,它们点燃生成氮化镁,故B正确;C.X是碳,它的单质有金刚石,金刚石的熔点高、硬度大,其他单质石墨质软,足球烯是分子晶体,熔点低,硬度小,故C错误;D.工业上利用电解Z(镁)的熔融氯化物的方法制备对应的单质镁,而铝不能用三氯化铝,因为三氯化铝是共价化合物,熔融态不能导电,故D错误;故选AB.【点评】本题考查结构位置性质关系应用,为高频考点,题目难度中等,试题侧重于学生的分析能力的考查,注意把握元素周期表的结构、元素周期律的递变规律.四.推断题(共1小题)11.(2016春•西安校级期末)如表为元素周期表短周期的一部分,请用化学用语(元素符号或化学式)回答相关问题:①②③④⑤⑥⑦⑧⑨(1)⑥元素在周期表中的位置为第三周期第ⅢA族.(2)表中序号元素中半径最大的常见离子是S2﹣.(3)表中最高价氧化物对应水化物的碱性最强的物质的电子式为,酸性最强的物质的化学式是HClO4,气态氢化物最稳定的物质的化学式是HF.(4)元素非金属性强弱比较有很多方法,其中③和⑧的非金属性强弱的探究方案中不可行的是A(填序号)A.比较两种氢化物的熔沸点高低B.比较氢化物的稳定性C.通过和铁反应,比较得电子能力D.通过置换反应(5)由①和②两种元素组成的化合物,同条件下与氧气密度相当,请写出该分子的电子式.(6)⑦与⑨两元素的单质反应生成1mol⑦的最高价化合物,恢复至室温,放热687kJ,已知该化合物的熔、沸点分别为﹣69℃和58℃,写出该反应的热化学方程式Si(s)+2Cl2(g)=SiCl4(l)△H=﹣687kJ/mol.【分析】由元素在周期表中的位置可知,①为H,②为N,③为O,④为F,⑤为Na,⑥为Al,⑦为Si,⑧为S,⑨为Cl,(1)⑥元素为Al;(2)第三周期中阴离子大于阳离子半径,且具有相同排布的离子中原子序数大的离子半径小;(3)NaOH的碱性最强,高氯酸的酸性在所有含氧酸中酸性最强,HF在氢化物中最稳定;(4)利用氢化物的稳定性、与氢气化合的难易、最高价含氧酸的酸性、得电子能力比较非金属性;(5)由①和②两种元素组成的化合物,同条件下与氧气密度相当,则化合物为N2H4;(6)Si与Cl两元素的单质反应生成1molCl4,恢复至室温,放热687kJ,由于该化合物的熔、沸点分别为﹣69℃和58℃,则常温下SiCl4为液态,据此结合热化学方程式的书写原则解答.【解答】解:由元素在周期表中的位置可知,①为H,②为N,③为O,④为F,⑤为Na,⑥为Al,⑦为Si,⑧为S,⑨为Cl,(1)⑥元素为Al,位于第三周期第ⅢA族,故答案为:第三周期第ⅢA族;(2)第三周期中阴离子大于阳离子半径,且具有相同排布的离子中原子序数大的离子半径小,则表中序号元素中半径最大的常见离子是S2﹣,故答案为:S2﹣;(3)表中最高价氧化物对应水化物的碱性最强的物质为NaOH ,其电子式为;高氯酸的酸性在所有含氧酸中酸性最强,其化学式为HClO4,气态氢化物最稳定的物质的化学式是HF,故答案为:;HClO4;HF;(4)A.比较两种氢化物的熔沸点高低,水中含氢键沸点高,但一般不能利用熔沸点比较非金属性,角度不合理,故A选;B.比较氢化物的稳定性,可知非金属性,故B不选;C.通过和铁反应,比较得电子能力,则O得到电子能力强,可比较非金属性,故C不选;D.通过置换反应,如氧气与硫化氢反应生成S,可比较非金属性,故D不选;故答案为:A;(5)由①和②两种元素组成的化合物,同条件下与氧气密度相当,则化合物为N2H4,电子式为,故答案为:;(6)Si与Cl两元素的单质反应生成1molSi的最高价化合物SiCl4,恢复至室温,放热687kJ,已知该化合物的熔、沸点分别为﹣69℃和58℃,则常温下SiCl4为液态,该反应的热化学方程式为Si(s)+2Cl2(g)=SiCl4(l)△H=﹣687kJ/mol,故答案为:Si(s)+2Cl2(g)=SiCl4(l)△H=﹣687kJ/mol.【点评】本题考查位置、结构与性质的关系,为高频考点,把握元素的位置、性质、元素化合物知识为解答的关键,侧重分析与应用能力的考查,注意元素周期律、元素化合物知识的应用,题目难度不大.第11页(共11页)。

初三化学元素周期表原子序数元素符号元素名称相对原子质量元素名称读音1 H 氢 1.0079 (qīng)2 He 氦 4.0026 (hài)3 Li 锂 6.941 (lǐ)4 Be 铍 9.0122 (pí)5 B 硼 10.811 (péng)6 C 碳 12.011 (tàn)7 N 氮 14.007 (dàn)8 O 氧 15.999 (yǎng)9 F 氟 18.998 (fú)10 Ne 氖 20.17 (nǎi)11 Na 钠 22.9898 (nà)12 Mg 镁 24.305 (měi)13 Al 铝 26.982 (lǚ)14 Si 硅 28.085 (guī)15 P 磷 30.974 (lín)16 S 硫 32.06 (liú)17 Cl 氯 35.453 (lǜ)18 Ar 氩 39.94 (yà)19 K 钾 39.098 (jiǎ)20 Ca 钙 40.08 (gài)21 Sc 钪 44.956 (kàng)22 Ti 钛 47.9 (tài)23 V 钒 50.94 (fán)24 Cr 铬 51.996 (gè)25 Mn 锰 54.938 (měng)26 Fe 铁 55.84 (tiě)27 Co 钴 58.9332 (gǔ)28 Ni 镍 58.69 (niè)29 Cu 铜 63.54 (tóng)30 Zn 锌 65.38 (xīn)31 Ga 镓 69.72 (jiā)32 Ge 锗 72.5 (zhě)33 As 砷 74.922 (shēn)34 Se 硒 78.9 (xī)35 Br 溴 79.904 (xiù)36 Kr 氪 83.8 (kè)37 Rb 铷 85.467 (rú)38 Sr 锶 87.62 (sī)39 Y 钇 88.906 (yǐ)40 Zr 锆 91.22 (gào)42 Mo 钼 95.94 (mù)43 Tc 锝 (99) (dé)44 Ru 钌 161.0 (liǎo)45 Rh 铑 102.906 (lǎo)46 Pd 钯 106.42 (bǎ)47 Ag 银 107.868 (yín)48 Cd 镉 112.41 (gé)49 In 铟 114.82 (yīn)50 Sn 锡 118.6 (xī)51 Sb 锑 121.7 (tī)52 Te 碲 127.6 (dì)53 I 碘 126.905 (diǎn)54 Xe 氙 131.3 (xiān)55 Cs 铯 132.905 (sè)56 Ba 钡 137.33 (bèi) 57-71 La-Lu 镧系57 La 镧 138.9 (lán)58 Ce 铈 140.1 (shì)59 Pr 镨 140.9 (pǔ)60 Nd 钕 144.2 (nǚ)61 Pm 钷 (147) (pǒ)62 Sm 钐 150.3 (shān)63 Eu 铕 151.96 (yǒu)64 Gd 钆 157.25 (gá)65 Tb 铽 158.9 (tè)66 Dy 镝 162.5 (dī)67 Ho 钬 164.9 (huǒ)68 Er 铒 167.2 (ěr)69 Tm 铥 168.9 (diū)70 Yb 镱 173.04 (yì)71 Lu 镥 174.967 (lǔ)72 Hf 铪 178.4 (hā)73 Ta 钽 180.947 (tǎn)74 W 钨 183.8 (wū)75 Re 铼 186.207 (lái)76 Os 锇 190.2 (é)77 Ir 铱 192.2 (yī)78 Pt 铂 195.08 (bó)79 Au 金 196.967 (jīn)80 Hg 汞 200.5 (gǒng)81 Tl 铊 204.3 (tā)82 Pb 铅 207.2 (qiān)83 Bi 铋 208.98 (bì)85 At 砹 (201) (ài)86 Rn 氡 (222) (dōng)87 Fr 钫 (223) (fāng)88 Ra 镭 226.03 (léi)89-103 Ac-Lr 锕系89 Ac 锕 (227) (ā)90 Th 钍 232.0 (tǔ)91 Pa 镤 231.0 (pú)92 U 铀 238.0 (yóu)93 Np 镎 (237) (ná)94 Pu 钚 (244) (bù)95 Am 镅 (243) (méi)96 Cm 锔 (247) (jú)97 Bk 锫 (247) (péi)98 Cf 锎 (251) (kāi)99 Es 锿 (252) (āi)100 Fm 镄 (257) (fèi)101 Md 钔 (258) (mén)102 No 锘 (259) (nuò)103 Lr 铹 (262) (láo)104 Rf 钅卢 (257) (lú)105 Db 钅杜 (261) (dù)106 Sg 钅喜 (262) (xǐ)107 Bh 钅波 (263) (bō)108 Hs 钅黑 (262) (hēi)109 Mt 钅麦 (265) (mài)110 Uun (281)111 Uuu (272)112 Uub (285)114 Uuq (289)(加括号的数据为该放射性元素半衰期最长同位素的质量数Welcome !!! 欢迎您的下载,资料仅供参考!。

【基础知识】议一议:元素周期表的编排依据?看一看:元素周期表的结构?1.元素周期表在编排时是将_______________________________________________的元素放在同一横行,并按照原子序数_________________________________从左到右排列。
将_______________________________________________的元素放在同一纵行,并按照电子层数________________________从上到下排列。
2.元素周期表中共有___________个周期,其中______________________是短周期,______________________是长周期,第________周期由于还有尚待发现的元素又被称为______________________3.数一数每一个周期分别有多少种元素:_______________________________________________________________________________ __________________________________________________4.元素周期表中共有___________个族,其中主族有__________个,分别用符号___________________________________________表示,副族有__________个,分别用符号_______________________________________________表示,此为还有一个_________族(位于第_______________纵行)和一个_________族。
5.元素周期表中从左到右每一个纵行分别是哪些族?_______________________________________________________________________________ _______________________________________________________________________________ ____________________________________________6.元素的原子序数=______________=_______________=__________________;元素所在的周期序数=_____________;主族元素所在的族序数=___________;主族元素(氧、氟除外)的最高化合价数值=____________________;ⅣA~ⅦA族元素的最低化合价和最高化合价的绝对值之和为_____________。

周练(8)1.元素周期表里金属元素和非金属元素分界线附近能找到( )A.新制农药元素B.制催化剂元素C.制半导体元素D.制耐高温合金元素2.YBa2Cu8O x (Y为元素钇)是磁悬浮列车中的重要超导材料,关于8939Y的说法不正确的是( )A.钇元素属于金属B.质子数与中子数之差为50C.原子的核外电子数是39 D.8939Y和9039Y是两种不同的核素3.根据下表信息,判断以下叙述正确的是( )A.M与T形成的化合物具有两性B.单质与稀盐酸反应的速率为L<Q C.氢化物的热稳定性为H2T<H2R D.氢化物的沸点为H2T<H2R4.X、Y、Z是3种短周期元素,其中X、Y位于同一族,Y、Z处于同一周期。
X原子的最外层电子数是其电子层数的3倍。
Z原子的核外电子数比Y原子的少1。
下列说法正确的是( )A.元素非金属性由弱到强的顺序为Z<Y<XB.Y元素最高价氧化物对应水化物的化学式可表示为H3YO4C.3种元素的气态氢化物中,Z的气态氢化物最稳定D.原子半径由大到小的顺序为Y>Z>X5.X、Y是元素周期表ⅦA族中的两种元素,下列叙述中能说明X的非金属性比Y强的是()A.X原子的电子层数比Y原子的电子层数多B.Y的气态氢化物比X的气态氢化物稳定C.X的氢化物的沸点比Y的氢化物的沸点低D.用石墨做电极电解等物质的量浓度的NaX和NaY的混合溶液,Y- 先被氧化6.下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。
向KMnO4第 2 页 共 8 页 晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
已知:2KMnO 4+16HCl=2KCl+ 5Cl 2↑+2MnCl 2+8H 2O对实验现象的“解释或结论”正确的是( )7.下列说法中正确的是 ( )A.ⅠA 、ⅡA 族元素的原子,其半径越大,越难失去电子B.元素周期表中从ⅢB 族到ⅡB 族10个纵行的元素都是金属元素C.原子及其离子的核外电子层数等于该元素所在的周期数D.所有主族元素的原子,都能形成单原子离子8.砹(At )是卤族元素中位于碘后面的元素,试推测砹和砹的化合物最不可能具备的性质是( )A .砹易溶于某些有机溶剂B .砹化氢很稳定不易分解C .砹是有色气体D .砹化银不溶于水或稀HNO 39.短周期元素A 、B 、C 原子序数依次递增,它们的原子的最外层电子数之和为10。
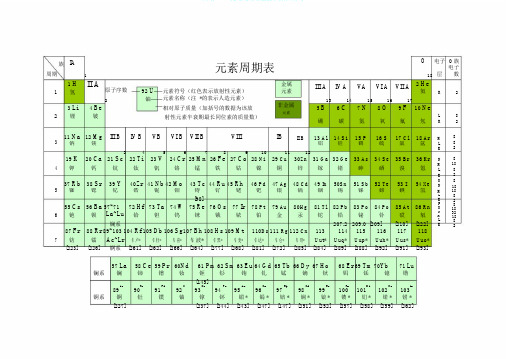
族 IA周期111 H II A原子序数氢2 23 Li4 Be锂 铍元素周期表92 U 元素符号(红色表示放射性元素) 金属 元素 铀 元素名称(注 *的表示人造元素) 非金属相对原子质量(加括号的数据为该放元素射性元素半衰期最长同位素的质量数)电子 0 族层电子18 数 III A IV AVAVI A VII A 2 HeK2氦13 14 15 16 175 B6 C7 N8 O9 F 10 Ne L 8 硼 碳 氮 氧 氟 氖 K2311 Na 12 MgIII BIV BVBVI B VII BVIIIIBII B13 Al 14 Si15 P16 S17 Cl18 ArM 钠镁铝硅磷硫氯氩L3 45 6 7 89 101112K19 K 20 Ca 21 Sc 22 Ti 23 V 24 Cr 25 Mn 26 Fe 27 Co 28 Ni 29 Cu 30Zn 31 Ga 32 Ge 33 As 34 Se 35 Br 36 Kr N 4钾 钙 钪 钛 钒 铬锰铁钴镍铜 锌 镓 锗砷硒溴氪M LK37 Rb 38 Sr 39 Y 40Zr 41 Nb 42 Mo 43 Tc 44 Ru 45 Rh 46 Pd 47 Ag 48 Cd 49 In 50Sn 51 Sb 52 Te 53 I 54 Xe ON 5 铷 锶 钇 锆 铌 钼 锝 钌 铑 钯 银 镉 铟 锡 锑 碲 碘 氙M[98]LK55 Cs 56 Ba 57~71 72 Hf 73 Ta 74 W 75 Re 76 Os 77 Ir 78 Pt 79 Au 80Hg 81 Tl 82 Pb 83 Po 84 Po 85 At 86 Rn P O 6铯 钡 La ~Lu 铪 钽 钨 铼 锇 铱 铂 金 汞 铊 铅 铋 钋 砹 氡 N M镧系207.2 209.0 [209] [210] [222] LK87 Fr 88 Rr 89~103 104 Rf 105 Db 106 Sg 107 Bh 108 Hs 109 Mt 110Ds 111 Rg 112 Cn113114 115 116 117 118 7钫 镭 Ac ~Lr钅卢* 钅杜* 钅喜*钅波* 钅黑* 钅麦*钅达*钅仑*钅哥*Uut*Uuq* Uup* Uuh* Uus* Uuo*[223][226]锕系 [261] [262] [266] [264][277] [268] [281] [272][285] [284] [289][288] [292] [291][293]8 828 18 8 2 818 18 8 2 8 18 32 18 8 2镧系 57 La 58 Ce 59 Pr 60Nd61 Pm 62 Sm 63 Eu 64 Gd 65 Tb 66 Dy 67 Ho 68 Er 69 Tm 70Yb 71 Lu 镧 铈 镨 钕 钷 钐 铕 钆 铽 镝 钬 铒 铥 镱 镥[145]89 Ac Th 91 Pa 92 U 93 Np 94 Pu 95 Am 96 Cm 97 Bk 98 Cf 99 Es Fm 101 Md102 No103 Lr90 100 锕系 锕钍 镤 铀 镎 钚 镅 * 锔 * 锫 * 锎 * 锿 * 镄 * 钔 * 锘 * 铹 *[227][237][244][243][247][147][251][252][257][258][259][262]。

浙江省宁波市高考化学专题八元素周期律和元素周期表Ⅰ复习训练编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(浙江省宁波市高考化学专题八元素周期律和元素周期表Ⅰ复习训练)的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为浙江省宁波市高考化学专题八元素周期律和元素周期表Ⅰ复习训练的全部内容。
专题八元素周期律和元素周期表Ⅰ1、关于11~17号元素的性质比较中:①元素的最高正化合价依次升高;②元素的非金属性逐渐增强;③元素的金属性依次减弱;④元素的最高价氧化物对应水化物的碱性逐渐减弱,酸性逐渐增强。
正确的说法是()A.①② B.③④ C.全都不正确 D.①②③④2、下列关于元素周期律的叙述正确的是( )A.随着元素原子序数的递增,原子最外层电子数总是从1到8重复出现B.元素的性质随着核电荷数的递增而呈周期性变化C.随着元素核电荷数的递增,元素的最高化合价从+1到+7,最低化合价从-7到-1重复出现D.元素性质的周期性变化是原子半径的周期性变化的必然结果3、下列事实不能作为实验判断依据的是( )A.钠和镁分别与冷水反应,判断金属活动性强弱B.铁投入CuSO4溶液中,能置换出铜,钠投入CuSO4溶液中不能置换出铜,判断钠与铁的金属活动性强弱C.酸性H2CO3<HCl,判断氯与碳的非金属活动性强弱D.Br2与I2分别与足量的H2反应的难易,判断溴与碘的非金属活动性强弱4、下列说法中,正确的是()A.核内质子数大于核外电子数的离子一定是非金属离子B.非金属阴离子的半径小于形成它的原子的半径C.金属阳离子的半径小于形成它的原子的半径D.原子序数的数值和这种原子的核外电子数相等5、已知元素砷(As)的原子序数为33,下列叙述正确的是( )A.砷元素的最高化合价为+3 B.砷元素是第四周期的主族元素C.砷原子的第3电子层含有18个电子 D.砷的氧化物的水溶液呈弱碱性6、据国外有关资料报道,在独居石(一种共生矿,化学成分为Ge、La、Nb…的磷酸盐)中,查明有尚未命名的116、124、126号元素,试判断116号元素位于周期表中的位置( ) A.第六周期第ⅥA族B.第七周期第ⅥA族C.第七周期第ⅧA族D.第八周期第ⅥA族7、下列各组顺序的排列不正确的是( )A.离子半径:F-〉Na+〉Mg2+〉Al3+ B.热稳定性:HCl〉H2S〉PH3C.酸性强弱:H2CO3〈H3PO4〈H2SO4 D.碱性强弱:NaOH〉KOH〉CsOH8、元素R的原子序数是15,下列关于R元素的说法中,错误的是()A.R的最高正化合价是+5 B.R是第2周期第ⅤA族的元素C.R的氢化物分子式是RH3D.R的最高价氧化物对应的水化物的水溶液呈酸性9、下列具有特殊性能的材料,由主族元素和副族元素组成的是()A.半导体材料砷化镓 B.吸氢材料镧镍合金C.透明陶瓷材料硒化锌D.新型纳米材料氮化镓10、有A、B、C、D四种元素,它们的原子序数依次增大,由B、C、D形成的离子具有相同的电子层结构。

初中化学元素周期表练习题
第一题
根据元素周期表的排列方式,回答以下问题:
1. 元素周期表是按照什么顺序排列的?
2. 元素周期表中最后一个元素是哪个?
3. 元素周期表中第一个元素是哪个?
第二题
选择题:
1. 元素周期表中水平行被称为什么?
a) 族
b) 周期
c) 阶段
2. 下列元素中,哪个是金属元素?
a) 氯
b) 硫
c) 钠
3. 下面有关元素周期表的说法中,哪个是错误的?
a) 元素周期表中,元素按照原子序数从小到大排列。
b) 元素周期表中,同一族的元素具有相似的化学性质。
c) 元素周期表中,同一周期的元素具有相似的原子半径。
4. 元素周期表中,第一周期有几个元素?
a) 7
b) 8
c) 9
第三题
根据元素周期表中元素的位置,填写以下表格:
第四题
解释以下概念:
1. 元素周期表中的周期是指什么?
2. 元素周期表中的族是指什么?
3. 元素周期表中,原子序数是什么意思?
以上是初中化学元素周期表练习题,希望能帮助你巩固对元素周期表的理解。
化学周练(8)
1.某元素原子的原子核外有三个电子层,最外层电子数是4,该原子核内的质子数是()
A.14B.15
C.16 D.17
2.(2011年中山高一检测)我国的纳米基础研究能力已跻身于世界前列,曾制得一种合成纳米材料,其化学式为RN。
已知该化合物中的R n+核外有28个电子。
则R元素位于元素周期表的()
A.第三周期第ⅤA族B.第四周期第ⅢA族
C.第五周期第ⅢA族D.第四周期第ⅤA族
3.下列说法正确的是()
A.碱性:LiOH>NaOH>KOH>RbOH
B.金属性:Rb>K>Na>Li
C.和酸反应时Fe能失2e-,Na失1e-,所以Fe的金属性强于Na
D.Rb不易与水反应放出H2
4.(2011年长沙高一检测)下列各表中的数字代表的是元素的原子序数。
表中数字所对应的元素与它们在周期表中的位置相符的是()
5.下列四种演示金属钾与水反应的实验装置,正确的是()
6.(2011年佛山高一检测)关于锂的结构和性质的判断,错误的是()
(a)与水反应比钠剧烈;(b)它的原子半径比钠小;(c)它的氧化物暴露于空气中易吸收二氧化碳;(d)它的阳离子的最外层电子数和钠的相同;(e)它是还原剂
A.只有(a) B.(c)和(e)
C.(b)和(d) D.(a)和(d)
7.A、B、C、D为短周期元素,在周期表中所处的位置如图所示,A、C两元素的原子核外电子数之和等于B元素原子的质子数。
(1)写出A元素的名称:________。
(2)B位于周期表中第________周期,第________族。
(3)C的原子结构示意图为________。
(4)D的单质与水反应的化学方程式为
________________________________________________________________________。
8.甲元素的原子序数是19;乙元素的原子核外有两个电子层,最外电子层上有6个电子;丙元素是元素周期表第ⅠA族中金属性最弱的碱金属元素。
由此推断:
(1)甲元素在周期表中位于第________周期;乙元素在周期表中位于第________族;丙元素的名称为________。
(2)甲的单质与水反应的离子方程式为
________________________________________________________________________。
乙单质与丙单质反应的化学方程式为
________________________________________________________________________。