初中化学酸碱盐溶液的导电性PPT课件
- 格式:ppt
- 大小:423.00 KB
- 文档页数:11

《化学《酸碱盐溶液导电性》ppt》xx年xx月xx日•引言•酸碱盐溶液导电性概述•酸碱盐溶液导电性的物理基础•酸碱盐溶液导电性的影响因素•酸碱盐溶液导电性的实际应用•研究酸碱盐溶液导电性的实验方案•结论与展望目录01引言酸碱盐溶液导电性是化学学科中重要的概念之一涉及电化学、物质性质等多个方面为后续学习电池、电解等知识点打下基础课程背景目的和意义提高学生对于化学学科的兴趣和热情为其他化学知识点的学习提供铺垫帮助学生理解酸碱盐溶液的导电原理和应用内容概述主要介绍酸碱盐溶液的导电性溶液中离子运动和导电的关系溶液导电能力的定量指标02酸碱盐溶液导电性概述物体由于内部自由电子的移动而具有传导电流的能力,不同物体导电能力不同。
物体传导电流的能力物质的导电能力由其内部自由电子的数量和运动状态决定。
决定导电性的因素导电性的定义溶液中离子存在酸碱盐溶液中存在可以自由移动的离子,这些离子在电场作用下可以定向移动,形成电流。
离子导电机制离子在电场作用下,正负电荷分离,产生定向移动,形成电流,实现溶液导电。
溶液导电的原因溶液中离子溶解酸碱盐溶解于水后,形成可以自由移动的离子。
离子在电场下的定向移动在外部电场作用下,溶液中离子发生定向移动,形成电流,实现酸碱盐溶液的导电。
酸碱盐溶液的导电过程03酸碱盐溶液导电性的物理基础在给定电场作用下,金属电极上的正负离子所具有的化学能电极电势描述了电极电势与溶液中离子浓度之间的关系,以及温度对电极电势的影响能斯特方程电极电势和能斯特方程离子扩散在浓度差的作用下,溶液中的离子从高浓度区域向低浓度区域移动的过程电导率衡量溶液导电能力的物理量,与溶液中离子浓度、离子迁移速率以及溶液温度等因素有关离子扩散和电导率电导衡量溶液导电能力的物理量,等于溶液电阻的倒数电导率与电导的关系在一定的温度和压力条件下,溶液的电导率越大,其电导也越大电导与电导率的关系04酸碱盐溶液导电性的影响因素酸碱盐溶液的导电性随着离子浓度的增加而增加。
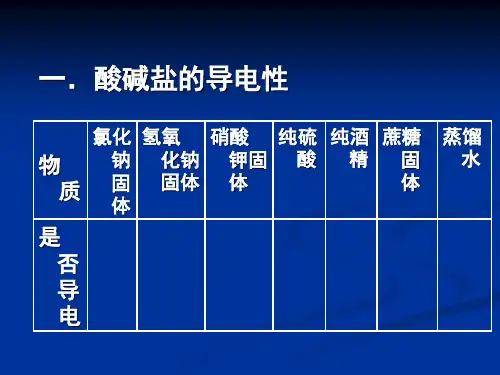



同样,氢氧化钠、氢氧化钾和氢氧化钡的溶液也能够导电,说明在水溶液中电离出能够自由移动的离子。
电离方程式: KOH = K+ + OH- Ba(OH2 = Ba2+ + 2 OHNaOH = Na+ + OH- 电离时生成的阴离子全部是氢氧根离子的化合物叫做碱。
全部
同样,碳酸钠、硫酸钾和氯化钡的溶液也能够导电,说明在水溶液中电离出能够自由移动的离子。
电离方程式: Na2CO3 = 2Na+ + CO3- MgSO4 = Ba2+ +
2OHBaCl2 = Ba+ + 2Cl- 电离时生成金属离子和酸根离子的化合物叫做盐。
通过对酸、碱、盐电离出离子的特点,你判断一下 NaHSO4、Cu2(OH2CO3应该属于哪一类化合物?
离子化合物:物质结构中含有离子,如:碱、盐等。
内因电离共价化合物:分子中共用电子对偏移程度较大,如:酸等。
外因:溶于水后,在水分子作用下电离。
溶液的导电性可用下式表示:酸碱盐外电场作用定向移动溶于水化合物自由移动的离子电离导电形成电流酸:HnR=nH++Rn- 碱:M(OHn= Mn+ + nOH-。




