菌落总数测定原始记录(确定版)
- 格式:doc
- 大小:23.50 KB
- 文档页数:2

X X X X检测有限公司
菌落总数与大肠菌群检验原始记录
主检:年月日校核:年月日
XXXX检测有限公司
菌落总数和大肠菌群检测原始记录
主检:年月日校核:年月日
XXXX检测有限公司
水质微生物检验原始记录
主检:年月日校核:年月日
XXXX检测有限公司
乳酸菌与大肠菌群检测记录
主检:年月日校核:年月日
XXXX检测有限公司
致病菌检验原始记录
主检:年月日校核:年月日
XXXX检测有限公司
霉菌和酵母菌检验原始记录
共页第页
培养温度:28±1℃培养时间:年月日时--- 年月日时:
菌落计数:
培养温度:28±1℃培养时间:年月日时--- 年月日时
主检:年月日校核:年月日
XXXX检测有限公司
商业无菌检验原始记录
共页第页
主检:日期:校核:日期:。
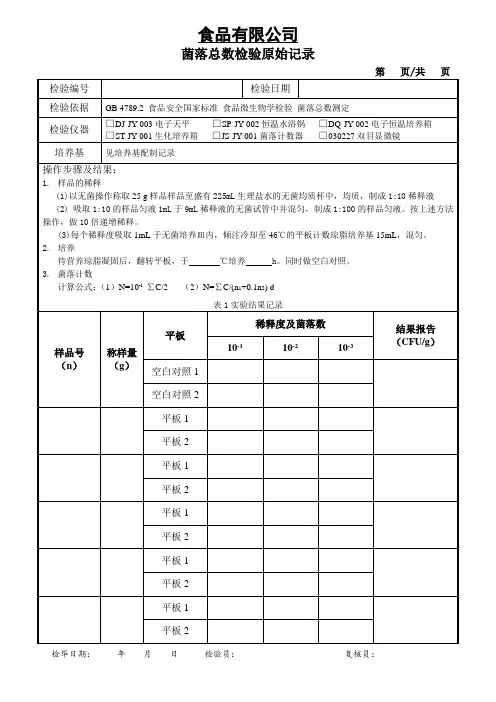
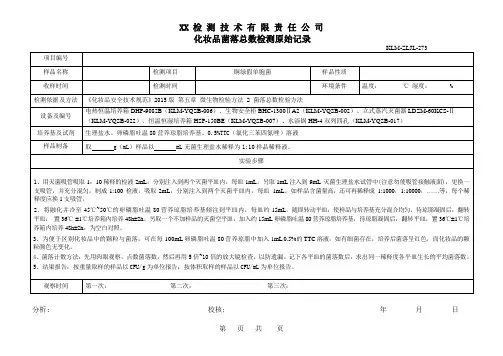

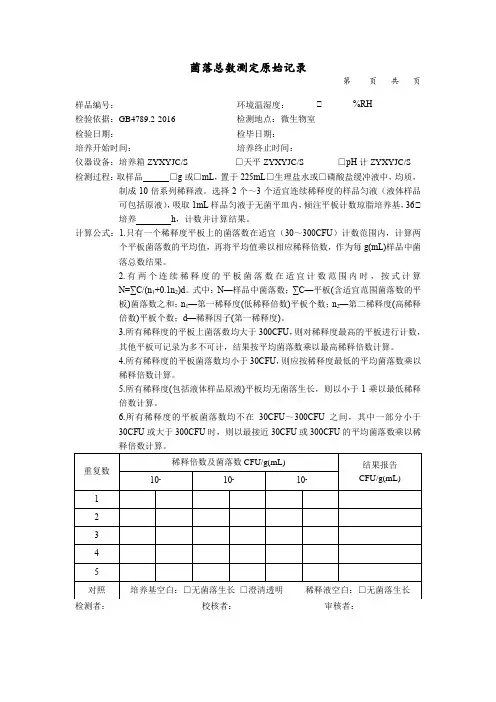
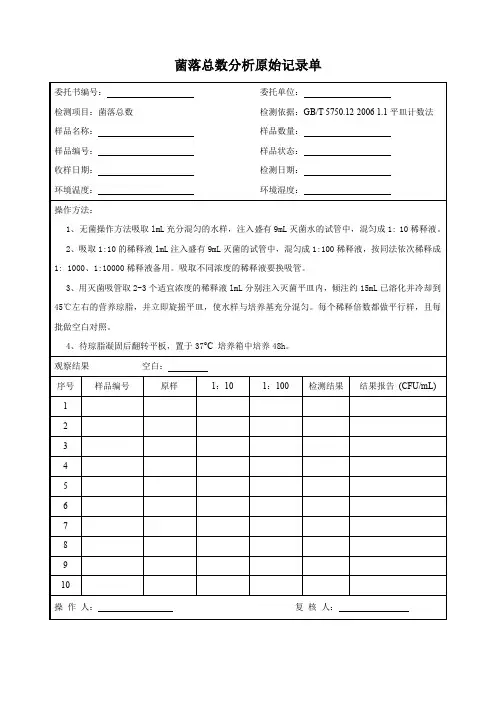
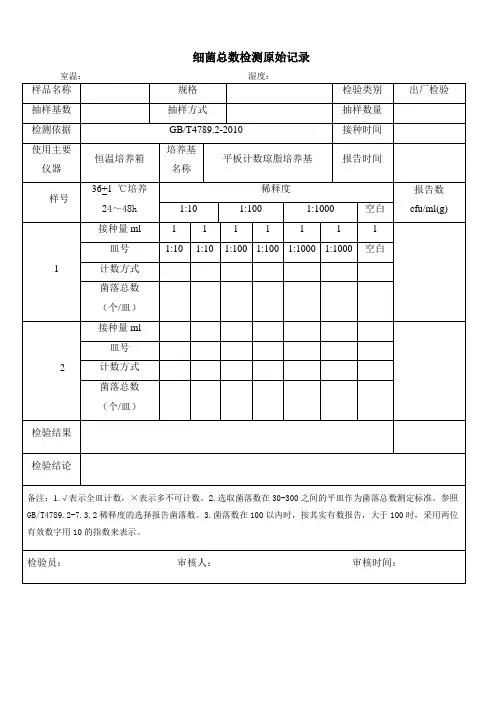
菌落总数测定原始记录第页共页样品编号:环境温湿度:℃ %RH检验依据:GB4789.2-2016 检测地点:微生物室检验日期:检毕日期:培养开始时间:培养终止时间:仪器设备:培养箱ZYXYJC/S- □天平ZYXYJC/S- □pH计ZYXYJC/S- 检测过程:取样品□g或□mL,置于225mL□生理盐水或□磷酸盐缓冲液中,均质,制成10倍系列稀释液。
选择2个~3个适宜连续稀释度的样品匀液(液体样品可包括原液),吸取1mL样品匀液于无菌平皿内,倾注平板计数琼脂培养基,36℃培养h,计数并计算结果。
计算公式:1.只有一个稀释度平板上的菌落数在适宜(30~300CFU)计数范围内,计算两个平板菌落数的平均值,再将平均值乘以相应稀释倍数,作为每g(mL)样品中菌落总数结果。
2.有两个连续稀释度的平板菌落数在适宜计数范围内时,按式计算N=∑C/(n1+0.1n2)d。
式中:N—样品中菌落数;∑C—平板(含适宜范围菌落数的平板)菌落数之和;n1—第一稀释度(低稀释倍数)平板个数;n2—第二稀释度(高稀释倍数)平板个数;d—稀释因子(第一稀释度)。
3.所有稀释度的平板上菌落数均大于300CFU,则对稀释度最高的平板进行计数,其他平板可记录为多不可计,结果按平均菌落数乘以最高稀释倍数计算。
4.所有稀释度的平板菌落数均小于30CFU,则应按稀释度最低的平均菌落数乘以稀释倍数计算。
5.所有稀释度(包括液体样品原液)平板均无菌落生长,则以小于1乘以最低稀释倍数计算。
6.所有稀释度的平板菌落数均不在30CFU~300CFU之间,其中一部分小于30CFU或大于300CFU时,则以最接近30CFU或300CFU的平均菌落数乘以稀释倍数计算。
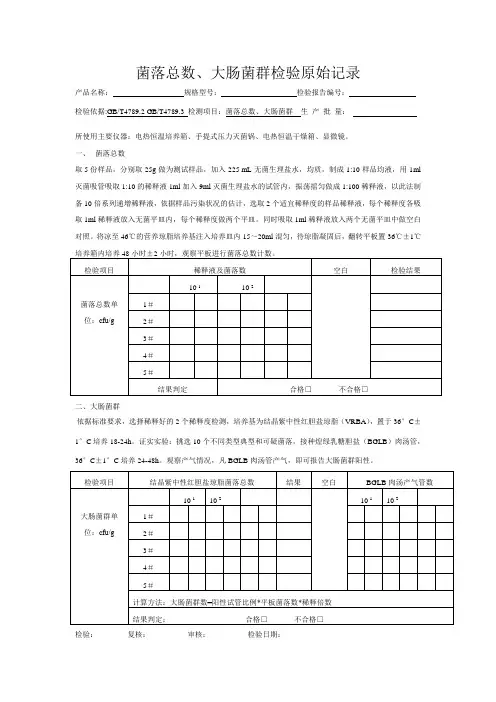
菌落总数、大肠菌群检验原始记录
产品名称:规格型号:检验报告编号:
检验依据:GB/T4789.2 GB/T4789.3 检测项目:菌落总数、大肠菌群生产批量:
所使用主要仪器:电热恒温培养箱、手提式压力灭菌锅、电热恒温干燥箱、显微镜。
一、菌落总数
取 5 份样品,分别取25g做为测试样品,加入225 mL无菌生理盐水,均质,制成1:10样品均液,用1ml 灭菌吸管吸取1:10的稀释液1ml加入9ml灭菌生理盐水的试管内,振荡摇匀做成1:100稀释液,以此法制备10倍系列递增稀释液,依据样品污染状况的估计,选取2个适宜稀释度的样品稀释液,每个稀释度各吸取1ml稀释液放入无菌平皿内,每个稀释度做两个平皿。
同时吸取1ml稀释液放入两个无菌平皿中做空白对照。
将凉至46℃的营养琼脂培养基注入培养皿内15~20ml混匀,待琼脂凝固后,翻转平板置36℃±1℃
二、大肠菌群
依据标准要求,选择稀释好的2个稀释度检测,培养基为结晶紫中性红胆盐琼脂(VRBA),置于36°C±1°C培养18-24h。
证实实验:挑选10个不同类型典型和可疑菌落,接种煌绿乳糖胆盐(BGLB)肉汤管,36°C±1°C培养24-48h。
观察产气情况,凡BGLB肉汤管产气,即可报告大肠菌群阳性。
检验:复核:审核:检验日期:。
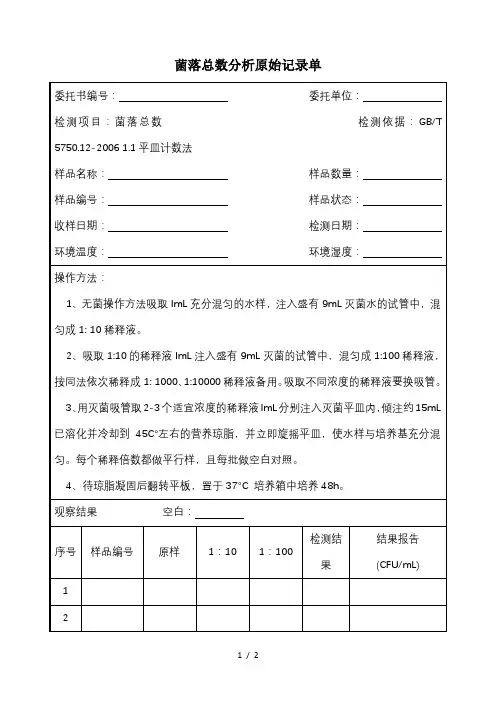
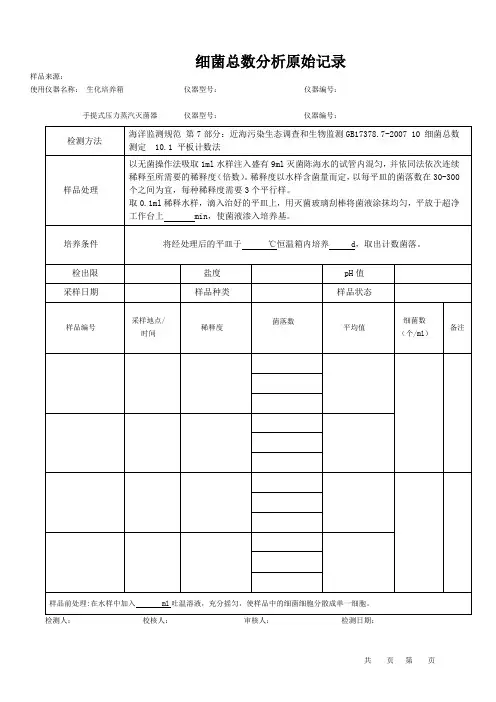
菌落总数测定原始记录事业部门:检测人员:样品名称:检验日期:环境温度:℃检验依据:GB 4789.2—20101.主要设备:天平培养箱2.检验过程:取样稀释□饭菜取样:称取25g样品置盛有225ml生理盐水的无菌均质容器内均质,为1:10样品匀液。
□空气样品:室内面积小于30㎡,在对角线里中外三点距墙1米位置取样室内面积大于30㎡,在四角和中间位置取样取样时将计数平板琼脂培养基打开平皿盖放置在工作台上,静置5分钟□手部取样:被检人五指并拢,用浸泡生理盐水的棉签,从指尖到指端涂搽两次,剪去手接触部分棉棒,将棉签放入10ML的生理盐水中□餐具接触面取样:用浸泡生理盐水的棉签,在被检测物体表面取25CM2的面积,涂抹两次使其充分接触,剪去手接触部分棉棒,将棉签放入10ML的生理盐水中倾注平板□空气样品:直接培养箱培养□接触面样品:用1mL无菌吸管吸取该样品匀液1mL,沿管壁缓慢注于盛有9mL生理盐水的无菌试管震荡或者使其混合均匀制成1:100样液;按上面程序更换吸管制作1:1000样液;分别将□1:10、□1:100、□1:1000样液吸取1ML于无菌平皿内,每个稀释度做两个平皿,分别取1ML空白稀释液作空白对比;及时将15-20ML 的46度平板计数培养基倾注平皿,并转动使其混合均匀;培养普通样品36℃±1℃培养48h±2h。
水品30℃±1℃培养72h±3h。
培养起止时间起:止:1:101:1001:1000空白12121212观察结果(个)计算结果报告3.计算方法:1)若只有一个稀释度平板上的菌落总数在适宜计数范围内,计算两个平板菌落总数的平均值,再将平均值乘以相应稀释倍数,作为每克(或毫升)中菌落总数结果。
2)若有两个连续稀释度的平板菌落总数在适宜计数范围内时,按式(Ⅰ)计算:N= ∑C/(n1+0.1n2)d (Ⅰ)式中:N——样品中菌落总数;∑C——平板(含适宜范围菌落总数的平板)菌落数之和;n1——第一个适宜稀释度平板数;n2——第二个适宜稀释度平板数;d——稀释因子(第一稀释度)。
菌落总数测定原始记录事部:品名称:境温度:℃人:日期:依据:GB 4789.2 — 20101.主要:天平培养箱2.程:□ 菜取:称取 25g 品置盛有225ml 生理水的无菌均容器内均,1:10品匀液。
□空气品:室内面小于 30 ㎡,在角里中外三点距 1 米位置取取稀注平板室内面大于30 ㎡,在四角和中位置取取将数平板脂培养基打开平皿盖放置在工作台上,静置 5 分□手部取:被人五指并,用浸泡生理水的棉,从指尖到指端涂搽两次,剪去手接触部分棉棒,将棉放入10ML 的生理水中□餐具接触面取:用浸泡生理水的棉,在被物体表面取25CM2 的面,涂抹两次使其充分接触,剪去手接触部分棉棒,将棉放入10ML 的生理水中□空气品:直接培养箱培养□接触面品:用 1mL 无菌吸管吸取品匀液1mL ,沿管壁慢注于盛有9mL 生理水的无菌管震或者使其混合均匀制成 1 :100 液;按上面程序更吸管制作1:1000 液;分将□1 :10、□1 :100 、□1: 1000 液吸取1ML 于无菌平皿内,每个稀度做两个平皿,分取1ML 空白稀液作空白比;及将15-20ML的46度平培养板数培养基注平皿,并使其混合均匀;普通品36 ℃±1 ℃培养48h ±2h 。
水品30℃±1℃培养起止培养 72h ±3h 。
起:止:1 : 10 1: 100 1:1000 空白1 2 1 2 1 2 1 2察果(个)算果告3.算方法:1 )若只有一个稀度平板上的菌落数在适宜数范内,算两个平板菌落数的平均,平均乘以相稀倍数,作每克(或毫升)中菌落数果。
2 )若有两个稀度的平板菌落数在适宜数范内,按式(Ⅰ)算:N= ∑C/(n 1+0.1n 2)d⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯(Ⅰ)再将式中:N——样品中菌落总数;∑C——平板(含适宜范围菌落总数的平板)菌落数之和;n 1——第一个适宜稀释度平板数;n 2——第二个适宜稀释度平板数;d ——稀释因子(第一稀释度)。
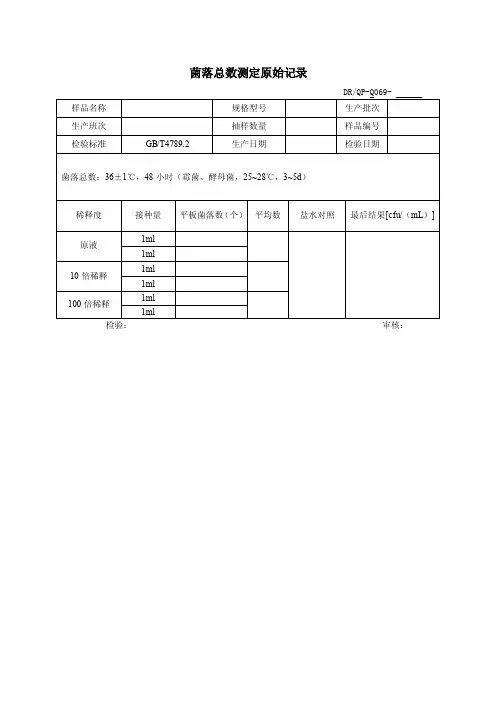
菌落总数测定原始记录
事业部门:检测人员:
样品名称:检验日期:
环境温度:℃检验依据:GB —2010 1.主要设备:天平培养箱
3.计算方法:
1)若只有一个稀释度平板上的菌落总数在适宜计数范围内,计算两个平板菌落总数的平均值,再将平均值乘以相应稀释倍数,作为每克(或毫升)中菌落总数结果。
2)若有两个连续稀释度的平板菌落总数在适宜计数范围内时,按式(Ⅰ)计算:
N= ∑C/(n1+d (Ⅰ)
式中:
N——样品中菌落总数;
∑C——平板(含适宜范围菌落总数的平板)菌落数之和;
n1——第一个适宜稀释度平板数;
n2——第二个适宜稀释度平板数;
d——稀释因子(第一稀释度)。
审核:。