ph缓冲溶液的配制方法
- 格式:doc
- 大小:108.50 KB
- 文档页数:3

中国PH计校正溶液配置的标准方法一、引言:根据目前市场的应用情况看来,中国即我国国内使用的PH计校正的缓冲溶液有三种,即标称pH4 ,pH7 和pH9的三种缓冲溶液,分别学名为如下,笔者根据多项资料整理可得,为的是您能方便快速弄明白这些问题,详情:1)pH4:0.05M 邻苯二甲酸氢钾溶液;2)pH7:0.025M 磷酸二氢钾和磷酸氢二钠混合盐溶液;3)pH9:0.01M 硼砂溶液;接下来介绍以上3种溶液的主要配置简单方法。
二、PH计校正溶液配置的标准方法1)pH4,邻苯二甲酸氢钾标准缓冲液:精密称取在115±5℃干燥2~3小时的邻苯二甲酸氢钾[KHC8H4O4]10.12g,加水使溶解并稀释至1000ml。
2)pH7,磷酸盐标准缓冲液(pH7.4):精密称取在115±5℃干燥2~3小时的无水磷酸氢二钠4.303g与磷酸二氢钾1.179g,加水使溶解并稀释至1000ml。
另补充:磷酸盐标准缓冲液(pH6.8) 精密称取在115±5℃干燥2~3小时的无水磷酸氢二钠3.533g与磷酸二氢钾3.387g,加水使溶解并稀释至1000ml。
3)pH9,硼砂标准缓冲液:精密称取硼砂[Na2B4O7·10H2O]3.80g(注意:避免风化),加水使溶解并稀释至1000ml,置聚乙烯塑料瓶中,密塞,避免与空气中二氧化碳接触。
总结:从现在使用PH计来看,中国境内即国产的PH计或者是酸度计,它的校正缓冲液拥有的情况有两种:1)即标准溶液是可以在市场上买到的,一般是在聚乙烯瓶中密闭保存的。
在室温条件下标准溶液一般以保存1~2个月为宜,当发现有浑浊、发霉或沉淀现象时,不能继续使用。
在4℃冰箱内存放,且用过的标准溶液不允许再倒回。
2)还可以自己买缓冲剂回去配置得。
但一般厂家发货时,由于国家规定发货时有的不准有液体或药物存在,所以只能是带有的是干燥的PH缓冲剂,客户使用时需要自己配置,只要使其溶解在预先煮沸15~30分钟的去离子水中,适当冲洗试剂袋中残留的试剂。

标准缓冲溶液(均用pH标准缓冲物质配制)1.1 苯二甲酸氢钾标准缓冲溶液:c(KHC8H4O4)=0.05 mol/L(25℃时,pHs=4.003)。
苯二甲酸氢钾的pH标准缓冲物质,有小塑料袋和瓶装两种,配制方法如下:a)袋装配制法:在250 mL(或500 mL)量瓶中(根据袋中标准缓冲物质量,选择量瓶大小),按袋上的说明配制成所需的浓度。
保存于聚乙烯瓶中。
b)瓶装配制法:称取5.10 g苯二甲酸氢钾(KHC8H4O4预先在115℃±5℃,烘2~3 h,于干燥器中冷却),溶于水并稀释至500 mL,混匀。
保存于聚乙烯瓶中。
1.2 0.025 mol/L磷酸二氢钾(KH2PO4)和0.025 mol/L磷酸氢二钠(Na2HPO4)混合标准缓冲溶液(25℃时,pHs=6.864):磷酸二氢钾和磷酸氢二钠的pH标准缓冲物质,有小塑料袋装(混合磷酸盐)和瓶装(两种pH标准缓冲物质分别包装)两种。
配制方法如下:a)袋装配制法:在量瓶(根据袋上说明确定量瓶大小)中按袋上说明配制成所需浓度后,保存于聚乙烯瓶中。
b)瓶装配制法:迅速称取3.40 g磷酸二氢钾(KH2PO4)和3.55 g磷酸氢二钠(Na2HPO4)(均预先在115±5℃烘2~3 h,于干燥器中冷却)溶于蒸馏水,转入1 000 mL量瓶中,加水至标线,混匀。
1.3 0.008 695 mol/L磷酸二氢钾(KH2PO4)和0.030 43 mol/L磷酸氢二钠(Na2HPO4)标准混合缓冲溶液(25℃时,pH=7.413):磷酸二氢钾和磷酸氢二钠两种pH标准缓冲物质分别用瓶包装,配制方法如下:迅速称取1.18 g磷酸二氢钾和4.31 g磷酸氢二钠(均预先在115℃±5℃烘2~3 h,于干燥器中冷却),溶于水,全量移入1 000 mL量瓶中,加水至标线,混匀。
保存于聚乙烯瓶中。
1.4 硼砂标准缓中溶液:c(Na2B4O7·10H2O)=0.010 mol/L(25℃时,pHs=9.182)。

ph缓冲溶液的配制方法PH缓冲溶液是指在一定范围内,具有缓冲pH值的溶液,适用于化学、生物、医药等各个领域的实验和应用。
在实验中,通常需要制备一定浓度和pH值的缓冲溶液,以保证实验结果的准确性和可重复性。
本文将介绍几种常见的缓冲溶液配制方法。
一、磷酸缓冲液(PBS)磷酸缓冲液是一种常用的生物化学实验缓冲液,可以用于细胞培养、酶活性测定、免疫学实验等等。
其配制方法如下:1. 准备250ml坐标瓶,称取1.37g Na2HPO4·12H2O和0.26g KH2PO4。
3. 将两个溶液混合,加入NaCl使溶液最终重量达到250g,调节pH值至7.4-7.6,如果pH值过低,可加入1M NaOH调节,反之加入1M HCl。
二、三氯醋酸缓冲液(TCA)三氯醋酸缓冲液是一种酸性缓冲液,适用于蛋白质的沉淀和提取等实验。
其配制方法如下:1. 准备250ml坐标瓶,在其中加入11.9g三氯乙酸,加入去离子水至250ml。
2. 调节溶液pH值至2.0-2.5,可使用无水HCl或NaOH来调节pH值。
3. 再加入去离子水,使溶液最终体积达到500ml,并根据需要添加NaCl和KCl等。
五、TRIS缓冲液TRIS缓冲液是一种常用的生化和细胞学实验用缓冲液,其缓冲范围在7.0~9.2之间。
其配制方法如下:1. 准备500ml坐标瓶,称取12.11g Tris-Base。
3. 在室温下缓慢加入0.1M HCl溶液,同时使用pH计监测溶液pH值,当pH值达到所需值时停止加入。
4. 将溶液体积补至500ml,并调节pH值。
可根据实验需要调节缓冲液中的NaCl或其他化学物质的浓度。
以上就是几种常见缓冲溶液的配制方法,需要注意的是在配制过程中,一定要严格按照实验要求和操作规程进行,以获得准确的实验结果。
同时,制备的缓冲液要遵循使用前检测pH值、滤过消毒等规定操作,以保证实验的可重复性和安全性。
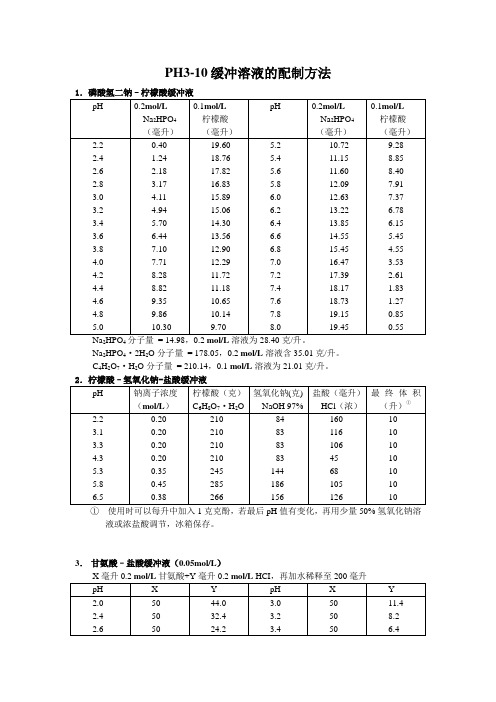
PH3-10缓冲溶液的配制方法Na 2HPO 4分子量 = 14.98,0.2 mol/L 溶液为28.40克/升。
Na 2HPO 4·2H 2O 分子量 = 178.05,0.2 mol/L 溶液含35.01克/升。
C 4H 2O 7·H 2O 分子量 = 210.14,0.1 mol/L 溶液为21.01克/升。
① 使用时可以每升中加入1克克酚,若最后pH 值有变化,再用少量50% 氢氧化钠溶液或浓盐酸调节,冰箱保存。
3. 甘氨酸–盐酸缓冲液(0.05mol/L )4.邻苯二甲酸–盐酸缓冲液(0.05 mol/L)邻苯二甲酸氢钾分子量= 204.23,0.2 mol/L邻苯二甲酸氢溶液含40.85克/升柠檬酸C6H8O7·H2O:分子量210.14,0.1 mol/L溶液为21.01克/升。
柠檬酸钠Na3 C6H5O7·2H2O:分子量294.12,0.1 mol/L溶液为29.41克/升。
柠檬酸C6H8O7·H2O: 2.1g柠檬酸钠Na3 C6H5O7·2H2O: 2.94gH2O: 100 ml6.乙酸–乙酸钠缓冲液(0.2 mol/L)Na2Ac·3H2O分子量= 136.09,0.2 mol/L溶液为27.22克/升。
7.磷酸盐缓冲液Na 2HPO 4·2H 2O 分子量 = 178.05,0.2 mol/L 溶液为85.61克/升。
Na 2HPO 4·12H 2O 分子量 = 358.22,0.2 mol/L 溶液为71.64克/升。
Na 2HPO 4·2H 2O 分子量 = 156.03,0.2 mol/L 溶液为31.21克/升。
Na 2HPO 4·2H 2O 分子量 = 178.05,1/15M 溶液为11.876克/升。
KH 2PO 4分子量 = 136.09,1/15M 溶液为9.078克/升。

各种缓冲液配制方法不同缓冲液的缓冲范围pH缓冲液是化学实验室中常用的一种试剂,可以帮助维持溶液的酸碱度。
下面介绍三种常用缓冲液的配制方法和缓冲范围。
一、甘氨酸-盐酸缓冲液(0.05 mol/L)配制方法:取X毫升0.2 mol/L甘氨酸和Y毫升0.2 mol/L 盐酸,加入适量的水稀释至200毫升。
缓冲范围:pH值在2.2至3.6之间,X和Y的取值见上表。
二、邻苯二甲酸-盐酸缓冲液(0.05 mol/L)配制方法:取X毫升0.2 mol/L邻苯二甲酸氢钾和Y毫升0.2 mol/L盐酸,加入适量的水稀释至20毫升。
缓冲范围:pH值在2.2至3.8之间,X和Y的取值见上表。
三、磷酸氢二钠-柠檬酸缓冲液配制方法:根据上表中的数据,取相应的0.2 mol/L和0.1 mol/L的Na2HPO4和柠檬酸,加入适量的水稀释至20毫升。
缓冲范围:pH值在2.2至8.0之间,具体取值见上表。
以上缓冲液的配制方法和缓冲范围可根据实验需要进行调整和改变。
在实验过程中,正确选择缓冲液可以提高实验的成功率和准确性。
以下是已经修改好的文章:柠檬酸的浓度可以用毫升表示,其浓度数据如下:9.28 mL8.85 mL8.40 mL7.91 mL7.37 mL6.78 mL6.15 mL5.45 mL4.55 mL3.53 mL2.61 mL1.83 mL1.27 mL0.85 mL0.55 mL对于Na2HPO4,其分子量为141.98,0.2 mol/L的溶液需要28.40 g/L。
而Na2HPO4·2H2O的分子量为178.05,0.2 mol/L的溶液需要35.61 g/L。
最后,Na2HPO4·12H2O的分子量为358.22,0.2 mol/L的溶液需要71.64 g/L。
对于C6H8O7·H2O,其分子量为210.14,0.1 mol/L的溶液需要21.01 g/L。
以下是柠檬酸-氢氧化钠-盐酸缓冲液的相关数据:pH: 2.2.3.1.3.3.4.3.5.3.5.8.6.5钠离子浓度(mol/L): 0.20.0.20.0.20.0.20.0.35.0.45.0.38柠檬酸(g) 氢氧化钠(g) 盐酸(mL)C6H8O7·H2O NaOH 97% HCl (浓)210 210 210210 245 285266 84 8383 144 186156 160 116106 45 68105 126最终体积(L):10使用时可以每升中加入1克酚。

我要配制ph=1.2和2的缓冲溶液(磷酸与磷酸盐),请问谁有配方?磷酸1级电离常数的PKa=2.18可以用H3PO4和磷酸二氢钠组成缓冲溶液。
以PH=2的缓冲溶液为例PH=PKa-lg([H3PO4]/[NaH2PO4])2=2.18-lg([H3PO4]/[NaH2PO4])[H3PO4]/[NaH2PO4]=3/2如果溶液的磷酸浓度为1摩尔/升,那么配制1升溶液需要磷酸的质量是1×3/5×98=58.8克需要磷酸二氢钠的质量是1×2/5×120=48克即称取磷酸58.5克,磷酸二氢钠48克,在充分搅拌的情况下,加水定容到一升即可。
PH=1.2的缓冲溶液,可依照上述计算方法计算出物料的质量。
【引用】常用pH缓冲溶液的配制和pH值2011-05-13 20:01:24| 分类:生物|字号订阅本文引用自DSC《常用pH缓冲溶液的配制和pH值》一、常用溶液的配制(文章来自:医药园() 整理:zfg)(一)溶液配制注意事项1.药品要有较好的质量试剂分为优级纯(保证试剂,Guaranteed reagent,G.R.)、分析试剂(Antalytical reagent,A.R.)化学纯(Chemical pure,C.P.)和实验试剂(Laboratory reagent,L.R.)等等。
工业用的化学试剂,杂质较多,只在个别情况下应用,如配洗液用的硫酸、配干燥剂的氯化钙等。
2.药品称量要精确。
3.配制试剂用水应用新鲜的去离子水或双蒸馏水,比电阻值在50万欧姆以上,pH在5.5~7.0之间才可应用,在组织培养等特殊用途时应注意此项要求,配制一般化验用溶液只要求用双蒸馏水或去离子水。
4.配好后的溶液,应立即除菌处理(如高压灭菌、抽滤或加抑菌物质),以防杂菌生长。
(二)0.067(1/15)Mol/L磷酸缓冲液1.1/15Mol/L磷酸二氢钾溶液的配制:称取磷酸二氢钾(KH2PO4,A.R.)9.08g,用蒸馏水溶解后,倾入1 000ml容量瓶内,再稀释至刻度(1 000ml)。
ph标准缓冲溶液配制PH标准缓冲溶液是实验室常用的一种溶液,它可以帮助实验人员在一定的PH范围内稳定样品的PH值。
在生物化学、分子生物学、生物工程等领域,PH标准缓冲溶液的配制和使用是非常重要的。
本文将介绍PH标准缓冲溶液的配制方法及注意事项,希望能为实验人员提供一些帮助。
首先,我们需要准备一些基本的试剂和设备,包括PH计、天平、磁力搅拌器、蒸馏水等。
在配制PH标准缓冲溶液之前,需要确保这些试剂和设备都是干净的,并且已经校准过。
接下来,我们需要选择合适的缓冲物质。
常用的缓冲物质有磷酸盐缓冲液、醋酸盐缓冲液、三羟甲基氨基甲烷缓冲液等。
选择缓冲物质时,需要考虑样品的PH范围和化学性质,选择最适合的缓冲物质。
在配制缓冲溶液时,需要按照一定的配比将缓冲物质和蒸馏水混合,直至溶解。
在这个过程中,可以使用PH计监测溶液的PH值,确保PH值在目标范围内。
如果PH值偏离目标范围,可以适当调整缓冲物质的用量,直至达到理想的PH值。
配制好的PH标准缓冲溶液需要进行标定。
标定的过程包括使用PH计测量溶液的PH值,并与已知PH值的标准溶液进行比较,调整PH值直至与标准溶液相符。
标定完成后,需要将溶液存储在密封的容器中,避免受到外界环境的影响。
在使用PH标准缓冲溶液时,需要注意以下几点。
首先,避免溶液受到污染,使用前需要确保溶液的清洁和透明度。
其次,在使用过程中需要严格按照实验方法操作,避免操作失误导致PH值的偏离。
最后,使用完毕后需要及时清洗使用的玻璃仪器,并将溶液妥善存放。
总的来说,PH标准缓冲溶液的配制和使用需要一定的技术和经验。
正确的配制方法和注意事项能够保证溶液的质量稳定性,为实验结果的准确性提供保障。
希望本文介绍的内容能够对实验人员有所帮助,谢谢阅读!。
ph=4的缓冲溶液配制方法缓冲溶液是一种能够维持溶液pH值相对稳定的溶液。
在实验室和许多生物学、化学和医学研究中,配制pH=4的缓冲溶液是非常常见的。
下面将介绍一种常见的方法来配制pH=4的缓冲溶液。
配制pH=4的缓冲溶液需要选择一个具有适当pKa值的酸和它的共轭碱,以便在溶液中维持所需的pH值。
常见的用于配制pH=4的缓冲溶液的酸包括柠檬酸、琥珀酸、乙酸等,这些酸具有适当的pKa值,使其能够在pH=4时处于酸性状态。
下面是一种用柠檬酸和柠檬酸钠配制pH=4缓冲溶液的方法:1.准备所需的实验器材和试剂,包括一定量的柠檬酸和柠檬酸钠,去离子水等。
2.准备一定体积的去离子水,将其加入一个干净的容器中。
3.使用天平称取所需量的柠檬酸。
根据所需浓度和溶液体积,确定所需的柠檬酸量。
4.将柠檬酸加入容器中的水中,并搅拌均匀。
保持搅拌直到溶液完全溶解。
5.使用天平称取所需量的柠檬酸钠。
根据所需浓度和溶液体积,确定所需的柠檬酸钠量。
6.将柠檬酸钠加入溶液中,并再次搅拌均匀。
保持搅拌直到溶液完全溶解。
7.使用pH计测量溶液的pH值。
如果溶液的pH值不是4,则需要调整。
8.调整溶液的pH值。
可以使用酸或碱来调整溶液的pH值。
根据具体情况,可添加少量的盐酸或氢氧化钠等来进行调整。
9.继续搅拌溶液,直到达到所需的pH=4。
10.使用pH计再次测量溶液的pH值,确保溶液的pH为4。
11.将溶液转移到干净的容器中,并用适当的密封方式保存。
以上是一种用柠檬酸和柠檬酸钠配制pH=4缓冲溶液的方法。
根据实验需要,还可以选择其它适当的酸和碱来调整和配制pH=4缓冲溶液。
缓冲溶液的配制和pH的测定
实验目的
1.了解缓冲溶液的配制方法。
2.学会使用酸度计测定溶液的pH。
实验原理
酸碱缓冲溶液一般是由浓度较大的弱酸及其共轭碱所组成,这类溶液不仅具有抗外加强酸强碱的作用,还有抗稀释的作用。
对于此类缓冲溶液,有以下公式:
pH=pKa+lg([B-]/[HB])
据此,可通过改变HB,B-的比例,配制成一定pH的缓冲溶液。
一般是先配制出大致所需的pH溶液,然后再测定其pH,再加酸或碱,使pH达到所需值。
实验步骤
1.配制NaAc-HAc,(CH2)6N4-HCl,NH3-NH4Cl缓冲溶液。
2.酸度计的校正。
3.缓冲溶液pH的测定。
常用pH缓冲液配置方法及注意事项常用pH缓冲溶液的配制和pH值序号溶液名称配制方法pH值1氯化钾-盐酸13.0 ml 0.2 mol/L HCl 与25.0 ml 0.2 mol/L KCl混合均匀后,加水稀释至100 ml1.72氨基乙酸-盐酸在500 ml 水中溶解氨基乙酸150 g,加480 ml浓盐酸,再加水稀释至1L2.33一氯乙酸-氢氧化钠在200 ml 水中溶解2 g 一氯乙酸后,加40 g NaOH,溶解完全后再加水稀释至1 L2.84邻苯二甲酸氢钾-盐酸把25.0 ml 0.2 mol/L的邻苯二甲酸氢钾溶液与6.0 ml0.1 mol/L HCl混合均匀,加水稀释至100 ml3.65邻苯二甲酸氢钾-氢氧化钠把25.0 ml 0.2 mol/L的邻苯二甲酸氢钾溶液与17.5ml 0.1 mol/L NaOH混合均匀,加水稀释至100 ml4.86六亚甲基四胺-盐酸在200 ml水中溶解六亚甲基四胺40 g,加浓HCl 10 ml,再加水稀释至1 L5.47磷酸二氢钾-氢氧化钠把25.0 ml 0.2 mol/L的磷酸二氢钾与23.6 ml 0.1mol/L NaOH混合均匀,加水稀释至100 ml6.88硼酸-氯化钾-氢氧化钠把25.0 ml 0.2 mol/L的硼酸-氯化钾与4.0 ml 0.1mol/L NaOH 混合均匀,加水稀释至100 ml8.09氯化铵-氨水把0.1 mol/L 氯化铵与0.1 mol/L 氨水以2:1比例混合均匀9.110硼酸-氯化钾-氢氧化钠把25.0 ml 0.2 mol/L 的硼酸-氯化钾与43.9 ml 0.1mol/L NaOH混合均匀,加水稀释至100 ml10.011氨基乙酸-氯化钠-氢氧化钠把 49.0 ml 0.1 mol/L 氨基乙酸-氯化钠与51.0 ml0.1 mol/L NaOH混合均匀11.612磷酸氢二钠-氢氧化钠把 50.0 ml 0.05 mol/L Na2HPO4与26.9 ml 0.1 mol/L NaOH 混合均匀,加水稀释至100 ml12.013氯化钾-氢氧化钠把 25.0 ml 0.2 mol/L KCl与66.0 ml 0.2 mol/L NaOH混合均匀,加水稀释至100 ml13.0一、常用溶液的配制(一)溶液配制注意事项1.药品要有较好的质量试剂分为优级纯(保证试剂,Guaranteed reagent,G.R.)、分析试剂(Antalytical reagent,A.R.)化学纯(Chemical pure,C.P.)和实验试剂(Laboratory reagent,L.R.)等等。