上海高考有机化学反应方程式--word
- 格式:docx
- 大小:350.19 KB
- 文档页数:7

光照 光照 光照 光照 高温 CaO △ 催化剂 加热、加压催化剂 △ 催化剂高中有機化學方程式匯總1. CH 4 + Cl 2 CH 3Cl + HCl2. CH 3Cl + Cl 2 CH 2Cl 2 + HCl3. CH 2Cl + Cl 2 CHCl 3 + HCl4. CHCl 3 + Cl 2 CCl 4+ HCl5. CH 4 C +2H 26. C 16H 34 C 8H 18 + C 8H 167. CH 3COONa + NaOH CH 4↑+ Na 2CO 38. CH 2 = CH 2 + Br 2 CH 2Br —CH 2Br9. CH 2 = CH 22OH10. CH 2 = CH 23—CH 2Br 11. CH 2 = CH 2CH 3 12. nCH 2 = CH 2 ] n13. nCH 22-CH=CH-CH 2] n14. 2CH 23CHO15. CH ≡CH + Br 2 CHBr = CHBr16. CHBr = CHBr+ Br 2 CHBr 2-CHBr 217. CH ≡CH + HCl H 2C = CHCl18. nCH 2 = CH [ CH 2-CH ] nCl Cl19. CH ≡CH + H 2O CH 3CHO20. CaC 2 + 2H 2O CH ≡CH ↑+ Ca(OH)2+ Br 222. + HO 2 +H 2O 23. + HO 3H+H 2O催化剂△浓硫酸170℃浓硫酸140℃催化剂△24.+ 3H2-NO22O26. 3CH≡C H27. CH3CH2Br + H228. CH3CH229. CH3CH22O30. 2CH3CH2OH+2Na 2CH3CH2ONa + H2↑31. 2CH3CH2OH+O2 2CH3CHO + 2H2O32. CH3CH2OH CH2 = CH2↑+ H2O33.C2H5OH+C2H5OH C2H5OC2H5+H2O34. 2O35. 2O -+H3O+2337+3HBr38. CH339. 2CH340. CH34+2Ag↓+3NH3+H2O 41CH32O↓+2H2O42. 2CH3COOH+2Na 2CH3COONa+H2↑43.2CH3COOH+Na2CO32CH3COONa+H2O+CO2↑44. CH3COOH+NaHCO3 CH3COONa+H2O+CO2↑45. CH3COOH + NaOH CH3COONa + H2O浓硫酸△催化剂催化剂催化剂催化剂催化剂△催化剂加热、加压+ 浓硫酸△+ 2H2OO OC —CO OCH2-CH246. 2CH3COOH + Cu(OH)2 (CH3COO)2Cu + 2H2O47.CH3COOH+CH3CH2OH CH3COOCH2CH3 +H2O48. CH3COOCH2CH3+NaOH CH3COONa+CH3CH2OH49. nOHCH2CH2COO H→[ OCH2CH2C ] n +H2O50. C6H12O6 (s) + 6O2 (g)6CO2 (g) + 6H2O (l)51. C6H12O62CH3CH2OH + 2CO252. C12H22O11+H2O C6H12O6+ C6H12O6蔗糖葡萄糖果糖53. C12H22O11 + H2O2C6H12O6麦芽唐葡萄糖54. (C6H10O5)n + nH2O n C6H12O6淀粉葡萄糖55. (C6H10O5)n + nH2O n C6H12O6纤维素葡萄糖56.C17H33COO-CH2C17H35COO-CH2C17H33COO-CH +3H2 C17H35COO-CHC17H33COO-CH2C17H35COO-CH257. C17H35COO-CH2CH2-OHC17H35COO-CH +3NaOH3C17H35COONa+ CH-OHC17H35COO-CH2CH2-OH58. CH2OH COOHCH2OH COOH1.HClClCHClCH+−→−+324光HClClCHClClCH+−→−+2223光2.3.4.5.6.7.8.222Br CH CH CH CH +=-= 9.10.11.12.13.14.15.16.17. OH NH Ag CHO CHOH HOCH 2342)(2)(+O H NH Ag COONH CHOH HOCH 2344232)(++↓+−→−∆18.19.20.21.高中有机化学知识点总结1.需水浴加热的反应有:(1)、银镜反应(2)、乙酸乙酯的水解(3)苯的硝化(4)糖的水解(5)、酚醛树脂的制取(6)固体溶解度的测定凡是在不高于100℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。

高中有机化学反应方程式汇总
1. 烷烃的燃烧反应
烷烃是一类只含有碳和氢元素的有机化合物。
烷烃在氧气存在下燃烧时,产生二氧化碳和水。
以甲烷(CH₄)为例:
CH₄ + 2O₂ -> CO₂ + 2H₂O
2. 单宁酸与金属离子的反应
单宁酸是一类含有羟基和酚羟基的有机酸,能与多种金属离子发生反应。
以单宁酸与铁离子(Fe³⁺)为例:
Fe³⁺ + 3C₇H₅O₅⁻ -> Fe(C₇H₅O₅)₃
3. 醇的脱水反应
醇是一类含有羟基的有机化合物。
醇在加热条件下可以发生脱水反应,生成烯烃。
以乙醇(C₂H₅OH)为例:
C₂H₅OH -> C₂H₄ + H₂O
4. 羧酸与碱的中和反应
羧酸是一类含有羧基的有机酸,能与碱发生中和反应,生成相应的盐和水。
以乙酸(CH₃COOH)与氢氧化钠(NaOH)为例:
CH₃COOH + NaOH -> CH₃COONa + H₂O
5. 醛酮的氧化反应
醛酮是一类含有羰基的有机化合物。
醛酮在氧化剂作用下可以发生氧化反应,生成酸和水。
以乙醛(CH₃CHO)为例:
CH₃CHO + [O] -> CH₃COOH
以上是高中有机化学中常见的反应方程式的汇总。
这些方程式有助于理解有机化学反应的基本原理和机制。
请注意,以上反应方程式仅供参考,实际反应条件可能会有所不同。
使用时请参考相关化学教材和实验指导。

高中有机化学反应方程式总结
有机化学是研究碳元素连接和结构的化学分支。
在高中化学课程中,学生将研究许多有机化合物的反应和方程式。
本文将总结高中有机化学反应的一些常见方程式。
1. 烷烃的燃烧反应
烷烃是由碳和氢元素构成的有机化合物。
它们在氧气中燃烧时会产生二氧化碳和水。
烷烃的燃烧反应方程式如下:
烷烃 + 氧气→ 二氧化碳 + 水
2. 烷烃的卤代反应
烷烃可以与卤素反应,生成相应的卤代烷。
反应中发生的是氢原子被卤素原子取代。
烷烃的卤代反应方程式如下:
烷烃 + 卤素→ 卤代烷 + 氢卤酸
3. 醇的燃烧反应
醇是由羟基(-OH)官能团连接的碳链。
醇在氧气中燃烧时会产生二氧化碳和水。
醇的燃烧反应方程式如下:
醇 + 氧气→ 二氧化碳 + 水
4. 醇的酸催化剂裂解反应
醇可以在酸催化剂的作用下裂解为烯或烃。
反应中发生的是醇
分子中的羟基被酸催化剂取代。
醇的酸催化剂裂解反应方程式如下:醇 + 酸→ 烯或烃
5. 羧酸的酯化反应
羧酸与醇反应可以生成酯。
反应中发生的是羧酸中的羟基被醇
取代。
羧酸的酯化反应方程式如下:
羧酸 + 醇→ 酯 + 水
这是一些高中有机化学反应的方程式总结。
希望对你的研究有
所帮助!。

光照 光照 光照 光照高温CaO △ 催化剂加热、加压催化剂 催化剂 △催化剂 △催化剂催化剂△高中有機化學方程式匯總令狐采学1. CH4 + Cl2CH3Cl + HCl2. CH3Cl + Cl2 CH2Cl2 + HCl3. CH2Cl + Cl2 CHCl3 + HCl4. CHCl3 + Cl2 CCl4+ HCl5. CH4 C +2H26. C16H34 C8H18 + C8H167. CH3COONa + NaOH CH4↑+ Na2CO38. CH2 = CH2 + Br2 CH2Br —CH2Br9. CH2 = CH2 + H2O CH3CH2OH10. CH2 = CH2 + HBr CH3—CH2Br11. CH2 = CH2 + H2 CH3—CH3CH2 ] n13. nCH2=CH-CH=CH2[CH2-CH=CH-CH2] n14. 2CH2 = CH2 + O2 2CH3CHO15. CH ≡CH + Br2 CHBr = CHBr16. CHBr = CHBr+ Br2CHBr2-CHBr2催化剂NaOHH 2O醇△催化剂△ 浓硫酸 170℃浓硫酸140℃ 催化剂 △ 17. CH≡CH + HCl H2C = CHCl18. nCH2 = CH [ CH2-CH ] nCl Cl19. CH≡CH + H2OCH3CHO 20. CaC2 + 2H2OBr + HBr+ HO NO2 +H2O+ HO - SO3H+H2O24.+ 3H2- +3H2O26. 3CH≡CH→27. CH3CH2Br + H2O CH3CH2OH + HBr28. CH3CH2Br + NaOH CH3CH2OH + NaBr29. CH3CH2Br+ NaOH CH2 = CH2 + NaBr +H2O30. 2CH3CH2OH+2Na 2CH3CH2ONa + H2↑31. 2CH3CH2OH+O2 2CH3CHO + 2H2O32. CH3CH2OH CH2 = CH2↑+ H2OBr催化剂△催化剂△△△33.C2H5OH+C2H5OH C2H5OC2H5+H2O34. OH+NaOH ONa+H2OOH+H2O O-+H3O+OH+ NaHCO33738. CH3CHO + H2 CH3CH2OH39. 2CH3CHO + O2 2CH3COOH40. CH3CHO+2Ag(NH3)2OH CH3COONH4+2Ag↓+3NH3+H2O41CH3CHO+2Cu(OH)2CH3COOH+Cu2O↓+2H2O42. 2CH3COOH+2Na 2CH3COONa+H2↑43.2CH3COOH+Na2CO3 2CH3COONa+H2O+CO2↑44. CH3COOH+NaHCO3 CH3COONa+H2O+CO2↑45. CH3COOH + NaOH CH3COONa + H2O46. 2CH3COOH + Cu(OH)2(CH3COO)2Cu + 2H2OCH3COOCH2CH3 +H2O催化剂催化剂催化剂催化剂催化剂△催化剂加热、加压+48. CH3COOCH2CH3+NaOH CH3COONa+CH3CH2OH49. nOHCH2CH2COOH→ [ OCH2CH2C ] n +H2O50. C6H12O6 (s) + 6O2 (g) 6CO2 (g) + 6H2O (l)51. C6H12O6 2CH3CH2OH + 2CO252. C12H22O11+H2OC6H12O6+ C6H12O6蔗糖葡萄糖果糖53. C12H22O11 + H2O2C6H12O6麦芽唐葡萄糖54. (C6H10O5)n + nH2O n C6H12O6淀粉葡萄糖55. (C6H10O5)n + nH2O n C6H12O6纤维素葡萄糖56.C17H33COO-CH2 C17H35COO-CH2C17H33COO-CH +3H2 C17H35COO-CHC17H33COO-CH2 C17H35COO-CH2 57. C17H35COO-CH2 CH2-OHC17H35COO-CH +3NaOH3C17H35COONa+ CH-OHCH2-OH 58. CH2OHCH2OH1.HClClCHClCH+−→−+324光2.3.4.5.6.7.8.9.10.11.12.13.14.15.16.17.18.19.20.21.高中有机化学知识点总结1.需水浴加热的反应有:(1)、银镜反应(2)、乙酸乙酯的水解(3)苯的硝化(4)糖的水解(5)、酚醛树脂的制取(6)固体溶解度的测定凡是在不高于100℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。
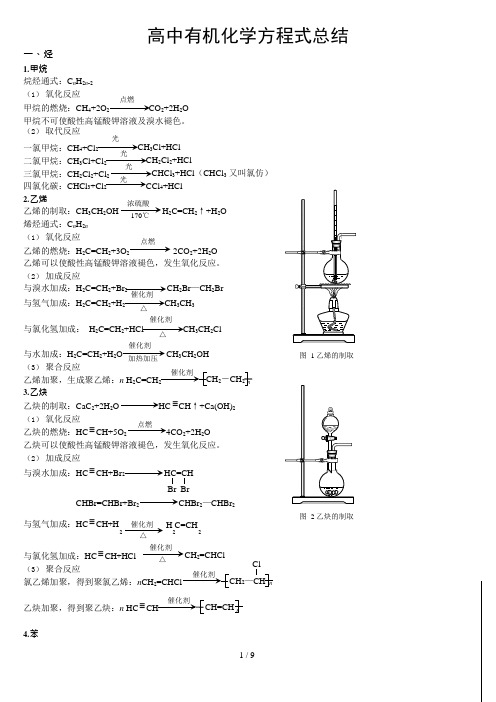
一、烃1. 甲烷烷烃通式:C n H 2n -2 (1) 氧化反应高中有机化学方程式总结点燃 甲烷的燃烧:CH 4+2O 2 CO 2+2H 2O 甲烷不可使酸性高锰酸钾溶液及溴水褪色。
(2) 取代反应 光一氯甲烷:CH 4+Cl 2 光二氯甲烷:CH 3Cl+Cl 2 光三氯甲烷:CH 2Cl 2+Cl 2 光CH 3Cl+HClCH 2Cl 2+HClCHCl 3+HCl (CHCl 3 又叫氯仿) 四氯化碳:CHCl 3+Cl 2CCl 4+HCl2. 乙烯乙烯的制取:CH 3CH 2OH 烯烃通式:C n H 2n (1) 氧化反应浓硫酸170℃点燃H 2C=CH 2↑+H 2O乙烯的燃烧:H 2C=CH 2+3O 2 2CO 2+2H 2O 乙烯可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2) 加成反应与溴水加成:H 2C=CH 2+Br 2 CH 2Br —CH 2Br催化剂 与氢气加成:H 2C=CH 2+H 2 △CH 3CH 3催化剂与氯化氢加成: H 2C=CH 2+HCl△CH 3CH 2Cl催化剂与水加成:H 2C=CH 2+H 2O (3) 聚合反应加热加压 CH 3CH 2OH 图 1 乙烯的制取乙烯加聚,生成聚乙烯:n H 2C=CH 23. 乙炔CH 2-CH 2 n 乙炔的制取:CaC 2+2H 2O HC ≡ C H ↑+Ca(OH)2 (1) 氧化反应 点燃乙炔的燃烧:HC ≡ CH+5O 2 4CO 2+2H 2O 乙炔可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2) 加成反应 与溴水加成:HC ≡ CH+Br 2HC=CH Br BrCHBr=CHBr+Br 2CHBr 2—CHBr 2图 2 乙炔的制取与氢气加成:HC ≡ CH+H催化剂 H C=CH2与氯化氢加成:HC ≡ CH+HCl(3) 聚合反应△2催化剂 22=CHClCl 氯乙烯加聚,得到聚氯乙烯:n CH 2=CHCl2—CH乙炔加聚,得到聚乙炔:n HC ≡ CHCH=CH n4. 苯催化剂催化剂n催化剂苯的同系物通式:C n H 2n-6 (1) 氧化反应 点燃苯的燃烧:2C 6H 6+15O 2 12CO 2+6H 2O 苯不能使溴水和酸性高锰酸钾溶液褪色。

光照 光照 光照 光照低温CaO △ 催化剂加热、加压 催化剂 催化剂 △催化剂 △ 催化剂 △高中有機化學方程式匯總之老阳三干创作1. CH4 + Cl2CH3Cl + HCl2. CH3Cl + Cl2 CH2Cl2 + HCl3. CH2Cl + Cl2 CHCl3 + HCl4. CHCl3 + Cl2 CCl4+ HCl5. CH4 C +2H26. C16H34 C8H18 + C8H167. CH3COONa + NaOH CH4↑+ Na2CO38. CH2 = CH2 + Br2 CH2Br —CH2Br9. CH2 = CH2 + H2O CH3CH2OH10. CH2 = CH2 + HBr CH3—CH2Br11. CH2 = CH2 + H2 CH3—CH3CH2 ] n13. nCH2=CH-CH=CH2[CH2-CH=CH-CH2] n15. CH≡CH + Br2 CHBr = CHBr16. CHBr = CHBr+ Br2CHBr2-CHBr217. CH≡CH + HCl H2C = CHCl18. nCH2 = CH [ CH2-CH ] nCl Cl催化剂NaOHH 2O醇 △催化剂 △ 浓硫酸 170℃浓硫酸140℃OH催化剂 △ 19. CH≡CH + H2O CH3CHO20. CaC2 + 2H2O CH≡CH↑+ Ca(OH)2-24.+ 3H2 -26. 3CH≡CH→27. CH3CH2Br + H2O CH3CH2OH + HBr28. CH3CH2Br + NaOH CH3CH2OH + NaBr29. CH3CH2Br+ NaOH CH2 = CH2 + NaBr +H2O30. 2CH3CH2OH+2Na 2CH3CH2ONa + H2↑31. 2CH3CH2OH+O2 2CH3CHO + 2H2O32. CH3CH2OH CH2 = CH2↑+ H2O 33.C2H5OH+C2H5OH C2H5OC2H5+H2O35. OH+H2O O -+H3O+△△催化剂 催化剂催化剂催化剂催化剂△3739. 2CH3CHO + O2 2CH3COOH40. CH3CHO+2Ag(NH3)2OH CH3COONH4+2Ag↓+3NH3+H2O41CH3CHO+2Cu(OH)2CH3COOH+Cu2O↓+2H2O42. 2CH3COOH+2Na 2CH3COONa+H2↑43.2CH3COOH+Na2CO3 2CH3COONa+H2O+CO2↑44. CH3COOH+NaHCO3 CH3COONa+H2O+CO2↑45. CH3COOH + NaOH CH3COONa + H2O46. 2CH3COOH + Cu(OH)2(CH3COO)2Cu + 2H2O48. CH3COOCH2CH3+NaOH CH3COONa+CH3CH2OH49. nOHCH2CH2COOH→ [ OCH2CH2C ] n +H2O50. C6H12O6 (s) + 6O2 (g) 6CO2 (g) + 6H2O (l)51. C6H12O6 2CH3CH2OH + 2CO252. C12H22O11+H2OC6H12O6+ C6H12O6蔗糖 葡萄糖 果糖53. C12H22O11 + H2O2C6H12O6麦芽唐葡萄糖54. (C6H10O5)n + nH2O n C6H12O6淀粉葡萄糖催化剂 加热、加压+ 55. (C6H10O5)n + nH2O n C6H12O6纤维素葡萄糖56.C17H33COO-CH2 C17H35COO-CH2 C17H33COO-CH +3H2 C17H35COO-CHC17H33COO-CH2 C17H35COO-CH257. C17H35COO-CH2 CH2-OHC17H35COO-CH +3NaOH3C17H35COONa+ CH-OH58. CH2OH COOH CH2OH COOH 1.HCl Cl CH Cl CH +−→−+324光2.3.4.5.6.7.8.9. 10.11.12.13.14.15.16.17.18.19.20.21.高中有机化学知识点总结1.需水浴加热的反响有:(1)、银镜反响(2)、乙酸乙酯的水解(3)苯的硝化(4)糖的水解(5)、酚醛树脂的制取(6)固体溶解度的测定但凡在不高于100℃的条件下反响,均可用水浴加热,其优点:温度变更平稳,不会大起大落,有利于反响的进行.2.需用温度计的实验有:(1)、实验室制乙烯(170℃)(2)、蒸馏(3)、固体溶解度的测定(4)、乙酸乙酯的水解(70-80℃)(5)、中和热的测定(6)制硝基苯(50-60℃)〔说明〕:(1)凡需要准确控制温度者均需用温度计.(2)注意温度计水银球的位置.3.能与Na反响的有机物有:醇、酚、羧酸等——凡含羟基的化合物.4.能产生银镜反响的物质有:醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖——凡含醛基的物质. 5.能使高锰酸钾酸性溶液褪色的物质有:(1)含有碳碳双键、碳碳叁键的烃和烃的衍生物、苯的同系物(2)含有羟基的化合物如醇和酚类物质(3)含有醛基的化合物(4)具有还原性的无机物(如SO2、FeSO4、KI、HCl、H2O2等)6.能使溴水褪色的物质有:(1)含有碳碳双键和碳碳叁键的烃和烃的衍生物(加成)(2)苯酚等酚类物质(取代)(3)含醛基物质(氧化)(4)碱性物质(如NaOH、Na2CO3)(氧化还原――歧化反响)(5)较强的无机还原剂(如SO2、KI、FeSO4等)(氧化)(6)有机溶剂(如苯和苯的同系物、四氯甲烷、汽油、已烷等,属于萃取,使水层褪色而有机层呈橙红色.)7.密度比水大的液体有机物有:溴乙烷、溴苯、硝基苯、四氯化碳等.8、密度比水小的液体有机物有:烃、大多数酯、一氯烷烃. 9.能产生水解反响的物质有卤代烃、酯(油脂)、二糖、多糖、蛋白质(肽)、盐.10.不溶于水的有机物有:烃、卤代烃、酯、淀粉、纤维素11.常温下为气体的有机物有:份子中含有碳原子数小于或等于4的烃(新戊烷例外)、一氯甲烷、甲醛.12.浓硫酸、加热条件下产生的反响有:苯及苯的同系物的硝化、磺化、醇的脱水反响、酯化反响、纤维素的水解13.能被氧化的物质有:含有碳碳双键或碳碳叁键的不饱和化合物(KMnO4)、苯的同系物、醇、醛、酚.大多数有机物都可以燃烧,燃烧都是被氧气氧化.14.显酸性的有机物有:含有酚羟基和羧基的化合物.15.能使蛋白质变性的物质有:强酸、强碱、重金属盐、甲醛、苯酚、强氧化剂、浓的酒精、双氧水、碘酒、三氯乙酸等.16.既能与酸又能与碱反响的有机物:具有酸、碱双官能团的有机物(氨基酸、蛋白质等)17.能与NaOH溶液产生反响的有机物:(1)酚:(2)羧酸:(3)卤代烃(水溶液:水解;醇溶液:消去)(4)酯:(水解,不加热反响慢,加热反响快)(5)蛋白质(水解)18、有明显颜色变更的有机反响:1.苯酚与三氯化铁溶液反响呈紫色;2.KMnO4酸性溶液的褪色;3.溴水的褪色;4.淀粉遇碘单质变蓝色.5.蛋白质遇浓硝酸呈黄色颜色反响时间:二O二一年七月二十九日。
有机化学反应方程式汇总
1.取代反应:
取代反应是有机化学中最常见的类型之一、它涉及将一个原子或官能
团从一个有机化合物中取代成另一个原子或官能团。
一个常见的例子是卤
素取代反应,例如醇与卤代烃反应,生成醚。
反应方程式如下:R-OH+R'-X→R-O-R'+HX
2.消除反应:
消除反应是通过去除一对相邻的官能团来生成双键或三键。
一个常见
的例子是醇的脱水反应,生成烯烃。
反应方程式如下:
R-OH→R-CH=CH2+H2O
3.加成反应:
加成反应是将两个或多个分子结合在一起形成一个新的化合物。
一个
常见的例子是烯烃与氢气的加成反应,生成饱和烃。
反应方程式如下:R-CH=CH2+H2→R-CH2-CH3
4.重排反应:
重排反应涉及有机化合物中的原子或官能团的重新排列,形成其他同
分异构体。
一个常见的例子是烷烃的重排反应,生成更稳定的同分异构体。
R-C(CH3)3→R-CH2-C(CH3)2-CH3
5.加成聚合反应:
加成聚合反应是通过将多个单体结合在一起形成聚合物。
一个常见的例子是乙烯的聚合反应,生成聚乙烯。
反应方程式如下:
nCH2=C H2→(CH2-CH2)n
以上只是有机化学反应方程式的一部分,还有许多其他类型的反应,如氧化反应、还原反应、环化反应等。
每个反应的具体方程式和反应条件都有所不同,所以需要根据具体情况进行研究和学习。
催化剂 3 2△ 加热、加压 △△ △ 3 高中有機化學方程式匯總1. CH 4 + Cl 22. CH 3Cl + Cl 2 光照 光照CH 3Cl + HClCH 2Cl 2 + HCl 3. CH 2Cl + Cl 2 光照 4. CHCl + Cl 光 照 CHCl 3 + HClCCl 4+ HCl 5. CH 4 高温 C +2H 2催化剂 6. C 16H 34 C 8H 18 + C 8H 167. CH 3COONa + NaOH CaOCH 4↑+ Na 2CO 3 8. CH 2 = CH 2 + Br 2CH 2Br —CH 2Br 9. CH 2 = CH 2 + H 2O催化剂 CH 3CH 2OH10. CH 2 = CH 2 + HBr 催化剂 △CH 3—CH 2Br 11. CH 2 = CH 2 + H 2 催化剂 CH 3—CH 3 12. nCH 2 = CH 2 催化剂 [ CH 2—CH 2 ] n13. nCH 2=CH-CH=CH 2催化剂 [CH 2-CH=CH-CH 2] n 14. 2CH 2 = CH 2 + O 2催化剂 2CH 3CHO15. CH ≡CH + Br 2CHBr = CHBr 16. CHBr = CHBr+ Br 2 CHBr 2-CHBr 217. CH ≡CH + HCl催化剂H 2C = CHCl18. nCH 2 = CH[ CH 2-CH ] n ClCl 19. CH ≡CH + H 2O催化剂 CH 3CHO20. CaC 2 + 2H 2OCH ≡CH ↑+ Ca(OH)2 21.+ Br 2 Br + HBr22.+ HO -NO 2 浓硫酸NO 2 +H 2O 23.+ HO -SO H △ SO 3H+H 2O2 5 2 5 △ △ △ 24. + 3H 2CH 3 催化剂 △ CH 325.+3HO -NO 2 催化剂O 2N NO 2 +3H 2O 26. 3CH ≡C H → 27. CH 3CH 2Br + H 2ONaOH NO 2 CH 3CH 2OH + HBr 28. CH 3CH 2Br + NaOH 3CH 2OH + NaBr29. CH 3CH 2Br+ NaOH 醇CH 2 = CH 2 + NaBr +H 2O 30. 2CH 3CH 2OH+2Na2CH 3CH 2ONa + H 2↑31. 2CH 3CH 2OH+O 2 催化剂△ 2CH 3CHO + 2H 2O 32. CH 3CH 2OH 浓硫酸170℃ CH 2 = CH 2↑+ H 2O33.C H OH+C H OH 140℃C 2H 5OC 2H 5+H 2O 34. OH+NaOHONa+H 2O 35. OH+H 2OO -+H 3O + 36. ONa+H 2O+CO 2OH+ NaHCO 3 OH 37. +3Br OHBrBr ↓+3HBr38. CH 3CHO + H 2催化剂 △ Br CH 3CH 2OH 39. 2CH 3CHO + O 2 催化剂 2CH 3COOH 40. CH 3CHO+2Ag(NH 3)2OH CH 3COONH 4+2Ag ↓+3NH 3+H 2O41CH 3CHO+2Cu(OH)2△ CH 3COOH+Cu 2O ↓+2H 2O42. 2CH 3COOH+2Na2CH 3COONa+H 2↑ 43.2CH 3COOH+Na 2CO 32CH 3COONa+H 2O+CO 2↑ 44. CH 3COOH+NaHCO 3 CH 3COONa+H 2O+CO 2↑45. CH 3COOH + NaOH CH 3COONa + H 2O4 2 33 2 2 2 46.2CH3COOH + Cu(OH)2(CH3COO)2Cu + 2H2O47.CH3COOH+CH3CH2OH浓硫酸CH3COOCH2CH3 +H2O48.CH3COOCH2CH3+NaOH CH3COONa+CH3CH2OH49.nOHCH2CH2COO H→[ OCH2CH2C ] n+H2O50. C6H12O6 (s) + 6O2 (g) 6CO2 (g) + 6H2O (l)51. C6H12O6催化剂2CH3CH2OH + 2CO252. C12H22O11+H2O 催化剂6H12O6+ C6H12O6蔗糖葡萄糖果糖53. C12H22O11 + H2O 催化剂2C6H12O6麦芽唐葡萄糖54. (C6H10O5)n + nH2O 催化剂n C6H12O6淀粉葡萄糖55.(C6H10O5)n + nH2O 催化剂n C6H12O6纤维素56.C17H33COO-CH2催化剂葡萄糖C17H35COO-CH2C17H33COO-CH +3H2加热、加压C17H35COO-CHC17H33COO-CH2C17H35COO-CH257.C17H35COO-CH2CH2-OHC17H35COO-CH +3NaOH 3C17H35COONa+ CH-OH C17H35COO-CH258.CH2OH+ COOH浓硫酸O OC —CO OCH2-CH2CH2-OH+ 2H2OCH2OH COOH △1.CH +Cl −光−→CH Cl +HClCH Cl +Cl −光−→CH Cl +HCl 2.3.4.5.6.7.8.CH 2=CH -CH =CH 2+Br2 9.10.11.12.13.14.15.16.17.HOCH2 (CHOH )4CHO + 2 Ag(NH3)2OH2 4 43 2 −−∆→ HOCH (CHOH ) COONH + 2 A g ↓ +3NH + H O18.19.20.21.高中有机化学知识点总结1. 需水浴加热的反应有:(1)、银镜反应(2)、乙酸乙酯的水解(3)苯的硝化(4)糖的水解(5)、酚醛树脂的制取(6)固体溶解度的测定凡是在不高于100℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落, 有利于反应的进行。
常见有机化学反应方程式总结有机化学是研究碳和其它元素之间的化学反应的科学领域。
有机化学反应方程式描述了有机化合物之间发生的化学变化,是有机化学研究的基本工具。
下面是一些常见的有机化学反应方程式的总结:1. 取代反应(Substitution reactions):-卤素代替反应:R-X+Y→R-Y+X-核磁代替反应:R-H+X→R-X+H2. 加成反应(Addition reactions):-单一加成反应:R=CH2+X-Y→R-CH2-X-Y-烯烃加成反应:R=CH2+H-CH=CH2→R-CH2-CH-CH33. 消除反应(Elimination reactions):-水解反应:R-X+H2O→R-OH+HX-甲醇酯化反应:R-COOH+CH3OH→R-CO-O-CH34. 氧化反应(Oxidation reactions):-伯醇氧化反应:R-CH2-CH2-CH2-OH→R-CH2-CH=CH2-OH-异醛氧化反应:R-CHO+[O]→R-COOH5. 还原反应(Reduction reactions):-烯烃还原反应:R-CH=CH-R→R-CH2-CH2-R-酮还原反应:R-CO-R→R-CH2-R6. 缩合反应(Condensation reactions):-酯缩合反应:R-COOH+R'-COOH→R-COO-R'+H2O-罗宾逊缩合反应:R-CHO+R'-COOH→R-CH=CH-CO-R'7. 加氢反应(Hydrogenation reactions):-炔烃加氢反应:R-CH=CH-R+H2→R-CH2-CH2-R8. 多聚反应(Polymerization reactions):-乙烯聚合反应:nCH2=CH2→-(-CH2-CH2-)n-9. 光化学反应(Photochemical reactions):-阳光下的氯代烃分解反应:R-CH2-Cl→R-CH2•+Cl•10. 还原消除反应(Reductive elimination reactions):-醇酸脱水反应:R-COOH→R-CO•+H2O以上仅是有机化学反应方程式的一小部分,还有许多其他种类的反应。
有机化学反应方程式
一、甲烷烷烃
CH4 + 2O2CO2 + 2H2O (高二下P8)
CH4+Cl2CH3Cl+HCl CH3Cl+Cl2CH2Cl2+HCl
CH2Cl2+Cl2CHCl3+HCl CHCl3+Cl2CCl4+HCl
二、乙烯、1,3-丁二烯和烯烃
C2H4 + 3O22CO2 + 2H2O (高二下P22)
CH
催化剂
n CH2=CH2CH2-CH2(高二下P21,课本上无反应条
件)
三、炔烃
2C2H2 + 5O24CO2 + 2H2O (高二下P31)
2C6H6 + 15O212CO2 + 6H2O (高二下P37)五、卤代烃
Cr CH 3COOH + CH 3CH 2OH
CH 3COOC 2H 5 + H 2O
( 高二下P59课本条件为:催化剂,加热,单向箭头→) ( 高三P178课本条件为:浓硫酸,加热,双向箭头
)
七、酚 +H 2O
+H 3O + ( 高三P166)
( 高三P168)
浓硫酸
△
八、乙醛、甲醛和醛 CH 3
CHO +H 2
CH 3CH 2OH
2CH 3CHO+5 O 2
4CO 2 + 4H 2O
(高三P172,课本反应条件:酸)
九、乙酸和醋酸 CH 3COOH
CH 3COO -
+H +
十、酯
十一、油脂、糖类、蛋白质、合成高分子化合物
油脂的
(高三P180,课本给出反应条件为浓硫酸,加热,双向箭头
)
(高三P180,课本给出反应条件,加热)
( 高二下P49,课本条件为催化剂)
(高三P180)
(氨基乙酸盐盐酸盐)(高三P182,课本写作:NH2.HCl)
溶液
(氨基乙酸钠)(高三P182)
(高三P182)。