空气比热容比数据处理表格
- 格式:xls
- 大小:10.00 KB
- 文档页数:1

干空气的物理性质温度t/ 0x09密度p /kg -3比定压热容cp/kJ •-kgy\x09 导热系数入/102W・m-1 •41\x09 粘度止/105Pa &09普兰德数Pr质量的物质,在温度升高时,所吸收的热量与该物质的质量和升高的温度乘积之比,称做这种物质的比热容(比热),用符号c表示。
其国际单位制中的单位是焦耳每千克开尔文或焦耳每千克每摄氏度。
J 是指焦耳,K是指热力学温标,即令 1 千克的物质的温度上升(或下降)1 开尔文所需的能量。
根据此定理,便可得出以下公式:Q 为吸收(或放出)的热量;m是物体的质量,AT是吸热(或放热)后温度的变化量,初中的教材里把AT写成At,其实这是不规范的(我们生活中常用C作为温度的单位,很少用K,而且△ T=A t ,因此中学阶段都肥t ,但国际或更高等的科学领域仍用AT)。
物质的比热容与所进行的过程有关。
在工程应用上常用的有定压比热容Cp、定容比热容Cv和饱和状态比热容三种。
定压比热容Cp:是单位质量的物质在压力不变的条件下,温度升高或下降1 ℃或1K 所吸收或放出的能量。
定容比热容Cv:是单位质量的物质在容积(体积)不变的条件下,温度升高或下降 1 ℃或1K 吸收或放出的能量。
饱和状态比热容:是单位质量的物质在某饱和状态时,温度升高或下降1 C或1K所吸收或放出的热量。
比热容是指没有相变化和化学变化时,一定量均相物质温度升高1K所需的热量利用比热容的概念可以类推出表示1mol物质升高1K所需的热量的摩尔热容。
与比热相关的热量计算公式:Q=cmA T Q吸(放)=cm(T初-T末)其中c为比热,m为质量,Q为能量热量。
吸热时为Q=cm A T升(用实际升高温度减物体初温),放热时为Q=cm AT降(用实际初温减降后温度)。
或者Q=cmA T=cm(T 末-T初),Q>0时为吸热,Q<0时为放热。

空气-蒸汽对流给热系数测定数据处理(数据表格、计算示例及图解)一、原始数据记录表二、计算结果表实验号流量温度(℃)m 3/h冷流体进口温度t1 冷流体出口温度t2 冷流体进口侧蒸汽温度T1冷流体出口侧蒸汽温度T2 1 5 35.8 76.8 102.9 102.4 2 7.5 36.6 76.5 101.9 101.2 3 10 37.2 76.9 102.2 101.8 4 12.5 38.4 77.5 102.5 102 5 15 40.1 77.8 102.4 101.9 6 17.5 41.9 78.3 102.5 101.9 7 20 43.4 78.6 102.4 101.8 8 22.544.1 78.5 102.5101.9序号Δt m \℃K W/m 2·℃Pr Re X Y m α21 43.2337 29.90223 0.597055 7324.592 1.143919 0.033442 0.020978 41.67203 2 41.99407 44.92077 0.596638 10982.84 0.826950.022261 0.020978 57.64489 3 41.92402 59.64674 0.595804 14633.02 0.656813 0.016765 0.020978 72.57683 4 41.33924 74.365130.5943118267.16 0.549236 0.013447 0.020978 86.79224 5 40.38487.940270.592657 21888.62 0.474507 0.011371 0.020978 100.4611 6 39.42766 101.6829 0.593118 25494.11 0.418598 0.009834 0.020978 113.8787 7 38.54594 114.7875 0.591641 29098.25 0.376053 0.008712 0.020978 126.7624 838.45563 126.43840.591149 32721.39 0.342197 0.007909 0.020978 139.3041计算示例:(以第一组为例)平均温度t 平均1=(t 1+t 2)/2=(35.8+76.8)/2=56.3℃ 此温度下,空气的各项物性分别为:空气进口处密度ρ’=1E-05*t 2-4.5E-03*t+1.2916=1.069947 空气的比热Cp :1005J/(kg ·℃)温度在60℃以下空气的导热系数λ=-2E-08*t 2+8*E-05*t+0.0244=0.028841空气的粘度μ=(-2E-06*t 2+5*E-03*t+1.7169)*1E-05=1.71338E-05序号平均温度t 平均空气进口处密度ρ’ 空气质量流量m 2 空气的比热Cp 实际流量V ’ 空气的导热系数λ空气的粘度μ NuNu/Pr 0.4ln(N u/Pr 0.4ln(R e)156.3 1.069947 0.001577 1005 0.001474 0.0288411.71338E-05 23.11853 28.41545 3.346933 8.898993 2 56.55 1.069104 0.002365 1005 0.002212 0.02 8861.71333E-05 31.95831 39.29159 3.671011 9.30409 3 57.05 1.067422 0.00315 1005 0.002951 0.02 88991.71324E-05 40.18246 49.43051 3.900568 9.591036 4 57.95 1.064407 0.003932 1005 0.003694 0.02 89691.71308E-05 47.93689 59.02894.078027 9.81286558.95 1.061076 0.004712 1005 0.00444 0.02 90461.7129E-05 55.33806 68.21856 4.222717 9.993722 6 60.1 1.05727 0.005487 1009 0.00519 0.02 91361.71268E-05 62.53688 77.06899 4.344701 10.1462 761 1.05431 0.006262 1009 0.005939 0.02 92061.71251E-05 69.44557 85.66854 4.450486 10.27843 861.3 1.053327 0.007041 1009 0.006685 0.0292291.71245E-0576.25566 94.10077 4.544366 10.39578标定用流体的体积流量V 1=5m 3/h ρf=7800kg/m 3 ρ=1.205kg/m 3,由此可得出实际的空气流量为:V ’=()ρρρρρρ--f f ’)’(V=)()( 1.205-78001.069947 1.069947-7800205.136005 =0.001474空气质量流量m 2=ρ’V ’=1.069947*0.001474=0.001577 d 2=0.016m l=1m 换热面积A=π*d 2*lm=0.020978d 4023.018.128.0=π K=m 122p 2t t -t m ?A c )(=43.2337*1*016.0*35.8-76.8*1005*0.001577π)(=29.90223Pr=λμ*p c =0.02884105-1.71338E *1005=0.597055Re===2d *V *4·d d πμρμρ’u 0.016*05-1.71338E * 1.069947*0.001474*4π=7324.592 X=8.022224.0Pr 1μλm = 1.1439190.00157705-1.71338E 0.597055*0.02884118.00.4=??? ??? 0.0334421==KY 8.0224.0222m m Pr=μλα=41.6720305-1.71338E0.0015770.0209780.597055*0.0288418.00.4=??? ??? 因为流体是被加热,故Nu 中n 取0.4,则:23.11853r *e *023.0u 4.08.0==P R N 28.415450.59705523.11853r 0.44.0==P Nu 3.3469330.59705523.11853ln Pr ln 0.44.0==??? ??Nu 8.898993Re ln =)(三、冷流体给热系数的准数式:Nu/Pr 0.4=ARe m,由实验数据作图拟合曲线方程,确定式中常数A 及m,如下:500010000150002000025000300003500040000450005000020406080100ReData: Data1_B Model: Allometric1Equation: y = a*x^b Weighting: y No weightingChi^2/DoF = 2.8642E-11R^2= 1 a 0.023±1.9337E-8b 0.8±8.3367E-8N u /P r 0.4作曲线如上,按照y=a*x^b 拟合,由表内数据可知a=0.023,b=0.8;与Nu/Pr 0.4=ARe m 比较,即确定常数A=0.023,m=0.8 ,与经验式Nu/Pr 0.4=0.023Re 0.8中数值完全一致.四、以ln(Nu/Pr 0.4)为纵坐标,ln(Re )为横坐标,如下:8.89.09.29.49.69.810.010.210.410.63.23.43.63.84.04.24.44.6ln(Nu/Pr0.4 Linear Fit of C1l n (N u /P r 0.4ln(Re)Equation y = a + b*xAdj. R-Squ 1ValueStandard ErC1Intercep -3.772 5.88102E-6C1Slope0.8 5.99225E-7作曲线如上,按照y=a+b*x 拟合,由表内数据可知a=-3.772,b=0.8;即ln(Nu/Pr 0.4)=-3.772+0.8*ln(Re),取e 的指数,两边消去ln ,则8.0Re ln 772.30.4)ln(N u/PrRe 023.0*Nu/Pr 8.00.4===-e e e ,与Nu/Pr 0.4=ARe m比较,即确定常数A=e -3.772=0.023,m=0.8 ,与经验式Nu/Pr 0.4=0.023Re 0.8中数值完全一致.。

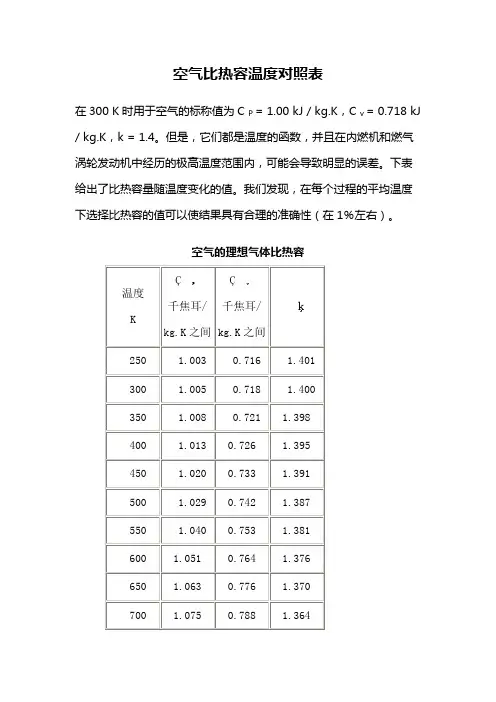
空气比热容温度对照表
比热容:
例如如图,同时加热时,沙子吸热温度升高的快,说明了不同物质吸热的本领是不一样的,这种差异性用比热容来描述。
注意:加热方式相同时,水和沙子在相同时间内吸收的热量是一样多的。
(1)定义:单位质量的某种物质,温度升高(或降低)l℃时所吸收(或放出)的热量叫做这种物质的比热容。
(2) 意义:反映条件相同的情况下,物质吸热本领的物理量。
(3) 单位:J/(kg·℃)读作焦每千克摄氏度。
(4)比热容表:各种物质的比热容可以在比热容表中查到,从表中可以看出,物质不同,比热容也不同,可见比热容是物质的特性之一。
注意:(1)一般来说,液体的比热比固体的大(水银除外)有些不同物体的比热容是相等的。
(2)用同一热源加热时,不同物体在相同时间内吸收的热量是相等的。

空气比热容温度对照表
比热容是指没有相变化和化学变化时,一定量均相物质温度升高1K所需的热量。
利用比热容的概念可以类推出表示1mol物质升高1K所需的热量的摩尔热容。
与比热相关的热量计算公式:Q=cm AT,即Q吸(放)=cm(T初-T末),其中c 为比热,m为质量,Q为能量热量。
吸热时为Q=cm AT升(用实际升高温度减物体初温),放热时为Q=cm AT降(用实际初温减降后温度)。
或者Q=cm AT=cm(T末-T初),Q>0时为吸热,Q<0时为放热。
比热容的计算公式一般为:
二Q
C~
Q 吸=cm (t-to )Q 放=cm (to-t )
c表示比热容
m表示物体的质量
t o表示物体的初温
t表示物体的末温
注释:【1 atm = 1 标准大气压=1.01 xiO5Pa 1 atm = 760 mmHg = 1.01325 X105 pa M0.1 Mpa = 1 Kgf/cm 2】
空气的比热容没有确定值,即便是在温度确定时,通常使用定压比热容或定容比热容来反映空气比热容的大小,这两者都与温度有关(温差不太大时可认为基本相等)。
一定质量的物质,在温度升高时,所吸收的热量与该物质的质量和升高的温度乘积之比,称做这种物质的比热容(比热),用符号c表示。
其国际
单位制中的单位是焦耳每千克开尔文[J /(kg K)]或焦耳每千克每摄氏度[J
/(kg •可。
J是指焦耳,K是指热力学温标,即令1千克的物质的温度上升(或下降)1开尔文所需的能量。
F面是空气比热容温度对照表:。
实验九 空气比热容比测定【实验目的】1. 观察绝热膨胀,等容升温等过程中的状态变化,进一步理解其中的物理规律。
2. 用绝热膨胀测定空气比热容比。
【实验原理】理想气体的定压摩尔热容为p C ,定容摩尔热容为v C ,气体的比热容比γ值为:vp C C =γ,γ又称摩尔热容比。
瓶内贮入气体后,将瓶内的气体看成由两部分组成,一部分是放气后进入大气的气体,另一部分是放气前在瓶内具有体积V 1,放气后,这部分气体充满贮气瓶,体积为V 2,以放气后留在瓶内的这部分气体为系统,实验中系统经三个状态,Ⅰ−−−→−绝热膨胀),,(011T V P Ⅱ−−−→−定容升温),,(20x T V P Ⅲ),,(022T V P 由于气体处于状态Ⅰ和状态Ⅲ时,气体的量不变,温度相同时应有2211V P V P =,另外状态Ⅰ至状态Ⅲ是绝热过程,应有γγ2011V P V P =,此二式联立解得1210lg lg lg lg P P P P --=γ。
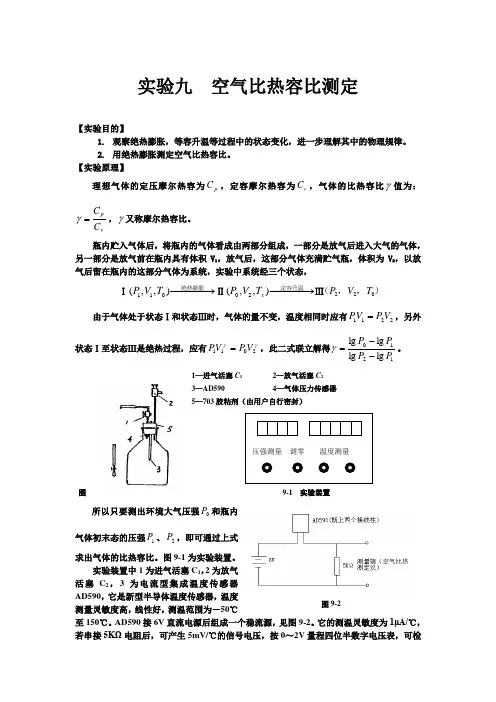
1—进气活塞C 1 2—放气活塞C 2 3—AD590 4—气体压力传感器 5—703胶粘剂(由用户自行密封)图9-1 实验装置所以只要测出环境大气压强0P 和瓶内气体初末态的压强1P 、2P ,即可通过上式求出气体的比热容比。
图9-1为实验装置。
实验装置中1为进气活塞C 1,2为放气活塞C 2,3为电流型集成温度传感器AD590,它是新型半导体温度传感器,温度测量灵敏度高,线性好,测温范围为-50℃至150℃。
AD590接6V 直流电源后组成一个稳流源,见图9-2。
它的测温灵敏度为1μA/℃,若串接5KΩ电阻后,可产生5mV/℃的信号电压,按0~2V 量程四位半数字电压表,可检测到最小0.02℃温度变化。
4为气体压力传感器探头,由同轴电缆线输出信号,与仪器内的放大器及三位半数字电压表相接。
当待测气体压强为环境大气压P 0时,数字电压表显示为0;当待测气体压强为P 0 +10.00kPa 时,数字电压表显示为200mV ;仪器测量气体压强灵敏度为20mV/kPa ,测量精度为5Pa 。

实验原理图1 实验图2三、实验仪器NCD-I型空气比热容比测量仪由如下几个部分组成:贮气瓶(由玻璃瓶、进气活塞、橡皮塞组成)、两只传感器(扩散硅压力传感器和电流型集成温度传感器AD590各一只)、测空气压强的三位半数字电压表、测空气温度的四位半数字电压表。
测空气压强的数字电压表用于测量超过环境气压的那部分压强,测量范围0~10000Pa,灵敏度为20mv/Kpa(表示1000Pa的压强变化将产生20mv的电压变化,或者50Pa/mv,单位电压变化对应50Pa的压强变化)。
实验时,贮气瓶内空气压强变化范围为6000Pa。
图4-6-1实验装置中,温度传感器3是新型半导体温度传感器,其测量灵敏度高,线性好,测温范围为-50~150℃,接6V直流电源后组成一个稳流源。
它的测温灵敏度单位为1μA/℃,若串接5KΩ电阻后,可产生5mv/℃的信号电压,接0~2V量程四位半数字电压表,可检测到最小0.02℃温度变化。
气体压力传感器探头4由同轴电缆线输出信号,与仪器内的放大器及三位半数字电压表相接。
当待测气体压强为环境大气压P0时,数字电压表显示为0,当待测气体压强为P0+10000Pa时,数字电压表显示为200mv,仪器测量气体压强灵敏度为20mv/ 1000Pa。
四、实验步骤1. 按图4-6-2接好仪器的电路,注意AD590的正负极不要接错。
用Forton式气压计测定大气压强P0,用水银温度计测量环境温度。
开启电源,将电子仪器部分预热20分钟,然后用调零电位器调节零点,把三位半数字电压表示值调到0。
2. 将活塞C2关闭,活塞C1打开,用打气球把空气稳定地徐徐进入贮气瓶B内,用压力传感器和AD590温度传感器测量空气的压强和温度,记录瓶内压强均匀稳定时压强P1和温度T0(室温为T0)(P1取值范围控制在130mV~150mV之间。
由于仪器只显示大于大气压强的部分,实际计算时式(3-5-4)中的压强P1应加上周围大气压强值)。

空⽓⽐热容温度对照表
空⽓⽐热容温度对照表
⽐热容是指没有相变化和化学变化时,⼀定量均相物质温度升⾼1K所需的热量。
利⽤⽐热容的概念可以类推出表⽰1mol物质升⾼1K所需的热量的摩尔热容。
与⽐热相关的热量计算公式:Q=cmΔT 即Q吸(放)=cm(T初-T末)其中c为⽐热,m为质量,Q为能量热量。
吸热时为Q=cmΔT升(⽤实际升⾼温度减物体初温),放热时为Q=cmΔT降(⽤实际初温减降后温度)。
或者Q=cmΔT=cm(T末-T 初),Q>0时为吸热,Q<0时为放热。
⽐热容的计算公式⼀般为。
Q吸=cm(t-to)Q放=cm(to-t)
c表⽰⽐热容.
m表⽰物体的质量
to表⽰物体的初温
t表⽰物体的末温
注释:【1 atm = 1 标准⼤⽓压=1.01×105Pa 1 atm=760 mmHg=
1.01325×10ˇ5 pa≈0.1 Mpa=1 Kgf/cm2】
空⽓在不同压⼒和温度下的⽐热容⽐。

1. 实验名称空气比热容比的测定 2. 实验目的(1)了解绝热、等容的热力学过程及有关状态方程。
(2)测定空气的比热容比。
3. 实验原理:主要原理公式及简要说明、原理图(1)热力学第一定律及定容比热容和定压比热容 热力学第一定律:系统从外界吸收的热量等于系统内能的增加和系统对外做功之和。
考虑在准静态情况下气体由于膨胀对外做功为PdV dA =,所以热力学第一定律的微分形式为PdV dE dA dE dQ +=+= (1)定容比热容C v 是指1mol 的理想气体在保持体积不变的情况下,温度升高1K 所吸收的热量。
由于体积不变,那么由(1)式可知,这吸收的热量也就是内能的增加(d Q =d E ),所以dTdE dT dQ C v v =⎪⎪⎭⎫⎝⎛=(2) 由于理想气体的内能只是温度的函数,所以上述定义虽然是在等容过程中给出,实际上任何过程中内能的变化都可以写成d E =C v dT定压比热容是指1mol 的理想气体在保持压强不变的情况下,温度升高1K 所吸收的热量。
即pp dT dQ C ⎪⎪⎭⎫⎝⎛=(3) 由热力学第一定律(3)式,考虑在定压过,就有dT dV pdT dE dT dQ pp +⎪⎭⎫⎝⎛=⎪⎭⎫ ⎝⎛(4) 由理想气体的状态方程PV =RT 可知,在定压过程中P R dT dV =,又利用v C dTdE=代入(4)式,就得到定压比热容与定容比热容的关系R C C v p +=(5)R 是气体普适常数,为8.31 J / mol· K ,引入比热容比γ为v p C C /=γ(6)在热力学中,比热容比是一个重要的物理量,它与温度无关。
气体运动理论告诉我们,γ与气体分子的自由度f 有关ff 2+=γ(7) 例如,对单原子气体(Ar 、He),3=f 67.1=γ对双原子气体(N 2、H 2、O 2)5=f40.1=γ,对多原子气体(CO 2、CH 4),6=f 33.1=γ(2)绝热过程系统如果与外界没有热交换,这种过程称为绝热过程,因此,在绝热过程中,d Q =0。

空气比热容温度对照表
比热容是指没有相变化和化学变化时,一定量均相物质温度升高1K所需的热量。
利用比热容的概念可以类推出表示1mol物质升高1K所需的热量的摩尔热容。
与比热相关的热量计算公式:Q=cmΔT 即Q吸(放)=cm(T初-T末)其中c为比热,m为质量,Q为能量热量。
吸热时为Q=cmΔT升(用实际升高温度减物体初温),放热时为Q=cmΔT降(用实际初温减降后温度)。
或者Q=cmΔT=cm(T末-T初),Q>0时为吸热,Q<0时为放热。
比热容的计算公式一般为。
Q吸=cm(t-to)Q放=cm(to-t)
c表示比热容.
m表示物体的质量
to表示物体的初温
t表示物体的末温
注释:【1 atm = 1 标准大气压=1.01×105Pa 1 atm=760 mmHg=
1.01325×10ˇ5 pa≈0.1 Mpa=1 Kgf/cm2】
空气在不同压力和温度下的比热容比。

007 实验报告 评分:课程: ******** 学期: ***** 指导老师: ****年级专业: ***** 学号:****** 姓名:!习惯一个人007实验3-5空气比热容比的测定一、实验目的1. 用绝热膨胀法测定空气的比热容。
2. 观察热力学过程中状态变化及基本物理规律。
3. 学习气体压力传感器和电流型集成温度传感器的原理及使用方法。
二、实验原理测量仪器如图4-6-1所示。
1为进气活塞C 1,2 为放气活塞C 2,3为电流型集成温度传感器,4为气体压力传感器探头。
实验时先关闭活塞C 2,将原处于环境大气压强为P 0、室温为T 0的空气经活塞C 1送入贮气瓶B 内,这时瓶内空气压强增大,温度升高。
关闭活塞C 1,待瓶内空气稳定后,瓶内空气达到状态Ⅰ(101,,V T P ),V 1为贮气瓶容积。
然后突然打开阀门C 2,使瓶内空气与周围大气相通,到达状态Ⅱ(),,220V T P 后,迅速关闭活塞C 2。
由于放气过程很短,可认为气体经历了一个绝热膨胀过程,瓶内气体压强减小,温度降低。
绝热膨胀过程应满足下述方程rr o r o r T p T p 1111--= (3-5-2) 在关闭活塞C 2之后,贮气瓶内气体温度将升高,当升到温度T 0时,原气体的状态为Ⅰ(101,,V T P )改变为状态Ⅲ(202,,V T P ),两个状态应满足如下关系: 021T pT p o =(3-5-3)由(3-5-2)式和(3-5-3)式,可得)lg /(lg )lg (lg 1210P P P P --=γ (3-5-4)利用(3-5-4)式可以通过测量P 0、P 1和P 2值,求得空气的比热容比γ值。
实验原理图1 实验图2三、实验仪器NCD-I型空气比热容比测量仪由如下几个部分组成:贮气瓶(由玻璃瓶、进气活塞、橡皮塞组成)、两只传感器(扩散硅压力传感器和电流型集成温度传感器AD590各一只)、测空气压强的三位半数字电压表、测空气温度的四位半数字电压表。