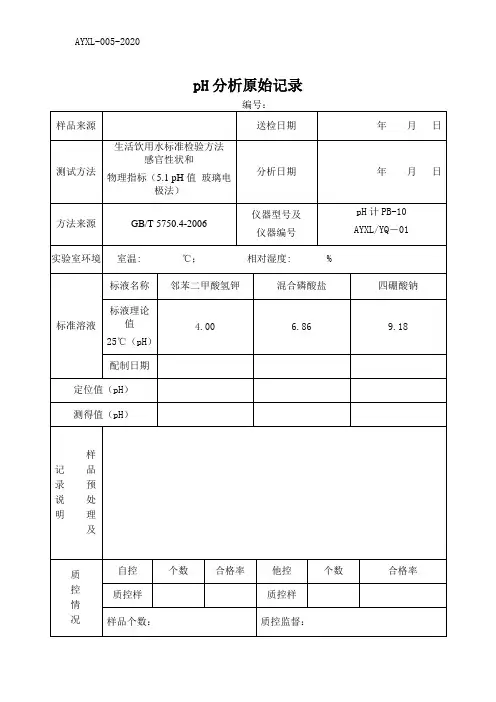
pH值测定原始记录
- 格式:docx
- 大小:15.25 KB
- 文档页数:1

水质现场检测记录受理编号:中坚()检[20 ] 号受检单位:检测日期:年月日检测项目:温度、游离性余氯环境条件:温度℃湿度 % 检验方法:直接测定法,N,N-二乙基对苯二胺分光光度法检验依据:《生活饮用水卫生标准检验方法》GB/T 5750. 11—2006《公共场所卫生标准检验方法》GB/T 18204. 28—2000使用仪器:水银温度计;余氯测定仪,仪器编号:,状态被监测单位陪同人员(签字):监测人:复核人:日期:年月日日期:年月页/共页附录B 水质中pH值检测原始记录样式四川中坚环境监测服务有限公司二次供水检测原始记录受理编号:中坚()检[20 ] 号检验项目: pH 检验日期:年月日检验方法:玻璃电极法室内温度:℃室内湿度: %检验依据:《生活饮用水标准检验方法》GB/T 5750.6.2-20061.试剂1.1苯二甲酸氢钾标准缓冲溶液:温度为20℃时,pH=4.001.2混合磷酸盐标准缓冲溶液:温度为20℃时,pH=6.881.3四硼酸钠标准缓冲溶液:温度为20℃时,pH=9.222. 仪器玻璃电极,仪器编号:,状态2.分析步骤2.1 测定前电极应放在纯水中浸泡24h以上。
仪器校准,按仪器使用说明校准。
2.2 选一种与被测水样pH值相近的缓冲溶液,重复测定1~2次,当水样pH<7.0时,使用苯二甲酸氢钾标准缓冲溶液定位,以混合磷酸盐标准缓冲溶液或四硼酸钠标准缓冲溶液复定位;当水样pH>7.0时,则用四硼酸钠标准缓冲溶液定位,以混合磷酸盐标准缓冲溶液或苯二甲酸氢钾标准缓冲溶液复定位。
2.3 用洗瓶以纯水缓缓淋洗6~8次,然后插入水样中,1min后直接测定读数。
检验者:复核者:日期:年月日日期:年月日。
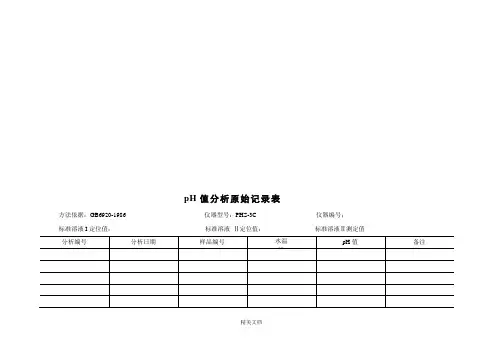
pH值分析原始记录表方法依据:GB6920-1986 仪器型号:PHS-3C 仪器编号;标准溶液I定位值:标准溶液Ⅱ定位值:标准溶液Ⅱ测定值精美文档分析:校核:审核:续表pH值分析原始记录表精美文档精美文档分析:校核: 审核:重量分析原始记录表样品名称: 分析项目:SS 收样日期: 容器介质:CN-CA 滤膜,孔径0.45μm 6分析:校核:审核:第页共页重量分析原始记录表精美文档分析:校核:审核:第页共页容量法分析原始记录表样品名称:分析项目:化学需氧量收样日期:分析日期:方法依据:GB11914-89 最低检出限:计算公式:ρCOD(O2,mg/L)=K(V0-V1)×C×8×1000/V2精美文档分析:校核:审核:第页共页容量法分析原始记录表精美文档分析:校核:审核:分光光度法分析原始记录表样品名称:分析项目:总磷收样日期:分析日期:方法依据:GB11893-98 仪器型号:仪器编号:最低检出限:测定波长:700nm 比色皿厚度:3cm 参比溶液:蒸馏水计算公式:ρ(p,mg/L)=K(A-A0)/(bV)精美文档加标溶液浓度(mg/L): 加标体积(ml):加标物质量(μg):校准曲线编号:绘制日期:回归方程:a = b = 相关系数:r =校准曲线检验(中等浓度标准溶液吸光值—空白值):原方程吸光度:现测吸光度:相对偏差(%):分析:校核:审核:第页共页分光光度法分析原始记录表样品名称:分析项目:氨-氮收样日期:分析日期:方法依据:GB7479-87 仪器型号: 仪器编号:最低检出限:测定波长:420nm 比色皿厚度:2cm 参比溶液:无氨水计算公式:ρ(NH3-N,mg/L)=(A-A0)/(bV)精美文档精美文档加标溶液浓度(mg/L ): 加标体积(ml ): 加标物质量(μg ):校准曲线编号: 绘制日期: 回归方程: a = b = 相关系数:r = 校准曲线检验(中等浓度标准溶液吸光值—空白值):原方程吸光度:现测吸光度: 相对偏差(%): 分析: 校核: 审核:第 页 共 页分光光度法分析原始记录表分析:校核:审核:第页共页溶解氧分析原始记录表方法依据:碘量法(GB7489-1987)仪器型号:样品类型:送样日期:分析日期:计算公式:溶解氧(O2, mg/l)= 80×C1×V1精美文档分析:校核:审核:溶解氧分析原始记录表续表精美文档分析:校核:审核:五日生化需氧量(BOD5)分析原始记录表(Ⅰ)方法依据:稀释与接种法(GB7488-1987)仪器型号:采样日期:V t-V e V t五日生化需氧量的计算公式:BOD5(mg/l)=[(c1 - c2)- (c3 - c4)]×V t V e培养前(进样)日期:年月日时分培养后(出样)日期:年月日时分精美文档分析:校核:审核:五日生化需氧量(BOD5)分析原始记录表(Ⅰ)续表精美文档分析:校核:审核:精美文档污水处理厂水质检测报告单(检测编号:)送样时间:检测日期:检测结果:(见下表)检测部门:化验室ps:具体情况,具体修改表格。
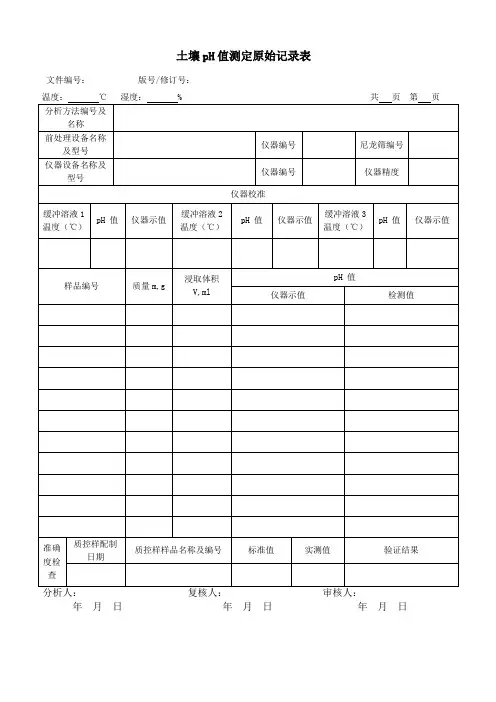
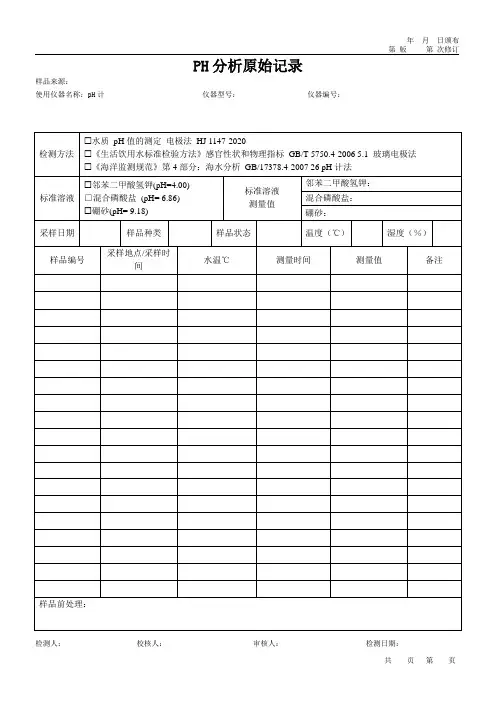

试验原始记录数据在进行试验时,需要记录一系列的原始数据,以便后续的数据分析和结果验证。
以下是一个关于一些试验的原始记录数据,共计1200字以上。
试验名称:酸碱中和实验试验目的:通过向酸性溶液中加入碱溶液,观察酸碱中和过程中溶液的pH值的变化。
试验材料:盛装有酸性溶液的玻璃烧杯、盛装有碱性溶液的滴液瓶、pH计、计时器、实验台。
试验步骤:1.使用pH计测量酸性溶液的初始pH值,并记录下来。
2.将酸性溶液倒入玻璃烧杯中,注意不要让溶液溅到皮肤或眼睛。
3.开始计时,每隔10秒钟向酸性溶液中滴加1滴碱性溶液,并用磁力搅拌子均匀搅拌。
4.每滴加一滴碱性溶液后,使用pH计测量溶液的pH值,并记录下来。
5.重复第4步,直到溶液的pH值达到中性(约为7)。
6.停止滴加碱性溶液,记录此时滴加的碱性溶液的总滴数,并计算出每滴碱溶液对应的pH值变化。
7.使用pH计测量中性溶液的pH值,并与初始pH值进行对比。
原始记录数据:试验时间:2024年1月1日9:00AM酸性溶液的初始pH值:3.5滴加碱溶液的时间(秒),碱溶液滴数,滴加后溶液的pH值10,1,3.720,2,4.130,3,4.440,4,4.850,5,5.260,6,5.670,7,6.080,8,6.490,9,6.7100,10,7.0滴加10滴碱溶液后,溶液的pH值达到中性,中性溶液的pH值为7.0。
试验结束后,需要对原始数据进行分析和总结。
根据实验记录,随着加入碱性溶液的滴数增加,酸性溶液的pH值逐渐增加,最终达到了中性状态。
从初始的酸性pH值3.5,到滴加10滴碱溶液后pH值为7.0,每滴碱溶液对应的pH值变化约为0.35、可见,滴加碱性溶液对酸性溶液的中和作用是明显的。
通过这个实验记录,我们可以观察到酸碱中和的过程,并了解到酸碱溶液在中和过程中pH值的变化。
这对于学习酸碱中和反应、了解物质性质具有重要意义,并且可以应用在很多实际生活和工业生产中。