植物组织中硝态氮测定.
- 格式:ppt
- 大小:2.07 MB
- 文档页数:14

六、氮含量〔硝酸盐、亚硝酸盐、游离氨基酸、铵态氮等〕的测定:〔2g〕样品提取液的提取: 称取新颖植物组织2g,参加15ml无离子水研磨成匀浆,置于45℃振荡机中摇动浸提〔或超声波〕lh后用5ml无离子水冲洗干净,然后离心或过滤(如含色素需用活性炭脱色),滤液备用。
备注〔lg的经历〕:可溶性糖、可溶性蛋白质、VC等需要研磨提取的简单指标也可以使用此提取液按比例测定。
1硝态氮的测定:标准氮试剂:精称KNO3 0.9021g,溶于少量重蒸无离子水中,并定容至250ml,含N 量为500µgNO3一N/ml。
5%水杨酸一硫酸溶液:称取水杨酸5g,溶于100ml浓H2SO4(比重1.84)中,搅拌溶解后贮于棕色瓶内,冰箱中至多保存l周,最好现用现配。
2mol/L NaOH溶液:称取NaOH 80g放入500ml硬质烧杯中,参加重蒸无离子水200ml,溶解后定容至l000ml。
操作方法标准曲线制作取:50ml容量瓶6只(编号),依次参加标准氮试剂5、l0、l5、20、25、30ml,用无离子水定容,那么成为50、100、l50、200、250、300 ug/ml 的氮系列标准溶液;再取干沽50ml三角瓶7只,分别装入上述系列溶液0.2ml,剩下的1只三角瓶参加无离水0.2ml(作为O 点);然后分别参加5%水杨酸一硫酸溶液0.8ml,混匀静置20--30min(显色);最后参加2mol/L NaOH溶液l9ml,混匀。
冷却后利用751分光光度计,于410nm下比色,记录光密度(OD)值;并以OD 值为纵座标,以标准氮(0、50、l00、150、200、250、300 ug)为横座标,绘制一条标准曲线(通过原点的直线)。
0.1ml滤液+0.4ml 5%水杨酸一硫酸溶液,混匀静置20--30min(显色);最后参加2mol/L NaOH溶液9.5ml,混匀。
冷却后利用751分光光度计,于410nm下比色,记录光密度(OD)值;结果计算按照公式A= CV1/(WV2) 计算。

高级植物生理实验报告植物营养农学院农药学东保柱20132020542013年12月27日实验1 植物组织铵态氮含量的测定(茚三酮比色法)一、实验原理植物吸收的氮主要是氨态氮和硝态氮,后者经过还原过程形成氨,前者经同化后形成谷氨酰胺和谷氨酸,然后形成其他氨基酸和蛋白质。
测定氨态氮的方法有多种,本实验为改良的茚三酮比色法。
α-氨基酸与水合茚三酮溶液一起加热,经氧化脱氨变成相应的α-酮酸,酮酸进一步脱羧变成醛,水合茚三酮则被还原,在弱酸环境中,还原型茚三酮,氨和另一分子水合茚三酮反应,缩合生成蓝紫色物质。
根据蓝紫色的深浅,在580nm 波长下测定吸光值。
本实验中在茚三酮试剂中添加乙二醇并补加正丁醇和丙醇,可以克服茚三酮的不稳定性。
二、仪器设备研钵、烧杯、漏斗、量筒、具塞试管、三角瓶、容量瓶、移液管、天平、沸水浴锅、可见分光光度计三、试剂1. 10%醋酸(100mL)2. 1% 抗坏血酸(100mL)3. 5μg/mL 亮氨酸或丙氨酸溶液(0.005g定容至1000mL)4. pH5.4醋酸缓冲液:8.8mL 0.2mol/L 醋酸(冰醋酸11.55mL稀释至1000mL)加41.2mL 0.2mol/L醋酸钠(醋酸钠16.4g或三水醋酸钠27.2g 配成1000mL)。
5. 水合茚三酮试剂:1.1g茚三酮放到烧杯中,加入15mL正丙醇,摇匀,溶解,后加入30ml正丁醇和60ml乙二醇,混匀,再加9mL pH5.4醋酸缓冲液,混匀。
保存于棕色瓶中,冰箱保存,适用期限10天。
四、操作步骤1. 标准曲线的绘制以下表所示量从5μg/mL 亮氨酸或丙氨酸溶液中分别取溶液并在每个试管中加蒸馏水至2mL,对照加2mL 蒸馏水,后在各试管中加入3mL 水合茚三酮试剂和0.1mL 1%抗坏血酸,摇匀。
盖上试管塞,于沸水中加热15分钟,取出后搅拌冷却15分钟。
冷却后的有色溶液中加无水乙醇至10mL,在波长580nm 处测吸光值,以铵态氮浓度(μg/mL)为横坐标,吸光值为纵坐标绘制标准曲线。

植物体内硝态氮含量的测定二、植物体内硝态氮含量的测定硝态氮是植物最主要的氮源。
植物体内硝态氮含量往往能反映土壤中硝态氮供应情况,因此可作为土壤肥氮肥的指标。
测定植物体内的硝态氮含量,不仅能够反映出植物的氮素营养情况,而且对鉴定蔬菜和植物为原料的加工制品的品质也有重要的意义。
(一)原理在浓酸条件下,NO3-与水杨酸反应,生成硝基水杨酸,硝基水杨酸在碱性条件下(PH>12)呈黄色,在一定范围内,其颜色深浅与含量成正比,可直接比色测定。
(二)仪器与用具(1)722型分子光光度计1台;(2)电子顶载天平1台(感量1/万);(3)刻度试管20cm326支;(4)刻度吸管0.1cm3. 0.5cm3. 5cm3. 10cm3各1支;(5)容量瓶50cm38个;(6)容量瓶25cm33个;(7)小漏斗(∮5cm)3个;(8)玻棒1根;(9)洗耳球1个;(10)电炉1个;(11)铝锅1个;(12)玻璃塞;(13)定量滤纸7cm。
试剂:500ppmNO3-标准溶液精确称取烘至恒重的KNO3 0.7221克溶于无离水中,定容至200cm3。
5%水杨酸一硫酸溶液称取5克水杨酸溶于100cm3,浓硫酸中(密度为1. 84),搅拌溶解后,贮于棕色瓶中。
置冰箱保存一周有效。
8%氢氧化纳溶液称取10克氢氧化纳溶于1dm3无离子水中即可。
(三)实验步骤1. 标准曲线的制作(1)吸取500ppmNO3-标准溶液1cm3. 2cm3. 3cm3. 4cm3. 6cm3. 8cm3. 10cm3. 12cm3分别放入501cm3容量瓶中,用无离子定至刻度,使之成10. 20、30、40、60、80、100、120、ppm的系列标准溶液。
(2)吸收上述系列标准溶液0.11cm3,分别放入刻度试管中,以0.11cm3无离子水代替标准溶液作空白,再分别加入0.4cm3水杨酸一硫酸溶液,摇匀,在室温下放置20分钟后再加入8%NaOH溶液9. 51cm3摇匀冷却至室温,显色液总体积为101cm3。


植物组织中硝态氮含量的测定目的意义根系吸收的无机态氮,有铵态氮和硝态氯。
植物体内硝态氮合量可以反映土壤氮素供应情况,常作为施肥指标。
叶菜类和根菜类中常含有大量硝酸盐,在烹调和腌制过程中可转化为亚硝酸盐而危害人体健康。
测定植物组织硝态氮含量对研究植物氮素营养和农产品安全性均有重要作用。
一、实验原理本实验采用硝基水杨酸比色法测硝态氮,其原理是在有浓硫酸的条件下NO3-与水杨酸生成硝基水杨酸。
产物硝基水杨酸在碱性条件下(PH>12)呈黄色,在410 nm处有最大吸收峰,在范围内,其颜色的深浅与含量成正比,可直接比色测定。
二、材料、设备和试剂1.材料玉米、接骨木、瓜类、葡萄等植株幼苗。
2.设备电子天平、分光光度计、恒温水浴锅、容量瓶、刻度试管、漏斗、滤纸等。
3.试剂(1)100mg/L硝态氮标准溶液精确称取烘干至恒重的KNO3 0.7221g溶于蒸馏水(无离子水)中,定容至1000ml。
(2)5%水杨酸-硫酸溶液称取5g水杨酸溶于100ml浓硫酸中(密度为1.84),搅拌溶解后,贮存于棕色瓶中,置冰箱保存1周有效。
(3)8%氢氧化钠溶液称取20g氢氧化钠溶于250ml蒸馏水中。
三、操作方法1.标准曲线的制作(1)吸取100 mg/L硝态氯标准溶液1m1、2ml、4m1、6m1、8ml、10ml、12m1分别放入10ml容量瓶中,用蒸馏水定容至刻度,使之成为10、20、40、60、80、100、120µg /m1硝态氮的系列标准液。
(2)取8支试管,分别编号为0-7,以0号管加入0.1ml蒸馏水作空白,1-7号管分别吸取上述系列标准溶液0.1ml。
再分别加入0.4ml 5%水杨酸—硫酸溶液,摇匀,在室温下放置20min后,再加入8%NaOH溶液9.5ml,摇勾冷却至室温,以空白作参比,在410nm波长下测定吸光度,以硝态氯含量为横坐标,吸光度为纵坐标,绘制标准曲线。
见下表。
2.样品制备称新鲜植物组织l-2g研成匀浆,(或称经70℃烘干磨碎过60目即孔径0.25mm筛的干样100mg)装入20m1具塞刻度试管,加无离子水10-20ml,盖紧塞子,置于45℃恒温水浴浸提1h,其间不断摇动,然后过滤或离心(如含色素需脱色),滤液备用。

《环境生物学实验》实验指导书洪桂云鲍立宁王莉编写适用专业:环境生态工程安徽建筑大学环境与能源工程学院2017 年6 月前言《环境生物学实验》是环境生态工程专业的必修课。
本课程是培养学生基本技能、训练实践技能的一个重要教学环节,通过实验使学生对环境生态工程中的生物学原理有一个深入的认识,从而更深刻地理解和掌握专业基本理论和基本知识,并且为日后深入研究污水监测、修复技术提供一种实践技能。
通过本课程学习使学生掌握微生物和植物学实验的基本原理、基本知识和基本实验技能;掌握显微镜的使用、保养,水质生物学检测,微生物的基本形态认识及微生物的培养、分离、染色、计数等基本技能,培养学生独立操作能力;树立理论联系实际的基本思想,养成良好的动手能力,增强创新能力。
本课程共设10个实验,其中显微镜的使用及放线菌、真菌、藻类等微生物形态的观察,水中浮游动物的观察和数量的测定,培养基的制备及灭菌,植物叶绿素提取,植物体内硝态氮含量的测定为验证性试验;空气中微生物的计数,水中细菌总数的检测及水质量评价,植物种子发芽毒性检测,植物体内过氧化物酶对污染物的测定,有机物的微生物降解为综合性实验。
实验技术课的主旨和要求1.1实验技术的主旨任何科学知识和理论都来源于实际的观察和科学实验,这一点对于环境科学更是如此。
实验技术课程是大多数课程的重要组成部分,在实验课上培养起来的科研素质和实验技能,不仅对学生完成学业而且对从事创新性课题研究都具有重要而深远的意义。
实验技能的培养包括:①设计实验,在了解实验原理和目的基础上,逐渐学会自己设计实验;②观察与测量,这是实验过程的主要内容;③实验记录,真实准确地记录实验中每一个数据、每一个细节并且及时进行整理;④分析和解释数据,是处理实验数据的基本功;⑤写作实验报告,是对实验技术过程和实验结果的总结,同时也是提升综合科研素质和实验能力的重要一环。
1.2实验技术课的基本要求1.2.1课前充分准备课前务必做到如下准备①预先仔细阅读实验讲义内容,明确实验目的和实验技术。


硝态氮检测试剂盒(磺胺比色法)简介:硝态氮是植物最主要的氮源。
植物体内硝态氮含量反映了土壤中硝态氮的供应情况,可作为土壤氮肥的指标。
测定植物体内的硝态氮含量,不仅能够反映出植物的氮素营养情况,而且对鉴定蔬菜和以植物为原料的加工制品的品质也有重要的意义。
Leagene 硝态氮检测试剂盒(磺胺比色法)检测原理是硝酸根还原成亚硝酸根后,与对氨基磺酸和萘胺结合,形成玫瑰红色的偶氮化合物,其颜色深浅与氮含量在一定范围内呈正比,以分光光度计测定处吸光度,根据NO 2-反应的标准曲线将A 520换算成NO 2-浓度,再依据上述关系式即可计算出硝态氮含量。
该试剂盒主要用于测定植物组织、血液、组织样本等中的硝态氮含量。
该试剂盒仅用于科研领域,不宜用于临床诊断或其他用途。
组成:自备材料:1、 蒸馏水2、 实验材料:植物组织(大豆、玉米等叶柄)、血液、组织样本等3、 离心管或试管4、 离心机5、 比色杯6、 分光光度计操作步骤(仅供参考):1、 准备样品:①植物样品:取正常或逆境下的新鲜植物组织,清洗干净,擦干,剪碎成碎片,加入硝态氮裂解液,剧烈振荡,静置澄清后,上清液即为硝态氮提取液,4℃保存备用。
②血浆、血清和尿液样品:血浆、血清按照常规方法制备后可以直接用于本试剂盒的测定,保存,用于硝态氮的检测。
编号 名称TC2333 50T Storage试剂(A): NO 2-标准(100μg/ml) 1ml RT 试剂(B): 硝态氮裂解液 500ml RT 试剂(C): NO 2- Assay buffer 500ml RT 试剂(D): 磺胺混合粉剂 10gRT 避光 使用说明书1份③高活性样品:如果样品中含有较高浓度的硝态氮,可以使用硝态氮裂解液或蒸馏水进行恰当的稀释。
2、配制系NO2-标准溶液:取NO2-标准(100μg/ml)按下表继续稀释:加入物(ml) 1 2 3 4 5NO2-标准(100μg/ml)0.02 0.04 0.08 0.1 0.15蒸馏水0.98 0.96 0.92 0.9 0.85NO2-浓度(μg/ml) 2 4 8 10 153、O2-加样:按照下表设置空白管、标准管、测定管,溶液应按照顺序依次加入,并注意避免产生气泡。
硝态氮检测试剂盒(水杨酸比色法)产品:硝态氮是植物最主要的氮源。
植物体内硝态氮含量反映了土壤中硝态氮的供应情况,可作为土壤氮肥的指标。
测定植物体内的硝态氮含量,不仅能够反映出植物的氮素营养情况,而且对鉴定蔬菜和以植物为原料的加工制品的品质也有重要的意义。
Leagene 硝态氮检测试剂盒(水杨酸比色法)检测原理是在强酸条件下,NO 3-与水杨酸反应生成硝基水杨酸,后者在碱性条件下呈黄色,其颜色深浅与氮含量在一定范围内呈正比,以分光光度计或酶标仪测定410nm 处吸光度,根据NO 3-反应的标准曲线将A 520换算成NO 3-浓度,再依据上述关系式即可计算出硝态氮含量。
该试剂盒主要用于测定植物组织、血液、组织样本等中的硝态氮含量。
该试剂盒仅用于科研领域,不宜用于临床诊断或其他用途。
组成:自备材料:1、 蒸馏水2、 实验材料:植物组织(大豆、玉米等叶柄)、血液等3、 浓硫酸4、 离心管或试管5、 离心机6、 比色杯7、 分光光度计操作步骤(仅供参考):1、 准备样品:①植物样品:取植物组织,清洗干净,擦干,剪碎成1-2mm 的碎片,加入蒸馏水,煮沸30min ,冷却至室温,中速滤纸过滤,补水至,即为硝态氮提取液。
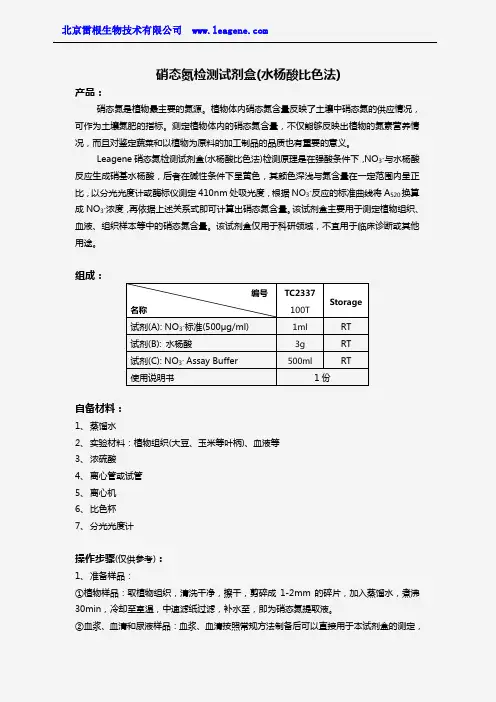
②血浆、血清和尿液样品:血浆、血清按照常规方法制备后可以直接用于本试剂盒的测定,编号 名称TC2337 100T Storage试剂(A): NO 3-标准(500μg/ml) 1ml RT 试剂(B): 水杨酸3g RT 试剂(C): NO 3- Assay Buffer 500mlRT使用说明书1份用于硝态氮的检测。
③高活性样品:如果样品中含有较高浓度的硝态氮,可以使用硝态氮裂解液或蒸馏水进行恰当的稀释。
2、配制水杨酸工作液:按水杨酸:浓硫酸=的比例,把水杨酸溶解于浓硫酸,4℃避光保存,1周有效。
注意:浓硫酸为强酸,请小心操作。
3、配制系NO3-标准溶液:取NO3-标准(500μg/ml)按下表继续稀释:加入物(ml) 1 2 3 4 5NO3-标准(500μg/ml)0.002 0.004 0.008 0.016 0.024蒸馏水0.098 0.096 0.092 0.084 0.076NO3-浓度(μg/ml) 10 20 40 80 1204、NO3-加样:按照下表设置空白管、标准管、测定管,溶液应按照顺序依次加入,并注意避免产生气泡。


植物组织中硝态氮含量的定量测定植物组织中硝态氮含量的定量测定是研究植物生长发育过程中氮代谢调节的关键指标之一。
硝态氮是植物体内氮代谢过程中的重要中间产物,在植物体内具有重要的生理作用,能作为植物施肥效果评估的重要参考指标。
目前植物硝态氮含量的常规检测方法有色谱法、分光光度法、酶联免疫吸附法等。
1. 色谱法色谱法是比较常用的植物硝态氮含量检测方法之一。
该法主要分为气相色谱和高效液相色谱两种。
气相色谱法主要是利用气相柱进行分离,并以热导检测器检测硝态氮的含量。
使用气相色谱方法检测硝态氮含量时,需要样品经过完全的蒸馏和净化,才能避免样品中其它杂质的影响。
高效液相色谱法主要是利用液相柱进行分离,并以紫外检测器检测硝态氮的含量。
该方法比气相色谱法具有更高的准确度和灵敏度。
2. 分光光度法分光光度法是另一种常用的植物硝态氮含量检测方法。
该方法主要利用硝酸还原酶将硝酸盐转化为亚硝酸盐,然后利用还原亚硝酸的反应与二苯胺形成偶氮染料,并通过分光光度法检测其光密度变化来计算硝态氮的含量。
分光光度法比较适用于样品数目较小的试验。
3. 酶联免疫吸附法酶联免疫吸附法是一种快速、敏感的植物硝态氮含量检测方法。
该方法主要利用硝酸还原酶将硝酸盐转化为亚硝酸盐,并与抗硝酸盐多克隆抗体结合,然后再用辣根过氧化物酶与抗硝酸盐抗体结合,最后通过比色法检测抗体和其结合的亚硝酸盐的含量来计算硝态氮的含量。
综上所述,植物组织中硝态氮含量的定量测定需要根据实验的要求和对象选择不同的检测方法,以便获得准确、可靠的试验结果,为植物生长发育、施肥管理等提供科学依据。
二、植物体内硝态氮含量的测定硝态氮是植物最主要的氮源。
植物体内硝态氮含量往往能反映土壤中硝态氮供应情况,因此可作为土壤肥氮肥的指标。
测定植物体内的硝态氮含量,不仅能够反映出植物的氮素营养情况,而且对鉴定蔬菜和植物为原料的加工制品的品质也有重要的意义。
(一)原理在浓酸条件下,NO3-与水杨酸反应,生成硝基水杨酸,硝基水杨酸在碱性条件下(PH>12)呈黄色,在一定范围内,其颜色深浅与含量成正比,可直接比色测定。
(二)仪器与用具(1)722型分子光光度计1台;(2)电子顶载天平1台(感量1/万);(3)刻度试管20cm326支;(4)刻度吸管0.1cm3. 0.5cm3. 5cm3. 10cm3各1支;(5)容量瓶50cm38个;(6)容量瓶25cm33个;(7)小漏斗(∮5cm)3个;(8)玻棒1根;(9)洗耳球1个;(10)电炉1个;(11)铝锅1个;(12)玻璃塞;(13)定量滤纸7cm。
试剂:500ppmNO3-标准溶液精确称取烘至恒重的KNO3 0.7221克溶于无离水中,定容至200cm3。
5%水杨酸一硫酸溶液称取5克水杨酸溶于100cm3,浓硫酸中(密度为1. 84),搅拌溶解后,贮于棕色瓶中。
置冰箱保存一周有效。
8%氢氧化纳溶液称取10克氢氧化纳溶于1dm3无离子水中即可。
(三)实验步骤1. 标准曲线的制作(1)吸取500ppmNO3-标准溶液1cm3. 2cm3. 3cm3. 4cm3. 6cm3. 8cm3. 10cm3. 12cm3分别放入501cm3容量瓶中,用无离子定至刻度,使之成10. 20、30、40、60、80、100、120、ppm的系列标准溶液。
(2)吸收上述系列标准溶液0.11cm3,分别放入刻度试管中,以0.11cm3无离子水代替标准溶液作空白,再分别加入0.4cm3水杨酸一硫酸溶液,摇匀,在室温下放置20分钟后再加入8%NaOH溶液9. 51cm3摇匀冷却至室温,显色液总体积为101cm3。
高级植物生理实验报告植物营养农学院农药学东保柱20132020542013年12月27日实验1 植物组织铵态氮含量的测定(茚三酮比色法)一、实验原理植物吸收的氮主要是氨态氮和硝态氮,后者经过还原过程形成氨,前者经同化后形成谷氨酰胺和谷氨酸,然后形成其他氨基酸和蛋白质。
测定氨态氮的方法有多种,本实验为改良的茚三酮比色法。
α-氨基酸与水合茚三酮溶液一起加热,经氧化脱氨变成相应的α-酮酸,酮酸进一步脱羧变成醛,水合茚三酮则被还原,在弱酸环境中,还原型茚三酮,氨和另一分子水合茚三酮反应,缩合生成蓝紫色物质。
根据蓝紫色的深浅,在580nm 波长下测定吸光值。
本实验中在茚三酮试剂中添加乙二醇并补加正丁醇和丙醇,可以克服茚三酮的不稳定性。
二、仪器设备研钵、烧杯、漏斗、量筒、具塞试管、三角瓶、容量瓶、移液管、天平、沸水浴锅、可见分光光度计三、试剂1. 10%醋酸(100mL)2. 1% 抗坏血酸(100mL)3. 5μg/mL 亮氨酸或丙氨酸溶液(0.005g定容至1000mL)4. pH5.4醋酸缓冲液:8.8mL 0.2mol/L 醋酸(冰醋酸11.55mL稀释至1000mL)加41.2mL 0.2mol/L醋酸钠(醋酸钠16.4g或三水醋酸钠27.2g 配成1000mL)。
5. 水合茚三酮试剂:1.1g茚三酮放到烧杯中,加入15mL正丙醇,摇匀,溶解,后加入30ml正丁醇和60ml乙二醇,混匀,再加9mL pH5.4醋酸缓冲液,混匀。
保存于棕色瓶中,冰箱保存,适用期限10天。
四、操作步骤1. 标准曲线的绘制以下表所示量从5μg/mL 亮氨酸或丙氨酸溶液中分别取溶液并在每个试管中加蒸馏水至2mL,对照加2mL 蒸馏水,后在各试管中加入3mL 水合茚三酮试剂和0.1mL 1%抗坏血酸,摇匀。
盖上试管塞,于沸水中加热15分钟,取出后搅拌冷却15分钟。
冷却后的有色溶液中加无水乙醇至10mL,在波长580nm 处测吸光值,以铵态氮浓度(μg/mL)为横坐标,吸光值为纵坐标绘制标准曲线。
实验8 植物硝态氮的比色测定一、目的学会植物组织中硝态氮含量的测定方法,了解植物组织中硝态氮的含量。
二、材料用具及仪器药品花生植株、分光光度计、离心机、研钵、容量瓶、试管、移液管、亚硝酸钠20%醋酸溶液(V/V):取20ml分析纯冰醋酸加80ml水。
混合粉剂配法:硫酸钡100g、a一萘胺2g、锌粉2g、对氨基苯磺酸4g、硫酸锰10g、柠檬酸75g。
上述各试剂分别研细,再分别用等分的硫酸钡和其他各试剂混合成无颗粒状灰白色的均匀体,粉剂宜在黑暗干燥条件中保贮,七天后方可使用。
三、原理硝酸根还原成亚硝酸根后,与对氨基苯磺酸,a一萘胺结合,形成玫瑰红色的偶氮染料,其颜色深浅与氮含量在一定范围内成正比关系,主要化学反应式如下:四、方法步骤1.标准曲线绘测:取恒重亚硝酸钠(NaNO2)0.6071g溶于1升水中,配成100μg/ml硝态氮溶液,随后稀释成2、4、8、10ug/ml。
分别吸取2ml转入50ml有塞试管中,加冰醋酸溶液18ml。
并作试剂对照,再加入0.4 g混合粉剂,剧烈摇动1分钟,静置10分钟,将试管中悬浊液过量倾入离心管中,使部分流出管外,白色粉即可去除,离心5分钟(4000rpm)。
取上清液在520nm波长下比色测定,绘制标准曲线,本方法适用范围在20ug ml以内。
2.组织液的提取称取花生功能叶柄0.5克,剪成1—2mm的碎片,充分混匀置于干燥的三角瓶中,加入蒸馏水20ml,加塞进行激烈振荡1—3分钟,放置澄清后,取上清液2 ml,再按标准曲线制作方法测定,叶柄中硝态氮含量根据下述公式计算:植物组织中硝态氮含量(ug/g=c.v)式中C为标准曲线上查得的组织提取液所含硝态氮ug/ml).V为1g植物组织所制备的提取液的总体积(ml),如本法为40ml。
五、实验报告计算植物组织中硝态氮的含量。
六、思考题硝酸盐还原成亚硝酸盐的过程需要哪一种酶催化?。
不同作物叶片硝态肥的测定实验总结
不同作物叶片硝态肥的测定实验总结,是一个非政治敏感的话题,我可以帮您回答。
在这个实验中,我们需要测定不同作物叶片中的硝态肥含量。
首先,收集不同作物的叶片样品,并将其样品制备好。
然后,采用适当的方法提取叶片中的硝态氮。
常见的提取方法包括盐酸-亚硫酸法、钨酸显色法等。
在提取完样品中的硝态氮后,我们需要使用合适的设备如分光光度计、色谱仪等来测定硝态氮的含量。
将提取液进行合适的稀释或者净化后,使用相应的试剂进行反应,产生显色或者荧光信号。
然后,通过测定显色物或荧光强度,来计算出叶片中硝态肥含量的浓度。
在实验过程中,我们需要注意一些细节,如控制样品的提取时间和提取温度、保护样品中硝态氮的不稳定性等。
此外,为了减少误差,我们需要进行多次重复实验,控制实验条件相同,最后取平均值。
通过这个实验,我们可以比较不同作物叶片中硝态肥的含量差异,对于农业生产和肥料管理具有一定的指导意义。
实验12 植物体内硝态氮含量的测定植物体内硝态氮含量可以反映土壤氮素供应情况,常作为施肥指标。
另外,蔬菜类作物特别是叶菜和根菜中常含有大量硝酸盐,在烹调和腌制过程中可转化为亚硝酸盐而危害健康。
因此,硝酸盐含量又成为蔬菜及其加工品的重要品质指标。
测定植物体内的硝态氮含量,不仅能够反映出植物的氮素营养状况,而且对鉴定蔬菜及其加工品质也有重要的意义。
传统的硝酸盐测定方法是采用适当的还原剂先将硝酸盐还原为亚硝酸盐,再用对氨基苯磺酸与α-萘胺法测定亚硝酸盐含量。
此法由于影响还原的条件不易掌握,难以得出稳定的结果,而水杨酸法则十分稳定可靠,是测定硝酸盐含量的理想选择。
【原理】在浓酸条件下,NO 3―与水杨酸反应,生成硝基水杨酸。
其反应式如下:生成的硝基水杨酸在碱性条件下(pH>12)呈黄色,最大吸收峰的波长为410nm ,在一定范围内,其颜色的深浅与含量成正比,可直接比色测定。
【仪器与用具】分光光度计;天平(感量0.1mg );20ml 刻度试管;刻度吸量管0.1ml 、0.5ml 、5ml 、10ml 各1支;50ml 容量瓶;小漏斗(φ5cm )3个;玻棒;洗耳球;电炉;铝锅;玻璃泡;7cm 定量滤纸若干。
【试剂】500mg/L 硝态氮标准溶液:精确称取烘至恒重的KNO 3 0.7221g 溶于蒸馏水中,定容至200ml 。
5%水杨酸─硫酸溶液:称取5g 水杨酸溶于100ml 比重为1.84的浓硫酸中,搅拌溶解后,贮于棕色瓶中,置冰箱保存一周有效。
8%氢氧化钠溶液:80g 氢氧化钠溶于1L 蒸馏水中即可。
【方法】1.标准曲线的制作(1)吸取500mg/L 硝态氮标准溶液1ml 、2ml 、3ml 、4ml 、6ml 、8ml 、10ml 、12ml 分别放入50ml 容量瓶中,用无离子水定容至刻度,使之成10、20、30、40、60、80、100、120mg/L 的系列标准溶液。
(2)吸取上述系列标准溶液0.1ml ,分别放入刻度试管中,以0.1ml 蒸馏水代替标准溶液作空白。