高效液相色谱法测定复方阿司匹林中有效成分
- 格式:doc
- 大小:28.50 KB
- 文档页数:3


高效液相色谱法测定阿司匹林肠溶片中阿司匹林含量本文采用高效液相色谱法(HPLC-VWD)对阿司匹林肠溶片中成分阿司匹林进行测定,对方法的系统适用性试验、特异性试验、精密度试验、检测限、定量限、线性关系和线性范围考察、重复性试验、准确度试验(加样回收试验)进行验证,证实本方法确实可靠。
本方法可测定浓度在0.999862mg/mL-0.01999724 mg/mL间的阿司匹林,检测下限可达0.1ug/mL。
标签:阿司匹林;HPLC-VWD;方法验证阿司匹林肠溶片的质量标准中,监测阿司匹林肠溶片中的阿司匹林含量是一项重要指标[1]。
本文采用高效液相色谱法测定阿司匹林肠溶片中的阿司匹林,分别对系统适用性试验、特异性试验、精密度试验、检测限、定量限、线性关系和线性范围考察、重复性试验、准确度试验(加样回收试验)进行验证[2]。
一、仪器与材料1.1 样品阿司匹林肠溶片(25mg)市售样品。
1.2 仪器及试药高效液相色谱仪:Thermo Fisher Ultimate 3000(VWD检测器)。
超声仪:上海科导SK7210LHC超声仪,35KHz。
色谱柱:Welch Xtimate C18(5um,150×4.6mm)。
0.45um有机性样品滤膜。
天平:赛多利斯电子天平(BSA224S-CW)(100g,0.01mg;220g,0.1g);梅特勒-托利多电子天平(MX5)(3g,0.001mg)。
试剂:甲醇,色谱级,德国默克,I866432 601。
乙腈:色谱纯,德国默克,JA050820。
四氢呋喃,色谱纯,德国默克,I826801615。
冰醋酸,分析纯,国药集团化学试剂有限公司,20140326。
水,为GB/T6682中规定的一级水。
阿司匹林,中国食品药品检定研究院,批号:100113-201405,纯度:99.8%。
水杨酸,中国食品药品检定研究院,批号:100106-201104,纯度:99.9%。

高效液相色谱法测定阿司匹林片的含量
一、目的
1.熟悉HPLC法测定的原理及操作。
2.掌握外标法测定阿司匹林片含量。
二、仪器与试药
1.仪器
美国PE型高效液相色谱仪Mettler AL204电子天平
容量瓶规格:50mL、100mL 刻度移液管规格:5mL
漏斗定量滤纸(直径10cm)
超声仪
2.试药
阿司匹林片规格:0.3g 阿司匹林对照品冰醋酸
氢氧化钾色谱甲醇超纯水
三、实验内容
1.色谱条件与系统适用性试验:用十八烷基硅烷键合硅胶为填充剂;以甲醇-1%冰醋酸(50:50)为流动相;流速为每分钟约1.0mL;检测波长280nm。
理论板数按阿莫西林峰计算应不低于1500。
2.对照溶液配制:取阿莫西林对照品适量,精密称定后,加1%冰醋酸无水甲醇溶液溶解并定量稀释制成每1mL中含50μg的溶液
3.样品测定:精密称取细粉适量(约相当于阿司匹林细粉0.05g),置50mL量瓶中,加1%冰醋酸无水甲醇溶液溶解并稀释至刻度,摇匀,精密量取续滤液3mL,置50 mL量瓶中,加1%冰醋酸无水甲醇溶液溶解并稀释至刻度,摇匀,取续滤液20μL注入液相色谱仪,记录色谱图;另取阿司匹林对照溶液同法测定。
按外标法以峰面积计算出样品中阿司匹林(C9H8O4)的含量。
本品含阿莫西林(C9H8O4)应为标示量的93.0%~107.0%。
四、注意事项:
1.高效液相色谱仪严格按照仪器操作规程操作。
2.小心进样操作,以免进样失败或损坏进样器。
五、思考题
高效液相色谱仪操作的注意事项有哪些?
六、参考文献
《中国药典》2010年版二部,285,化学工业出版社。

高效液相色谱法测定阿司匹林肠溶片中阿司匹林的含量-药学论文-基础医学论文-医学论文——文章均为WORD文档,下载后可直接编辑使用亦可打印——阿司匹林肠溶片为非甾体类抗炎药,临床可用于抗血栓,也可用于治疗不稳定性心绞痛,是《国家基本药物目录》列入的品种。
本文采用高效液相色谱法测定阿司匹林肠溶片中阿司匹林的含量,该方法简单,快速,重现性好,回收率高,可用于该制剂的质量控制。
1 仪器与试药1.1 仪器:大连依利特P230 型高效液相色谱仪;UV230+紫外可见检测器;手动进样器;超声仪(型号KQ5200E,功率200W,频率40KHz);电子天平(赛多利斯科学仪器有限公司,0.0001g)。
1.2 试药:阿司匹林对照品(中国食品药品检定研究院,批号:100113);阿司匹林肠溶片(亚宝药业太原制药有限公司,批号:131210;石家庄康力药业有限公司,批号:121037;神威药业集团有限公司,批号:1306072),甲醇为色谱纯,水为超纯水,其他试剂均为分析纯。
2 方法与结果2.1 色谱条件:色谱柱为Hypersil ODS2 柱(250mm4.6mm,5m);流动相:甲醇∶0.5%乙酸溶液(37∶63);流速:0.8mlmin-1;柱温:25∶;检测波长:267nm;理论板数按阿司匹林计不得少于3000。
2.2 溶液的制备:对照品溶液的制备:精密称取一定量阿司匹林对照品,置100ml 量瓶中,加1%醋酸甲醇溶解并定容制成100gml-1的对照品溶液。
供试品溶液的制备:取供试品(石家庄康力药业有限公司,批号:121037)约0.03g,精密称定,置100ml 量瓶中,用1%冰醋酸甲醇溶液溶解并定容,过滤,取续滤液,作为供试品溶液。
阴性样品溶液的制备:按处方比例取辅料制成空白制剂,按供试品溶液制备方法制成阴性样品溶液。
2.3 专属性实验:在2.1色谱条件下,分别吸取供试品溶液、对照品溶液、阴性样品溶液各10L,注入液相色谱仪,记录色谱图。
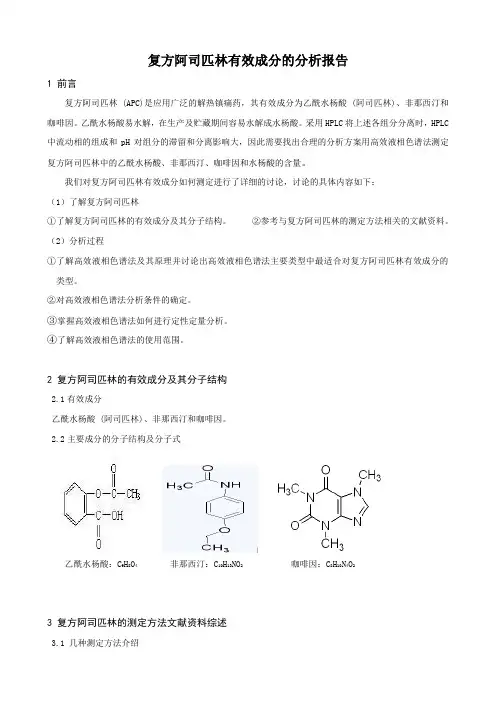
复方阿司匹林有效成分的分析报告1 前言复方阿司匹林 (APC)是应用广泛的解热镇痛药,其有效成分为乙酰水杨酸 (阿司匹林)、非那西汀和咖啡因。
乙酰水杨酸易水解,在生产及贮藏期间容易水解成水杨酸。
采用HPLC 将上述各组分分离时,HPLC 中流动相的组成和pH 对组分的滞留和分离影响大,因此需要找出合理的分析方案用高效液相色谱法测定复方阿司匹林中的乙酰水杨酸、非那西汀、咖啡因和水杨酸的含量。
我们对复方阿司匹林有效成分如何测定进行了详细的讨论,讨论的具体内容如下:(1)了解复方阿司匹林①了解复方阿司匹林的有效成分及其分子结构。
②参考与复方阿司匹林的测定方法相关的文献资料。
(2)分析过程①了解高效液相色谱法及其原理并讨论出高效液相色谱法主要类型中最适合对复方阿司匹林有效成分的类型。
②对高效液相色谱法分析条件的确定。
③掌握高效液相色谱法如何进行定性定量分析。
④了解高效液相色谱法的使用范围。
2 复方阿司匹林的有效成分及其分子结构2.1有效成分乙酰水杨酸 (阿司匹林)、非那西汀和咖啡因。
2.2主要成分的分子结构及分子式乙酰水杨酸:C 9H 8O 4 非那西汀:C 10H 13NO 2 咖啡因:C 8H 10N 4O 23 复方阿司匹林的测定方法文献资料综述3.1 几种测定方法介绍容量分析法、紫外分光光度法、酸碱滴定法、高效液相色谱分析法。
例如中国药典[1]中采用容量分析法、赵怀清等[2]用胶束薄层色谱法、罗国安等[3]用PLS-紫外光光度法、左文坚等[4]用区带毛细管电泳法等进行了测试研究。
但我们使用的方法是高效液相色谱法。
3.2 高效液相色谱法的简单介绍高效液相色谱法是20世纪70年代发展起来的一项高效、快速的分离分析技术。
其流动相为液体。
在经典的液体柱色谱法基础上,引入了气相色谱法的理论,在技术上采用了高压泵、高效固定相和高灵敏度检测器,实现了分析速度快,分离效率高和操作自动化。
它可用来进行液固吸附、液液分配、离子交换和空间排阻色谱分析,应用非常广泛。

临床医药文献电子杂志Electronic Journal of Clinical Medical Literature2019 年 第 6 卷第 30 期2019 Vol.6 No.30169·实验研究·高效液相色谱法测定复方阿司匹林片剂的含量葛炜炜(江苏省南通市中医院,江苏 南通 226000)【摘要】目的 使用高效液相色谱法测定复发阿司匹林片剂中阿司匹林的含量。
方法 仪器选择岛津安捷伦液相色谱仪,色谱柱采用Inertsil ODS-SP ,柱温30℃,进样量10 uL ,流动相采用水-乙腈,流速1.0 mL/min ,波长237 mm 。
结果 浓度在0.01~0.05 mg/mL 范围内的阿司匹林线性关系良好,平均回收率为101.81%,RSD 为0.69%。
结论 高效液相色谱法简单准确,在测定复方阿司匹林片剂中阿司匹林含量时十分适用。
【关键词】高效液相色谱法;复发阿司匹林片;含量测定【中图分类号】R917 【文献标识码】A 【文章编号】ISSN.2095-8242.2019.30.169.01复方阿司匹林片是非那西丁和阿司匹林两种药物的复方制剂,质量比约为1:50(8.4mg :400mg ),临床药学研究认为[1]复方阿司匹林片的作用大于非那西丁和阿司匹林两种药物单个作用的叠加,在治疗稳定或不稳定心绞痛、急性心肌梗死时有显著疗效,但复方阿司匹林片稳定性较差,配伍较为严重,因此在临床应用并不广泛,采取有效的检测方法对复方阿司匹林片各物质含量进行测定是分析药物稳定性,提高用药合理性的基础前提。
有研究指出[2-3]使用高效液相色谱法能准确测定阿司匹林含量,但采用水-甲醇的流动相体系时阿司匹林和水杨酸分离度不佳,降解严重,检测精密度无法达到要求。
本次研究采取水-乙腈为流动相,建立高效液相色谱法进行检测,结果表明分离度和准确性良好,现详述如下。
1 仪 器1.1 仪器和试剂仪器选择岛津安捷伦液相色谱仪,包括紫外检测器、自动进样器和四元输液泵。


阿司匹林的纯度检测及含量测定阿司匹林,作为一种常见的药物,在医药领域发挥着重要作用。
无论是用于缓解疼痛、退热,还是在心血管疾病的预防和治疗中,其纯度和含量的准确测定都至关重要。
这不仅关系到药物的疗效,还直接影响着患者的健康和安全。
要了解阿司匹林的纯度检测及含量测定,首先得清楚阿司匹林的化学性质。
阿司匹林的化学名称为乙酰水杨酸,其分子结构包含一个乙酰基和一个水杨酸基团。
纯度检测的方法多种多样。
其中,色谱法是一种常用且有效的手段。
高效液相色谱法(HPLC)可以精确地分离和检测阿司匹林中的杂质。
在进行 HPLC 分析时,样品会被注入到色谱柱中,不同的成分会在流动相的带动下以不同的速度通过色谱柱,从而实现分离。
通过与标准品的对比,可以判断样品中是否存在杂质以及杂质的种类和含量。
另一种常用的纯度检测方法是红外光谱法。
阿司匹林具有特定的红外吸收峰,通过对样品红外光谱的分析,可以与标准图谱进行对比,从而判断其纯度。
如果样品的红外光谱与标准图谱存在差异,就可能表明存在杂质。
而对于阿司匹林的含量测定,容量分析法是经典的方法之一。
比如酸碱滴定法,利用阿司匹林分子中的羧基能与碱发生中和反应的性质。
首先将阿司匹林溶解在适当的溶剂中,然后用已知浓度的碱溶液进行滴定,通过消耗碱溶液的体积来计算阿司匹林的含量。
此外,还有紫外分光光度法也常用于阿司匹林的含量测定。
阿司匹林在特定波长下具有一定的吸光度,通过测量样品在该波长下的吸光度,并与标准曲线对比,就可以计算出阿司匹林的含量。
在进行纯度检测和含量测定的实验过程中,有许多需要注意的事项。
首先是样品的处理,要确保样品充分溶解并且不发生分解或变质。
其次,实验所使用的试剂和仪器都需要经过严格的校准和验证,以保证实验结果的准确性。
在实际应用中,阿司匹林的纯度和含量测定对于药品生产企业来说意义重大。
在生产过程中,通过定期对产品进行检测,可以及时发现问题,调整生产工艺,确保产品质量符合标准。

CHINESE COMMUNITY DOCTORS 实验研究中国社区医师2020年第36卷第27期在2010年版《中国药典》阿司匹林类药物均包含了其有效成分含量测定项以及游离水杨酸限量的检查,两者的分析与处理方式一样,但检测波长存在差异,阿司匹林检测波长为276nm,水杨酸为303nm。
药典指出,测定阿司匹林类药物的有效成分含量与游离水杨酸限量时,采用甲醇处理样品易挥发,且易产生误差[1]。
本研究采用高效液相法(HPLC 法)对其有效成分含量与游离水杨酸限量进行测定,探究该方法的检测效果,为临床后期检测提供参考依据。
资料与方法仪器与试药:仪器为LC-2010A 高效液相色谱仪;VIS-7200A 型可见光分度计。
阿司匹林与水杨酸对照物;阿司匹林肠溶片,阿司匹林泡腾片;色谱纯包括甲醇与乙腈;超纯水;分析纯为其余试剂。
方法与结果:①制备溶液:将水杨酸对照品50mg 置于量瓶50mL 中,用1%冰乙酸乙醇溶液溶解定容,获得水杨酸贮备液1mg/mL。
再于量瓶50mL 中倒入贮备液5mL,再次定容,得到0.1mg/mL 的水杨酸工作液。
于量瓶100mL 内置入阿司匹林50mg ,5份,分别置入0、1.5mL、5.0mL、7.5mL、15mL 的水杨酸工作液1mg/mL,再用1%冰乙酸乙醇溶液溶解定容,得到0、0.3%、1.0%、1.5%、3.0%水杨酸的0.5mg/mL 阿司匹林对照液[2-3]。
取试药10片,研磨,并在100mL 烧杯中置入适量,并加上一定量的1%冰乙酸乙醇溶液,经过10min 超声,定量置入的量瓶100mL 中,随后过1%冰乙酸乙醇溶液定容并离心,供试品为离心后的上清液,阿司匹林肠溶片与上述制备方法相同,最终获得阴性对照液。
②色谱条件:Sepax GP-C18柱色谱柱,0.2%磷酸水溶液-乙腈流动相,测定28min,30℃,1.0mL/min 流速,303nm 波长,5μL 进样体积[4-5]。

高效液相色谱法测定复方阿司匹林中有效成分
用超纯水稀至lOOOmL摇匀。
4、液相色谱分离条件:G&色谱柱;流动相:甲醇:1%冰穂酸溶液(50: 50); 流速:1.0
ml/min;检测波长:276 nm;柱温:30°C o
5、标准曲线制作:将浓度分别为25、5()、125、250j.ig/mL阿司匹林标准溶液,进样
2()pL,二次进样,以浓度C(Mg/mL)对应二次测定峰面积平均值A制作工作曲线,并进行回归分析,得回归方程。
6、样品测定:将样品溶液用0.45pm的微孔滤膜过滤,进样20P L,分别进样二次,用回归
方程计算阿司匹林肠溶片中阿司匹林含量。
五、数据记录及处理
1•数据记录
C(ppm)Ai A2A平均
000
25177165.4171.2
50325.9328.6327.25
125796.9803.1800
250160&11609.91609
c样品672.1665.7668.9
2.标准曲线的绘制:
根据上表数据,以浓度(C)为横坐标,峰面积(A平均)为纵坐标作图,得到标准曲线如下图:
阿司匹林标准曲线
如有侵权请联系告知删除,感谢你们的配合!。

科技论坛高效液相色谱法测定复方阿司匹林片中阿司匹林的溶出度杨云雷1宋金环2(1、哈药集团制药总厂,黑龙江哈尔滨1500002、哈尔滨誉衡药业有限公司,黑龙江哈尔滨150000)复方阿司匹林片为一复方解热镇痛药,能恢复体温调节中枢感受神经元的正常反应性而起退热镇痛作用。
阿司匹林是一种历史悠久的解热镇痛药。
阿司匹林用于治感冒、发热、关节痛、风湿病,用于预防和治疗缺血性心脏病、心肺梗塞、脑血栓形成。
溶出度是指药物从片剂等固体制剂在规定溶剂中溶出的速度和程度。
高效液相色谱法(High Performance Liquid Chromatography \HPLC)以液体为流动相,采用高压输液系统,将具有不同极性的单一溶剂或不同比例的流动相泵入装有固定相的色谱柱,在柱内各成分被分离后,进入检测器进行检测,从而实现对试样的分析。
本文采用高效液相法,又根据本实验采用高效液相色谱法对复方阿司匹林片中的阿司匹林的溶出度进行了含量测定。
1仪器与试药1.1仪器:RC806溶出试验仪(北京中西远大科技有限公司);U-PLC 超高效液相色谱系统(沃特世科技(上海)有限公司);瑞士梅特勒-托利多M S 精密天平(梅特勒-托利多中国公司);GW-UN 超纯水器(北京普析通用仪器有限责任公司);DOA-P504-BN 无油隔膜真空泵(上海洽姆仪器科技有限公司);SCQ-1020超声波清洗器(上海声彦超声仪器有限公司);TU-1901双光束紫外可见分光光度计(北京普析通用仪器有限责任公司)。
1.2色谱柱:奥泰公司C18色谱柱(284mm ×4.6mm,5μm)。
1.3对照品:阿司匹林购自中国药品生物制品检定所。
1.4试剂:甲醇为色谱纯;水为纯化水,其它试剂均为分析纯。
1.5试药:复方阿司匹林片。
1.6人工胃液配置:取氯化钠2.0g,加盐酸7mL,加水至1000mL 。
2测定方法确定2.1色谱条件依据查阅文献及考查的结果,确定色谱条件如下。
高效液相色谱法同时测定复方阿司匹林片中各种有效成分及游离水杨酸周考文;刘玉红;纪晓琳;张斌【期刊名称】《生命科学仪器》【年(卷),期】2005(003)006【摘要】利用HPLC法同时测定APC片中阿司匹林(A)、非那西汀(P)、咖啡因(C)和游离水杨酸的含量.在C18柱上以甲醇-水-乙酸-磷酸(体积比46.0:52.0:1.5:0.5)为流动相,在流速0.8mL·min-1和检测波长279nm时,三种有效成分和游离水杨酸都能被很好地检测.A组分在0.27~80.27.μg·mL-1范围内的回归方程为Y=1415.5X+11278,相关系数为0.9998,平均回收率为99.84%;P组分在0.19~57.34μg·mL-1范围内的回归方程为Y=1730.8X+624.7,相关系数为0.9996,平均回收率为100.29%;C组分在0.04~12.39μg·mL-1范围内的回归方程为Y=656.2X+6635.2,相关系数为0.9996,平均回收率为100.57%.方法适用于APC 片中各成分的同时测定.【总页数】3页(P31-33)【作者】周考文;刘玉红;纪晓琳;张斌【作者单位】北京联合大学生物化学工程学院,北京,100023;北京联合大学生物化学工程学院,北京,100023;北京联合大学生物化学工程学院,北京,100023;北京联合大学生物化学工程学院,北京,100023【正文语种】中文【中图分类】R9【相关文献】1.高效液相色谱法同时测定复方乙酰水杨酸片中各有效成分的含量 [J], 王腾;王晓敏;张亚运;姜玉婷;张志红;沈齐英2.高效液相色谱法测定复方乙酰水杨酸片中游离水杨酸含量 [J], 李锐;赵琪钟3.HPLC法测定菊蓝抗流感片中乙酰水杨酸和游离水杨酸的含量 [J], 袁晓芳;张同波;郝立芳4.高效液相色谱法测定阿司匹林肠溶片中游离水杨酸的含量 [J], 王卫;孙悦5.高效液相色谱法测定复方阿司匹林片中阿司匹林的溶出度 [J], 杨云雷;宋金环因版权原因,仅展示原文概要,查看原文内容请购买。
现行版《中国药典》中阿司匹林制剂含量测定方法《中国药典》中阿司匹林制剂含量测定方法主要有两种,分别是非溶剂萃取滴定法和高效液相色谱法。
以下将对这两种方法进行详细介绍。
一、非溶剂萃取滴定法非溶剂萃取滴定法是根据阿司匹林和碘化钾在氯仿中反应生成碘仿和氯化铯的性质,通过滴定法分析阿司匹林的含量。
具体步骤如下:1.取1g阿司匹林制剂,粉碎并称定准确质量。
将其置于锥形瓶中。
2.加入50mL氯仿,并摇匀,使阿司匹林溶解。
3.加入几滴硬脂酸二十酯溶液,防止氯仿挥发。
4. 加入一定量的0.1mol/L碘化钾溶液,并用碘酊滴定至淡黄色为止。
记下滴定所需的溶液体积V15.重复上述步骤,用纯化水代替阿司匹林制剂进行滴定,得到滴定所需的溶液体积V26. 计算阿司匹林的含量:阿司匹林的含量(mg/g)=(V1-V2)×0.346二、高效液相色谱法高效液相色谱法是利用高效液相色谱仪对阿司匹林制剂中阿司匹林的保持时间进行测定,根据保持时间与标准品的对照关系来测定阿司匹林的含量。
具体步骤如下:1.选取适宜的色谱柱和流动相。
2.首先对色谱柱进行平衡,保证色谱柱完全脱离有机溶剂并处于稳态。
3.准备阿司匹林制剂溶液,经过适当稀释后,用注射器将样品注入色谱柱,进行进样。
4.通过流动相和柱温的调节,使样品在色谱柱内迅速分离。
5.仪器记录阿司匹林的保持时间,并与标准阿司匹林品进行对照。
6.根据阿司匹林的保持时间与标准品的对照关系,计算出阿司匹林的含量。
以上就是《中国药典》中阿司匹林制剂含量测定方法的介绍。
这两种方法都可以用来测定阿司匹林制剂的含量,并且具有一定的准确性和重复性。
在实际应用中,选取适合的方法进行检测,可以帮助保证阿司匹林制剂的质量和安全性。
石河子大学生命科学学院设计实验报告复方阿司匹林有效成分的检测学院:生命科学学院专业:生物科学班级:生科二班姓名:米桃桃20151006043孙淑文20151006057指导老师:王爱英复方阿司匹林中有效成分的分析测定实验设计一、实验题目复方阿司匹林中有效成分的分析测定二、实验目的1.掌握复方阿司匹林中有效成分的分析方法2.分析得出复方阿司匹林中有效成分3.培养综合知识的运用能力。
三、实验原理复方阿司匹林是用于感冒发热、头痛、神经痛、牙痛、肌肉痛、月经痛等的治疗的药物。
其主要成分有阿司匹林、非那西丁和咖啡因。
我们用紫外分光光度法进行定量分析,其具有快速、灵敏度高及分析混合物中各组分有时不需要事先分离等优点。
四、仪器及药品药品/试剂:复方阿司匹林、乙酰水杨酸的标准溶液、0.1mol/LNaOH 溶液仪器:单波长分光光度计(氘灯、单色器、石英吸收池、斩光器、检测器)、显示器、电子天平、移液管(1,2,3,4,5ml)、烧杯、容量瓶(100ml的1个,50ml的6个)、吸耳球、洗瓶、胶头滴管、玻璃棒2个、10ml量筒、比色皿两套五、实验过程1.乙酰水杨酸标准溶液的制备:准确称取0.0500g的乙酰水杨酸置于100ml的烧杯中,用0.1mol/LNaOH溶解后,转移到100ml容量瓶中,以0.1mol/LNaOH溶液稀释至刻度,摇匀。
此溶液浓度为0.5mg/ml。
2.将5个50ml容量瓶按1-5号依次编号。
分别取乙酰水杨酸标准溶液1.00、2.00、3.00、4.00、5.00ml于相应编号的容量瓶中,各加入0.1mol/LNaOH溶液,稀释至刻度,摇匀。
3.波长选择:用1ml石英吸收池,以0.1mol/LNaOH作为参比溶液,在230~350nm波长范围内测定一份乙酰水杨酸标准溶液的紫外吸收光谱,确定最大吸收波长。
4.标准曲线绘制:在选定的波长下,以0.1mol/LNaOH溶液作为参比溶液,由低浓度到高浓度测定乙酰水杨酸标准溶液系列以及未知溶液的吸光度。
高效液相色谱法测定阿司匹林片的含量高效液相色谱法测定阿司匹林片的含量一、目的1.熟悉HPLC法测定的原理及操作。
2.掌握外标法测定阿司匹林片含量。
二、仪器与试药1.仪器美国PE型高效液相色谱仪Mettler AL204电子天平容量瓶规格:50mL、100mL 刻度移液管规格:5mL漏斗定量滤纸(直径10cm)超声仪2.试药阿司匹林片规格:0.3g 阿司匹林对照品冰醋酸氢氧化钾色谱甲醇超纯水三、实验内容1.色谱条件与系统适用性试验:用十八烷基硅烷键合硅胶为填充剂;以甲醇-1%冰醋酸(50:50)为流动相;流速为每分钟约1.0mL;检测波长280nm。
理论板数按阿莫西林峰计算应不低于1500。
2.对照溶液配制:取阿莫西林对照品适量,精密称定后,加1%冰醋酸无水甲醇溶液溶解并定量稀释制成每1mL中含50μg的溶液3.样品测定:精密称取细粉适量(约相当于阿司匹林细粉0.05g),置50mL量瓶中,加1%冰醋酸无水甲醇溶液溶解并稀释至刻度,摇匀,精密量取续滤液3mL,置50 mL量瓶中,加1%冰醋酸无水甲醇溶液溶解并稀释至刻度,摇匀,取续滤液20μL注入液相色谱仪,记录色谱图;另取阿司匹林对照溶液同法测定。
按外标法以峰面积计算出样品中阿司匹林(C9H8O4)的含量。
本品含阿莫西林(C9H8O4)应为标示量的93.0%~107.0%。
四、注意事项:1.高效液相色谱仪严格按照仪器操作规程操作。
2.小心进样操作,以免进样失败或损坏进样器。
五、思考题高效液相色谱仪操作的注意事项有哪些?六、参考文献《中国药典》2010年版二部,285,化学工业出版社。