有机物的结构(表示与空间构型)
- 格式:pptx
- 大小:383.30 KB
- 文档页数:18

clf3的杂化类型和空间构型1.引言1.1 概述首先,我们来概述一下本文将要讨论的主题:clf3的杂化类型和空间构型。
CLF3是指氯氟二氯亚磷酸酯,它是一种很重要的有机化合物,广泛应用于化学工业和生物医学领域。
在本文的正文部分,我们将详细探讨clf3的杂化类型和空间构型。
首先,我们将介绍clf3的杂化类型,包括sp3、sp2和sp杂化。
这些杂化类型决定了clf3分子中原子之间的键的类型和性质,对于理解clf3的化学性质及其反应机制至关重要。
我们将深入探讨不同杂化类型在clf3分子中的分布和效果,并探讨其在化学反应中的作用。
接着,我们将研究clf3的空间构型。
空间构型描述了氯氟二氯亚磷酸酯分子中原子之间的空间排列方式。
在研究空间构型时,我们将讨论clf3分子的平面构型、立体构型以及可能的几何异构性。
通过分析clf3的空间构型,我们可以更加深入地了解clf3分子的立体化学性质和空间取向。
本文的目的在于通过对clf3的杂化类型和空间构型的研究,增进我们对该化合物的认识和理解。
同时,通过对clf3的杂化类型和空间构型的分析,我们也可以展望进一步研究的方向,拓展对clf3分子的应用和改进的可能性。
总而言之,本文将探讨clf3的杂化类型和空间构型,通过对其杂化类型和空间构型进行分析,深入了解clf3分子的化学性质和立体构型,并展望进一步研究的方向。
这将有助于我们更好地理解和应用clf3这一重要有机化合物。
1.2文章结构文章结构部分主要介绍了整篇文章的组织结构和各个章节的内容概述。
本文的结构可以分为引言、正文和结论三个部分。
引言部分旨在介绍本文的研究背景和目的。
简要概述了clf3的杂化类型和空间构型以及本文的目的。
通过引言,读者可以对本文的主要内容和意义有一个初步的了解。
正文部分是本文的主体,包括了clf3的杂化类型和空间构型的详细讨论。
在2.1小节中,将详细介绍clf3的杂化类型。
这部分将重点分析clf3杂化类型的定义、特征和应用领域,并给出相关的研究成果和实例展示。

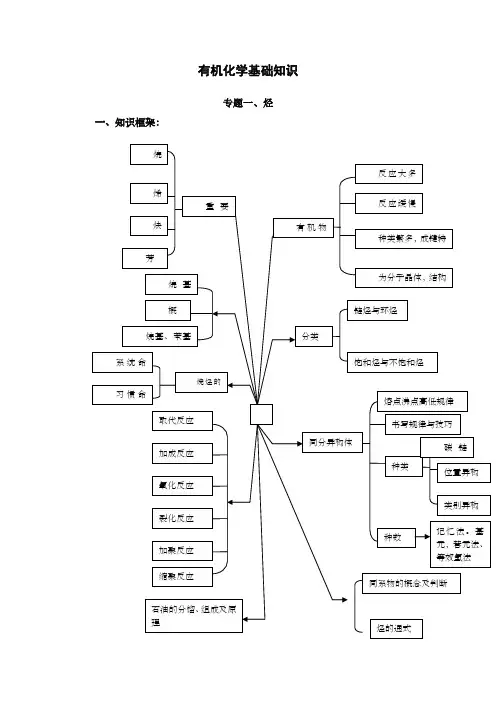
有机化学基础知识专题一、烃一、知识框架:二:有机物的结构、分类与命名一、有机物中碳原子的成键特点:有机物通常指含碳元素的化合物,或碳氢化合物及其衍生物总称为有机物。
其中碳原子最外层有四个电子,可以形成四跟键,碳碳之间既能形成单键,又能形成双键和三键,结合总成有机物的元素多种多样,从而决定了有机物种类的繁多。
二、有机物分子的空间构型与碳原子成键方式的关系3、有机物结构的表示方式:结构式、结构简式、键线式(1)结构式——完整的表示出有机物分子中每一个原子的成键情况。
(2) 结构简式——结构式的缩减形式a、结构式中表示单键的“——”可以省略,例如乙烷的结构简式为:CH3CH3b、“C=C”和“C≡C”中的“=”和“≡”不能省略。
例如乙烯的结构简式不能写为:CH2CH2,可是醛基、羧基则可简写为—CHO和—COOHc、准确表示分子中原子的成键情况。
如乙醇的结构简式可写成CH3CH2OH或C2H5OH而不能写成OHCH2CH3(3)键线式——只要求表示出碳碳键和与碳原子相连的基团,一个拐点和终点均表示一个碳原子。
4、同分异构现象有机物中存在分子式相同,结构不同的现象叫做同分异构现象,具有同分异构现象的化合物互称为同分异构体。
同分异构现象并非仅存在于有机物中,在无机物中也是存在的,如氰酸和异氰酸5、同分异构体的种类及肯定方式①碳链异构——由于碳原子的排列方式不同引发的同分异构现象A 首先写出无支链的烷烃碳链,即取得一种异构体的碳架结构。
B 在主链上减一个碳作为一个支链(甲基),连在此碳链上得出含甲基的同分异构体。
C在主链上减两个碳作为一个乙基支链或两个甲基的各类通分异构体。
②官能团位置异构在有机物中,有机物官能团位置的不同也会致使同分异构现象,比如:丙醇就有两种同分异构体:CH 3CH 2CH OH 和 CH 3CHCH 3A 先排碳链异构,再排官能团位置B 甲基上的3个H 位置相同C 处于对称位置的H ,具有相同的化学环境,因此当官能团取代这些H 时,有机物具有同一种结构③官能团类别异构: 例如:分子式为C 2H 6O 的有机物可能有乙醇和乙醚 A 碳原子数相同的醇和醚是同分异构体 B 碳原子数相同的羧酸和酯是同分异构体C 碳原子数相同的二烯烃和炔烃是同分异构体D 碳原子数相同的烯烃和环烷烃是同分异构体 ④立体异构A 顺反异构(存在于烯烃中)反式:相同基团在双键对角线位置 顺式:不同基团在双键对角线位置 B 对映异构——存在于手性分子中a 、手性分子——若是一对分子,它们的组成和原子的排列方式完全相同,但犹如左手和右手一样互为镜像,在三维空间里不能重叠,这对分子互称为手性异构体。

化学中的分子结构和空间构型分子结构和空间构型是化学中的重要概念,它们对于理解分子性质和反应机制具有重要意义。
在化学中,分子结构指的是分子中原子的相对位置和连接方式,而空间构型则描述了分子在三维空间中的排列方式。
本文将从分子结构和空间构型的基本概念、分子结构的表示方法和空间构型的分类等方面进行阐述。
首先,分子结构是指分子中原子之间的连接方式和排列。
原子之间的连接通过共价键或离子键实现,而原子之间的排列、相对位置则决定了分子的性质和反应行为。
分子结构的表示通常使用结构式、线角式、空间填充式等形式。
其中,结构式是一种常用的表示方法,它通过线段和点的连接来表达分子中的原子和它们之间的键。
线角式则通过将原子用线段表示,连接处的角度表示键的方向。
空间填充式则是以实心球来表示原子,通过球的大小来表示原子的大小,以及原子之间的空间关系。
这些表示方法可以有效地帮助我们理解分子结构和进行分子的模拟研究。
其次,空间构型描述了分子在三维空间中的排列方式。
分子的空间构型与原子的相对位置和取向有关,因此空间构型也影响着分子的性质和反应机制。
常见的空间构型包括线性构型、平面构型、三角锥构型、四面体构型等。
线性构型指的是分子中原子的排列呈直线状,如氨分子等。
平面构型指的是分子中原子排列在同一平面上,如苯分子等。
三角锥构型指的是分子中一个原子为顶点,其余原子排列在底面的三角形上,如三氯化硼分子等。
四面体构型指的是分子中一个原子为中心,三个原子排列在其周围的三个顶点上,如甲烷分子等。
空间构型的不同将导致分子具有不同的对称性和性质,进而影响分子的化学反应。
另外,化学中的分子结构和空间构型还涉及到立体化学的研究。
立体化学是研究分子空间构型和立体异构体的学科,它对于理解分子的构建和反应机理非常重要。
在研究立体化学时,我们常常使用斜角投影法和虚化键线法等技术来表示分子的三维构型。
斜角投影法是一种常用的表示方法,它使用斜线和角度表示分子中的原子和键,可以清晰地展示分子的空间构型。


有机化合物的结构除了分子式,有机化合物的结构还可以通过分子模型来描述。
分子模型使用球和棒表示原子和键的结构。
原子通常使用彩色小球表示,而连接原子的化学键则使用棒状物表示。
有机化合物的结构包括分子中原子之间的连接方式以及它们在空间中的排列方式。
分子中原子之间的连接通常使用共价键来实现。
共价键是一种通过原子之间的电子共享来保持原子在一起的键。
这种共享可以将原子连接成链、环和分支等不同的结构。
化合物中的共价键可以是单键、双键或三键,它们的强度和长度会有所不同。
有机化合物的结构也涉及键的性质。
共价键可以是极性的或非极性的。
极性键是由于连接原子之间电子的不均匀分布而产生的。
一个极性键可能会由于一个原子吸引更多的电子而带有部分负电荷,而另一个原子可能会带有部分正电荷。
这种区分正负电荷的分布对于有机化合物的反应和性质具有重要影响。
另一个重要的结构概念是立体化学。
立体化学描述了有机化合物中原子或基团在空间中的排列方式。
有机化合物可以具有手性和非手性结构。
手性分子是在镜面上不对称的分子,它们可以存在两个镜像异构体,称为对映体。
非手性分子是镜面对称的分子,它们没有对映体。
手性分子和非手性分子可以具有不同的化学性质,并且在生物学和药学领域中具有重要的应用。
至此所述,有机化合物的结构是通过分子式和分子模型来描述的。
分子式提供了关于元素的数量和种类的信息,而分子模型则展示了原子之间的连接方式和在空间中的排列方式。
这些结构信息对于理解有机化合物的性质和反应机理至关重要,也对于合成有机化合物和设计新药物具有重要意义。

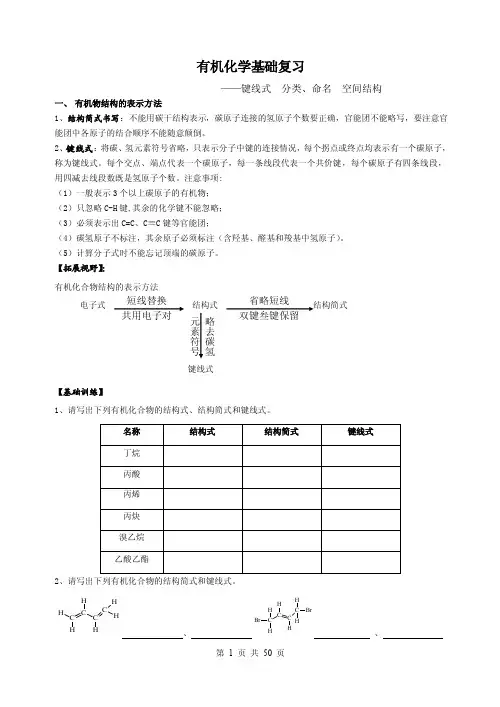
有机化学基础复习——键线式 分类、命名 空间结构一、 有机物结构的表示方法1、结构简式书写:不能用碳干结构表示,碳原子连接的氢原子个数要正确,官能团不能略写,要注意官能团中各原子的结合顺序不能随意颠倒。
2、键线式:将碳、氢元素符号省略,只表示分子中键的连接情况,每个拐点或终点均表示有一个碳原子,称为键线式。
每个交点、端点代表一个碳原子,每一条线段代表一个共价键,每个碳原子有四条线段,用四减去线段数既是氢原子个数。
注意事项: (1)一般表示3个以上碳原子的有机物; (2)只忽略C-H 键,其余的化学键不能忽略; (3)必须表示出C=C 、C ≡C 键等官能团;(4)碳氢原子不标注,其余原子必须标注(含羟基、醛基和羧基中氢原子)。
(5)计算分子式时不能忘记顶端的碳原子。
【拓展视野】:有机化合物结构的表示方法电子式结构式 结构简式键线式【基础训练】1、请写出下列有机化合物的结构式、结构简式和键线式。
2、请写出下列有机化合物的结构简式和键线式。
C CC C HHHHH H、C C C C H BrH BrHHH H、略去碳氢元素符号短线替换 共用电子对省略短线 双键叁键保留CH 3CH 2CH 2CH3CH 3CHCH 2CH 3CH3CH 3CH CHCH3C C C C HH HH HHH H、3、有机化合物的结构简式可进一步简化,如:请写出下列有机物分子的分子式:⑪ ; ⑫ ;⑬Cl;⑭ ;(5)OO; (6)OOH。
二、 有机物命名1、系统命名法命名含官能团的简单有机物的基本步骤是: (1) __________________。
A 、选择官能团中没有碳原子数,则母体的必须_________的碳链作主链。
B 、官能团中俼碳原子,则母体的必须尽可能多地 。
(2) _________________。
(3)__________________。
2、命名的5个必须:①取代基的位号必须用阿拉伯数字“2,3,4,……”表示;②相同取代基的个数,必须用中文数字“二、三、四,……”表示; ③位号2,3,4等相邻时,必须用逗号“,”表示(不能用顿号“、”); ④名称中凡阿拉伯数字与汉字相邻时,必须用短线“-”隔开;⑤若有多种取代基,不管其位号大小如何,都必须把简单的写在前面,复杂的写在后面。
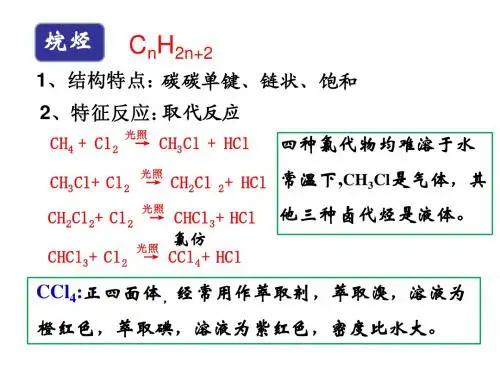

一. 四种基本构型及简单变换:甲烷、乙烯、乙炔、苯1.甲烷的正四面体结构:在甲烷分子中,一个碳原子和任意两个氢原子可确定一个平面,其余两个氢原子分别位于平面的两侧,即甲烷分子中有且只有三原子共面(称为三角形规则)。
当甲烷分子中某氢原子被其他原子或原子团取代时,,可将它看作是原来氢原子位置。
CH 3CH 3左侧甲基和②C 构成“甲烷”分子,此分子中④H 、①C 、②C 构成三角形,同理①C 、②C 、③H 也构成了三角形,即乙烷分子中最多有2个碳原子(①C 、②C )和2个氢原子(③H 、④H )4个原子共面。
CH 3CH 2CH 3其结构式可写成如图2所示。
左侧甲基和②C 构成“甲烷分子”。
此分子中⑤H ,①C ,②C 构成三角形。
中间亚甲基和①C ,③C 构成“甲烷”分子。
此分子中①C ,②C ,③C 构成三角形,同理②C ,③C ,④H 构成三角形,即丙烷分子中最多三个碳原子(①C ,②C ,③C )两个氢原子(④H ,⑤H)五原子可能共面。
2.乙稀的平面结构:乙烯分子中的所有原子都在同一平面内,键角为120°。
当乙烯分子中某氢原子被其他原子或原子团取代时,则代替氢原子的原子一定在乙烯的平面内。
其结构式可写成如图4所示。
三个氢原子(①②③)和三个碳原子(④⑤⑥)六原子一定共面。
根据三角形规则[⑤C ,⑥C ,⑦H构成三角形]。
⑦H 也可能在这个平面上。
最多7原子共面。
同理可推出CH 3CH=CHCH 3至少6个原子,至多8个原子共面。
(CH 3)2C=C(CH 3)2至少6个原子(6个碳原子),至多10个原子共面(6个碳原子和4个氢原子),每个甲基可提供一个氢原子在乙烯平面.3.苯的平面结构苯分子所有原子在同一平面内, 键角为120°。
当苯分子中的一个氢原子被其他原子或原子团取代时,代替该氢原子的原子一定在苯分子所在平面内。
甲苯中的7个碳原子(苯环上的6个碳原子和甲基上的一个碳原子),5个氢原子(苯环上的5个氢原子)这12个原子一定共面。
有机化合物的r构型与s构型有机化合物的构型分为R构型和S构型,用于描述分子空间位置的立体化学特征。
这两种构型是基于施密特命名法(Cahn-Ingold-Prelog命名法)而得出的。
施密特命名法基于一系列的规则,以给予有机化合物中手性中心的排列次序进行命名。
手性中心指的是一个碳原子,其上连接了四个不同的取代基团。
为了区分这四个取代基团之间的排列方式,施密特命名法引入了R构型和S构型的概念。
R构型和S构型可以通过以下步骤来确定:1. 确定手性中心:找到有机化合物中的手性中心,即一个碳原子,其上连接了四个不同的取代基团。
2. 给予优先级:对于每个手性中心,为其连接的取代基团分配优先级。
这可以通过比较取代基团所连接的原子的原子序数来确定。
原子序数越大,其优先级越高。
3. 确定相对位置:将取代基团的优先级从高到低排列。
如果优先级最高的取代基团在垂直向上,其他取代基团按顺时针方向排列,则为R构型。
相反,如果优先级最高的取代基团在垂直向上,其他取代基团按逆时针方向排列,则为S构型。
R构型和S构型是对有机化合物立体结构的描述,主要用于区分光学异构体。
光学异构体是指化学结构相同但在空间构型上有所不同的分子。
R构型和S构型的命名方式能够清晰地描述化合物中各个取代基团之间的空间排列关系。
这有助于我们理解分子的立体化学特征,并为有机合成和药物研发提供指导。
总结来说,R构型和S构型是用于描述有机化合物空间排列关系的构型命名方法,其基于施密特命名法的规则。
通过辨别手性中心上连接的取代基团的优先级和相对位置,我们可以确定有机化合物的R构型或S构型。
这种命名方法对于理解和描述有机化合物的立体化学特征非常重要。