初中化学化合价一览表---王健版
- 格式:xls
- 大小:45.00 KB
- 文档页数:1
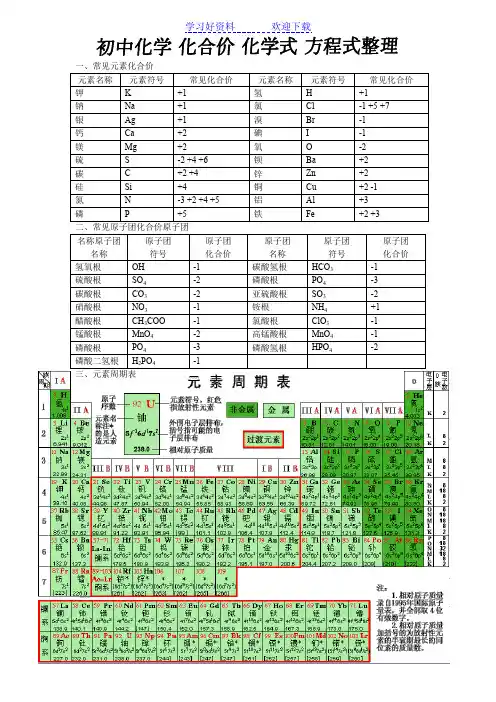
一、常见元素化合价四、化学式1、非金属单质:1、氢气H2金刚石/石墨C 氮气N2氧气O2磷P 硫S 氯气Cl22、金属单质:钠Na 镁Mg 铝Al 钾K 钙Ca 铁Fe 锌Zn 铜Cu 钡Ba 钨W 汞Hg3、非金属氧化物:水H2O 一氧化碳CO 二氧化碳CO2 五氧化二磷P2O5二氧化氮NO2二氧化硅SiO2二氧化硫SO2三氧化硫SO3一氧化氮NO4、金属氧化物:氧化镁MgO 氧化铜CuO 氧化钡BaO 氧化亚铜Cu2O 氧化钠Na2O 氧化亚铁FeO三氧化二铁(铁红)Fe2O3四氧化三铁Fe3O4三氧化二铝Al2O3三氧化钨WO3氧化银Ag2O 氧化铅PbO 二氧化锰MnO25、常见的酸:硫酸H2SO4盐酸HCl 硝酸HNO3磷酸H3PO4硫化氢H2S 溴化氢HBr 碳酸H2CO3醋酸CH3COOH6、常见的碱:氢氧化钠NaOH 氢氧化钙Ca(OH)2氢氧化钡Ba(OH)2氢氧化镁Mg(OH)2氢氧化铜Cu(OH) 2氢氧化钾KOH 氢氧化铝Al(OH) 3氢氧化铁Fe(OH) 3氢氧化亚铁Fe(OH) 27、常见的盐—氯化物/盐酸盐:氯化钾KCl 氯化钠(食盐)NaCl 氯化镁MgCl2氯化钙CaCl2氯化铜CuCl2氯化锌ZnCl2氯化钡BaCl2氯化铝AlCl3氯化亚铁FeCl2氯化铁FeCl3氯化银AgCl8、常见的盐—硫酸盐:硫酸铜CuSO4硫酸钡BaSO4硫酸钙CaSO4硫酸钾K2SO4硫酸镁MgSO4硫酸亚铁FeSO4硫酸铁Fe2 (SO4) 3硫酸铝Al2 (SO4) 3硫酸氢钠NaHSO4硫酸氢钾KHSO4亚硫酸钠NaSO39、常见的盐—硝酸盐:硝酸钠NaNO3硝酸钾KNO3硝酸银AgNO3硝酸镁MgNO3硝酸铜Cu(NO3) 2硝酸钙Ca(NO3) 2亚硝酸钠NaNO310、常见的盐—碳酸盐/碳酸氢盐:碳酸钠Na2CO3碳酸氢钠NaHCO3碳酸钙CaCO3碳酸镁MgCO3碳酸钾K2CO3碳酸氢钾KHCO311、常见的盐—酸式盐/碱式盐:碳酸氢钠NaHCO3碳酸氢钾KHCO3碳酸氢铵NH4HCO3磷酸二氢钾KH2PO4 / 碱式碳酸铜Cu2 (OH) 2CO312、常见有机物:甲烷CH4乙炔C2H2甲醇CH3OH 乙醇C2H5OH 乙酸CH3COOH13、常见结晶水合物:石膏CaSO4•2H2O 明矾KAl(SO4) 2•12H2O 绿矾FeSO4•7H2O 蓝矾CuSO4•5H2O碳酸钠晶体Na2CO3•10H2O14、常见化肥:尿素CO(NH2) 2硝酸铵NH4NO3硫酸铵(NH4) 2SO4碳酸氢铵NH4HCO3磷酸二氢钾KH2PO415、常见沉淀及其颜色:碳酸钙CaCO3(白色)氯化银AgCl(白色)碳酸钡BaCO3(白色)硫酸钡BaSO4(白色)氢氧化亚铁Fe(OH) 2(白色)硫化锌ZnS (白色)硫化锑Sb2S3(橙红色)氢氧化铁Fe(OH) 3(红褐色)氢氧化铜Cu(OH)2(天蓝色)硫化铁FeS (黑色)氢氧化铝Al(OH) 3(白色)二氧化锰MnO2(黑色)氢氧化银AgOH (白色)磷酸银Ag3PO4(白色)硫酸钙CaSO4(白色)碳酸银Ag2CO3(淡黄色)二硫化铁FeS2(黄色)氢氧化镁Mg(OH) 2(白色)硫酸铅PbSO4(白色)碱式碳酸铜Cu(OH) 2CO3(暗绿色)溴化银AgBr(淡黄色)碘化银AgI(黄色)硫化铜CuS(黑色)硫化铅PbS(棕黑色)16、常见俗名与化学式:硫酸盐类:1.皓矾:ZnSO4·7H2O2.钡餐,重晶石:BaSO43.绿矾,皂矾,青矾:FeSO4·7H2O4.芒硝,朴硝,皮硝:Na2SO4·10H2O5.明矾:KAl(SO4) 2·12H2O6.生石膏:CaSO4·2H2O 熟石膏:2CaSO4·H2O7.胆矾、蓝矾:CuSO4·5H2O8.莫尔盐:(NH4)2SO4、FeSO4·6H2O 矿石类:1.莹石:CaF22.光卤石:KCl.MgCl2·6H2O3.黄铜矿:CuFeS24.矾土:Al2O3·H2O、Al2O3·3H2O和少量Fe2O3、SiO25.磁铁矿石:Fe3O46.赤铁矿石:Fe2O37.褐铁矿石:2Fe2O3·3H2O8.菱铁矿石:Fe2CO39.镁铁矿石:Mg2SiO410.苏口铁:碳以片状石墨形式存在11.白口铁:碳以FeC3形式存在12.高岭石:Al2 (Si2O5)(OH) 4或(Al2O3、2SiO2·2H2O) 13.正长石:KAlSi3O814.石英:SiO215.硼砂:Na2B4O7·10H2O16.脉石:SiO217.刚玉(蓝宝石.红宝石):天然产的无色氧化铝晶体18.黄铁矿(愚人金):FeS219.炉甘石:ZnCO320.智利硝石:NaNO321.滑石:3MgO、4SiO2·H2O 22.大理石(方解石、石灰石):CaCO323.孔雀石:CuCO3、Cu(OH)224.白云石:MgCO3、CaCO325.冰晶石:Na3AlF626.高岭土:Al2O3、2SiO2·2H2O 27.锡石:SnO228.辉铜矿:Cu2S气体类:1.高炉煤气:CO、CO2等混合气体2.水煤气:CO、H23.天然气(沼气):CH44.液化石油气:C3H8,C4H10为主5.焦炉气:CH4、CO、H2、C2H4为主6.裂解气:C2H4为主7.爆鸣气:H2、O28.笑气:N2O9.裂化气:C1~C4的烷烃、烯烃10.电石气:C2H2(通常含H2S、PH3等)有机类:1.福尔马林(蚁醛):HCHO2.蚁酸:HCOOH3.尿素:(NH4CNO)或CO(NH2) 24.氯仿:CCl45.木精(工业酒精):CH3OH6.甘油:CH2OH-CHOH- CH2OH7.硬脂酸:C17H35COOH 8.软脂酸:C15H31COOH 9.油酸:C17H33OH10.肥皂:C17H35COONa 11.银氨溶液:[Ag(NH3) 2]+ 12.乳酸:CH3-CHOH-COOH13.葡萄糖:C6H12O614.蔗糖:C12H22O1115.核糖:CH2OH-(CHOH) 3CHO16.脱氧核糖:CH2OH-(CHOH) 2CH2-CH317.淀粉:(C6H10O5)n18.火棉,胶棉:主要成份都是[(C6H7O2)-(ONO2) 2]n 只是前者含N量高19.尿素:CO(NH2) NH4CNO为氰酸铵(互为同分异构体)20.氯仿:CHCl321.油酸:C17H33COOH 22.银氨溶液:[Ag(NH3) 2]OH23.脱氧核糖:CH2OH-(CHOH) 2CH2-CHO其他类:1.白垩:CaCO32.石灰乳、消石灰、熟石灰:Ca(OH) 23.熟石膏:2CaSO4·H2O4.足球烯:C605.铜绿:Cu2 (OH) 2CO36.纯碱(碱面):Na2CO37.王水:HCl、HNO3 (3:1) 8.水玻璃(泡火碱) :Na2SiO39.小苏打:NaHCO310.苏打:Na2CO311.大苏打(海波):Na2S2O312.盐卤:MgC12·6H2O13.雌黄:As2S314.雄黄:As4S415.朱砂:HgS 16.石棉:CaO、3MgO、4SiO217.砒霜:As2O318.泻盐:MgSO4·7H2O 19.波尔多液:CuSO4、Ca(OH) 220.钛白粉:TiO221. 纯碱、苏打、口碱:Na2CO322. 双氧水:H2O223.生石灰:CaO 24. 火碱、烧碱、苛性钠:NaOH17、常见固体、液体颜色:固体的颜色1、红色固体:铜,氧化铁2、绿色固体:碱式碳酸铜3、蓝色固体:氢氧化铜,硫酸铜晶体4、紫黑色固体:高锰酸钾5、淡黄色固体:硫磺6、无色固体:冰,干冰,金刚石7、银白色固体:银,铁,镁,铝,汞等金属8、黑色固体:铁粉,木炭,氧化铜,二氧化锰,四氧化三铁,(碳黑,活性炭)9、红褐色固体:氢氧化铁10、白色固体:氯化钠,碳酸钠,氢氧化钠,氢氧化钙,碳酸钙,氧化钙,硫酸铜,五氧化二磷,氧化镁液体的颜色1、无色液体:水,双氧水2、蓝色溶液:硫酸铜溶液,氯化铜溶液,硝酸铜溶液3、浅绿色溶液:硫酸亚铁溶液,氯化亚铁溶液,硝酸亚铁溶液4、黄色溶液:硫酸铁溶液,氯化铁溶液,硝酸铁溶液5、紫红色溶液:高锰酸钾溶液6、紫色溶液:石蕊溶液气体的颜色1、红棕色气体:二氧化氮2、黄绿色气体:氯气3、无色气体:氧气,氮气,氢气,二氧化碳,一氧化碳,二氧化硫,氯化氢气体等大多数气体。
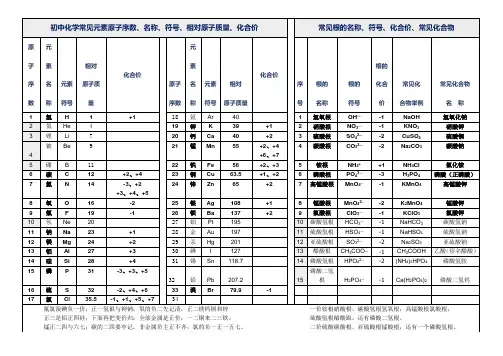

初三化学常用化合价《初三化学常用化合价》同学们,今天咱们来好好唠唠化学式,这化学式啊,和化合价可是关系紧密呢。
首先,咱得知道化合价是个啥。
化合价就像是原子在化学世界里的一种“价值标签”,每个原子都有自己常见的化合价。
比如说氢,它的化合价通常是 +1价,氧呢,一般是 -2价。
这化合价就像是原子在组建分子这个“小家庭”时带的一种“经济实力”,有正有负。
那这化合价和化学式有啥关系呢?咱们就像搭积木一样来构建化学式。
比如说水,化学式是H₂O。
这里面氢是 +1价,氧是 -2价,为了让这个“小家庭”整体的“经济收支”平衡,就得有两个氢原子(2×( +1) =+2)和一个氧原子(1×( -2) = -2)结合,这样整体就不带电了,就像咱们过日子,收入和支出得平衡。
那原子们是怎么结合到一起形成分子的呢?这就涉及到化学键啦。
化学键就像是原子之间的小钩子。
比如说离子键,就像带正电和带负电的原子像超强磁铁般吸在一起。
就好比男生(带正电的原子)和女生(带负电的原子)互相吸引,紧紧地靠在一起,像氯化钠(NaCl),钠原子(Na)失去一个电子带正电,氯原子(Cl)得到一个电子带负电,它们就靠这种离子键结合在一起啦。
还有共价键呢,这就像是原子们共用小钩子连接。
就像两个小伙伴一起拉着一个东西,谁也不放手。
比如说氧气(O₂),两个氧原子就是通过共用小钩子(共价键)结合在一起的。
再来说说分子的极性。
这分子的极性就类似小磁针。
像水是极性分子,氧一端就像磁针南极带负电,氢一端就像北极带正电。
你可以想象水是一个有方向的小磁针,它的正负极分布不均匀。
而二氧化碳(CO₂)呢,是直线对称的,就像一个两边完全一样的哑铃,它就是非极性分子,不存在这种一端正电一端负电的情况。
在化学里还有个很有趣的东西叫配位化合物。
这里面中心离子就像是聚会的主角,周围的配体呢,就像是提供孤对电子共享的小伙伴。
比如说在[Cu(NH₃)₄]²⁺这个配位化合物里,铜离子(Cu²⁺)就是主角,氨分子(NH₃)就是小伙伴,氨分子把自己的孤对电子拿出来和铜离子共享,就像小伙伴们围绕着主角一起玩耍。

钾 K +1 氯 Cl -1,+1,+5,+7钠 Na +1 氧 O -2,-1银 Ag +1 硫 S -2,+4,+6钙 Ca +2 碳 C +2,+4镁 Mg +2 硅 Si +4钡 Ba +2 氮 N -3,+2,+3,+4,+5锌 Zn +2 磷 P -3,+3,+5铜 Cu +1,+2 硫酸根 SO4 -2铁 Fe +2,+3,碳酸根 CO3 -2铝 Al +3 硝酸根 NO3 -1锰 Mn +2,+4,+6,+7 氢氧根 OH -1氢 H +1 铵根 NH4 +1氟 F -1 磷酸根 PO4 -3 氯酸根 ClO3 -1(Cl +5价)关于化合价的口诀,方便大家记忆:氢+1,氧-2,银锂钠钾+l价,锌镁钙钡+2价,铝+3,硅+4.只遇金属或是氢,氮磷-3硫-2,氟氯溴碘总-1.可变价,不可怕,具体判断"和为零".单质为零要记清."亚铜" +1"铜" +2,"亚铁" +2"铁" +3,置换反应铁+2,复分解时价不变.关于化合价要准确记着金属元素化合价和原子团的化合价。
一般非金属元素化合价是让你求的,所以只需要你了解非金属元素一般显负价,当含氧时显正价就可以了。
具体是几不需要。
正一氢银和钠钾,正二钙钡镁锌汞,铜是一二,铁二三,铝的价态是正三。
原子团化合价口诀OH氢氧根-1价,NO3硝酸根-1价SO4硫酸根-2价CO3碳酸根-2价PO4磷酸根-3价NH4铵根+1价这种原子团化合价的记法便于掌握原子团的组成、名称、化合价。
我们的学生一般都背这个。
一价钾钠氯(-1)氢银,二钾氧(-2)钙钡镁锌三铝四硅五价磷二三铁,二四炭,二四六硫都齐全铜汞二价最常见一价高锰、氯、硝酸根二价锰、硫、碳酸根三价磷酸根元素化合价常用口诀表(金属显正价,非金属显负价)一价钾钠氯氢银,二价氧钙钡镁锌,三铝四硅、五价磷,二三铁、二四碳,二四六硫都齐全,铜汞二价最常见,单质价数都为零。
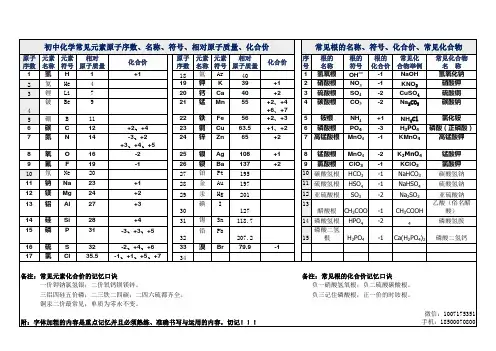
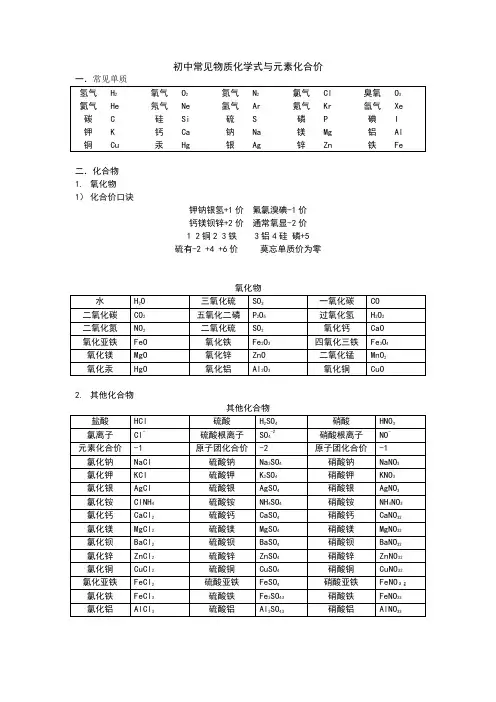

初中化学常见化合价《初中化学常见化合价》嘿,同学们!今天咱们来好好唠唠化学式,这可离不开初中化学常见化合价这个重要的知识哦。
首先,啥是化合价呢?咱可以把化合价想象成原子在形成化合物时的一种“价值”或者说它的一种“社交能力”。
就好比在一个社交场合里,不同的人有不同的交往方式和影响力,原子也是这样。
那这个化合价和化学式有啥关系呢?咱们举个例子,就像盖房子得有设计图一样,化学式就是化合物的“设计图”,而化合价就是那些小砖头(原子)的搭配规则。
比如说水,化学式是H₂O。
氢的化合价一般是 +1价,氧的化合价一般是 -2价。
你看,这就像两个人合作干活,两个氢原子每个都有 +1的“价值”,氧原子有 -2的“价值”,它们组合起来就刚刚好,整体不带电,就像收支平衡一样。
再来说说化学键。
化学键就像是原子之间的小钩子,把原子们连接在一起组成分子或者化合物。
这里面有离子键和共价键呢。
离子键啊,就像是带正电和带负电的原子像超强磁铁般吸在一起。
比如说氯化钠(NaCl),钠原子(Na)最外层有1个电子,它很容易就把这个电子给扔出去,这样它就带了正电,变成了钠离子(Na⁺),就像一个慷慨的人把自己的东西送出去了,自己变得有点“轻装上阵”但带正电了。
而氯原子(Cl)最外层差1个电子就满了,它就把钠给的电子拿过来,变成了氯离子(Cl⁻),带负电了。
这时候钠离子和氯离子就像磁铁的正负两极,紧紧地吸在一起,这种吸引力就是离子键。
共价键呢,就像是原子们共用小钩子连接。
就像两个人共同拿着一个东西一样。
比如说氢气(H₂),两个氢原子都想让自己的最外层电子达到稳定状态,于是它们就商量好,共用一对电子,就像两个小伙伴一起拉着一个小钩子,这样就形成了共价键,它们就组成了氢气分子。
还有化学平衡呢,这就好比拔河比赛。
反应物和生成物就像两队人。
刚开始的时候,可能反应物这边力量大(反应正向进行得快),但是随着反应的进行,生成物这边的“力量”(浓度)也在增加,慢慢的,就会达到一种正逆反应速率相等、浓度不再变化的状态,这就像拔河比赛两队人都用同样大的力气拉着绳子,绳子不动了,这就是化学平衡状态。

常用化合价口诀一价氢氟钾钠银二价氧钙镂顿锌)初中常用3三铝四硅五氮磷一至五价都有氮正一铜氢钾钠银三铝四硅四六硫一五七氯二三铁碳有正四与正二负一溟碘与氛纵常用化合价口诀一价氢氯钾钠银二价氧钙镁饭锌二三铁.二四碳二四八?硫都齐全三铝四硅五氮磷铜汞二价最常见二三恢.二四碳铜汞二价最常见正二铜镂钙顿锌二四五氮三五磷二四六七猛为正再把负价牢记心负二氧硫三氮磷初中常用1钠钾银氢一价阳氛氯澳碘一价阴二价氧硫碳氮镁铁锡钙總锁汞锌三价铁钏硼铝偌四价碳硅一二铜氮磷三五硫四八镭二四六七爪质零初中常用2钾K钠Na H Ag正一价钙Ca镁Mg锌Zn饭Ba正二价铜Cu有正一正二.铝A1正三 F Cl Br I 负一价通常氧0为负二价铁Fe有正二和正三二、四二、四C 二、四./\ S都齐全钾钠银氢正一价钙樸锁锌正二价铝是正三氧负二氮是负一最常见硫有负二正四六正二正三铁可变正一二铜二四碳一价氢钠钾.氟氯溟碘银二氧汞铅铜.领锲钙和锌三铝四硅五价磷二三铁,二四碳二四六硫最常见莫忘爪质为零价初中常用4一价氢氮钾钠银二价氧钙饭镁锌三铝四硅五氮磷二三铁,二四碳,二四六硫都齐全铜汞二价最常见的质为零要记淸负一氢氧硝酸根负二碳酸硫酸根负三记住磷酸根正一价的是钱根初中常用5一价氢氯钾钠银二价氧钙饭镁锌铝三铜二最常见铁有+2和+3氮磷都有负三正三五:不同磷三氮二四。
二四六硫都齐全:边记边用就会熟。
一价簸氯钾钠银二价钙钺镁铜锌铝是正三永不变铁有正二和正三四是碳硅五是磷硫有变价二四六氢一氧二为根木化合价,要记清遇到敢质皆标0初中常用7一价钾钠氢氮银二价氧钙锁钱锌三铝四硅五价磷二、三铁.二、四碳,二四六硫都齐全铜汞二价垠常见莫忘总质零价现化合价口诀三一价氢氯钾钠银:二价氧钙做镁锌, 三铝四硅五价磷:二三铁,二四碳? 二四/弋硫都齐全:铜汞二价最常见。
一五七氮常常见,讥质零价永不变。
化合价口诀四氢钾钠银正一价:镁锌狈钙正二价:氛氮渎碘负一价:通常氧显负二价:铜正一二铝正三:铁有正二和正三:碳有正二和正四:硫有负二正四八:负三正五氮和磷:二四六七症为正。

初中化学化合价一览表在初中化学中,化合价是非常重要的概念。
它能够帮助我们了解元素之间的化学反应以及化合物的构成。
因此,在化学学习中了解化合价表是非常必要的。
下面是一个初中化学化合价一览表,方便大家查阅和学习。
一、氢族元素(IA族)氢(H):+1二、碱金属元素(IA族)锂(Li):+1钠(Na):+1钾(K):+1铷(Rb):+1铯(Cs):+1铪(Fr):+1三、碱土金属元素(IIA族)铍(Be):+2镁(Mg):+2钙(Ca):+2锶(Sr):+2钡(Ba):+2镭(Ra):+2四、硼族元素(IIIA族)硼(B):+3铝(Al):+3镓(Ga):+3铟(In):+3镥(Tl):+3五、碳族元素(IVA族)碳(C):+4,-4(与金属或氢元素结合时为+4,与非金属结合时为-4)硅(Si):+4六、氮族元素(VA族)氮(N):+3,+5磷(P):+3,+5砷(As):+3,+5锑(Sb):+3,+5铋(Bi):+3,+5七、氧族元素(VIA族)氧(O):-2硫(S):-2硒(Se):-2碲(Te):-2钋(Po):-2八、卤素元素(VIIA族)氟(F):-1氯(Cl):-1溴(Br):-1碘(I):-1砹(At):-1九、惰性气体(VIIIA族)氦(He):0氖(Ne):0氩(Ar):0氪(Kr):0氙(Xe):0氡(Rn):0通过以上初中化学化合价一览表,我们可以清楚地看到各个元素的化合价。
熟练掌握这些化合价,对于理解化学反应的过程以及化合物的构成起到了重要的作用。
同时,掌握化合价还能够帮助我们预测元素之间的化学反应、反应类型以及化合物的稳定性。
总结起来,初中化学化合价一览表是化学学习中必备的工具之一。
希望大家通过不断地学习和实践,掌握这些化合价规律,为自己的化学学习打下坚实的基础。
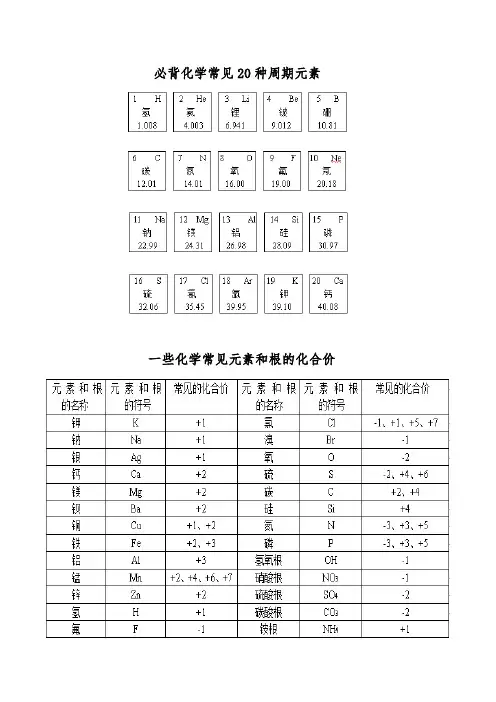
必背化学常见20种周期元素一些化学常见元素和根的化合价
关于化合价的口诀,方便大家记忆:
氢+1,氧-2,
银锂钠钾+l价,
锌镁钙钡+2价,
铝+3,硅+4.
只遇金属或是氢,
氮磷-3硫-2,
氟氯溴碘总-1.
可变价,不可怕,
具体判断"和为零".
单质为零要记清.
"亚铜" +1"铜" +2,
"亚铁" +2"铁" +3,
置换反应铁+2,
复分解时价不变.
关于化合价要准确记着金属元素化合价和原子团的化合价。
一般非金属元素化合价是让你求的,所以只需要你了解非金属元素一般显负价,当含氧时显正价就可以了。
具体是几不需要。
金属元素化合价口诀
正一氢银和钠钾,正二钙钡镁锌汞,铜是一二,铁二三,
铝的价态是正三。
原子团化合价口诀
OH-氢氧根-1价,NO3-硝酸根-1价(其中N为+5价),SO42-硫酸根-2价(S为+6价),CO32-碳酸根-2价
PO43-磷酸根-3价(其中P为+5价),NH4+铵根+1价(其中N为-3价)
这种原子团化合价的记法便于掌握原子团的组成、名称、化合价。
我们的学生一般都背这个。
一价钾钠氯(-1)氢银,二钾氧(-2)钙钡镁锌
三铝四硅五价磷
二三铁,二四炭,二四六硫都齐全
铜汞二价最常见
一价高锰、氯、硝酸根
二价锰、硫、碳酸根
三价磷酸根。
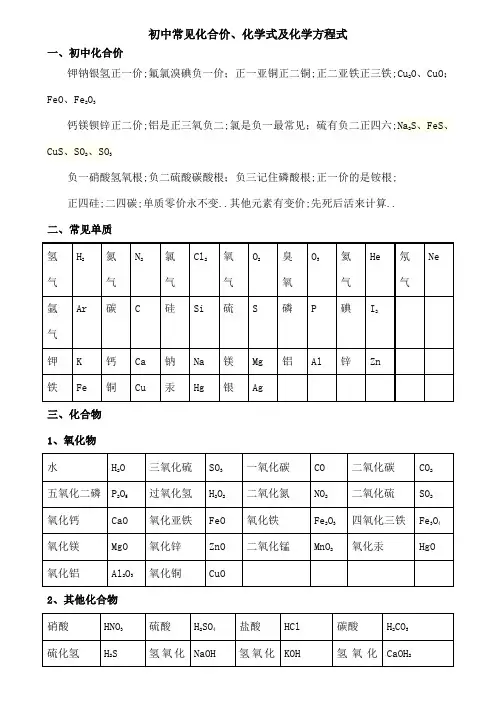
初中常见化合价、化学式及化学方程式一、初中化合价钾钠银氢正一价;氟氯溴碘负一价;正一亚铜正二铜;正二亚铁正三铁;Cu 2O 、CuO ;FeO 、Fe 2O 3钙镁钡锌正二价;铝是正三氧负二;氯是负一最常见;硫有负二正四六;Na 2S 、FeS 、CuS 、SO 2、SO 3负一硝酸氢氧根;负二硫酸碳酸根;负三记住磷酸根;正一价的是铵根; 正四硅;二四碳;单质零价永不变..其他元素有变价;先死后活来计算.. 二、常见单质三、化合物 1、氧化物2、其他化合物3、常见有机化合物 初中化学方程式全已配平一、化合反应1、镁在空气中燃烧:2Mg+O 点燃2MgO2、铁在氧气中燃烧:3Fe+2O 点燃Fe 3O 43、铝在空气中燃烧:4Al+3O 点燃2Al 2O 34、氢气在空气中燃烧:2H 2+O 点燃2H 2O5、红磷在空气中燃烧:4P+5O 点燃2P 2O 56、硫粉在空气中燃烧:S+O 2点燃SO 27、碳在氧气中充分燃烧:C+O 2点燃 CO 28、碳在氧气中不充分燃烧:2C+O 2 点燃2CO9、二氧化碳通过灼热碳层:C+CO 2高温2CO 10、一氧化碳在氧气中燃烧:2CO+O 2 点燃2CO 211、二氧化碳和水反应二氧化碳通入紫色石蕊试液:CO 2+H 2O=H 2CO 3 12、生石灰溶于水:CaO+H 2O=CaOH 213、无水硫酸铜作干燥剂:CuSO 4+5H 2O=CuSO 4·5H 2O 14、钠在氯气中燃烧:2Na+Cl 2点燃2NaCl 二、分解反应15、实验室用双氧水制氧气:2H 2O 2MnO 22H 2O+O 2↑ 16、加热高锰酸钾:2KMnO 4△K 2MnO4+MnO 2+O 2↑ 17、水在直流电的作用下分解:2H 2O 通电2H 2↑+O 2↑ 18、碳酸化学性质不稳定而分解:H 2CO 3=H 2O+CO 2↑19、高温煅烧石灰石二氧化碳工业制法:CaCO 3高温CaO+CO 2↑ 20、加热氯酸钾分解:2KClO 3=2KCl+3O 2↑21、氧化汞加热分解:2HgO △2Hg+O 2↑三、置换反应单质+化合物→新的单质+新的合化物 22、锌和稀盐酸反应实验室制氢气:Zn+2HCl=ZnCl 2+ H 2↑ 锌和稀硫酸反应实验室制氢气:Zn+H 2SO 4=ZnSO 4+ H 2↑ 23、镁和稀盐酸反应:Mg+2HCl=MgCl 2+H 2↑ 镁和稀硫酸反应:Mg+H 2SO 4=MgSO 4+ H 2↑ 24、铁和稀盐酸反应:Fe+2HCl=FeCl 2+ H 2↑ 铁和稀硫酸反应:Fe+H 2SO 4=FeSO 4+ H 2↑ 25、铝和稀盐酸反应:2Al+6HCl=2AlCl 3+3H 2↑铝和稀硫酸反应:2Al+3H 2SO 4=Al 2SO 43+3 H 2↑ 26、铁和硫酸铜溶液反应:Fe+CuSO 4 =FeSO 4+Cu 铝和硫酸铜溶液反应:2Al+3CuSO 4=Al 2SO 43+3Cu 27、铜和硝酸银反应:Cu+2AgNO 3=CuNO 32+2Ag 28、氢气还原氧化铜:H 2+CuO △Cu+H 2O29、木炭还原氧化铜:C+2CuO 高温 2Cu+CO 2↑ 30、焦炭还原氧化铁:3C+2Fe 2O 高温 4Fe+3CO 2↑ 31、水蒸气通过灼热碳层:H 2O+C 高温 H 2+CO 四、复分解反应复分解反应是由两种互相交换成分;生成另外两种化合物的反应..复分解反应的实质是:发生复分解反应的两种物质在水中交换离子;结合成难的物质——、或最常见的为水;可简记为AB+CD=AD+CB 酸+碱-----盐+水32、盐酸和氢氧化钠反应:HCl+NaOH=NaCl+H 2O 33、中和胃酸的反应:3HCl+AlOH 3 =AlCl 3+3H 2O 34、熟石灰和硫酸的反应:2HCl+CaOH 2=CaCl 2+2H 2O35. 盐酸和氢氧化钾反应:HCl+KOH=KCl+H 2O 硫酸和氢氧化钾反应: 36. 盐酸和氢氧化铁反应:3HCl+ FeOH 3=FeCl 3+3H 2O 37. 硫酸和氢氧化铁反应:3H 2SO 4+2FeOH 3=Fe 2SO43+6H 2O38.硫酸和氢氧化钾反应:H 2SO4+2KOH=K 2SO 4+2H 2O 盐酸和氢氧化钾的反应 39.硫酸和氢氧化铜反应:H 2SO4+CuOH 2 =CuSO 4+2H 2O 盐酸和氢氧化铜的反应 酸+盐-----另一种酸+另一种盐40、盐酸和硝酸银的反应:HCl+AgNO 3=AgCl↓+HNO 3 41、硫酸和氯化钡反应:H 2SO 4+BaCl 2 =BaSO 4↓+2HCl 42、碳酸钙和过量盐酸反应:CaCO 3+2HCl=CaCl 2 +H 2O+CO 2↑43、碳酸钠和过量盐酸反应:Na 2CO 3+2HCl= 2NaCl+H 2O+CO 2↑ 44、碳酸氢钠和盐酸反应:NaHCO 3+HCl=NaCl+H 2O+CO 2↑ 45.碳酸镁与稀盐酸反应: MgCO 3+2HCl=MgCl 2+H 2O+CO 2↑ 碱+盐-----另一种碱+另一种盐46、氢氧化钠和和硫酸铜反应:2NaOH+CuSO 4=CuOH 2↓+Na 2SO 4 47、氢氧化钙和碳酸钠反应:CaOH 2+Na 2CO 3=CaCO 3↓+2NaOH 48.氢氧化钠与氯化铁:3NaOH+FeCl 3=FeOH 3↓+3NaCl 49.氢氧化钠与氯化镁:2NaOH+MgCl 2 = MgOH 2↓+2NaCl 50. 氢氧化钠与氯化铜:2NaOH+CuCl 2= CuOH 2↓+2NaCl 盐+盐-----两种新盐51、硝酸银和氯化钠反应:NaCl+AgNO 3=AgCl↓+NaNO 3 52、硫酸钠和氯化钡反应:Na 2SO 4+BaCl 2=BaSO 4↓+2NaCl 53、氯化钙和碳酸钠反应:CaCl 2+Na 2CO 3=CaCO 3↓+2NaCl 碱性氧化物+酸----- 盐+ 水54、过量盐酸除铁锈:Fe 2O 3+ 6HCl=2FeCl 3+ 3H 2O Fe+2HCl=FeCl 2+ H 2↑ 55、过量硫酸除铁锈:Fe 2O 3 +3H 2SO 4=Fe 2SO 43+3H 2O Fe+H 2SO 4=FeSO 4+ H 2↑ 56、氧化铜和硫酸反应:CuO +H 2SO 4=CuSO 4+H 2O 57. 氧化铜和稀盐酸反应:CuO +2HCl=CuCl 2+H 2O 58. 氧化镁和稀硫酸反应:MgO+ H 2SO 4 =MgSO 4+ H 2O 59. 氧化钙和稀盐酸反应:CaO +2HCl=CaCl 2+H 2O其他60、甲烷在空气中燃烧:CH 4+2O 点燃 CO 2+2H 2O 61、酒精在空气中燃烧:C 2H 5OH+3O 点燃2CO 2+3H 2O 62、一氧化碳还原氧化铜:CO+CuO 加热 Cu+CO 263、一氧化碳还原氧化铁:3CO+Fe 2O 3 高温 2Fe+3CO 264、二氧化碳通过澄清石灰水检验二氧化碳:CaOH 2+CO 2=CaCO 3↓+H 2O 65、氢氧化钠和二氧化碳反应除去二氧化碳:2NaOH+CO 2 =Na 2CO 3 +H 2O 66、氢氧化钠吸收二氧化硫:2NaOH+SO 2 =Na 2SO 3 +H 2O67、石灰石或大理石与稀盐酸反应二氧化碳的实验室制法:CaCO 3+2HCl=CaCl 2+H 2O+CO 2↑ 68、葡萄糖在酶的作用下与氧气反应: 69、植物光合作用:。