树突状细胞 -张学光——免疫学课件PPT
- 格式:ppt
- 大小:5.59 MB
- 文档页数:57


树突状细胞的特性及应用172河北医药2004年2月第26卷第—HebeiMedicalJo—urnal,Feb2004,—V ol26—,No.2树突状细胞的特性及应用张庆九李春晖焦保华树突状细胞(Dendriticcell,I)C)是机体免疫系统中最强有力的一种专职的抗原呈递细胞(APC),在免疫应答的启动,调控上起着关键的作用LII.现代抗肿瘤免疫疗法利用Dc负载肿瘤相关抗原(T从)制成的肿瘤疫苗(瘤苗),在转移性前列腺癌,恶性黑色素瘤,多发性骨髓瘤和慢性髓性白血病(CML)等几种恶性肿瘤的治疗上已取得喜人的效果.现对树突状细胞的生物特性,来源,抗瘤机制,肿瘤疫苗疗法等进行综述1Dc生物学特性IX;最初是Steirmlan和Cohn等1973年从小鼠脾组织中分离发现的,因其形态具有树突样或伪足样突起而命名.目前一致认为,凡具有典型的树突状形态,膜表面高表达MttCⅡ类分子,能移行至淋巴器官和刺激初始型T细胞增殖活化,并具有一些相对特异性表面标志的一类细胞,方能称之为DE,DE广泛分布于全身各脏器,数量极微,约占外周血白细胞总数的1%,DC的前体细胞由骨髓进入外周血,再分布到全身各组织.13t2主要分为髓系D(=(myeloiddrivedDC)和淋巴系DC(1ymphoidrelatedoc)两大类.成熟的DC表现出6个主要特征:(1)细胞形态不规则,表面有许多膜样或树突佯突起;(2)细胞表面具有丰富的有助于抗原提呈的分子,如持续,高水平的表达MItCI类,Ⅱ类分子,共刺激分子cD帅(.)和cD86(13,:),细胞粘附分子CD(LFAI),CDm,C(ICA),C(ICAM.),co,8(LFA])和CD.∞(ICAM2),以及淋巴细胞功能相关抗原LFA1,LFA1等.人血中的I)C前体开始表达c.:,但随着成熟渐渐失去表达,而粘附分子,共刺激分子,MHC抗原随着成熟而表达增加J.活化后,特别是cD柏L活化后,c,c上调.在成熟中,cD86出现早,而cD町出现晚,血中DC前体几乎不能检测到..(3)在混合淋巴细胞反应中,既能激活MHC相同的自身反应性T细胞,又能激活MHC不同的同种反应性T细胞,而其最大特点是能够显着刺激初始型T细胞(NaiveTcel1)增殖并建立初级免疫应答.(4)具有向局部淋巴细胞T细胞区迁移的能力.(5)DC激发T细胞增殖及抗原提呈能力是巨噬细胞和B细胞的100~1000倍b1.(6)新近发现的D(:SIGN(DCslx~cificICAM3grabbingnoninten)分子在启动静息T细胞免疫反应中的作用引起人们的注意,Dc SIGN是DC特异表达的,第一个被鉴定的DC限制性分子,介导Dc与静息T细胞的强烈粘附从而发挥I)C诱导的T细胞增殖作用.另外,在体内外,J)C具有与其他APC不同的功能特征,可递呈抗原给静息T细胞的能力是I)(:最重要的功能之一. 其能力是其他APc的10—100倍.正是由于DC的上述特征使作者单位:050000~aI_lgN科大学第二医院神经外科其成为体内抗原提呈能力最强的AP【=,也是唯一一类可直接活化静息T细胞的APE.2树突状细胞的来源近几年来,随着人们在DC的起源,分类,摄取和加工处理抗原的机制以及引起DC迁移和成熟的信号传导等领域研究的深入,有关人DC大量培养和扩增的方法日益成熟.目前,树突状细胞有三个来源:骨髓,外周血和新生儿脐带血.从骨髓中分离获得树突状细胞的CD互的祖系细胞,或从外周血或新生儿脐带血于体外经14d培养分化(在GMCSF和TNFa存在的情况下)成为成熟的CD,C跽,HIADR的树突状细胞;或者用外周血纯化的CD;单核细胞或粘附单核细胞在二种细胞因子(GMCSF和IL4或ILl3)的培养刺激下成为CD,c聪的未成熟树突状细胞,再经TNFa或(和)CL刺激形成成熟的树突状细胞.3树突状细胞抗肿瘤的分子机制研究证明J,树突状细胞与肿瘤的发生,发展具有以下密切关系.(1)以肿瘤抗原体外专一性地冲击致敏,激活功能最强的APC树突状细胞,可保证肿瘤抗原被有效摄取.(2)树突状细胞通过细胞表面高水平的MHCI,Ⅱ类分子呈递了丰富的肿瘤抗原肽,使相应的T细胞受体(TCR)被充分占据;同时,树突状细胞提供高水平的协同刺激分子B7..(cD),B7.:(cD86),cD的分子等,使T细胞被充分激活.(3)树突状细胞与T细胞结合后,可以大量分泌:,激发T细胞增殖,诱导特异性细胞毒性T淋巴细胞(CTL)生成,主导了TH,型的免疫应答,有利于肿瘤细胞的清除.(4)树突状细胞还能分泌趋化因子(DCCCK),专一性地趋化初始型T细胞,通过促进T细胞聚集,增强对T细胞的激发.另外,肿瘤病人可以在中枢神经系统检测到T淋巴细胞和主要组织相容性抗原.采用细胞因子修饰的肿瘤细胞瘤苗能够产生抗中枢神经肿瘤的免疫反应,因此免疫反应可以介入中枢神经系统疾病.4关于各种类型的树突状细胞疫苗'目前已研究了各种形式肿瘤抗原体外冲击致敏树突状细胞制备的疫苗.(1)细胞性肿瘤抗原:经放射线照射灭活的肿瘤细胞,肿瘤细胞反复冻融上清或肿瘤细胞冻融后膜碎片或超声破碎方法制备肿瘤细胞的蛋白提取物直接体内免疫后都只产生极弱的抗肿瘤免疫效应,已极少作为肿瘤疫苗单独用于临床.(2)肿瘤抗原多肽:应用经弱酸洗脱肿瘤细胞表面的MHCI类抗原多肽冲击树突状细胞,其靶向性更好,肿瘤抗原浓度更高,可产生"冲击致敏"的效应,促进T细胞有效激活.(3)肿瘤抗原基因:将肿瘤抗原基因转移进树突状细胞,体内诱发特异性抗肿瘤免疫功能.其方式有多种:用脂质体介导单纯疱疹病毒(Hsv)蛋白抗原编码基因冲击树突状细胞,或脂质体介导河北医2004年2月第26卷第2期HebeiMedicalJournal一,Feb2004,V ol26,No.2 酪氨酸酶基因转移入树突状细胞;用肿瘤细胞的RNA作为抗原冲击树突状细胞,或用低免疫原性肿瘤的RNA(总RNA或polyA+RNA)冲击树突状细胞,免疫接种后可诱导出强烈抗肿瘤免疫力;用腺病毒载体介导肿瘤抗原基因对成熟树突状细胞的转染;用黑色素瘤抗原基因质粒通过基因枪技术转染体外培养的树突状细胞等.(4)抗独特型抗体:抗独特型抗体是肿瘤抗原的内影像,可模拟肿瘤抗原被机体识别,激发针对肿瘤细胞的免疫功能.临床首例应用树突状细胞治疗肿瘤就是应用抗独特型抗体致敏树突状细胞来做为瘤苗.(5)与细胞因子联合使用:是体内介导TH.型应答的细胞因子,与抗原冲击的树突状细胞瘤苗联合应用于肿瘤治疗,收到更佳的抗癌效果.某些情况下甚至逆转由树突状细咆诱导的耐受.(6)肿瘤相关抗原和肿瘤特异性抗原:粒细胞,巨噬细胞集落刺激因子(GMCSF)可以促进树突状细胞的成熟,维持树突状细胞的存活.将GMCSF基因经腺病毒载体介导转入树突状细胞,具有更强的体内激发肿瘤特异性CTL的能力.用腺病毒将I基因转染树突状细胞,也可协同增强T细胞功能,促进机体的抗肿瘤效应.Fms样酪氨酸激酶Ⅲ(肿,酪氨酸激酶受体家族Ⅲ成员之一)配体(n凡L)也是一种细胞因子,能与树突状细胞或B细胞表面的受体结合,促进树突状细胞的成熟,故也有人应用肿L联合树突状细胞瘤苗增强抗肿瘤疗效".此外,曹雪涛等还将重组腺病毒介导的GMCSF基因转染的树突状细胞经肿瘤抗原冲击致敏后,与肿瘤细胞融合制备出免疫原性更强的新型瘤苗,他们还报道了肿瘤抗原多肽致敏的,淋巴细胞趋化因子基因修饰的树突状细胞诱导特异性抗肿瘤免疫应答的实验结果.法国与意大利合作小组"发现,肿瘤抗原冲击的树突状细胞胞浆内形成许多包含抗原多肽的小体(exoc~omes或dexosomes).实际上,树突状细胞除了细胞间直接接触和通过分泌细胞因子起作用外,人和小鼠的树突状细胞均能分泌或外排exo~ome.s,这种小体中不含凋亡小体,胞浆膜或内质网组组等,表达MHCI,Ⅱ类分子和cDIi6,具抗原呈递能力,能在体外刺激抗原特异性cT细胞的增殖,因而有诱导T细胞免疫反应的功能.从树突状细胞上清分离和纯化这些小体给荷瘤小鼠皮下注射(5/*gexo—sor-麟)也诱导了极强的抗肿瘤效应,在体内诱导出高水平的cT1J,并能治愈荷瘤小鼠,提示作为无细胞体系诱导体内免疫功能的应用途径,eXOC~OIIIeS也可以说是一种新型的亚细胞成分的树突状细胞瘤苗.(7)直接应用Dc:将Dc在体外进行扩增后再回输体内,以求获得更多的CTL,这本身就是一种过继性免疫治疗,而且大多数肿瘤组织内浸润Dc的数量与肿瘤患者的预后直接相关,浸润DC多则预后好.5DC的输注途径和剂量输注途径早期D(=的输注途径多采用静脉注射.近年来,采用皮下,皮内,淋巴管内,瘤体内注射的方法得到了广泛的应用.目前,多数学者认为,皮内,瘤体内注射可能更有利于DC发挥其生物学功能.DC发挥其抗肿瘤免疫效应的基础是D(=负载肿瘤抗原后,能够迁移至T淋巴细胞富集的二级淋巴器官,从而激活抗肿瘤免疫反应.因此,DC的输注途径与其能否更好地发挥生物学功能密切相关.(1)静脉及淋巴管内注射:l73Mackensen等对七HC的静脉及淋巴管内注射进行了比较,作者用转移性恶性黑色素瘤患者外周血cD五造血干细胞来源的DC 经放射性标记后,静脉或淋巴管内注射,丫照相机全身拍照观察.发现DC经静脉注射后在肺内作短暂停留,最后定位于脾和肝脏7d以上:DC注入足背淋巴管内后,可迅速迁移至引流淋巴结并停留24h以上,实验说明淋巴管内注射与静脉注射相比,更有利于DC发挥其抗肿瘤作用.(2)真皮内注射:Thomas等则比较了多种DC的输注形式后,发现真皮内注射DC后,10min内就可见标记的DC迁移入引流淋巴结,4h后引流淋巴结显象最明显,证实真皮内注射可以使DC快速迁移至引流淋巴结且可以滞留较长时间,说明真皮内注射可能是DC疫苗抗肿瘤治疗的另一较佳输注途径.(3)瘤体内注射:目前,I)C疫苗抗肿瘤治疗临床试验,大都采用肿瘤细胞抗原肽,肿瘤细胞溶解物或凋亡的肿瘤细胞先体外致敏DE,然后回输体内.6树突细胞瘤苗的剂量和用法一般用的方案是:致敏树突状细胞制成1×1个细胞/0.5n1l,注射用细胞悬液,每次剂量为1×1个细胞,每周1次,连续用4周,然后间隔2周,再次接种以增强免疫,总接种量为5×1个树突状细胞.研究认为DC注射的细胞数量与肿瘤缓解的时间成正比.但是否细胞数量越高,治疗效果越好,有无平台效应,细胞数量多少为最佳尚需进一步研究.7展望树突状细胞加肿瘤抗原将会成为有效的肿瘤免疫基因治疗手段.由于DC疫苗能促进同种异体T细胞增殖的特性及其强大的抗原提呈功能,不仅能将抗原提呈给M/-ICⅡ类分子促进cDT细胞增殖,又能提呈给MHCI类分子促进c聪T细胞增殖,诱发机体强烈的细胞免疫应答;同时研究还发现,DC在体液免疫中也发挥重要作用,可直接参与调节B细胞的成熟和分化,刺激B细胞增殖产生大量的IsA和IgM,全面调动机体的抗肿瘤免疫力,在机体抵御恶性肿瘤中发挥重要作用.DC疫苗的初步临床试用也显示出了良好的疗效.该疗法可望成为肿瘤生物治疗的又一新兴手段.参考文献】gl,En~emanEG.Dendriticcellsincancerimmunotherapy.AnnReviro—munol,2000,18:245—273.●2TakamizawaM,RivasA,FagnoniF,eta1.Dendriticcellsthatprocessandpr一~-,entnominalantigenstonaiveTlymphoeytesalederivedfromCD2pre—cursol~.Jlnmaunol,1997,158:2134-2142.3ShortmanK.|]umetoration:dendriticcells:multiplesubLypes,multipleori—gins,multiplefunctic~ns.1nmaunolCellBoil,2000,78:161—165.4BarmhemauJ,BriereJ,CauxC,etaI.Immunologyofdendn'ticcells.A/lnul~.evlnrnunol,2OO0,18:767.8l1.5LevinD,ConstantS,PasqualiniT,eta】.Roleofdendriticcellsinthepriming ofCITlymphocytestopeptideantigeninvivo.Jlmmund,1993.151:6742.6St~rmtan.DC—SIGN:Aguidetos0fT1emysteriesofdentin'ticceils.Cells.2000,100:491494.7GeijtenbeekTBH,TorensmaR,V anVlletSJ,eta1.IdentificatonofDC.SIGN, anoveldendriticcellspecificICAMsreceptorthatsupportsprimaryimmuneres.Cell,2000,100:575-585.8ChenSR,AkSMF.TanimotoK,eta1.AbsenceofCPositivematureand activateddendriticcellsatc锄cernodulesfrompatients山bepatocellular carcinomarelevancetohepatocarcinogenesis.CancerLe~em,2000,148:49.174河~t,lN药2004年2月第26趁第—2lt~J—Hebe—iMedicalJo—urnal,Feb2004,V ol26,No.2,.9曹雪涛.树突状细胞基础与临床研究新进展.中国免疫学杂志,1998,14:161—167.1O孙劲旅,张锦.树突状细胞与肿瘤免疫研究进展.tf1国肿瘤I临床与康复,1998,5:80—82.11叶闻斐,秦慧莲,何球藻.兀与FI-1]及其在体外诱导树突状细胞增殖的作用.闷外医学免疫学分册,1998,21:74-76.12曹雪涛,叶天星.树突状细胞研究在免疫学中的意义及发展趋势.困外医学免疫学分册,1998,21:281,285.13QuahB,O'NeillliC.Review:the)p】ieationofdendriticcell—derivedexo—s(m1esintumourimmunotherapy.CancerBiotherRadiopharm,21300,159 185,194.14M~tckensenA.KrauseT,BlumU,eta1.Homingofintravenouslyandinira—lymphatica]lyinjectedhumandendriticcellsgeneratedinvitroncoilhe—matopoieticprogenitorcells.Cancerlmmunollmmunother,lI9,48:1l8一l】2.15l!aonmsR,ChambersM,BoytarR,eta1.Metastaticlesionsinthejoint一elatedthacuteinflammatoryarthritisafterdendriticcellimmunotherapyfor metastaticmelanoma.MelanomaRes.l999.9:474.481.树突状细胞在脑胶质瘤治疗中的应用李春晖张庆九焦保华胶质瘤的主动免疫治疗(activeimmtmotherapy)一直是胶质瘤治疗研究的热点,然而有关肿瘤的免疫逃避,肿瘤特异性抗原以及肿瘤治疗中免疫的合适方法,路径等都是研究者必须妥善解决的问题.树突状细胞(dendriticce]ls,DEs)是摄取,加工,递呈抗原的最重要的专职抗原递呈细胞(antigenpresentingcell, APC),它递呈抗原的能力最强.1DEs的获得1.1DEs的来源Ronani描述了将从化疗病人骨髓抑制期间的外周血中获取的单核细胞进行培养,得到大量的树突状细胞.从这种状态下获取的单核细胞其造血干细胞的比例较稳定状态下获取的单核细胞造血干细胞的比例高.Koch等…发现培养从外周血中纯化的人CD;造血干细胞可诱导细胞表型和功能特异性DEs,是DEs个体发育和成熟理论的主要突破.Caux等的报道与此有明显争议(是否DEs直接生成于早期造血干细胞或衍生于血单核细胞?)他们阐述了DCs两种不同的发展途径.当CD;造血=F细胞(来自于人脐带血)在GMCSF+TNF-a中培养5~7d后,:两种DEs前体出现:第一种前体由表达CD..和CD.缺失而确认,将成熟为DCs,并带有表皮郎罕氏细胞的特点(表达Birbeck颗粒滞后抗原和粘滞素).第二种前体,CD..一CD将成熟为CD+DEs(缺乏Birbeck颗粒滞后抗原和B粘滞素).而cD前体代表双潜能细胞,在有巨噬细胞集落刺激因子(GM—CSF)诱导时可有不同的反应,成为类巨噬细胞.1.2D【的培养实验中应用的DEs主要通过培养骨髓细胞获得.骨髓细胞自股骨,胫骨中获得,在GM.CSF+II厂4或GM, CSF+a中培养,在第8天可见到大量具有DCs形态学特点的细胞集合体增生.每只小鼠培养DCs的产量大约为10×1 (GM—CSF+IL广4),6×1(GM—CSF+TNF—a)和5×lo'(GM—CSF). 流式细胞技术评价这些DEs的抗原表达,包括c,C,CD.(Mac一1),CDt8,cD-Io,cD8【】(B7),cI(B7.2),并指细胞抗原NLIX;.45和MT1C—I型,U型抗原.在GM—CSF+IIJ_4中培养的细作者单位:O5OOOO河北医科大学第二医院神经外科胞MHC,Ⅱ类分子和共刺激分子(costimulatorymolecules)岛_l,岛.2 的水平最高,而且是更加有效的同基因混合淋巴细胞反应刺激物.人DCs主要将从外周血中分离的单核细胞进行培养,其DEs培养结果与上述相同.2DEs的功能DCs是最有效的同种异体混合淋巴细胞反应刺激物.DEs可传递抗原给T,B淋巴细胞,DEs对外生抗原有吞饮作用.在细胞内,抗原被加工成短肽,递呈到DEs细胞表面的MHC分子上.作为初级淋巴细胞基本要求的共刺激分子在DEs上有高水平表达,这些共刺激分子包括cD町(.)cD龉(岛.)和cD舶….在共刺激分子存在的条件下,已致敏的淋巴细胞被递呈给免疫系统,这提供了一种对抗自身免疫的保护作用.侵入抗原被摄取后,可能在TNF-ct的影响下,DCs转变为成熟树突状细胞,迁移到局部淋巴结,将抗原递呈给T淋巴细胞.DEs再成熟前摄取,加工抗原的能力较强,抗原递呈功能较弱,而成熟后抗原递呈功能较强,摄取,加工抗原的能力较弱.3DEs在脑胶质瘤中的应用中枢神经系统很长时间内被认为免疫豁免区,免疫活性在颅内受限制的机制还不能被完全理解,但好象包括明显解剖学特点,如淋巴引流的缺如,血脑屏障的存在,并且在主要组织相容性复合体存在的情况下,小胶质细胞和星形细胞可递呈抗原.但中枢神经系统的免疫豁免不是绝对的,Esther等将小鼠脑组织与GM-CSF共同培养,得到了具有良好抗原递呈功能的DCs,Stao发现小鼠的垂体问质细胞中主要成分为DEs.在实验性过敏性脑脊髓炎中,对髓磷脂基础蛋白的外周免疫引出的特异性抗原诱导了细胞毒性T淋巴细胞(CTL)介导的脱髓鞘作用,暗示中枢神经系统特异性免疫反应来自于合适的靶抗原的递呈和有效的诱导免疫反应….4DEs疫苗的制备多种应用DEs诱导免疫反应的方法已得到研究:提取肿瘤细胞蛋白或肽致敏DEs,将转录肿瘤相关抗原的基因转导入DEs,DEs与肿瘤细胞共同培养,DEs与肿瘤细胞融合等.。

树突状细胞的生物学功能的研究进展树突状细胞(dendritic cells,DC)是目前人体内最活跃,功能最强大的专职抗原呈递细胞,是人体对免疫原产生免疫应答的重要细胞之一。
DC 广泛存在于血液、淋巴、肝脾及皮肤黏膜等组织,能激活功能性淋巴细胞,并产生细胞毒作用,提高机体免疫水平。
DC对抗原和弱抗原都有很高的呈递效率,只需少量的抗原及DC即可激活T细胞,因此成为抗肿瘤和抗病毒免疫研究中的热点。
1DC的来源与分化发育DC 的产生分两个阶段:从祖细胞分化为未成熟DC和未成熟DC受外界刺激( 如细菌产物、坏死物及及各种细胞因子) 分化成熟。
1.1DC的分化体内DC 起源于多能造血干细胞,按来源其分化途径分为两条: ①髓系分化途径。
称为髓系DC( myebiod,DC1) ,最终分化为朗格汉斯细胞和间质DC两个亚群。
DC1 由髓样干细胞在粒细胞巨噬细胞集落刺激因子( granulocyte-macrophagecolony stimulati ng factor,GM-CSF) 、肿瘤坏死因子α刺激下诱生为DC。
亦有来源于外周血单核细胞,也称为DC1 前体细胞,在GM-CSF、白细胞介素4( interleukin-4,IL-4) 作用下或穿越内皮细胞并吞噬异物后分化为DC。
②淋巴系分化途径。
为淋巴系DC( lymphoid,DC2) ,最终分化为类浆细胞DC。
DC2 的前体细胞不表达髓系抗原,也无吞噬、吞饮抗原能力,低表达GM-CSF,高表达IL-3 受体,在IL-3 刺激下分化为DC2。
目前对DC 亚群及分化的研究主要来源于体外培养的方法,体内天然DC 亚群的分类仍有待于进一步研究[1]。
1.2DC的表型变化DC的发育分为成熟与未成熟阶段,两者具有不同的生物学特征和细胞表型。
正常情况下,体内多数DC 处于未成熟阶段,其广泛分布于全身各外周组织,高表达吞噬相关受体( Fc 受体、补体受体、甘露糖受体) ,而不表达或低表达共刺激分子和黏附分子( CD14、CD54、CD40、CD80) 。
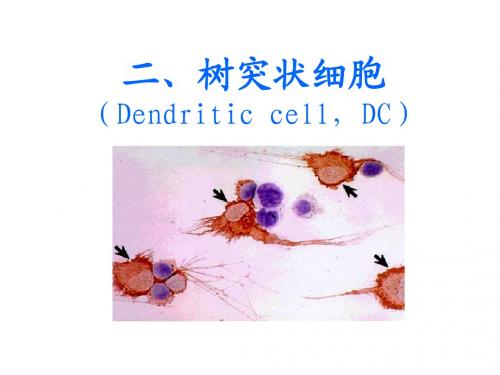


名词解释dc树突状细胞
DC树突状细胞是一种极其重要的免疫系统细胞,它是体内专职的抗原提呈细胞,在免疫应答启动和调节过程中扮演关键角色。
树突状细胞因其成熟时形态特征而得名,具有许多分支状突起,类似于神经元的树突,故称“树突状细胞”。
DC细胞广泛分布于身体各组织中,包括皮肤、黏膜、血液以及淋巴器官等,并且它们可以从这些部位捕获抗原(如病原体、肿瘤抗原等)。
一旦吞噬了抗原,DC会将其处理并结合到主要组织相容性复合体分子上,然后迁移至淋巴结,在那里与初始T细胞接触,激活T细胞并指导其分化为效应T细胞或记忆T细胞,从而触发适应性免疫反应。
树突状细胞可以根据其来源和功能进一步细分为不同的亚群,例如髓样DC、淋巴样DC、浆细胞样DC等,每种类型的DC都有独特的生物学特性和功能。
通过研究和利用DC的功能特性,科学家们开发出了DC疫苗等免疫疗法,用于治疗癌症和其他疾病。