仿制药参比制剂目录(第五批)
- 格式:doc
- 大小:104.00 KB
- 文档页数:7
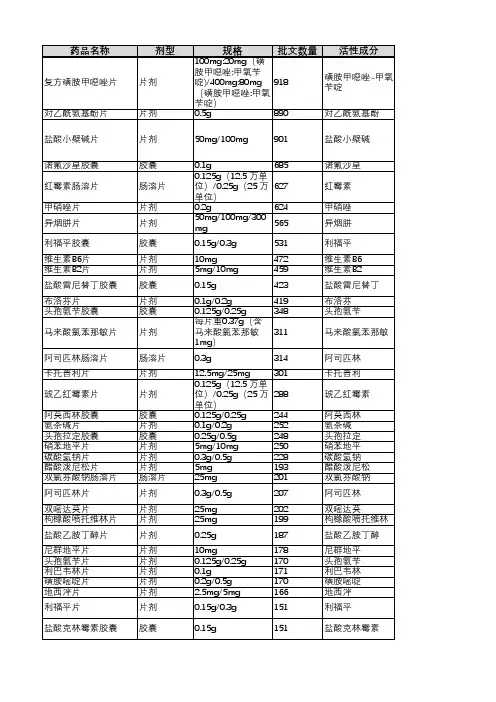


国家药监局关于发布仿制药参比制剂目录(第三十九批)的通告正文:----------------------------------------------------------------------------------------------------------------------------------------------------国家药品监督管理局通告2021年第20号国家药监局关于发布仿制药参比制剂目录(第三十九批)的通告经国家药品监督管理局仿制药质量和疗效一致性评价专家委员会审核确定,现发布仿制药参比制剂目录(第三十九批)。
特此通告。
附件:仿制药参比制剂目录(第三十九批)国家药监局2021年3月1日附件仿制药参比制剂目录(第三十九批)序号药品通用名称英文名称/商品名规格备注1备注239-1匹维溴铵片Pinaverium Bromide Tablets/ Dicetel50mgAbbott Laboratories Limited国内上市的原研药品原研进口39-2盐酸阿莫罗芬乳膏Amorolfine Hydrochloride Cream/Loceryl(罗每乐)0.25%Galderma Laboratorium GmbH国内上市的原研药品原研进口39-3硫酸异帕米星注射液Isepamicin Sulfate Injection/Exacin(依克沙)2ml:400mg(按异帕米星(C22H43N5O12)计)Asahi Kasei Pharma Corporation国内上市的原研药品原研进口39-4硫酸异帕米星注射液Isepamicin Sulfate Injection/Exacin(依克沙)2ml:200mg(按异帕米星(C22H43N5O12)计)Asahi Kasei Pharma Corporation国内上市的原研药品39-5盐酸美金刚多奈哌齐缓释胶囊Memantine Hydrochloride Extended-release and Donepezil Hydrochloride Capsules/Namzaric 7mg/10mgAllergan Sales LLC未进口原研药品美国橙皮书39-6盐酸美金刚多奈哌齐缓释胶囊Memantine Hydrochloride Extended-release and Donepezil Hydrochloride Capsules/Namzaric 14mg/10mgAllergan Sales LLC未进口原研药品美国橙皮书39-7盐酸美金刚多奈哌齐缓释胶囊Memantine Hydrochloride Extended-release and Donepezil Hydrochloride Capsules/Namzaric 21mg/10mgAllergan Sales LLC未进口原研药品美国橙皮书39-8盐酸美金刚多奈哌齐缓释胶囊Memantine Hydrochloride Extended-release and Donepezil Hydrochloride Capsules/Namzaric 28mg/10mgAllergan Sales LLC未进口原研药品美国橙皮书39-9赖氨洛芬注射液Ibuprofen Lysine Injection/NeoProfen20mg/2mlRecordati Rare Diseases Inc.未进口原研药品美国橙皮书39-10盐酸苯达莫司汀注射液Bendamustine Hydrochloride Injection/Belrapzo100mg/4ml(25mg/ml)Eagle Pharmaceuticals, Inc.未进口原研药品美国橙皮书39-11米哚妥林胶囊Midostaurin Capsules/Rydapt25mgNovartis Pharmaceuticals Corporation未进口原研药品美国橙皮书39-12盐酸米诺环素缓释片Minocycline Hydrochloride Extended Release Tablets/Solodyn 55mgMedicis Pharmaceutical Corp未进口原研药品美国橙皮书39-13盐酸米诺环素缓释片Minocycline Hydrochloride Extended Release Tablets/Solodyn65mgMedicis Pharmaceutical Corp未进口原研药品美国橙皮书39-14盐酸米诺环素缓释片Minocycline Hydrochloride Extended Release Tablets/Solodyn 80mgMedicis Pharmaceutical Corp未进口原研药品美国橙皮书39-15盐酸米诺环素缓释片Minocycline Hydrochloride Extended Release Tablets/Solodyn 105mgMedicis Pharmaceutical Corp未进口原研药品美国橙皮书39-16盐酸米诺环素缓释片Minocycline Hydrochloride Extended Release Tablets/Solodyn 115mgMedicis Pharmaceutical Corp未进口原研药品美国橙皮书39-17盐酸去氧肾上腺素滴眼液Phenylephrine Hydrochloride Ophthalmic Solution2.5%Akorn Operating Co Llc未进口原研药品美国橙皮书39-18盐酸去氧肾上腺素滴眼液Phenylephrine Hydrochloride Ophthalmic Solution 10%Akorn Operating Co Llc未进口原研药品美国橙皮书39-19奥利司他咀嚼片Orlistat Chewable Tablet/Alli27mgGlaxoSmithKline (Ireland)Limited未进口原研药品欧盟上市39-20依达拉奉注射液Edaravone Injection100ml:30mgMitsubishi Tanabe Pharma Corporation国内上市的原研药品原研进口39-21马来酸阿伐曲泊帕片Avatrombopag Maleate Tablets/Doptelet(苏可欣)20mgAkaRx Inc.国内上市的原研药品原研进口39-22地高辛片Digoxin Tablets/Lanoxin0.125mgConcordia Pharmaceuticals Inc未进口原研药品美国橙皮书39-23盐酸奥洛他定滴眼液Olopatadine Hydrochloride ophthalmic solution 0.2%/ Pataday 0.2%Alcon Laboratories Inc未进口原研药品美国橙皮书39-24富马酸喹硫平片Quetiapine Fumarate Tablets/ Seroquel25mgAstraZeneca Pharmaceuticals LP未进口原研产品美国橙皮书39-25富马酸喹硫平片Quetiapine Fumarate Tablets/ Seroquel300mgAstraZeneca Pharmaceuticals LP未进口原研产品美国橙皮书39-26沙美特罗替卡松吸入粉雾剂Salmeterol Xinafoate and Fluticasone Propionate Powder for Inhalation/Advair Diskus 100mcg/50mcgGlaxo Smith Kline未进口原研药品美国橙皮书39-27沙美特罗替卡松吸入粉雾剂Salmeterol Xinafoate and Fluticasone Propionate Powder for Inhalation/Advair Diskus 250mcg/50mcgGlaxo Smith Kline未进口原研药品美国橙皮书39-28沙美特罗替卡松吸入粉雾剂Salmeterol Xinafoate and Fluticasone Propionate Powder for Inhalation/Advair Diskus 500mcg/50mcgGlaxo Smith Kline未进口原研药品美国橙皮书39-29沙美特罗替卡松吸入粉雾剂Salmeterol Xinafoate and Fluticasone Propionate Powder for Inhalation/Seretide Diskus 50mcg/100mcgGlaxo Wellcome UK Ltd未进口原研药品欧盟上市39-30沙美特罗替卡松吸入粉雾剂Salmeterol Xinafoate and Fluticasone Propionate Powder for Inhalation/Seretide Diskus 50mcg/250mcgGlaxo Wellcome UK Ltd未进口原研药品欧盟上市39-31沙美特罗替卡松吸入粉雾剂Salmeterol Xinafoate and Fluticasone Propionate Powder for Inhalation/Seretide Diskus 50mcg/500mcgGlaxo Wellcome UK Ltd未进口原研药品欧盟上市39-32雷诺嗪缓释片Ranolazine Prolonged-Release Tablets /Ranexa500mgMenarini International Operations Luxembourg S.A未进口原研药品欧盟上市39-33交联玻璃酸钠注射液Hyaluronic acid, stabilized single injection/ Durolane3 ml:玻璃酸钠60mgBioventus LLC未进口原研药品欧盟上市39-34特立氟胺片Teriflunomide Tablets/Aubagio14mgSanofi-Aventis Groupe未进口原研药品欧盟上市39-35盐酸美金刚片Memantine Hydrochloride Tablets/Ebixa5mgH. Lundbeck A/S未进口原研药品欧盟上市39-36盐酸美金刚片Memantine Hydrochloride Tablets/Ebixa15mgH. Lundbeck A/S未进口原研药品欧盟上市39-37中长链脂肪乳/氨基酸(16)/葡萄糖(30%)注射液Medium and Long Chain Fat Emulsion / Amino Acids (16) / Glucose (30%) Injection/NuTRIflex Lipid plus1875mlB.Braun Melsungen AG未进口原研药品欧盟上市39-38脂肪乳氨基酸(17)葡萄糖(19%)注射液Fat Emulsion, Amino Acids(17) And Glucose(19%) Injection/Kabiven2053mlFresenius Kabi国际公认的同种药品欧盟上市39-39左甲状腺素钠片Levothyroxine Sodium Tablets200μgMerck Serono GmbH/Merck Sante/Merck Gesellschaft mbH 未进口原研药品欧盟上市39-40依普利酮片Eplerenone Tablets25mgファイザー株式会社未进口原研药品日本上市39-41依普利酮片Eplerenone Tablets50mgファイザー株式会社未进口原研药品日本上市39-42依普利酮片Eplerenone Tablets100mgファイザー株式会社未进口原研药品日本上市39-43枸橼酸坦度螺酮片Tandospirone Citrate Tablets 5mg大日本住友製薬株式会社未进口原研日本上市39-44别嘌醇片Allopurinol Tablets / Zyloric 50mgグラクソ?スミスクライン株式会社未进口原研药品日本上市39-45别嘌醇片Allopurinol Tablets / Zyloric 100mgグラクソ?スミスクライン株式会社未进口原研药品日本上市39-46吡仑帕奈片Perampanel Tablets/Fycompa2mgEisai Inc/Eisai Europe Limited未进口原研药品英国上市39-47吡仑帕奈片Perampanel Tablets/Fycompa4mgEisai Inc/Eisai Europe Limited未进口原研药品英国上市39-48吡仑帕奈片Perampanel Tablets/Fycompa8mgEisai Inc/Eisai Europe Limited未进口原研药品英国上市39-49吡仑帕奈片Perampanel Tablets/Fycompa12mgEisai Inc/Eisai Europe Limited未进口原研药品英国上市39-50硫酸吗啡缓释片Morphine Sulphate Sustained-release Tablets 30mgNapp Pharmaceuticals Limited未进口原研药品英国上市39-51拉莫三嗪分散片Lamotrigine Dispersible Tablets/Lamictal2mgThe Wellcome Foundation Ltd.未进口原研药品英国上市7-25对乙酰氨基酚片Paracetamol Tablets/Panadol Advance Tablets0.5gGlaxoSmithKline Consumer Healthcare欧盟上市备注1由“欧盟上市(上市国家:英国;产地:德国)”更正为“欧盟上市”7-88盐酸溴己新片Bromhexine Hydrochloride Tablets/Bisolvon8mgBoehringer Ingelheim Pharma GmbH & Co. KG/Sanofi-Aventis Deutschland GmbH 未进口原研药品持证商发生变更,增加持证商Sanofi-Aventis Deutschland GmbH23-219脂肪乳氨基酸(17)葡萄糖(19%)注射液Fat Emulsion,Amino Acids(17) And Glucose(19%) Injection/Kabiven1026mlFresenius Kabi AB国内上市的国际公认药品持证商更新为Fresenius Kabi AB23-220脂肪乳氨基酸(17)葡萄糖(19%)注射液Fat Emulsion,Amino Acids(17) And Glucose(19%) Injection/Kabiven2053mlFresenius Kabi AB国内上市的国际公认药品持证商更新为Fresenius Kabi AB27-104米力农注射液Milrinone Injection /Primacor 1mg/ml Solution for Injection10mg/10mlAventis Pharma Limited/Sanofi-Aventis/Sanofi未进口原研药品规格更新为10mg/10ml备注1.未在国内上市品种,需参照原食品药品监管总局2015年第230号公告等的相关要求开展研究,通用名、剂型等经药典委核准后为准。
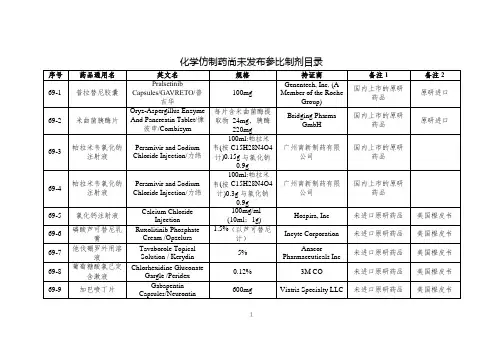

国家药监局关于发布仿制药参比制剂目录(第三十八批)的通告正文:----------------------------------------------------------------------------------------------------------------------------------------------------国家药品监督管理局通告2021年第18号国家药监局关于发布仿制药参比制剂目录(第三十八批)的通告经国家药品监督管理局仿制药质量和疗效一致性评价专家委员会审核确定,现发布仿制药参比制剂目录(第三十八批)。
特此通告。
附件:仿制药参比制剂目录(第三十八批)国家药监局2021年2月20日附件仿制药参比制剂目录(第三十八批)序号药品通用名称英文名称/商品名规格持证商备注1备注238-1噻托溴铵奥达特罗吸入喷雾剂Tiotropium Bromide and Olodaterol Hydrochloride Inhalation Spray/Spiolto(思合华)每瓶60喷,每喷含噻托铵2.5μg(相当于噻托溴铵一水合物3.124μg)和奥达特罗2.5μg(相当于盐酸奥达特罗2.736μg)Boehringer Ingelheim International GmbH国内上市的原研药品原研进口38-2噻托溴铵喷雾剂Tiotropium Bromide Spray每瓶60喷,每喷含噻托铵2.5μg,药液浓度含噻托铵0.2262mg/mlBoehringer Ingelheim International GmbH国内上市的原研药品原研进口38-3硝酸咪康唑阴道软胶囊Miconazole Nitrate Vaginal Soft Capsules/Gyno-Daktarin(达克宁)0.4gJanssen-Cilag N.V.国内上市的原研药品原研进口38-4硝酸咪康唑阴道软胶囊Miconazole Nitrate Vaginal Soft Capsules/Gyno-Daktarin(达克宁)1.2gJanssen-Cilag N.V.国内上市的原研药品原研进口38-5丁丙诺啡纳洛酮舌下片Buprenorphine Hydrochloride and Naloxone Hydrochloride Sublingual Tablets 丁丙诺啡2mg/纳洛酮0.5mg(均以碱基计)Indivior UK Limited国内上市的原研药品原研进口38-6丁丙诺啡纳洛酮舌下片Buprenorphine Hydrochloride and Naloxone Hydrochloride Sublingual Tablets 丁丙诺啡8mg/纳洛酮2mg(均以碱基计)Indivior UK Limited国内上市的原研药品原研进口38-7羧甲基纤维素钠滴眼液Carboxymethylcellulose Sodium Eye Drops0.4ml:2mgAllergan Pharmaceuticals Ireland国内上市的原研药品原研进口38-8复方倍他米松注射液Compound Betamethasone Injection/得宝松1ml:二丙酸倍他米松(以倍他米松计)5mg与倍他米松磷酸钠(以倍他米松计)2mg MSD Merck Sharp & Dohme AG国内上市的原研药品原研进口38-9注射用全氟丁烷微球Perflubutane Microspheres for Injection/Sonazoid(示卓安)每瓶中含微球的体积为16μlGE Healthcare AS国内上市的原研药品原研进口38-10索磷维伏片Sofosbuvir,Velpatasvir and Voxilaprevir tablets/Vosevi(沃士韦)每片含 400mg 索磷布韦、100mg 维帕他韦和 100mg 伏西瑞韦Gilead Sciences Ireland UC国内上市的原研药品原研进口38-11复合维生素片Vitamin Complex Tablets/ Elevit Pronatal(爱乐维)复方制剂Bayer S.A.国内上市的原研药品原研进口38-12盐酸奥洛他定鼻喷雾剂Olopatadine Hydrochloride Nasal Spray/Patanase0.665mg/sprayNovartis Pharmaceuticals Corp未进口原研药品美国橙皮书38-13盐酸环丙沙星滴眼液Ciprofloxacin Ophthalmic Solution/Ciloxan0.30%Novartis Pharmaceuticals Corp未进口原研药品美国橙皮书38-14硫酸麻黄碱注射液Ephedrine Sulfate Injection/Akovaz50mg/mlExela Pharma Sciences LLC未进口原研药品美国橙皮书38-15艾考糊精腹膜透析液Icodextrin Peritoneal Dialysis Solution/Extraneal 含7.5%艾考糊精(2L/袋、2.5L/袋)Baxter Healthcare Corporation未进口原研药品美国橙皮书38-16艾考糊精腹膜透析液Icodextrin Peritoneal Dialysis Solution/Extraneal 含7.5%艾考糊精(1.5L/袋、2L/袋、2.5L/袋)Baxter A/S未进口原研药品欧盟上市38-17氨基酸(15)腹膜透析液Amino Acids (15) Peritoneal Dialysis Solution 2.0LBaxter Healthcare Ltd.未进口原研药品欧盟上市38-18氨基酸(15)腹膜透析液Amino Acids (15) Peritoneal Dialysis Solution 2.5LBaxter Healthcare Ltd.未进口原研药品欧盟上市38-19麦芽酚铁胶囊Ferric Maltol Capsules /Feraccru每片含铁30mgNorgine B.V.未进口原研药品欧盟上市38-20氯甲西泮注射液Lormetazepam Injection/ Sedalam10ml:2mgDr. Franz K?hler Chemie GmbH未进口原研药品欧盟上市38-21硝酸异康唑阴道片Isoconazole Nitrate Vaginal Tablets300mgバイエル薬品株式会社未进口原研药品日本上市38-22盐酸头孢卡品酯片Cefcapene Pivoxil Hydrochloride Tablet/Flomox 100mg塩野義製薬株式会社未进口原研药品日本上市38-23氧氟沙星滴耳液Ofloxacin Ear Drops0.30%アルフレッサファーマ株式会社/第一三共株式会社未进口原研药品日本上市38-24氟骨化三醇片Falecalcitriol Tablets/Fulstan0.15μg大日本住友製薬株式会社未进口原研药品日本上市38-25氟骨化三醇片Falecalcitriol Tablets/Fulstan0.3μg大日本住友製薬株式会社未进口原研药品日本上市38-26注射用盐酸吡柔比星Pirarubicin Hydrochloride for Injection/Pinorubin 10mg日本マイクロバイオファーマ株式会社未进口原研药品日本上市38-27注射用盐酸吡柔比星Pirarubicin Hydrochloride for Injection/Pinorubin 20mg日本マイクロバイオファーマ株式会社未进口原研药品日本上市38-28注射用盐酸吡柔比星Pirarubicin Hydrochloride for Injection/Pinorubin 30mg日本マイクロバイオファーマ株式会社未进口原研药品日本上市38-29注射用盐酸多柔比星Doxorubicin Hydrochloride for Injection /Adriacin 10mgアスペンジャパン株式会社未进口原研药品日本上市38-30美沙拉秦缓释颗粒Mesalazine Sustained-release Granules /Pentasa 1g,按美沙拉秦(C7H7NO3)计Ferring S.A.S未进口原研药品法国上市38-31美沙拉秦缓释颗粒Mesalazine Sustained-release Granules /Pentasa 2g,按美沙拉秦(C7H7NO3)计Ferring S.A.S未进口原研药品法国上市38-32富马酸伏诺拉生片Vonoprazan Fumarate Tablets /Vocinti(沃克)10mgTakeda Pharmaceutical Company Limited国内上市的原研药品原研进口38-33富马酸伏诺拉生片Vonoprazan Fumarate Tablets /Vocinti(沃克)20mgTakeda Pharmaceutical Company Limited国内上市的原研药品原研进口38-34碳酸镧颗粒Lanthanum Carbonate Oral Powder/ Fosrenol 1000mgShire Development LLC/Takeda Pharmmaceuticals USA INC 未进口原研药品美国橙皮书38-35尼莫地平口服溶液Nimodipine Oral Solution / Nymalize6mg/mlArbor Pharmaceuticals, LLC未进口原研药品美国橙皮书38-36氟尿嘧啶注射液Fluorouracil Injection/ Fluorouracil500mg/10mlAccord Healthcare, Inc国际公认的同种药品美国橙皮书38-37小儿复方氨基酸注射液(19AA-Ⅰ)10% Amino Acid Injection /Trophamine 10%10%(500ml)B Braun Medical Inc未进口原研药品美国橙皮书38-38氯化钾缓释片Potassium Chloride Extended Release Tablets/K-Tab20mEq(相当于1.5g氯化钾)Abbvie Inc未进口原研药品美国橙皮书38-39盐酸吡格列酮片Pioglitazone Hydrochloride Tablets/Actos45mgTakeda Pharmaceuticals USA Inc未进口原研药品美国橙皮书38-40盐酸丁螺环酮片Buspirone Hydrochloride Tablet15mgTeva Pharmaceuticals USA Inc.国际公认的同种药品美国橙皮书38-41盐酸罗匹尼罗缓释片Ropinirole Hydrochloride Sustained-release Tablets 8mgGLAXO SMITHKLINE/SmithKline Beecham Limited未进口原研药品欧盟上市38-42亚叶酸钙注射液Calcium Folinate Injection5ml:50mgHospira UK Ltd未进口原研药品欧盟上市38-43苯磺酸氨氯地平片Amlodipine Besylate Tablets10mg(以C20H25CLN2O5计)Pfizer未进口原研药品欧盟上市38-44甲氨蝶呤注射液Methotrexate Injection2ml:50mgPfizer Pharma Pfe GmbH未进口原研药品欧盟上市38-45多西他赛注射液Docetaxel Injection/Taxotere20mg/1mlSanofi Mature IP未进口原研药品欧盟上市38-46盐酸罗哌卡因注射液Ropivacaine Hydrochloride Injection/Naropin/Naropeine/Naropina20mg/10mlAspen Pharma Trading Limited未进口原研药品欧盟上市38-47盐酸坦索罗辛口崩缓释片Tamsulosin Hydrochloride Oral Dispersible Sustained Release Tablets0.2mgAstellas Pharma Inc/アステラス製薬株式会社未进口原研药品日本上市38-48钆特醇注射液Gadoteridol Injection/ ProHance10ml:2.793gブラッコスイス株式会社未进口原研药品日本上市38-49钆特醇注射液Gadoteridol Injection/ ProHance15ml:4.1895gブラッコスイス株式会社未进口原研药品日本上市38-50注射用头孢他啶Ceftazidime For Injection/Modacin1.0gグラクソ?スミスクライン株式会社未进口原研药品日本上市38-51注射用氨曲南Aztreonam For Injection1.0g日本エーザイ株式会社未进口原研药品日本上市5-19卡托普利片Captopril Tablets/Captopril12.5mgDaiichi Sankyo Espha Co., Ltd./アルフレッサファーマ株式会社日本橙皮书增加持证商アルフレッサファーマ株式会社5-20卡托普利片Captopril Tablets/Captopril25mgDaiichi Sankyo Espha Co., Ltd./アルフレッサファーマ株式会社日本橙皮书增加持证商アルフレッサファーマ株式会社21-102注射用环磷酰胺Cyclophosphamide for Injection/Endoxan(安道生)1gBaxter Oncology GmbH/Baxter Healthcare Ltd国内上市的原研药品增加持证商Baxter Healthcare Ltd23-48阿普司特片Apremilast Tablet /Otezla10mgCelgene Corp/Amgen Inc未进口原研药品增加持证商Amgen Inc23-49阿普司特片Apremilast Tablet /Otezla20mgCelgene Corp/Amgen Inc未进口原研药品增加持证商Amgen Inc27-412阿普司特片Apremilast Tablet /Otezla30mgCelgene Corp/Amgen Inc未进口原研药品增加持证商Amgen Inc27-372苯磺酸氨氯地平片Amlodipine Besylate Tablets5mg(以C20H25CLN2O5计)Pfizer Luxembourg Sarl/Pfizer Limited/Pfizer未进口原研药品增加持证商Pfizer Luxembourg Sarl/Pfizer;不限定商品名8-175盐酸齐拉西酮胶囊Ziprasidone Hydrochloride Capsules/Zeldox20mg(按齐拉西酮计)Pfizer Australia Pty Limited / Pfizer Pharma PFE GmbH原研进口持证商变更,增加变更后持证商Pfizer Pharma PFE GmbH8-225盐酸齐拉西酮胶囊Ziprasidone Hydrochloride Capsules/Zeldox40mg(按齐拉西酮计)Pfizer Australia Pty Limited / Pfizer Pharma PFE GmbH原研进口持证商变更,增加变更后持证商Pfizer Pharma PFE GmbH21-111沙美特罗替卡松吸入粉雾剂Salmeterol Xinafoate and Fluticasone Propionate Powder for Inhalation/Seretide(舒利迭)50ug/100ug/泡Laboratoire GlaxoSmithKline国内上市的原研药品药品通用名称修订为“沙美特罗替卡松吸入粉雾剂”21-112沙美特罗替卡松吸入粉雾剂Salmeterol Xinafoate and Fluticasone Propionate Powder for Inhalation/Seretide(舒利迭)50ug/250ug/泡Laboratoire GlaxoSmithKline国内上市的原研药品药品通用名称修订为“沙美特罗替卡松吸入粉雾剂”21-113沙美特罗替卡松吸入粉雾剂Salmeterol Xinafoate and Fluticasone Propionate Powder for Inhalation/Seretide(舒利迭)50ug/500ug/泡Laboratoire GlaxoSmithKline国内上市的原研药品药品通用名称修订为“沙美特罗替卡松吸入粉雾剂”21-116沙美特罗替卡松吸入气雾剂Salmeterol Xinafoate and Fluticasone Propionate Aerosol/Seretide(舒利迭)25ug/125ug/揿Laboratoire GlaxoSmithKline国内上市的原研药品药品通用名称修订为“沙美特罗替卡松吸入气雾剂”22-122氟维司群注射液Fulvestrant Injection/Faslodex(芙仕得5ml:0.25gAstraZeneca UK Limited/AstraZeneca AB国内上市的原研药品持证商发生变更,增加变更后持证商AstraZeneca AB23-217中长链脂肪乳/氨基酸(16)/葡萄糖(36%)注射液Medium and Long Chain Fat Emulsion,Amino Acids(16)and Glucose(36%) Injection625mlB. Braun melsungen ag国际公认的同种药品英文名称修订为“Medium and Long Chain Fat Emulsion,Amino Acids(16)and Glucose(36%) Injection”23-218中长链脂肪乳/氨基酸(16)/葡萄糖(36%)注射液Medium and Long Chain Fat Emulsion,Amino Acids(16)and Glucose(36%) Injection1250mlB. Braun melsungen ag国际公认的同种药品英文名称修订为“Medium and Long Chain Fat Emulsion,Amino Acids(16)and Glucose(36%) Injection”27-326琥珀酸索利那新片Solifenacin Succinate Tablets/Vesicare5mgAstellas Pharma US Inc未进口原研药品更新持证商为Astellas Pharma US Inc27-327琥珀酸索利那新片Solifenacin Succinate Tablets/Vesicare10mgAstellas Pharma US Inc未进口原研药品更新持证商为Astellas Pharma US Inc备注1.未在国内上市品种,需参照原总局2015年第230号公告等的相关要求开展研究,通用名、剂型等经药典委核准后为准。

国家药品监督管理局药品注册司关于公布第五批化学药品说明书目录的通知文章属性•【制定机关】国家药品监督管理局•【公布日期】2002.04.29•【文号】药监注函[2002]125号•【施行日期】2002.04.29•【效力等级】部门规范性文件•【时效性】现行有效•【主题分类】药政管理正文国家药品监督管理局药品注册司关于公布第五批化学药品说明书目录的通知(药监注函[2002]125号)各省、自治区、直辖市药品监督管理局:按照《关于贯彻实施23号局令,统一药品批准文号工作的通知》(国药监注[2001]187号)的安排,我司已完成第五批化学药品说明书的编写工作(目录见附件),现公布在国家药品监督管理局和中国药品生物制品检定所的网站上,网址分别为http://和http://。
请各省、自治区、直辖市药品监督管理局做好以下工作:一、说明书的印刷版本另行下发,请及时通知辖区内的药品生产企业根据网上公布的说明书参考样稿和企业的实际情况拟定本企业产品的说明书。
二、各生产企业要按照《关于做好统一换发药品批准文号工作的通知》(国药监注[2001]582号)的要求,将说明书和按照23号局令设计的包装、标签以及相应的档案资料上报后,由各省、自治区、直辖市药品监督局按照有关要求严格进行审核,完成后及时上报我司进行统一换发药品批准文号的工作。
特此通知附件:第五批化学药品说明书目录(136个)国家药品监督管理局药品注册司二00二年四月二十九日附件:第五批化学药品说明书目录(136个)1.阿莫西林干混悬剂2.阿奇霉素分散片3.阿司匹林肠溶胶囊(150mg)4.阿昔洛韦胶囊5.苯甲醇注射液6.苯甲酸雌二醇软膏7.玻璃酸钠注射液8.茶苯海明含片9.垂体后叶注射液10.果糖二磷酸钠注射液11.醋酸曲安奈德尿素软膏12.多烯酸乙酯胶丸13.泛影葡胺注射液14.呋喃硫胺片15.伏格列波糖片16.氟罗沙星注射液17.复方氨基酸注射(18-F)18.佐匹克隆片19.复方对乙酰氨基酚片(II)20.复方桔油乳21.复方酮康唑软膏22.复方土槿皮酊23.复方营养混悬剂24.复方樟柳碱注射液25.左炔诺孕酮炔雌醚片26.甘露聚糖肽口服液27.葛根素葡萄糖注射液28.谷氨酸钾注射液29.哈拉宗片30.甲磺酸培氟沙星胶囊31.甲磺酸双氢麦角毒碱片32.甲胂酸钠注射液33.甲硝唑乳膏34.结合雌激素片35.聚甲基丙烯酸乙氧乙酯气雾剂36.卡托普利注射液37.抗A、抗B血型定型试剂(单克隆抗体)38.苦参碱注射液39.兰索拉唑胶囊40.兰索拉唑片41.雷尼替丁氯化钠注射液42.联苯双酯口服混悬液43.磷霉素钙片44.硫普罗宁片45.硫酸罗通定片46.硫酸特布他林胶囊47.氯化钠注射液48.氯屈膦酸二钠片49.氯屈膦酸二钠注射液50.罗通定片51.马来酸咪达唑仑片52.马洛替酯片53.吗啡阿托品注射液54.麦白霉素胶囊55.麦白霉素片56.美扑伪麻咀嚼片57.左炔诺孕酮聚己内酯棒58.门冬氨酸钾镁片59.尼莫地平分散片60.尼莫地平缓释胶囊61.尼莫地平缓释片62.尼莫地平胶囊63.尼莫地平注射液64.尼群地平胶囊65.浓过氧化氢溶液66.诺氟沙星脚气水67.泮托拉唑钠肠溶胶囊68.脾氨肽口服液69.葡萄糖酸钙锌口服溶液70.氢化可的松片71.氢化可的松注射液72.曲昔匹特片73.乳果糖口服溶液74.乳酸依沙丫啶注射液75.三磷酸腺苷二钠注射液76.输血用1号抗凝液77.石杉碱甲胶囊78.输血用2号抗凝液79.双氯芬酸缓释胶囊80.双氯芬酸钾片81.双氯芬酸钠缓释微丸82.双氯芬酸钠片83.天麻素胶囊84.天麻素片85.天麻素注射液86.酮康唑片87.头孢妥仑匹酯片88.维生素C泡腾片89.维生素D2片90.维生素E(天然型)胶丸91.维四高丝注射液92.无极膏93.西吡氯铵漱口液94.硝苯地平注射液95.硝酸毛果芸香碱片96.硝酸异山梨酯片97.小儿复方磺胺甲恶唑片98.小儿甘草锌片99.锌布片100.胸腺肽注射液101.亚锡硫乙甘肽冻干品102.亚锡双半胱氨酸冻干品103.盐酸安他唑啉片104.盐酸奥昔布宁片105.盐酸班布特罗口服液106.盐酸川芎嗪注射液107.盐酸丁咯地尔注射液108.盐酸恩丹西酮胶囊109.盐酸氟西汀胶囊110.盐酸黄酮哌酯胶囊111.盐酸芦氟沙星片112.盐酸特拉唑嗪片113.盐酸妥拉唑啉注射液114.氧氟沙星滴眼液115.依地酸钙钠注射液116.依托度酸片117.胰酶糖衣片(肠溶片)118.异丁司特缓释胶囊119.吲哚美辛控释片120.右旋糖酐20葡萄糖注射液121.右旋糖酐铁注射液122.注射用单磷酸阿糖腺苷123.注射用低分子量肝素钠124.注射用核糖核酸125.注射用甲氧异腈126.注射用降纤酶127.注射用平阳霉素128.注射用缩宫素129.注射用头孢呋肟钠130.注射用胸腺肽131.注射用胸腺五肽132.注射用胰蛋白酶133.注射用异环磷酰胺134.注射用转移因子135.转移因子注射液136.阿司匹林肠溶胶囊(75mg)。
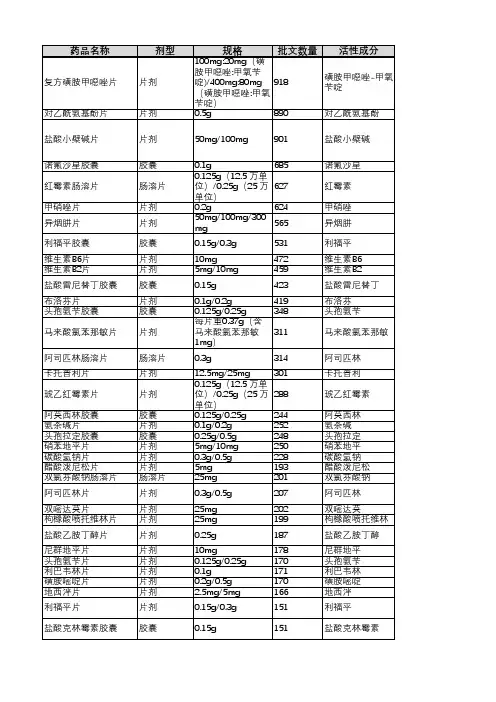
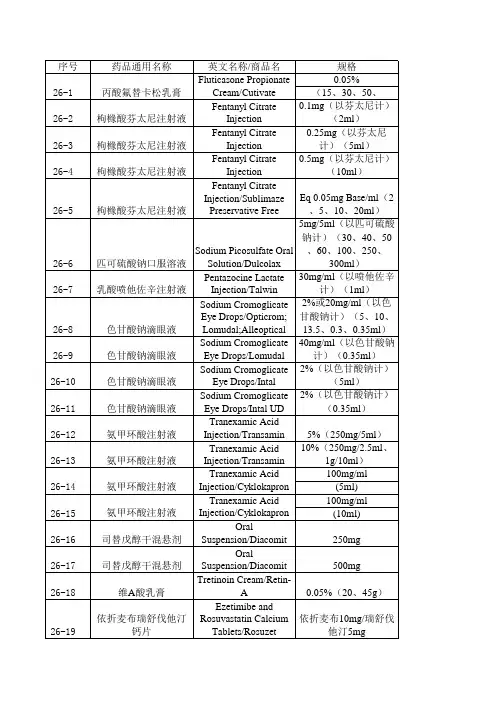
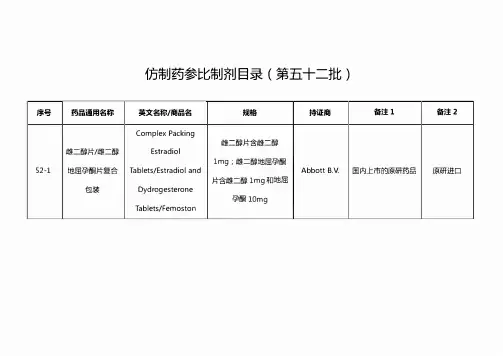
仿制药参比制剂目录(第五十二批)序号药晶通用每精:英文包称/商局每规幡持证商备注1备注2 Complex Packing幢二醇片台幢二醇雌二醇片/雌二醇Estradiollmg;雌二醇地屈孕酣52-1地屈孕酣片复合Tablets/Estradiol and Abbott B.V. 国内上市的原研药昂原研进口片含雌二醇lmg和地屈包装Dyd r ogesterone孕酣lOmgTablets/Femoston序号药晶通用各称英文窑称/商晶窑规幡持证商备注1备注2Complex Packing雌二醇片含雌二醇雌二醇片/雌二醇Estradiol2mg; I脏二醇地屈孕酣52-2地屈孕酣片复合Tablets/Estradiol and Abbott B.V. 国内上市的原研药晶原研进口片含雌二醇2mg和地屈包装Dyd r ogesterone孕酣lOmgTablets/FemostonBisoprolol Fumarate 富马酸比索洛尔S mg与比索j吾尔氨氯地523and Amlodipine 苯磺酸氢氯地平(按氢Merck Kft 国内上市的原研药昂原研进口平片Besylate Tablets 氢地平计)S mgAmiodarone HCI Baxter盐酸肢确嗣注射52-4Premixed 360mg/200ml Healthcare 来进口原研药晶美国橙皮书液(预混)I时ection/r、�exterone Corporation序号药晶通用各称英文窑称/商晶窑规幡持证商备注1备注2Amiodarone HCI Baxter盐酸肢确酣注射52-5Premixed 150mg/100ml Healthcare 来进口原研药昂美国橙皮书液(预混)I时ection/「、�exterone CorporationTriamcinolone曲安奈德缰稽洼Acetonide Extended Flexion52-632mg/支来进口原研药晶美国橙皮书射混悬液Release I叮ectable Theraps IncSuspension /ZilrettaPotassium CitrateMission52-7相梅酸押缓释片Extended r elease 5 MEQ ( 0.54g ) 来进口原研药昂美国橙皮书PharmaTablets/ Urocit-K序号药晶通用各称英文窑称/商晶窑规幡持证商备注1备注2Potassium CitrateMission52-8相梅酸押缓释片Extended Release 10 MEQ ( 1.08g ) 来进口原研药昂美国橙皮书PharmaTablets/ Urocit-KPotassium CitrateMission529何悔酸拥缰稽片Extended Release 15 MEQ ( 1.62g) 未进口原研药自美国橙皮书PharmaTablets I Urocit-KHope硫代硫酸钢注射Sodium Thiosulfate 12.S g/SOml52-10Pharmaceutic 来进口原研药昂美国橙皮书液I町ection( 250m g/ml)als序号药晶通用各称英文窑称/商晶窑规幡持证商备注1备注2LidocaineHydrochloride and l.7ml: 2%盐酸利多卡盐酸利多卡因肾52-11Epinephrine Bitartrate 因和肾上腺素(酒石酸Deproco Inc 国际公认的同种药晶美国橙皮书上腺素注射液I时ection/Lignospan氢盐)1:100,000Standard碳酸氢纳/葡萄糖Duosol with 2 mmol/1SOOOml (大袋 B.Braun52122mmol/l押电解Potassium solution for 欧盟上市4555时,小袋555rnl) Aviturn AG质血j虑置换液haemofiltrationVortioxetine Oral 20 mg/ml (以伏硫西汀H.Lundbeck52-13伏硫西汀滴剂来进口原研药昂欧盟上市Drops/Brintellix 计)A/S序号药晶通用各称英文窑称/商晶窑规幡持证商备注1备注2Aztreonam For Gilead52-14氨曲南眼入溶液Inhalation 75mg Sciences 来进口原研药昂欧盟上市Solution/Cayston Ireland UCTizanidineHydrochloride Novartis盐酸苦于L尼定缓52-15Extended-release 6mg Pharma 来进口原研药晶欧盟上市程胶囊Capsules/ Sirdalud Schweiz AGMRTolvaptan Orally大摞裂菜株式52-16托伐普坦口崩片Disintegrating 7.5mg 来进口原研药晶日本上市会吐Tablets/Samsca ®OD序号药晶通用各称英文窑称/商昂每规幡持证商备注1备注2Tolvaptan Orally大I军裂菜株式52-17托伐普坦口崩片Disintegrating lSmg 来进口原研药昂日本上市会社Tablets/Samsca ®ODTolvaptan Orally大I军裂菜株式52”18 托伐蔷坦口崩片Disintegrating 30mg 未进口原研药自日本上市会社Tablets/Samsca ®ODEA制药株式会复方聚乙二醇电Polyethylene Glycol丰士52-19解质散(儿童Electrolytes Powder 6.9 g/包来进口原研药昂日本上市( EA 77一型)( L D)株式会社)序号药晶通用各称英文窑称/商昂每规幡持证商备注1备注2每贴台氟比i备芬20mg大正制药株式52-20氟比;各芬贴剂Flurbiprofen Patches (面积7cmx10cm,含来进口原研药昂日本上市会社膏量0.84g/70cm2)每贴含氟比洛芬40mg大E制药株式52-21氟比j各芬贴剂Flurbiprofen Patches (面积10cmx14cm,未进口原研药自日本上市会社含膏量1.68g/140cm2)每贴含氧比jg芬60mg大正制药株式52-22氟比j备芬贴剂Flurbiprofen Patches (面积15cmx14cm,来进口原研药晶日本上市会吐含膏量2.52g/210cm2)Meiji Seika 7Fosfomycin Sodium52-23注射用磷霉素纳l g Y JL,x株式会来进口原研药昂日本上市For Injection/Fosmicin社序号药晶通用各称英文窑称/商昂每规幡持证商备注1备注2Meiji Seika 7Fosfomycin Sodium52-24注射用磷霉素纳2g Y J L,x株式会来进口原研药昂日本上市For Injection/Fosmicin社Sofalcone Fine 大正裂菜株式52-25素;去翻细粒20% ( 0.5g/袋)未进口原研药昂日本上市Granules /Solon 会社Ketotifen Fumarate J /\ J L,子,f又富马酸酣蕾芬滴52-26Ophthalmic 0.05% 77-x株式来进口原研药晶日本上市眼液Solution/Zaditen 会吐Novartis甲苯磺酸拉帕苔Lapatinib Ditosylate52-27250mg Europharm 来进口原研药晶英国上市尼片Tablets/TyverbLimited序号药晶通用各称英文窑称/商昂每规幡持证商备注1备注2Mesalazine Dr.Falk52-28美沙拉奏栓Suppositories/Salofalk 0.259 Pharma 国内上市的原研药昂原研进口(莎尔福)GmbHMesalazine Dr.Falk52-29美沙拉秦栓Suppositories/Salofalk lg Pharma 国内上市的原研药自原研进口(莎尔福)GmbHMesalazine Dr.Falk52-30美沙拉秦灌肠液Enemas/Salofalk (莎60g:4g Pharma 国内上市的原研药晶原研进口尔福)GmbHMesalazine Enteric-Dr.Falk52-31美沙拉奏肠溶片coated Tablets lg Pharma 国内上市的原研药昂原研进口/Salofalk (莎尔福)GmbH序号药晶通用各称英文窑称/商昂每规幡持证商备注1备注2Ivabradine盐酸{尹伐布雷定52-32Hydrochloride Smg Amgen Inc. 来进口原研药昂美国橙皮书片Tablets/Coria n orIvabradine盐酸伊伐布雷定52”33 Hydrochloride 7.Smg Amgen Inc. 未进口原研药自美国橙皮书片Tablets/Coria n or依i若肝素铀注射Enoxaparin Sodium 30mg/0.3ml Sanofi Aventis52-34未进口原研药晶美国橙皮书液Injection/ Lovenox (lOOmg/mL) US LLC依i苦肝素纳注射Enoxaparin Sodium 40mg/0.4mL Sanofi Aventis5235未进口原研药昂美国橙皮书液Injection/ Lovenox (lOOmg/mL} US LLC依i苦肝素纳注射Enoxaparin Sodium 60mg/0.6mL Sanofi Aventis52-36来进口原研药晶美国橙皮书液I时ection/Lovenox (lOOmg/mL) US LLC序号药晶通用各称英文窑称/商昂每规幡持证商备注1备注2依诺肝素纳注射Enoxaparin Sodium 80mg/0.8ml Sanofi Aventis52-37来进口原研药晶美国橙皮书液Injection/ Lovenox (lOOmg/mL) US LLC依i若肝素铀注射Enoxaparin Sodium lOOmg/lmL Sanofi Aventis52-38来进口原研药昂美国橙皮书液Injection/ Lovenox (lOOmg/mL) US LLCIrbesartan Tablets Sanofi Aventis52-39厄贝沙坦片75mg 来进口原研药昂美国橙皮书/Aprovel US LLCIrbesartan Tablets Sanofi Aventis52-40厄贝沙坦片lSOmg 未进口原研药晶美国橙皮书/Aprovel US LLCIrbesartan Tablets Sanofi Aventis52-41厄贝沙坦片300mg 来进口原研药昂美国橙皮书/Aprovel US LLC序号药晶通用各称英文窑称/商昂每规幡持证商备注1备注2Novartis甲横酸{尹马蔷尼Imatinib Mesylate52-42lOOmg Europharm 来进口原研药昂欧盟上市片Tablets/GlivecLimitedlmg Contains at leastOmega-3Acid Ethyl欧米加“子酸乙自旨900mg of the Ethyl52-43Esters Soft BASF AS 来进口原研药晶欧盟上市软胶囊Esters of Omega-3Capsules/OmacorFattay AcidsGedeon52-44左快i苦孕酣片Levonorgestrel Tablets 0.75mg 来进口原研药昂欧盟上市Richter Pie.序号药晶通用各称英文窑称/商昂每规幡持证商备注1备注2MedaPyridostigmine Pharmaceutic52-45j臭。
如何选择正确的参⽐制剂系列之注射⽤奥美拉唑钠(洛赛克)20200524如何选择正确的参⽐制剂系列之注射⽤奥美拉唑钠(洛赛克)在⼯作中经常遇到客户由于⽆法正确选择参⽐制剂,导致消耗很⼤的⼈⼒财⼒,少则万⼋千,多则⼏⼗万甚⾄上百万的,做半天研究发现参⽐制剂选错了,好尴尬。
⽼板好⼼疼。
今天⼩编在这和⼤家聊聊注射⽤奥美拉唑钠(洛赛克)这个品种,希望对⼤家有所帮助。
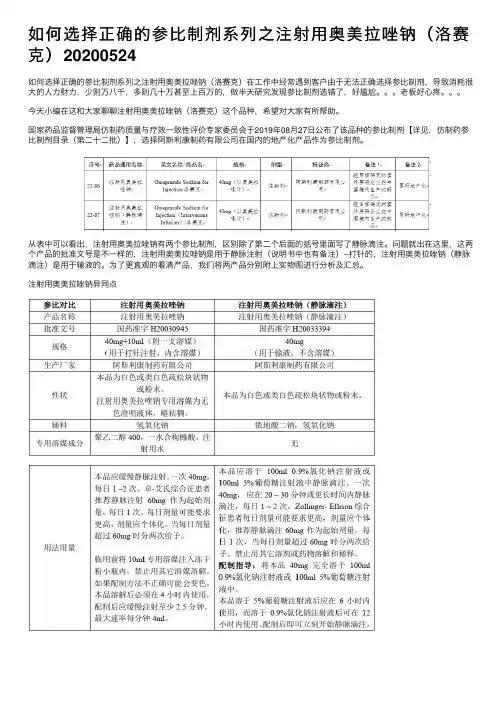
国家药品监督管理局仿制药质量与疗效⼀致性评价专家委员会于2019年08⽉27⽇公布了该品种的参⽐制剂【详见,仿制药参⽐制剂⽬录(第⼆⼗⼆批)】,选择阿斯利康制药有限公司在国内的地产化产品作为参⽐制剂。
从表中可以看出,注射⽤奥美拉唑钠有两个参⽐制剂,区别除了第⼆个后⾯的括号⾥⾯写了静脉滴注。
问题就出在这⾥,这两个产品的批准⽂号是不⼀样的,注射⽤奥美拉唑钠是⽤于静脉注射(说明书中也有备注)--打针的,注射⽤奥美拉唑钠(静脉滴注)是⽤于输液的。
为了更直观的看清产品,我们将两产品分别附上实物图进⾏分析及汇总。
注射⽤奥美拉唑钠异同点北京康瑞凯医药科技有限公司简介(进⼝参⽐制剂供应商),成⽴于2017年03⽉,本公司⽬前主营经营范围:为全国药品⽣产/研发企业、科研院校等提供【参⽐制剂】;具体包括:【国内进⼝上市参⽐制剂】;很多产品可同时提供近效期,中效期,新上市三个阶段的多批次产品,满⾜仿制药研发及⼀致性评价需求。
【地产化参⽐制剂】;很多产品可同时提供近效期,中效期,新上市三个阶段的多批次产品,满⾜仿制药研发及⼀致性评价需求。
【注射液⼀致性评价所需各种包装(塑料瓶、玻璃瓶、直⽴软袋)葡萄糖注射液、氯化钠注射液、林格注射液等】、避光输液器、避光注射器等;中检所对照品、医药杂质对照品、医药中间体等产品,同时为部分研发企业提供仿制药研发流程指导技术服务等。
欢迎交流探讨。
如何查询参⽐制剂如何查询仿制药的参⽐制剂?仿制药开发选择参⽐制剂是第⼀步,所谓万事开头难,中间也难,结尾发现更难,就算做仿制药选对参⽐制剂也不会事半功倍,但如果选错了,就意味着后⾯所有的⼯作都得重头再来,有些⼈就会感⾔做对⽆功,做错还要受罚,真的是太难了,所以慢慢制药路千万别栽在第⼀步,所以查询参⽐制剂是⾮常重要的需要专业的数据库查询如:药智⽹、药渡、药融云、医药魔⽅等都是能查询到的,下⾯简单介绍⼀下怎么查询仿制药的参⽐制剂。
在公众号查询参⽐制剂可以在公总号搜索⼀些参⽐制剂数据,但是数据完整度不⾼,数据精准度也是不⾼的,整合之后的信息不利于分析。
药智⽹查询参⽐制剂可以在⽣产检验数据下选择(橙⽪书数据、参⽐制剂备案数据库、仿制药参⽐制剂⽬录)能查询参⽐制剂,确定参⽐制剂。
药渡查询参⽐制剂可以在全球药物下查询橙⽪中的参⽐制剂,以及直接查询参⽐制剂。
药融云查询参⽐制剂可以在⼀致性评价数据中查询仿制药的参⽐制剂⽬录、参⽐制剂备案、美国橙⽪书等数据。
但是这些数据会遇到⼀定问题,原研未在国内上市,原研撤市、品种太⽼⽆法追溯、参⽐⽬录未收录、多个规格买哪个等等,⾯都这些问题最早的查询参⽐制剂的⽅法就是看“美国橙⽪书”包含上市和终⽌的药品(⾮安全性有效性原因撤市),RLD就是FDA指定的参⽐制剂了,就是原研药,制药原研不是因为安全性或者有效性撤市的药品,仿制药是可以继续⽤RLD进⾏申请的。
RLD如果撤市在哪⾥查询,RS(对照药品)出现了就是仿制药在⽣物等效性试验(BE)中的对照药品。
如果RLD撤市FDA⼀般会从ANDA(仿制药)去选择RS,选RLD等效的、销量⼤的尽可能包含所有规格的。
在仿制药参⽐制剂⽬录中可以通过信息来源进⾏条件筛选选择(第⼀到四⼗四批),确定参⽐制剂在美国橙⽪书中可以选择是否是参⽐制剂还有对照标准制剂(RS)确定参⽐制剂。
总的来说查询参⽐制剂是药物研发的第⼀步,选择对了才能进⾏接下来的处⽅⼯艺的研究,质量的研究,稳定性的研究,药物毒理研究等等,万事开头难,下⼀步更能难,第⼀步做了,那么接下来的⼜要推翻重新做,所以选择参⽐制剂是⾮常重要的,⼀般我们公司会在药融云数据库中确定参⽐制剂,还有能查询药物研发中的数据,以及药物报告和毒理数据助⼒研发。
重庆市医疗保障局关于做好第五批国家组织药品集中带量采购结果落地实施相关工作的通知文章属性•【制定机关】重庆市医疗保障局•【公布日期】2021.09.10•【字号】渝医保发〔2021〕58 号•【施行日期】2021.10.01•【效力等级】地方规范性文件•【时效性】现行有效•【主题分类】药政管理,卫生医药、计划生育其他规定,政府采购正文重庆市医疗保障局关于做好第五批国家组织药品集中带量采购结果落地实施相关工作的通知各区县(自治县)医疗保障局,两江新区社会保障局、高新区政务服务和社会事务中心、万盛经开区人力社保局,有关医疗机构,有关企业,重庆药品交易所:为贯彻落实《中共中央国务院关于深化医疗保障制度改革的意见》(中发〔2020〕5号)、《国务院办公厅关于推动药品集中带量采购工作常态化制度化开展的意见》(国办发〔2021〕2号)等有关文件精神,常态化制度化推进药品集中带量采购工作,进一步降低群众用药负担,现就做好第五批国家组织药品集中带量采购结果落地实施有关工作通知如下:一、实施范围(一)机构范围。
全市行政区域内政府举办(含党政机关和事业单位举办)的公立医院、国企医院和在渝部队医院等,鼓励社会办医药机构和医保定点零售药店参加。
(二)药品范围。
第五批国家组织药品集中带量采购的中选药品(详见附件1)。
二、采购周期及协议签订(一)全国实际中选企业数为1家或2家的,本轮采购周期原则上为1年;全国实际中选企业数为3家的,本轮采购周期原则上为2年;全国实际中选企业数为4家及以上的,本轮采购周期原则上为3年。
(二)采购周期内采购协议每年一签。
续签采购协议时,约定采购量原则上不少于该中选药品上年约定采购量。
(三)采购周期内若提前完成当年约定采购量,超出部分中选企业仍按中选价进行供应,直至采购周期届满。
三、工作任务(一)落实约定任务量。
第五批国家组织药品集中采购首年约定采购量按照国家联采办公布的《全国药品集中采购文件》(GY-YD2021-2)中相关规则确定。