元素周期表中元性质递变规律
- 格式:doc
- 大小:149.50 KB
- 文档页数:6

元素周期表的周期性规律与元素性质变化及元素周期表的趋势元素周期表是化学中重要的工具,它以一种有序的方式展示了所有已知化学元素的信息。
元素周期表的设计有助于我们理解元素的性质和规律,在化学研究和实践中发挥着重要的作用。
本文将探讨元素周期表的周期性规律、元素性质变化以及元素周期表的趋势。
1. 元素周期表的周期性规律元素周期表按照原子序数的顺序排列,将元素按照一定的规律分类。
周期表的每一横行称为一个周期,每一竖列称为一个族。
这种排列方式揭示了许多元素性质的周期规律。
1.1 原子半径的周期性变化原子半径是一个元素的原子中心到其最外层电子的平均距离。
从周期表中可以看出,原子半径随着周期数的增加而减小,而在同一周期内,随着原子序数的增加,原子半径也逐渐减小。
这是因为随着电子层数的增加,同时核吸引力对电子的作用也增强,使得电子云更加紧密,从而缩小了原子半径。
1.2 电离能和电子亲和能的周期性变化电离能是指从一个原子或离子中移去一个电子所需的能量,而电子亲和能是指一个原子或离子吸引并获得一个额外电子所释放出的能量。
这两个性质也有周期性变化。
在周期表中,可以观察到电离能和电子亲和能随着原子序数的增加而增加。
这是因为随着电子层数和核电荷的增加,电子与原子核的相互作用也相应增强,因此需要更多的能量才能移除一个电子或者吸收一个电子。
2. 元素性质的变化元素周期表不仅展示了元素的周期性规律,还反映了元素性质的变化。
不同族和周期的元素具有特定的化学性质,可以根据周期表的排列来预测元素的性质。
2.1 金属、非金属和类金属根据周期表可以将元素分为金属、非金属和类金属。
在周期表的左侧,大部分元素都是金属,具有良好的导电性、热导性和延展性。
在周期表的右侧,有一群非金属元素,它们通常是不良导体,脆弱且不可塑性。
在中间部分,是一些性质介于金属和非金属之间的元素,被称为类金属。
2.2 元素的化合价和氧化性元素的化合价指的是一个元素与其他元素形成化合物时所带的电荷。

1 元素周期表中元素及其化合物的递变性规律1.1 原子半径(1)除第1周期外,其他周期元素(惰性气体元素除外)的原子半径随原子序数的递增而减小;(2)同一族的元素从上到下,随电子层数增多,原子半径增大。
1.2 元素化合价(1)除第1周期外,同周期从左到右,元素最高正价由碱金属+1递增到+7,非金属元素负价由碳族-4递增到-1(氟无正价,氧无+6价,除外);(2)同一主族的元素的最高正价、负价均相同1.3 单质的熔点(1)同一周期元素随原子序数的递增,元素组成的金属单质的熔点递增,非金属单质的熔点递减;(2)同一族元素从上到下,元素组成的金属单质的熔点递减,非金属单质的熔点递增1.4 元素的金属性与非金属性(1)同一周期的元素从左到右金属性递减,非金属性递增;(2)同一主族元素从上到下金属性递增,非金属性递减。
1.5 最高价氧化物和水化物的酸碱性元素的金属性越强,其最高价氧化物的水化物的碱性越强;元素的非金属性越强,最高价氧化物的水化物的酸性越强。
1.6 非金属气态氢化物元素非金属性越强,气态氢化物越稳定。
同周期非金属元素的非金属性越强,其气态氢化物水溶液一般酸性越强;同主族非金属元素的非金属性越强,其气态氢化物水溶液的酸性越弱。
1.7 单质的氧化性、还原性一般元素的金属性越强,其单质的还原性越强,其氧化物的氧离子氧化性越弱;元素的非金属性越强,其单质的氧化性越强,其简单阴离子的还原性越弱。
2. 推断元素位置的规律判断元素在周期表中位置应牢记的规律:(1)元素周期数等于核外电子层数;(2)主族元素的序数等于最外层电子数;(3)确定族数应先确定是主族还是副族,其方法是采用原子序数逐步减去各周期的元素种数,即可由最后的差数来确定。
最后的差数就是族序数,差为8、9、10时为VIII族,差数大于10时,则再减去10,最后结果为族序数。
2.原子、离子半径的比较(1)原子的半径大于相应阳离子的半径。
(2)原子的半径小于相应阴离子的半径。


元素周期表中元素及其化合物的递变性规律1 原子半径(1)除第1周期外,其他周期元素(惰性气体元素除外)的原子半径随原子序数的递增而减小;(2)同一族的元素从上到下,随电子层数增多,原子半径增大。
2 元素化合价(1)除第1周期外,同周期从左到右,元素最高正价由碱金属+1递增到+7,非金属元素负价由碳族-4递增到-1(氟无正价,氧无+6价,除外);(2)同一主族的元素的最高正价、负价均相同3 单质的熔点(1)同一周期元素随原子序数的递增,元素组成的金属单质的熔点递增,非金属单质的熔点递减;(2)同一族元素从上到下,元素组成的金属单质的熔点递减,非金属单质的熔点递增4 元素的金属性与非金属性(1)同一周期的元素从左到右金属性递减,非金属性递增;(2)同一主族元素从上到下金属性递增,非金属性递减。
5 最高价氧化物和水化物的酸碱性元素的金属性越强,其最高价氧化物的水化物的碱性越强;元素的非金属性越强,最高价氧化物的水化物的酸性越强。
6 非金属气态氢化物元素非金属性越强,气态氢化物越稳定。
同周期非金属元素的非金属性越强,其气态氢化物水溶液一般酸性越强;同主族非金属元素的非金属性越强,其气态氢化物水溶液的酸性越弱。
7 单质的氧化性、还原性一般元素的金属性越强,其单质的还原性越强,其氧化物的氧离子氧化性越弱;元素的非金属性越强,其单质的氧化性越强,其简单阴离子的还原性越弱。
推断元素位置的规律判断元素在周期表中位置应牢记的规律:(1)元素周期数等于核外电子层数;(2)主族元素的序数等于最外层电子数。
阴阳离子的半径大小辨别规律由于阴离子是电子最外层得到了电子而阳离子是失去了电子所以, 总的说来(1) 阳离子半径<原子半径(2) 阴离子半径>原子半径(3) 阴离子半径>阳离子半径或者说,电子越多半径越大.以上不适合用于稀有气体!快速背出元素周期表的方法化合价:一价请驴脚拿银,(一价氢氯钾钠银)二价羊盖美背心。

元素周期性规律总结
1 元素周期表中元素及其化合物的递变性规律
1.1 原子半径
(1)除第1周期外,其他周期元素(惰性气体元素除外)的原子半径随原子序数的递增而减小;
(2)同一族的元素从上到下,随电子层数增多,原子半径增大。
(3)离子半径先比较核外电子层数,电子层数越多,则半径越大,若电子层数相同,则比较核电荷数,核电荷数小的离子半径大。
1.2 主族元素化合价
(1)除第1周期外,同周期从左到右,元素最高正价由碱金属+1递增到+7,非金属元素负价由碳族-4递增到-1(氟无正价,氧无+6价,除外);
(2)同一主族的元素的最高正价、负价均相同
(3)主族元素的最高正价和+最低负价的绝对值=8
1.3 单质的熔点
(1)同一周期元素随原子序数的递增,元素组成的金属单质的熔点递增,非金属单质的熔点递减;
(2)同一族元素从上到下,元素组成的金属单质的熔点递减,非金属单质的熔点递增
1.4 元素的金属性与非金属性
(1)同一周期的元素从左到右金属性递减,非金属性递增;
(2)同一主族元素从上到下金属性递增,非金属性递减。
2. 推断元素位置的规律
判断元素在周期表中位置应牢记的规律:
(1)元素周期数等于核外电子层数;
(2)主族元素的序数等于最外层电子数;
(3)确定族数应先确定是主族还是副族,其方法是采用原子序数逐步减去各周期的元素种数,即可由最后的差数来确定。
最后的差数就是族序数,差为8、9、10时为VIII族,差数大于10时,则再减去10,最后结果为族序数。

化学元素周期表有哪些规律对于这些了无生趣的化学元素,同学们总是很无奈,抓不住其中的规律,今天查字典化学网的小编为同学们搜集整理了化学元素周期表的规律,相信对同学们一定会有所帮助。
跟着小编一起来看看化学元素表的规律吧!一、元素周期表中元素及其化合物的递变性规律1、原子半径(1)除第1周期外,其他周期元素(惰性气体元素除外)的原子半径随原子序数的递增而减小;(2)同一族的元素从上到下,随电子层数增多,原子半径增大。
2、元素化合价(1)除第1周期外,同周期从左到右,元素最高正价由碱金属+1递增到+7,非金属元素负价由碳族-4递增到-1(氟无正价,氧无+6价,除外);(2)同一主族的元素的最高正价、负价均相同。
3、单质的熔点(1)同一周期元素随原子序数的递增,元素组成的金属单质的熔点递增,非金属单质的熔点递减;(2)同一族元素从上到下,元素组成的金属单质的熔点递减,非金属单质的熔点递增。
4、元素的金属性与非金属性(1)同一周期的元素从左到右金属性递减,非金属性递增;(2)同一主族元素从上到下金属性递增,非金属性递减。
5、最高价氧化物和水化物的酸碱性元素的金属性越强,其最高价氧化物的水化物的碱性越强;元素的非金属性越强,最高价氧化物的水化物的酸性越强。
6、非金属气态氢化物元素非金属性越强,气态氢化物越稳定。
同周期非金属元素的非金属性越强,其气态氢化物水溶液一般酸性越强;同主族非金属元素的非金属性越强,其气态氢化物水溶液的酸性越弱。
7、单质的氧化性、还原性一般元素的金属性越强,其单质的还原性越强,其氧化物的氧离子氧化性越弱;元素的非金属性越强,其单质的氧化性越强,其简单阴离子的还原性越弱。
二、推断元素位置的规律判断元素在周期表中位置应牢记的规律:1、元素周期数等于核外电子层数;2、主族元素的序数等于最外层电子数;3、确定族数应先确定是主族还是副族,其方法是采用原子序数逐步减去各周期的元素种数,即可由最后的差数来确定。

(完整版)化学元素周期表的规律总结化学元素周期表的规律总结?比如金属性非金属性等元素周期表中元素及其化合物的递变性规律1 原子半径(1)除第1周期外,其他周期元素(惰性气体元素除外)的原子半径随原子序数的递增而减小;(2)同一族的元素从上到下,随电子层数增多,原子半径增大。
2 元素化合价(1)除第1周期外,同周期从左到右,元素最高正价由碱金属+1递增到+7,非金属元素负价由碳族-4递增到-1(氟无正价,氧无+6价,除外);(2)同一主族的元素的最高正价、负价均相同(3) 所有单质都显零价3 单质的熔点(1)同一周期元素随原子序数的递增,元素组成的金属单质的熔点递增,非金属单质的熔点递减;(2)同一族元素从上到下,元素组成的金属单质的熔点递减,非金属单质的熔点递增4 元素的金属性与非金属性(1)同一周期的元素电子层数相同。
因此随着核电荷数的增加,原子越容易得电子,从左到右金属性递减,非金属性递增;(2)同一主族元素最外层电子数相同,因此随着电子层数的增加,原子越容易失电子,从上到下金属性递增,非金属性递减。
5 最高价氧化物和水化物的酸碱性元素的金属性越强,其最高价氧化物的水化物的碱性越强;元素的非金属性越强,最高价氧化物的水化物的酸性越强。
6 非金属气态氢化物元素非金属性越强,气态氢化物越稳定。
同周期非金属元素的非金属性越强,其气态氢化物水溶液一般酸性越强;同主族非金属元素的非金属性越强,其气态氢化物水溶液的酸性越弱。
7 单质的氧化性、还原性一般元素的金属性越强,其单质的还原性越强,其氧化物的阳离子氧化性越弱;元素的非金属性越强,其单质的氧化性越强,其简单阴离子的还原性越弱。
一、原子半径同一周期(稀有气体除外),从左到右,随着原子序数的递增,元素原子的半径递减;同一族中,从上到下,随着原子序数的递增,元素原子半径递增。
二、主要化合价(最高正化合价和最低负化合价)同一周期中,从左到右,随着原子序数的递增,元素的最高正化合价递增(从+1价到+7价),第一周期除外,第二周期的O、F元素除外;最低负化合价递增(从-4价到-1价)第一周期除外,由于金属元素一般无负化合价,故从ⅣA族开始。

一、原子半径同一周期(稀有气体除外),从左到右,随着原子序数的递增,元素原子的半径递减;但由于阴离子是电子最外层得到了电子而阳离子是失去了电子所以, (同种元素) (1) 阳离子半径<原子半径(2) 阴离子半径>原子半径(3) 阴离子半径>阳离子半径。
短周期中电子填充到最外电子层,同层电子间屏蔽效应弱,因此有效核电荷增加显著,而电子层数不变,核对外层电子吸引力逐渐变大,所以短周期元素原子半径从左到右递减较快。
长周期元素中,从第3(ⅢB)族开始,电子填充至到次外层上,这新增加到次外层上的电子对外层电子屏蔽作用强。
因此,随核电荷的增加而有效核电荷却增加不多。
同一族元素中,由上至下虽然核电荷增加较多,但相邻两元素之间依次增加一个电子层因而屏蔽作用也较大,结果有效核电荷增加不显著。
同一族中,从上到下,随着原子序数的递增,元素原子半径递增。
主族中从上到下核电荷明显增大,但随电子层数的增加,屏蔽作用增加,因而有效核电荷增加不明显,由于电子层数的增加,原子半径明显增大;副族的过渡元素,第一过渡系与第二过渡系由于有效核电荷增大不及电子层增加的作用,原子半径增大。
但由于镧系收缩,使第二、第三过度系同族元素的半径几乎不变,有的甚至减小。
二、电离能同周期主族元素从左到右作用到最外层电子上的有效核电荷逐渐增大,半径逐渐减小,电离能也逐渐增大,稀有气体由于具有稳定的电子层结构,其电离能最大,故同周期元素从强金属性逐渐变到非金属性,直至强非金属性。
同周期副族元素从左至右,由于有效核电荷增加不多,原子半径减小缓慢,有电离能增加不如主族元素明显。
由于最外层只有两个电子,过渡元素均表现金属性。
同一主族元素从上到下,原子半径增加,有效核电荷增加不多,则原子半径增大的影响起主要作用,电离能由大变小,元素的金属性逐渐增强。
同一副族电离能变化不规则。
三、电子亲和能变化趋势与电离能相似,具有大的电离能的元素一般电子亲和能也很大四、电负性一周期从左至右,有效核电荷递增,原子半径递减,对电子的吸引能力渐强,因而电负性值递增;同族元素从上到下,随着原子半径的增大,元素电负性值递减。

元素周期表的全部规律总结元素周期表是化学中一个重要的基础工具,通过元素周期表可以展示元素的性质和规律。
在元素周期表中,元素按照其原子序数递增的顺序排列,同时具有一些规律,包括周期性表现和族内相似性等。
本文将总结元素周期表中的一些重要规律,帮助读者更深入地了解元素周期表的精彩之处。
周期性表现元素周期表中的元素按照原子序数大小排列,可以看到元素的性质会出现周期性变化。
其中,主要的周期性表现有原子半径、电离能、电负性和金属性等。
•原子半径:原子半径随着周期的增加而递减,在周期表的同一周期内,原子半径会从左至右递减。
这是因为原子核内的正电荷数目增加,吸引外层电子,使得原子半径减小。
而在周期表的同一族内,原子半径会从上至下递增。
原因是原子的外层电子层数增加,电子云外围更为扩散,导致原子半径增大。
•电离能:电离能是指从原子或离子中移去一个电子所需要的能量。
随着周期的增加,电离能会递增,在周期表的同一周期内,电离能会从左至右递增,而在同一族内,电离能会从上至下递减。
这是因为原子核的正电荷数目增加,电子与原子核之间的相互作用增强,因此需要更多的能量去移除外层电子。
•电负性:电负性是元素吸引电子的能力。
在周期表中,从左至右逐渐增大,从下至上逐渐减小。
在同一族内,电负性基本相同。
电负性高的元素更容易得到电子,而电负性低的元素更容易失去电子。
•金属性:元素周期表中,金属性随着周期的增加而递减。
在周期表的左侧是金属性最强的元素,例如金属元素钠、铜等;而在周期表的右侧是非金属元素,如氧、氟等。
组和周期的特点元素周期表中,元素被按照周期数和组数分组。
每个周期表示一个主能级,组数表示元素的价电子数,组内元素有着相似的性质,包括外层电子排布和化学性质。
•主A族元素:主A族元素的元素化合物中,元素以价电子原子形式存在。
主A族元素的氧化状态为1+。
主A族元素在化学反应中往往失去一个电子,形成+1价阳离子。
•主B族元素:主B族元素的元素化合物中,元素以价电子离子形式存在。

元素周期表中元素的周期性与规律元素周期表是化学中最重要的工具之一,它将所有已知元素按照一定的规律排列起来。
这种排列方式展示了元素的周期性和规律,为我们研究和理解元素的性质提供了巨大的便利。
本文将探讨元素周期表中元素的周期性与规律,以及其对化学研究和实际应用的重要意义。
1.周期性的基本概念元素周期表的核心思想是将元素按照原子核中电子排布的规律进行分类。
元素周期表中的每一行称为一个周期,每一列称为一个族。
根据元素的原子序数增加,元素的性质会呈现出周期性的变化,即相似性质的元素在同一周期或同一族中。
2.周期表中的周期性规律2.1 原子半径的变化原子半径是指原子核到最外层电子轨道的平均距离。
在元素周期表中,原子半径会随着周期数的增加而逐渐减小,因为随着原子序数的增加,电子层数逐渐增加,核外电子与原子核的相互吸引力增强。
而在同一周期中,原子半径会随着原子序数的增加而逐渐增大,因为随着电子层的增加,电子轨道的平均半径变大。
2.2 电离能的变化电离能是指从一个原子中移除一个电子所需的能量。
元素周期表中,电离能会随着周期数的增加而逐渐增大,因为随着原子序数的增加,电子层数增多,外层电子与原子核的相互吸引力增强,需要更大的能量才能将电子从原子中移除。
而在同一周期中,电离能会随着原子序数的增加而逐渐减小,因为随着电子层数的增加,电子层内的屏蔽效应增强,电子的吸引力减弱。
2.3 电负性的变化电负性是指原子对电子的吸引能力。
在元素周期表中,电负性会随着周期数的增加而逐渐增大,因为原子核的电荷数增加,对电子的吸引力也随之增强。
而在同一周期中,电负性会随着原子序数的增加而逐渐减小,因为电子层内的屏蔽效应增强,电子与原子核的吸引力减弱。
3.周期性规律的实际应用元素周期表中的周期性规律为我们研究和应用化学提供了指导。
通过元素周期表,我们可以预测和解释元素的性质和行为。
例如,通过周期表中的电负性规律,我们可以预测元素之间的化学键类型;通过周期表中的电离能规律,我们可以预测元素的反应性和稳定性;通过周期表中的原子半径规律,我们可以推测元素的物理性质等。
化学元素周期表的规律总结化学元素周期表的规律总结?比如金属性非金属性等元素周期表中元素及其化合物的递变性规律1原子半径(1)除第1周期外,其他周期元素(惰性气体元素除外)的原子半径随原子序数的递增而减小;(2)同一族的元素从上到下,随电子层数增多,原子半径增大。
2元素化合价(1)除第1周期外,同周期从左到右,元素最高正价由碱金属+1递增到+7,非金属元素负价由碳族-4递增到-1(氟无正价,氧无+6价,除外);(2)同一主族的元素的最高正价、负价均相同(3)所有单质都显零价3单质的熔点(1)同一周期元素随原子序数的递增,元素组成的金属单质的熔点递增,非金属单质的熔点递减;(2)同一族元素从上到下,元素组成的金属单质的熔点递减,非金属单质的熔点递增4元素的金属性与非金属性(1)同一周期的元素电子层数不异。
因此跟着核电荷数的增长,原子越容易得电子,从左到右金属性递减,非金属性递增;(2)同一主族元素最外层电子数相同,因此随着电子层数的增加,原子越容易失电子,从上到下金属性递增,非金属性递减。
5最高价氧化物和水化物的酸碱性元素的金属性越强,其最高价氧化物的水化物的碱性越强;元素的非金属性越强,最高价氧化物的水化物的酸性越强。
6非金属气态氢化物元素非金属性越强,气态氢化物越稳定。
同周期非金属元素的非金属性越强,其气态氢化物水溶液一般酸性越强;同主族非金属元素的非金属性越强,其气态氢化物水溶液的酸性越弱。
7单质的氧化性、复原性一般元素的金属性越强,其单质的还原性越强,其氧化物的阳离子氧化性越弱;元素的非金属性越强,其单质的氧化性越强,其简单阴离子的还原性越弱。
1、原子半径同一周期(稀有气体除外),从左到右,随着原子序数的递增,元素原子的半径递减;同一族中,从上到下,随着原子序数的递增,元素原子半径递增。
二、主要化合价(最高正化合价和最低负化合价)同一周期中,从左到右,跟着原子序数的递增,元素的最高正化合价递增(从+1价到+7价),第一周期除外,第二周期的O、F元素除外;最低负化合价递增(从-4价到-1价)第一周期除外,由于金属元素一般无负化合价,故从ⅣA族开始。
元素周期表元素及化合物的递变规律
1、原子半径
(1)除第1周期外,其他周期元素(惰性气体元素除外)的原子半径随原子序数的递增而减小;
(2)同一族的元素从上到下,随电子层数增多,原子半径增大。
2、元素化合价
(1)除第1周期外,同周期从左到右,元素最高正价由碱金属+1递增到+ 7,非金属元素负价由碳族-4递增到-1(氟无正价,氧无+6价,除外);
(2)同一主族的元素的最高正价、负价均相同。
3、单质的熔点
(1)同一周期元素随原子序数的递增,元素组成的金属单质的熔点递增,非金属单质的熔点递减;
(2)同一族元素从上到下,元素组成的金属单质的熔点递减,非金属单质的熔点递增。
4、元素的金属性与非金属性
(1)同一周期的元素从左到右金属性递减,非金属性递增;
(2)同一主族元素从上到下金属性递增,非金属性递减。
5、最高价氧化物和水化物的酸碱性
元素的金属性越强,其最高价氧化物的水化物的碱性越强;元素的非金属性越强,最高价氧化物的水化物的酸性越强。
6、非金属气态氢化物
元素非金属性越强,气态氢化物越稳定。
同周期非金属元素的非金属性越强,其气态氢化物水溶液一般酸性越强;同主族非金属元素的非金属性越强,其气态氢化物水溶液的酸性越弱。
7、单质的氧化性、还原性
一般元素的金属性越强,其单质的还原性越强,其氧化物的氧离子氧化性越弱;元素的非金属性越强,其单质的氧化性越强,其简单阴离子的还原性越弱。
《元素性质的递变规律》知识清单一、原子半径的递变规律原子半径是描述原子大小的一个物理量。
在元素周期表中,原子半径呈现出明显的递变规律。
同一周期,从左到右,原子序数逐渐增大,核电荷数逐渐增多,对核外电子的吸引力逐渐增强,原子半径逐渐减小。
例如,在第三周期中,钠(Na)的原子半径最大,氯(Cl)的原子半径最小。
同一主族,从上到下,电子层数逐渐增多,原子半径逐渐增大。
例如,碱金属元素中,锂(Li)的原子半径最小,铯(Cs)的原子半径最大。
需要注意的是,稀有气体元素的原子半径测量方法与其他元素不同,一般不参与原子半径递变规律的比较。
二、电离能的递变规律电离能是指气态原子或离子失去一个电子所需要的最小能量。
同一周期,从左到右,元素的第一电离能总体上呈现逐渐增大的趋势。
但在第二主族和第五主族元素出现反常,这是因为其原子的电子排布结构相对稳定。
同一主族,从上到下,元素的第一电离能逐渐减小。
这是由于电子层数增加,原子半径增大,原子核对最外层电子的吸引力减弱。
电离能的大小可以反映原子失去电子的难易程度,电离能越大,原子越难失去电子,元素的金属性越弱;电离能越小,原子越容易失去电子,元素的金属性越强。
三、电负性的递变规律电负性是用来描述不同元素的原子对键合电子吸引力的大小。
同一周期,从左到右,元素的电负性逐渐增大。
同一主族,从上到下,元素的电负性逐渐减小。
电负性的数值可以衡量元素的金属性和非金属性的强弱。
电负性数值越大,元素的非金属性越强;电负性数值越小,元素的金属性越强。
一般来说,电负性差值大于 17 的两种元素原子之间通常形成离子键,电负性差值小于 17 的两种元素原子之间通常形成共价键。
四、元素化合价的递变规律元素的化合价与原子的最外层电子数密切相关。
同一周期,从左到右,最高正化合价逐渐升高(除 O、F 外),最低负化合价的绝对值逐渐减小。
同一主族,元素的最高正化合价和最低负化合价相同(除 O、F 外)。
元素的化合价具有周期性变化,这与元素原子的核外电子排布周期性变化密切相关。
一、电子填充的方式遵循能量最低的原理;原子的价电子构型是由最高能级组构成,而不是由最外层电子
二、周期表与原子电子层结构
七个周期,周期数=电子层数=最高能级序号
十六个族=七主七副+八零族
三、周期表元素性质周期性变化规律
1、原子半径:从上到下半径依次增大;从左到右半径依次减小
2.电离能:反应离子或原子失去电子的能力。
电离能越小,失电子性越强,金属性越强。
某些最外层半满或全满元素能量低、稳定,难失电子,I反常高。
大致:从左到右电离能增大;从上到下电离能减小。
3.电子亲和能:反映原子得电子能力,E A绝对值↑(代数值↓)、得电子↑、非金属性↑
同周期代数值从左到右趋于减小;同主族从上到下趋于增大
4.电负性:反映分子中原子(或离子)对成键电子的吸引能力。
“x”示之。
同周期:从左至右逐渐增大;同主族:从上而下逐渐减小。
x↑,吸引电子能力↑,非金属性↑。
金属性最强的是Fr,非金属性最强的是F.
额外赠送:a.离子在外电场或另外离子的影响下,原子核与电子云会发生相对位移而变形的现象,称为离子的极化。
b. (polarization power) 离子使异号离子极化的作用,称为极化作用。
正离子电荷越高,半径越小,离子势φ(Z/r)越大,则极化作用越强
1.下列说法正确的是
2.门捷列夫对化学这一学科发展的最大贡献在于发现了化学元素周期律。
下列事实不能用于元素周期律解释的只有:()
3.下表中的事实与推论不符的是:()
5.X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图所示,下列说法正确的是( )。
元素周期表中元性质递变规律
————————————————————————————————作者:————————————————————————————————日期:
专题一主要知识点
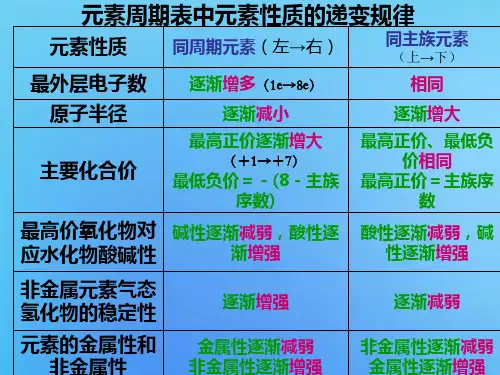
1. 元素周期表中元素性质的递变规律
同周期(从左到右)同主族(从上到下)原子半径逐渐减小逐渐增大
电子层排布电子层数相同
最外层电子数递增
电子层数递增最外层电子数相同
失电子能力逐渐减弱逐渐增强得电子能力逐渐增强逐渐减弱金属性逐渐减弱逐渐增强非金属性逐渐增强逐渐减弱
主要化合价最高正价(+1 →+7)
非金属负价 == ―(8―族
序数)
最高正价 == 族序数
非金属负价 == ―(8―族序
数)
最高氧化物的
酸性
酸性逐渐增强酸性逐渐减弱
对应水化物的
碱性
碱性逐渐减弱碱性逐渐增强
非金属气态氢化物的形成难易、稳定性形成由难→易
稳定性逐渐增强
形成由易→难
稳定性逐渐减弱
2.
3.几个规律:
①金属性强弱:单质与水或非氧化性酸反应难易;
单质的还原性(或离子的氧化性);
M(OH)n的碱性;
金属单质间的置换反应;
原电池中正负极判断,金属腐蚀难易;
非金属性强弱:与氢气反应生成气态氢化物难易;
单质的氧化性(或离子的还原性);
最高价氧化物的水化物(H n RO m)的酸性强弱;
非金属单质间的置换反应。
②半径比较三规律:
阴离子与同周期稀有气体电子层结构相同;阳离子与上周期稀有气体电子层结构相同。
(1)电子层数越多,半径越大
(2)电子层数相同,核电荷数越多,半径越小
(3)电子层数和核电荷数相同,最外层电子数越多,半径越大
③元素化合价规律
主族最高正价 == 最外层电子数,非金属的负化合价 == 最外层电子数-8,最高正价数和负化合价绝对值之和为8;其代数和分别为:0、2、4、6。
化合物氟元素、氧元素只有负价(-1、-2),但HFO中0为+1价;金属元素只有正价;
④熔沸点高低的比较:详细见《导学》P24
原子晶体>离子晶体>分子晶体
⑤1-20号元素符号、名称、原子结构、特殊化学性质。
⑥电子式的书写
原子的电子式
离子的电子式:
分子或共价化合物电子式
离子化合价电子式,。