化学原理2习题答案2
- 格式:ppt
- 大小:108.00 KB
- 文档页数:14

化学原理课后习题及答案化学原理课后习题及答案化学是我们在学校才开头学习到的。
大家是否有印象的呢。
化学原理课后习题及答案,我们来看看。
欢迎大家参考借鉴。
化学原理系:专业:班级:姓名:学号:学习情境一:物质结构一、选择题1.19K原子价电子的四个量子数,其正确组合是( A )。
A、4,0,0,-1/2B、4,1,0,+1/2C、4,1,1,1/2D、3,0,0,-1/22.原子中3d和4s电子的能量相比时( D )。
A.3d确定大于4sB.4s确定大于3dC.3d与4s确定相等D.不同原子中状况可能不同3.准备原子轨道数目的量子数是( A )。
A. nB. lC. n,lD. n,l,m4.3d轨道的磁量子数可能有( D )。
A.1,2,3B.0,1,2C.0,±1D.0,±1,±25.在苯和H2O分子间存在着( C )。
A.色散力和取向力C.色散力和诱导力 B.取向力和诱导力D.色散力, 取向力和诱导力6.关于下列对四个量子数的说法,正确的是( D )。
A.电子的自旋量子数是1/2,在某一个轨道中有两个电子,所以总自旋量子数是1或0B.磁量子数m=0的轨道都是球形的轨道C.角量子数l的可能取值是从0到n的正整数D.多电子原子中电子的能量准备于主量子数n和角量子数l7.Cr3+的外层电子排布式为( D )。
A. 3d24s1B. 3d34s0C. 3s23p63d64s1D. 3s23p63d38.今有一种元素,其原子中有5个半布满的d轨道,该元素是( A )。
A. 24CrB.21ScC. 26FeD. 30Zn9.下列各组分之间只存在色散力的是( B )。
A.氦和水B.二氧化碳气体C.溴化氢气体D.甲醇和水 10.下列物质中,用3p轨道和sp杂化轨道成键的是( B )。
A. BF3B. BeCl2C. NH3D.H2O11.在下列所示的电子排布中,哪些是不存在的(BC)。


一、选择题1.下列物质中,所有原子最外层均达到8电子稳定结构的化合物是 A .5PClB .4CClC .4P (正四面体形)D .3NH答案:B 【详解】A. P 最外层有5个电子,与其他原子间共用3对电子成为稳定结构,Cl 最外层有7个电子,与其他原子间共用1对电子成为稳定结构,显然5PCl 中的P 最外层不满足8电子稳定结构,A 项错误;B. C 最外层有4个电子,与其他原子间共用4对电子成为稳定结构,则4CCl 中的原子最外层均满足8电子稳定结构,B 项正确;C. 画出正四面体图形,每个P 占据正四面体的一个顶点,每个P 与其他3个P 形成3对共用电子,从而使每个P 最外层均满足8电子稳定结构,但P 属于单质,C 项错误;D. N 最外层有5个电子,与其他原子间共用3对电子成为稳定结构,H 最外层有1个电子,与其他原子间共用1对电子成为2电子稳定结构,3NH 中N 原子最外层达到8电子稳定结构,而H 达到2电子稳定结构,D 项错误; 答案选 B 。
2.原子序数依次增大的元素a 、b 、c 、d ,它们的最外层电子数分别为1、6、7、1。
a -的电子层结构与氦相同,b 和c 的次外层有8个电子,c -和d +的电子层结构相同。
下列叙述错误的是( )A .元素的非金属性强弱次序为c b a >>B .a 和其他3种元素均能形成共价化合物C .d 和其他3种元素均能形成离子化合物D .元素a 、b 、c 各自最高和最低化合价的代数和分别为0、4、6 答案:B 【详解】A .根据题意可推知,a 为H ,b 为S ,c 为Cl ,d 为K 。
同一周期从左到右,非金属性增强,非金属性:Cl S H >>,选项A 正确;B .H 和K 只能形成离子化合物KH ,选项B 错误;C .K 和H 、S 、Cl 能分别形成离子化合物:KH 、2K S 、KCl ,选项C 正确;D .H 、S 、Cl 的最高化合价分别为1+、6+、7+,最低化合价分别为1-、2-、1-,故元素a 、b 、c 各自最高和最低化合价的代数和分别为0、4、6,选项D 正确。

第二章 化学反应的基本原理和大气污染1、是非题(对的在括号内填“+”号,错的填“-”号)(1)r S ∆ 为正值的反应均是自发反应。
(-) (2)某一给定反应达到平衡后,若平衡条件不变,分离除去某生成物,待达到新的平衡,则各反应物和生成物的分压或浓度分别保持原有定值。
(-)(3)对反应系统122()()()(),(298.15)131.3r m C s H O g CO g H g H K kJ mol θ-+=+∆= 。
由于化学方程式两边物质的化学计量数(绝对值)的总和相等,所以增加总压力对平衡无影响。
(-) (4)上述(3)中反应达到平衡后,若升高温度,则正反应速率v (正)增加,逆反应速率v (逆)减小,结果平衡向右移动。
(-)(5)反应的级数取决于反应方程式中反应物的化学计量数(绝对值)。
(-) (6)催化剂能改变反应历程,降低反应的活化能,但不能改变反应的rmG θ∆。
(+)(7)在常温常压下,空气中的N 2 和O 2 能长期存在而不化合生成NO 。
且热力学计算表明22()()2()N g O g NO g +=的(298.15)0r m G K θ∆ ,则N 2 和O 2混合气必定也是动力学稳定系统。
(+)(8)已知4CCl 不会与2H O 反应,但422()2()()4()CCl l H O l CO g HCl aq +=+的1(298.15)379.93r m G K kJ mol θ-∆=- ,则必定是热力学不稳定而动力学稳定的系统。
(+)2、选择题(将所有正确答案的标号填入空格内)(1)真实气体行为接近理想气体性质的外部条件是 (b )(a )低温高压 (b )高温低压 (c )低温低压 (d )高温高压 (2)某温度时,反应22()()2()H g Br g HBr g +=的标准平衡常数2410K θ-=⨯,则反应2211()()()22HBr g H g Br g =+的标准平衡常数K θ等于 (b )(a )21410-⨯ (b (c )2410-⨯ (3)升高温度可以增加反应速率,最主要是因为 (b )(a )增加了分子总数(b )增加了活化分子的百分数 (c )降低了反应的活化能 (d )促使平衡向吸热方向移动(4)已知汽车尾气无害化反应221()()()()2NO g CO g N g CO g +=+的(298.15)0r m H K θ∆≤,要有利于取得有毒气体NO 和CO 的最大转化率,可采取的措施是 ( c) (a )低温低压 (b )高温高压 (c )低温高压 (d )高温低压(5)温度升高而一定增大的量是 (bc )(a ) r m G θ∆ (b )吸热反应的平衡常数K θ(c )液体的饱和蒸气压 (d )反应的速率常数k(6)一个化学反应达到平衡时,下列说法中正确的是 ( a) (a )各物质的浓度或分压不随时间而变化(b )r m G θ∆=0(c )正、逆反应的速率常数相等(d )如果寻找到该反应的高效催化剂,可提高其平衡转化率3、填空题(1)对于反应: 1223()3()2();(298)92.2r m N g H g NH g H K kJ mol θ-+=∆=-若升高温度(约升高100 K),则下列各项将如何变化(填写:不变,基本不变,增大或减小。
2021届高考化学三轮复习检测训练 化学反应原理(2)1.尿素[CO (NH 2)2]是一种用途广泛的化学品。
(1)尿素溶液可用作脱硝剂。
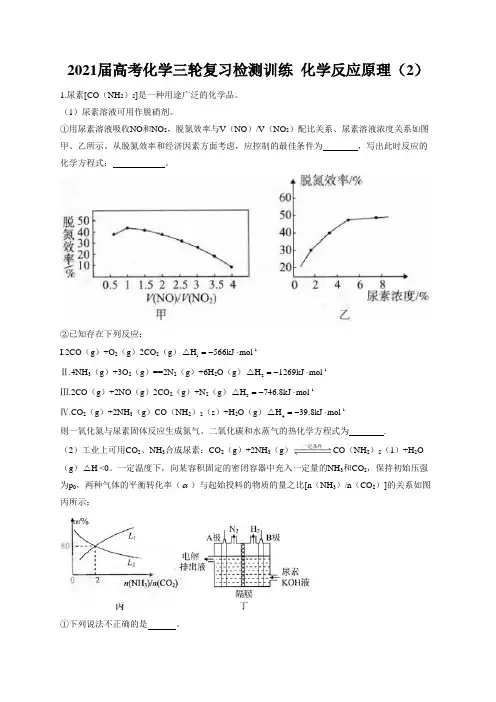
①用尿素溶液吸收NO 和NO 2,脱氮效率与V (NO )/V (NO 2)配比关系、尿素溶液浓度关系如图甲、乙所示。
从脱氮效率和经济因素方面考虑,应控制的最佳条件为 ,写出此时反应的化学方程式: 。
②已知存在下列反应:I.2CO (g )+O 2(g )2CO 2(g )-11H 566kJ mol =-⋅△Ⅱ.4NH 3(g )+3O 2(g )==2N 2(g )+6H 2O (g )-12H 1269kJ mol =-⋅△ Ⅲ.2CO (g )+2NO (g )2CO 2(g )+N 2(g )-13H 746.8kJ mol =-⋅△ Ⅳ.CO 2(g )+2NH 3(g )CO (NH 2)2(s )+H 2O (g )-14H 39.8kJ mol =-⋅△则一氧化氮与尿素固体反应生成氮气、二氧化碳和水蒸气的热化学方程式为 . (2)工业上可用CO 2、NH 3合成尿素:CO 2(g )+2NH 3(g )一定条件CO (NH 2)2(1)+H 2O(g )H △<0。
一定温度下,向某容积固定的密闭容器中充入一定量的NH 3和CO 2,保持初始压强为p 0,两种气体的平衡转化率(α)与起始投料的物质的量之比[n (NH 3)/n (CO 2)]的关系如图丙所示:①下列说法不正确的是 。
A.升温、增加压强都能提高NH3的转化率B.在一定条件下,混合气体的密度不再变化时,该反应达到最大限度C.及时分离出尿素和水蒸气,化学平衡常数一定增大D.尿素在土壤中可能转化为碳酸铵②图丙中NH3的平衡转化率的变化可用(填“L1”或“L2”)表示;该反应的平衡常数K p= (用平衡分压代替平衡浓度进行计算,分压=总压×物质的量分数)。
(3)如图丁所示装置(A、B极均为惰性电极)可用于电解尿素[CO(NH2)2]的碱性溶液制取氢气,该装置中A极的电极反应式为。
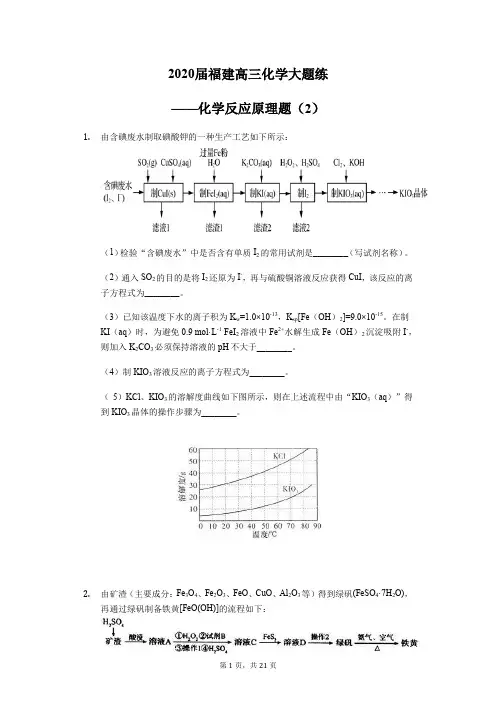
2020届福建高三化学大题练——化学反应原理题(2)1.由含碘废水制取碘酸钾的一种生产工艺如下所示:(1)检验“含碘废水”中是否含有单质I2的常用试剂是________(写试剂名称)。
(2)通入SO2的目的是将I2还原为I-,再与硫酸铜溶液反应获得CuI,该反应的离子方程式为________。
(3)已知该温度下水的离子积为K w=1.0×10-13,K sp[Fe(OH)2]=9.0×10-15。
在制KI(aq)时,为避免0.9 mol·L-1 FeI2溶液中Fe2+水解生成Fe(OH)2沉淀吸附I-,则加入K2CO3必须保持溶液的pH不大于________。
(4)制KIO3溶液反应的离子方程式为________。
(5)KCl、KIO3的溶解度曲线如下图所示,则在上述流程中由“KIO3(aq)”得到KIO3晶体的操作步骤为________。
2.由矿渣(主要成分:Fe3O4、Fe2O3、FeO、CuO、Al2O3等)得到绿矾(FeSO4·7H2O),再通过绿矾制备铁黄[FeO(OH)]的流程如下:已知:①FeS2和铁黄均难溶于水②生成氢氧化物沉淀的pH回答下列问题(1)写出酸浸过程中,Fe3O4所发生的离子反应方程式________________________________。
(2)加入试剂B,控制溶液pH的范围__________。
(3)请写出溶液C→溶液D的离子方程式__________________________________________。
(4)操作2为__________、__________、过滤、洗涤;绿矾制铁黄的化学反应方程式为_______________________。
(5)为测定制备的铁黄的纯度,取样品10.00 g,用稀硫酸溶解并配成250 mL溶液,每次取25 mL,并加入5.000 mol/L的KI溶液5 mL,用0.5000 mol/L Na2S2O3溶液滴定(),三次测定消耗Na2S2O3溶液的体积如下:则制得铁黄的纯度为__________。


第二章化学反应的基本原理一、判断题(正确请画“√”,错误的画“×”)1.当温度接近0K时,所有的放热反应可以认为都是自发进行的反应。
2.△S >0的反应,必定是自发反应。
3.对于一个反应如果△H>△G,则该反应必定是熵增的反应。
4.△Gθ值大,平衡常数Kθ值就愈大。
5.平衡常数K值越大,则反应速度越快。
6.对于△H<0的反应,提高温度速度常数k值减小。
7.对于△Hθ>0的可逆反应,提高温度平衡常数Kθ值增大。
8.NO的△f Gθm(298.15K)>0,空气中的N2和O2在常温常压下稳定共存。
但在高温常压时能发生反应,说明该反应是△Hθ>0, △Sθ>0的反应。
9.反应CO(g) = C(s)+1/2O2 (g)的△G>0,正向非自发,加入催化剂后降低了活化能,则反应正向进行。
10.在一个封闭系统中进行的可逆反应达到平衡后,若平衡条件体积和温度不变,则系统中各组分的浓度或分压不变。
11.一定温度下,对于△υg=0的可逆反应,达平衡后改变系统中某组分的浓度或分压,平衡不移动。
12.一定温度下,对于△υg≠0的可逆反应,达到平衡后,加入惰性气体,保持总压力不变,平衡不发生移动。
13.某可逆反应在一定条件下,转化率α值增大,则在该条件下平衡常数K值也一定增大。
14.对于一个复杂反应,当总反应的标准摩尔吉布斯函数变为:△Gθ总=△Gθ1+△Gθ2则该反应的平衡常数Kθ总=Kθ1+Kθ215.单质的△f Gθm(298.15K)值一定为零。
16. 反应级数取决于反应方程式中反应物的计量系数。
17. 自发进行的反应,一定具有较小的活化能。
18. 基元反应是指一步完成的简单反应。
19. 其它条件固定时,活化能小的反应,其反应速度快。
20. 化学平衡是指系统中正逆反应活化能相等的状态。
21. 反应的活化能越高,则该反应的平衡常数就越小。
22.平衡常数Kθ值小于1,则△Gθ>0。

2020年苏教版化学反应原理(选修)课后练习(2)一、单选题(本大题共3小题,共9.0分)1.若要在铜片上镀银时,下列叙述中错误的是将铜片接在电源的正极将银片接在电源的正极在铜片上发生的反应是:在银片上发生的反应是:可用溶液作电解质溶液可用溶液作电解质溶液.A. B. C. D.2.下列事实,与电化学腐蚀无关的是A. 埋在潮湿土壤里的铁管比埋在干燥土壤里的铁管更易被腐蚀B. 为保护海轮的船壳,常在船壳上镶入锌块C. 在空气中,金属银的表面生成一层黑色的物质D. 镀银的铁制品,镀层部分受损后,露出的铁表面易被腐蚀3.含 NaOH 的稀溶液与足量的稀盐酸反应,放出的热量,表示该反应的热化学方程式为A.B.C.D.二、填空题(本大题共1小题,共1.0分)4.如图各烧杯中盛有海水,铁在其中会发生腐蚀。
铁腐蚀的速率由快至慢的顺序为______。
三、简答题(本大题共5小题,共25.0分)5.氢氧燃料电池是最常见的燃料电池,该电池在正极通入氧气,在负极通入氢气,而电解质溶液通常是KOH溶液。
请写出氢氧燃料电池的电极反应式及电池反应方程式。
氢氧燃料电池有何优点?6.镍镉可充电电池在现代生活中有广泛应用。
该电池的电解质溶液为KOH溶液,它的充、放电反应按下式进行:已知、、NiOOH都难溶于KOH溶液。
请分别写出该电池在充电及放电时的电极反应式。
7.请说明以下防锈方法的原理。
在电线的外面长包裹一层塑料。
海轮的外壳除了喷上一层漆外,还会附上一些镁块。
减少钢铁中的含碳量,可以增强钢铁的耐腐蚀能力。
大型水闸常与直流电源的负极相连,再在电极的正极连上惰性电极,置于水中。
8.市场出售的“热袋”中的主要成分是铁粉、炭粉、木屑、少量氯化钠和水等,“热袋”用塑料袋密封,使用时从袋中取出轻轻揉搓就会放出热量,用完后袋内有大量铁锈生成。
请指出炭粉和氯化钠的作用。
请写出“热袋”中所形成的原电池的电极反应式及电池反应方程式,并分析铁锈产生的原因。

第二章 化学反应的基本原理一、判断题(正确请画“√”,错误的画“×”)1.当温度接近0K 时,所有放热反应可以认为都是自发进行的反应。
解:对。
根据吉布斯赫姆赫磁公式ΔG = Δ H – T ΔS 判断。
2.△S>0的反应,必定是自发反应。
解:错,不能判断,因为△S 作判据只适用于孤立系统中。
3.对于一个定温反应,如果△H>△G ,则该反应必定是熵增的反应。
解:对。
根据吉布斯赫姆赫磁公式ΔG = Δ H – T ΔS 判断。
则ΔS = (Δ H –ΔG )/T4.△G θ值大,平衡常数K θ值就愈大。
解:错。
ln K θ (T ) = - Δ r G m θ (T )/RT 。
需要考虑温度。
5.平衡常数K 值越大,则反应速度越快。
解:错。
平衡常数K 值是热力学问题,而反应速度是动力学问题6.对于△H<0的反应,提高温度,速度常数k 值减小。
解 错7.对于△H θ>0的可逆反应,提高温度,平衡常数K θ值增大。
解:对。
ln K θ (T ) = - ΔH θ /RT +△S θ/R8.NO 的△f G θm (298.15K )>0,空气中的N 2和O 2在常温常压下稳定共存。
但在高温常压时能发生反应,说明该反应是△H θ>0, △S θ>0的反应。
RTE aAe k -=解:对。
低温稳定,即不反应,高温不稳定,说明反应是△H θ>0,△S θ>0的反应。
ΔG = Δ H – T ΔS9.反应CO (g )=C (s )+1/2O 2(g )的△G>0,正向非自发,加入催化剂后降低了活化能,则反应正向进行。
解:错,催化剂不能改变反应方向。
10.在一个封闭系统中进行的可逆反应达到平衡后,若平衡体积和温度不变,则系统中各组分的的浓度和分压不变。
解:对,平衡状态下各组分浓度不变。
11.一定温度下,△v g =0的可逆反应达到平衡后,改变系统中某组分的浓度或分压,平衡不移动。

第七章浓度极化1.写出液相传质总流量的表达式及其所传导的电流的表达式。
2.分析稳态过程和暂态过程的区别和联系。
3.指出液相中各部分液层厚度的数量级。
4.分别写出用反应物粒子和可溶产物粒子表示的稳态扩散电流密度公式, 其中的z是粒子的荷电荷数吗?为什么?5.什么是极限扩散电流密度?6.说明双电层、扩散层、边界层的区别。
7.如何研究浓度极化的动力学特征?8.画出产物可溶和产物不溶时典型浓度极化曲线。
9.推导O与R均可溶且初始浓度均不为零的浓度极化公式。
10.简述平衡电位与稳定电位的区别和联系。
11.平板电极恒电位极化时, 暂态过程扩散层真实厚度大约是有效厚度的多少倍?12.以浓度分布曲线说明, 恒电位和恒电流条件下的非稳态扩散中浓度极化是如何发展的。
13.进行电位阶跃实验, 计算电流强度如何确定电极面积?14.微电极研究电极过程有何优点?15.对于一个可用半无限边界条件的方程来描述的电化学体系, 电池壁必须离开电极五倍“扩散层厚度”以上。
某物质的扩散系数D=10-5cm2/s, 求对于100s 的电位阶跃实验时间, 工作电极和电池壁之间的距离要求多大?16.如何根据J、J0、Jd的相对大小判断R.D.S?17.RED有何特点?18.如何用RED判断电极过程的R.D.S.19.RRED有何作用?20. 25℃下以3.0×103安培/米2的电流密度在静止的电解液中恒电流电解还原某有机物, 每一个有机物分子与6个电子相结合, 若液相传质步骤控制着整个电极过程的速度, 有机物的扩散系数为2×10-9米2/秒, 其浓度为10-2M, 扩散层的有效厚度约为5×10-4米, 求过渡时间。
当恒电流极化10-4秒时, 紧靠电极表面的液层中反应物的浓度是多少?21.在25℃下醌在光滑的铂电极上还原为氢醌。
已知醌在溶液中的浓度是0.01M, 它的扩散系数为9.5×10-10米2/秒, 扩散层厚度约为5×10-4米, 求在电流密度为1.0安培/米2 时的浓度过电位(假定反应物的电迁移和对电流可略去不计)。
基础化学第二版习题答案第一章:原子结构与元素周期表1. 根据质子数确定元素:- 质子数为1的元素是氢(H)。
- 质子数为6的元素是碳(C)。
2. 元素周期表中元素的排列规律:- 元素按照原子序数递增排列。
- 元素周期表分为s区、p区、d区和f区。
3. 元素周期表中的族和周期:- 每个周期代表一个电子壳层。
- 每个族代表一个价电子层。
第二章:化学键与分子结构1. 离子键与共价键的区别:- 离子键是由正负离子之间的静电吸引力形成的。
- 共价键是由两个原子共享电子对形成的。
2. 极性分子与非极性分子:- 极性分子具有不对称的电荷分布。
- 非极性分子的电荷分布是对称的。
3. 分子间作用力:- 包括氢键、范德华力等。
第三章:化学计量学1. 摩尔的概念:- 摩尔是化学中用于表示物质量的单位。
2. 摩尔质量的计算:- 摩尔质量是元素的相对原子质量,以克/摩尔为单位。
3. 化学方程式的平衡:- 确保方程式两边的原子数相等。
第四章:溶液与溶解度1. 溶液的类型:- 包括水溶液、有机溶液等。
2. 溶解度的定义:- 溶解度是在特定条件下,物质在溶剂中的最大溶解量。
3. 溶液的浓度表示方法:- 包括摩尔浓度、质量浓度等。
第五章:化学反应速率与化学平衡1. 反应速率的影响因素:- 包括温度、浓度、催化剂等。
2. 化学平衡的定义:- 反应物和生成物的浓度不再随时间变化的状态。
3. 勒夏特列原理:- 描述了化学平衡对系统条件变化的响应。
第六章:氧化还原反应1. 氧化与还原的定义:- 氧化是电子的损失,还原是电子的获得。
2. 氧化还原反应的平衡:- 涉及电子的转移,需要考虑电子的平衡。
3. 氧化还原电位:- 描述了氧化还原反应的倾向性。
第七章:酸碱平衡1. 酸与碱的定义:- 酸是能够释放氢离子的物质,碱是能够释放氢氧根离子的物质。
2. pH的定义:- pH是溶液酸度的度量,表示为氢离子浓度的负对数。
3. 缓冲溶液:- 能够抵抗小量酸或碱添加引起的pH变化。
2020届福建高三化学大题练——化学反应原理题(2)1.由含碘废水制取碘酸钾的一种生产工艺如下所示:(1)检验“含碘废水”中是否含有单质I2的常用试剂是________(写试剂名称)。
(2)通入SO2的目的是将I2还原为I-,再与硫酸铜溶液反应获得CuI,该反应的离子方程式为________。
(3)已知该温度下水的离子积为K w=1.0×10-13,K sp[Fe(OH)2]=9.0×10-15。
在制KI(aq)时,为避免0.9 mol·L-1 FeI2溶液中Fe2+水解生成Fe(OH)2沉淀吸附I-,则加入K2CO3必须保持溶液的pH不大于________。
(4)制KIO3溶液反应的离子方程式为________。
(5)KCl、KIO3的溶解度曲线如下图所示,则在上述流程中由“KIO3(aq)”得到KIO3晶体的操作步骤为________。
2.由矿渣(主要成分:Fe3O4、Fe2O3、FeO、CuO、Al2O3等)得到绿矾(FeSO4·7H2O),再通过绿矾制备铁黄[FeO(OH)]的流程如下:已知:①FeS2和铁黄均难溶于水②生成氢氧化物沉淀的pH回答下列问题(1)写出酸浸过程中,Fe3O4所发生的离子反应方程式________________________________。
(2)加入试剂B,控制溶液pH的范围__________。
(3)请写出溶液C→溶液D的离子方程式__________________________________________。
(4)操作2为__________、__________、过滤、洗涤;绿矾制铁黄的化学反应方程式为_______________________。
(5)为测定制备的铁黄的纯度,取样品10.00 g,用稀硫酸溶解并配成250 mL溶液,每次取25 mL,并加入5.000 mol/L的KI溶液5 mL,用0.5000 mol/L Na2S2O3溶液滴定(),三次测定消耗Na2S2O3溶液的体积如下:则制得铁黄的纯度为__________。
高二化学化学反应原理练习题及答案一、选择题1. 下面哪项不属于氧化还原反应?A. 酸碱反应B. 燃烧反应C. 电解反应D. 金属腐蚀反应2.化学方程式2H₂ + O₂ → 2H₂O中,还原剂是?A. H₂OB. H₂C. O₂D. 以上都不对3. 化学反应原理中,电离作用最明显的是?A. 酸碱中和反应B. 酸与碱溶液的电离反应C. 氧化还原反应D. 沉淀反应4. 铜与稀硫酸反应,生成物是?A. CuSO₄ + SO₂ + H₂OB. CuSO₄ + H₂SO₄C. CuSO₄ + 2H₂OD. 以上都不对5. 某氧化物化合物可以与酸反应,并且会产生水,该氧化物化合物的通式是?A. MOB. MO₂C. M₂O₃D. M₂O二、填空题1. 某物质发生氧化反应的过程中,丧失了大量的电子,属于_________作用。
2. 需要外界供电才能进行的化学反应称为____________反应。
3. H₂O → H₂ + O₂这个化学反应是一个_________反应。
4. 化学方程式CaCO₃ → CaO + ________ + CO₂中,需要填写的是什么?三、解答题1. 请结合化学原理,解释电解质溶液导电的原因。
电解质溶液可以导电的原因是其中存在着能够离解成离子的物质。
当电解质溶液中加入电极板时,溶液中的离子会受到电场的作用,正离子会向阴极电极移动,负离子则向阳极电极移动。
这个移动的过程就形成了电流。
所以电解质溶液可以导电。
2. 铜与硫酸反应的离子方程式为Cu + H₂SO₄ → CuSO₄ + H₂↑,请写出该反应的原子方程式。
Cu + H₂SO₄ → CuSO₄ + H₂↑Cu + H₂SO₄ → CuSO₄ + H₂O + SO₂↑3. 根据氧化还原反应理论,解释为什么金属腐蚀会放出气体。
金属腐蚀是一种氧化还原反应,金属失去电子形成阳离子,在金属表面形成了氧化物。
同时,在反应中,金属原子被氧化,释放出的电子转移给了其他物质。
化学反应原理第二章测试题含答案(共7页)--本页仅作为文档封面,使用时请直接删除即可----内页可以根据需求调整合适字体及大小--高二化学反应原理第二章化学反应的方向、限度和速率测试题含答案质量检测第Ⅰ卷(选择题,共54分)一、选择题(本题包括18个小题,每题3分,共54分。
每题只有一个选项符合题)1.下列反应中,一定不能自发进行的是()(s)====2KCl(s)+3O2(g) ΔH=- kJ·mol-1 ΔS=1 110 J·mol-1·K-1(g)====C(s,石墨)+1/2 O2(g) ΔH = kJ·mol-1ΔS=- J·mol-1·K-1(OH)2(s)+2H2O(l)+O2(g)====4Fe(OH)3(s)ΔH =- kJ·mol-1 ΔS =- J·mol-1·K-1(s)+CH3COOH(aq)====CO2(g)+CH3COONH4(aq)+H2O(l)ΔH = kJ·mol-1ΔS = J·mol-1·K-12.下列反应中,熵减小的是()A、(NH4)2CO3(s)=NH4HCO3(s)+NH3(g)B、2N2O5(g)=4NO2(g)+O2(g)C、 MgCO3(s)=MgO(s)+CO2(g)D、2CO(g)=2C(s)+O2(g)3.反应4NH3(气)+5O2(气) 4NO(气)+6H2O(气)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了,则此反应的平均速率v(X)(反应物的消耗速率或产物的生成速率)可表示为( )A. (NH3) = mol/(L·s) B.v (O2) = mol/(L·s)C.v (NO) = mol/(L·s) D.v (H2O) = mol/(L·s)4.将4molA气体和2molB气体在2L的容器中混合,在一定条件下发生如下反应:2A(g)+B (g) 2C(g),若经2s后测得C的浓度为·L-1,现有下列几种说法:①用物质A的浓度变化表示的反应速率为·L-1·s-1②用物质B的浓度变化表示的反应速率为 mol·L-1·s-1③平衡时物质A的转化率为70%,④平衡时物质B的浓度为·L-1,其中正确的是()A.①③ B. ①④ C. ②③ D. ③④235. 在2L 的密闭容器中,发生以下反应:2A (气)+B(气) 2C (气)+D (气)若最初加入的A和B 都是4 mol ,在前10s A 的平均反应速度为 mol/(L ·s),则10s 时,容器中B 的物质的量是( )A. molB. molC. molD. mol·l -1的硫酸和过量的锌粉反应,在一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向溶液中加入适量的 〔 〕A 碳酸钠固体B 水C 硝酸钾溶液D 硫酸铵固体7. 将ag 块状碳酸钙与足量盐酸反应,反应物损失的质量随时间的变化曲线下图所示,在相同的条件下,bg(b<a)粉末状的碳酸钙与同浓度的盐酸反应,则相应的曲线(图中虚线所示)正确的是〔 〕A B C D8. 在容积为1L 的密闭容器里,装有4molNO 2,在一定温度时进行下面的反应:2NO 2(g)N 2O 4(g),该温度下反应的平衡常数K =,则平衡时该容器中NO 2的物质的量为 ( ) A .0mol B .1mol C .2mol D .3mol 9. 在一定条件下,可逆反应X(g)十3Y(g)2Z(g)达到平衡时,X 的转化率与Y 的转化率之比为1∶2,则起始充入容器中的X 与Y 的物质的量之比为( ) A .1∶1 B .1∶3 C .2∶3D .3∶210. 在一固定容积的密闭容器中,加入4 L X(g)和6 L Y(g),发生如下反应:X(g)+n Y(g)2R(g)+W(g),反应达到平衡时,测知X 和Y 的转化率分别为25%和50%,则化学方程式中的n 值为( )A .4B .3C .2D .1 11. 可逆反应2SO 2 +O 22SO 3的平衡状态下,保持恒温恒容向容器中加入一定量的O 2,下列说法正确的是(K 为平衡常数,Qc 为浓度商)( )不变,K 变大,O 2转化率增大 B. Qc 不变,K 变大,SO 2转化率减小损失质量O 损失质量损失质量损失质量O4C. Qc 变小,K 不变,O 2转化率减小D. Qc 增大,K 不变,SO 2转化率增大 12. 反应N 2O 4(g)2NO 2(g);△H= +57 kJ·mol -1,在温度为T 1、T 2时,平衡体系中NO 2的体积分数随压强变化曲线如图所示。