YYT0287-2003工作环境5s核查表
- 格式:doc
- 大小:138.00 KB
- 文档页数:6



资料范本本资料为word版本,可以直接编辑和打印,感谢您的下载YYT0287-2003医疗器械质量管理体系用于法规的要求地点:__________________时间:__________________说明:本资料适用于约定双方经过谈判,协商而共同承认,共同遵守的责任与义务,仅供参考,文档可直接下载或修改,不需要的部分可直接删除,使用时请详细阅读内容国家食品药品监督管理局发布200×-××-××实施200×-××-××发布医疗器械质量管理体系用于法规的要求Medical devices Quality Management Systems Requirements for Regulatory Purposes(ISO 13485:2003,IDT)(征求意见稿)YY/T 0287-2003代替 YY0287-1996YY中华人民共和国医药行业标准ICS备案号:目录TOC \o "1-3" \h \z HYPERLINK \l "_Toc43611950" 前言PAGEREF _Toc43611950 \h 3HYPERLINK \l "_Toc43611951" 0引言 PAGEREF _Toc43611951 \h 4HYPERLINK \l "_Toc43611952" 0.1总则 PAGEREF_Toc43611952 \h 4HYPERLINK \l "_Toc43611953" 0.2过程方法 PAGEREF_Toc43611953 \h 4HYPERLINK \l "_Toc43611954" 0.3与其他标准的关系 PAGEREF _Toc43611954 \h 4HYPERLINK \l "_Toc43611955" 0.4与其它管理体系的相容性PAGEREF _Toc43611955 \h 5HYPERLINK \l "_Toc43611956" 1范围 PAGEREF _Toc43611956 \h 5HYPERLINK \l "_Toc43611957" 1.1总则 PAGEREF_Toc43611957 \h 5HYPERLINK \l "_Toc43611958" 1.2应用 PAGEREF_Toc43611958 \h 5HYPERLINK \l "_Toc43611959" 2引用标准 PAGEREF_Toc43611959 \h 6HYPERLINK \l "_Toc43611960" 3术语和定义 PAGEREF_Toc43611960 \h 6HYPERLINK \l "_Toc43611961" 4质量管理体系 PAGEREF_Toc43611961 \h 7HYPERLINK \l "_Toc43611962" 4.1总要求 PAGEREF_Toc43611962 \h 7HYPERLINK \l "_Toc43611963" 4.2文件要求 PAGEREF_Toc43611963 \h 8HYPERLINK \l "_Toc43611964" 5管理职责 PAGEREF_Toc43611964 \h 9HYPERLINK \l "_Toc43611965" 5.1管理承诺 PAGEREF_Toc43611965 \h 9HYPERLINK \l "_Toc43611966" 5.2 以顾客为关注焦点 PAGEREF _Toc43611966 \h 9_Toc43611967 \h 9HYPERLINK \l "_Toc43611968" 5.4 策划 PAGEREF_Toc43611968 \h 10HYPERLINK \l "_Toc43611969" 5.5职责、权限和沟通 PAGEREF _Toc43611969 \h 10HYPERLINK \l "_Toc43611970" 5.6管理评审 PAGEREF_Toc43611970 \h 10HYPERLINK \l "_Toc43611971" 6资源管理 PAGEREF_Toc43611971 \h 11HYPERLINK \l "_Toc43611972" 6.1资源提供 PAGEREF_Toc43611972 \h 11HYPERLINK \l "_Toc43611973" 6.2人力资源 PAGEREF_Toc43611973 \h 11HYPERLINK \l "_Toc43611974" 6.3 基础设施 PAGEREF_Toc43611974 \h 12HYPERLINK \l "_Toc43611975" 6.4 工作环境 PAGEREF_Toc43611975 \h 12HYPERLINK \l "_Toc43611976" 7产品实现 PAGEREF_Toc43611976 \h 12HYPERLINK \l "_Toc43611977" 7.1产品实现的策划 PAGEREF_Toc43611977 \h 12HYPERLINK \l "_Toc43611978" 7.2与顾客有关的过程 PAGEREF _Toc43611978 \h 13HYPERLINK \l "_Toc43611979" 7.3 设计和开发 PAGEREF_Toc43611979 \h 13_Toc43611980 \h 15HYPERLINK \l "_Toc43611981" 7.5生产和服务提供 PAGEREF_Toc43611981 \h 16HYPERLINK \l "_Toc43611982" 7.6监视和测量装置的控制 PAGEREF _Toc43611982 \h 18HYPERLINK \l "_Toc43611983" 8测量、分析和改进 PAGEREF_Toc43611983 \h 19HYPERLINK \l "_Toc43611984" 8.1总则 PAGEREF_Toc43611984 \h 19HYPERLINK \l "_Toc43611985" 8.2监视和测量 PAGEREF_Toc43611985 \h 19HYPERLINK \l "_Toc43611986" 8.3不合格品的控制 PAGEREF_Toc43611986 \h 20HYPERLINK \l "_Toc43611987" 8.4数据分析 PAGEREF_Toc43611987 \h 20HYPERLINK \l "_Toc43611988" 8.5改进 PAGEREF_Toc43611988 \h 21HYPERLINK \l "_Toc43611989" 附录A PAGEREF _Toc43611989 \h 22HYPERLINK \l "_Toc43611990" 附录B PAGEREF _Toc43611990 \h 25HYPERLINK \l "_Toc43611992" 参考文献目录 PAGEREF_Toc43611992 \h 50前言本标准等同采用ISO13485:2003《医疗器械质量管理体系用于法规的要求》本标准将取消并代替YY/T0287:1996和YY/T0288:1996。


工作环境控制程序1.目的为了保证产品的质量,保证产品的原材料、成品不会受到损坏,保障生产安全,发挥员工的积极性,特制定生产环境控制程序。
2. 适用范围本程序适用于本公司产品实现过程中的工作环境要求。
3. 组织和职责3.1生产技术部负责对工作环境进行管理和监督。
4. 步骤和方法4.1 识别工作环境要求4.1.1 生产技术部组织公司各有关职能部门依据国家相应的环保、安全、职业健康相关要求,对生产、研发等环节进行工作场所的环境因素识别,环境因素的识别应着重考虑:a) 人员与产品或工作环境的接触会对产品的质量有不利的影响。
b) 工作环境条件对产品质量产生不利的影响。
c) 易于对其他产品、工作环境或人员产生污染的产品。
4.1.2 对于确定存在上述工作环境需求的工作场所,生产技术部应制定相应的环境因素控制方案报总经理批准后实施,配备必要的控制设施、具体落实对每一确定的环境因素的控制。
4.2 维持工作环境4.2.1 各部门应确保自己范围的工作环境符合相应规定要求,并负责相关设施的日常维护保养工作。
4.2.2 5S小组按《5S简介和要求》组织对工作环境的检查以及评比,并将检查结果填写在相应的5S《核查表》。
对于检查所发现的问题,要求责任部门限期纠正。
若属于新发现的环境因素或以往措施不得力的,再次进行识别和制定相应控制措施。
4.2.3 5S的定义、目的和场所的要求,详见办公室编制的三层次文件《5S简介和要求》。
ISO13485:2003医疗器械质量体系内审员培训【课程描述】ISO13485:2003《医疗器械质量管理体系用于法规的要求》是以ISO9001标准为基础,应用于医疗器械的独立标准。
本课程将透彻的讲解医疗器械行业认证要求,使您全面掌握有关ISO 13485:2003的标准要求,掌握医疗器械行业相关要求及质量体系内部审核的技巧和方法。
【课程帮助】【课程对象】医疗器械行业凡生产二类、三类产品的医疗器械生产企业必须有2-4名内审员,未配有内审员的企业应派人员参加培训。
5S简介和要求
一、5S的定义和目的
1S——整理
定义:区分要用和不要用的,不要用的清除掉
目的:把“空间”腾出来活用。
2S——整顿
定义:要的东西依规定定位、定量摆放整齐,明确标识。
目的:不要浪费“时间“找东西。
3S——清扫
定义:清除职场内的脏污,并防止污染的发生。
目的:清除“脏污”,保持职场干干净净,明明亮亮。
4S——清洁
定义:将上面3S实施的做法制定化,规范化,并维持成果。
目的:通过制度化来维护成果,并显现异常之所在。
5S——素养
定义:人人依规定行事,从心态上养成好习惯。
目的:改变“人质”,养成工作讲究认真的习惯。
二、要求
要求行政部和5S小组至少每月检查一次,检查内容参考Q/MDK 03.640.A-07A《查核表》,并打分。
平均分值说明如下:
4分——非常好
3分——好
2分——需要加油
1分——尚早
0分——完全不行
三、记录
ISO13485:2003医疗器械质量体系内审员培训
【课程描述】
ISO13485:2003《医疗器械质量管理体系用于法规的要求》是以ISO9001标准为基础,应用于医疗器械的独立标准。
本课程将透彻的讲解医疗器械行业认证要求,使您全面掌握有关ISO 13485:2003的标准要求,掌握医疗器械行业相关要求及质量体系内部审核的技巧和方法。
【课程帮助】
【课程对象】
医疗器械行业凡生产二类、三类产品的医疗器械生产企业必须有2-4名内审员,未配有内审员的企业应派人员参加培训。
【课程大纲】
第一部分
◆ 医疗器械行业质量管理体系基础简介
◆ ISO13485 质量体系医疗器械用于法规目的的体系要求讲解:
4 质量管理体系
5 管理职责
6 资源管理
7 产品实现
8 测量、分析和改进
◆ ISO13485体系文件要求与过程控制:风险分析/評估
第二部分
◆ 医疗器械的法规要求
欧洲医疗器械指令MDD、有源植入性医疗器械指令AIMD、体外诊断医疗器械指令IVDD、我国的GMP等。
◆ ISO13485 内部审核工作的策划
◆ 内部审核技巧
◆ 第三方质量体系认证过程和认证中常见的问题
◆ 考试
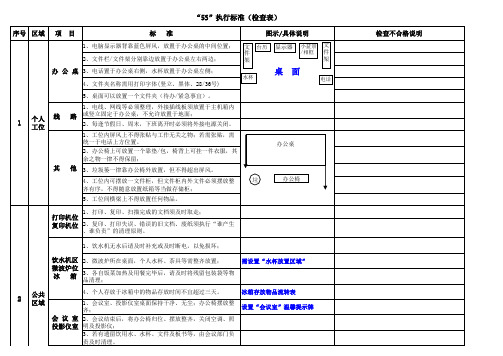
工作环境5s核查表
共4页第1页
查核人/日期:
共4页第2页
查核人/日期:
共4页第3页
查核人/日期:
共4页第4页
查核人/日期:。