醛固酮拮抗剂在心衰中的应用PPT课件
- 格式:pptx
- 大小:704.05 KB
- 文档页数:20





醛固酮在心力衰竭过程中的作用及醛固酮受体拮抗剂的应用作者:90303101 汪冠宏90303102 卢松鹤90303103 王志辉90303104 潘新磊90303105 钟波90303106 黄知03口腔摘要:以前,人们认为醛固酮拮抗剂对心力衰竭的保护作用源于其利尿作用。
近年来发现,除了利尿作用外,醛固酮拮抗剂在心力衰竭病人体内能够抑制心肌重构。
这也成为近年来对醛固酮拮抗剂的研究重点,是醛固酮拮抗剂在心力衰竭治疗过程中地位日益重要。
本文作者就醛固酮在心力衰竭发展过程中的作用以及醛固酮拮抗剂临床应用进行讨论。
关键词:心力衰竭醛固酮螺内酯伊普利酮心力衰竭是指由于心脏工作能力减损,心排血量降低,静脉系统淤血及动脉系统灌注不足的一组心脏循环症候群。
由于各种原因所导致的心力衰竭其治疗及预后又不甚理想,短期及长期死亡率高居不下,而近年来报道醛固酮拮抗剂的治疗可以有效降低患者死亡率。
所以,我们在这里为这一类药品的作用原理以及研究进展进行总结。
1.醛固酮在心力衰竭患者体内的合成:在心力衰竭发生过程中,由于心脏泵出血量不足,使心输出量下降,心脏充盈压上升。
而心输出量下降会反射性兴奋交感神经系统,造成肾素-血管紧张素-醛固酮系统(RAAS)分泌的增加。
由于受到血管紧张素Ⅱ和Ⅲ的作用,在肾上腺皮质球状带中,醛固酮合酶利用11脱氧皮质酮合成醛固酮。
这个过程除了受血管紧张素调节之外,还受钾离子调节,此外,促肾上腺皮质激素(ACTH)和钠离子也有一定调节作用。
这是经典的RAAS调节机制。
而在近些年的研究中发现,应用了ACE抑制剂和血管紧张素受体1拮抗剂的患者,并不能完全阻断醛固酮的生成,反而使醛固酮水平反弹性升高,其在心力衰竭患者血浆水平可达正常20倍。
原因在于在心衰患者体内,醛固酮合成升高而肝脏清除减少。
这种现象被称作“醛固酮逃逸”(Aldosterone Escape)[1]。
由此人们发现了除了肾上腺皮质之外,心肌细胞、血管内皮细胞、间质细胞和平滑肌细胞也可以局部合成醛固酮,并且不依赖血管紧张素的调节。

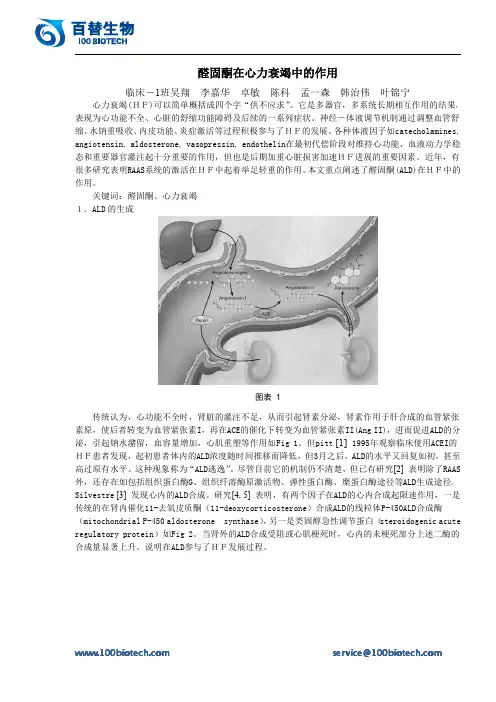
醛固酮在心力衰竭中的作用临床-1班吴翔李嘉华卓敏陈科孟一森韩治伟叶锦宁心力衰竭(HF)可以简单概括成四个字“供不应求”。
它是多器官,多系统长期相互作用的结果,表现为心功能不全、心脏的舒缩功能障碍及后续的一系列症状。
神经-体液调节机制通过调整血管舒缩、水钠重吸收、内皮功能、炎症激活等过程积极参与了HF的发展。
各种体液因子如catecholamines, angiotensin,aldosterone,vasopressin,endothelin在最初代偿阶段对维持心功能、血液动力学稳态和重要器官灌注起十分重要的作用,但也是后期加重心脏损害加速HF进展的重要因素。
近年,有很多研究表明RAAS系统的激活在HF中起着举足轻重的作用。
本文重点阐述了醛固酮(ALD)在HF中的作用。
关键词:醛固酮、心力衰竭1.ALD的生成图表1传统认为,心功能不全时,肾脏的灌注不足,从而引起肾素分泌,肾素作用于肝合成的血管紧张素原,使后者转变为血管紧张素I,再在ACE的催化下转变为血管紧张素II(Ang II),进而促进ALD的分泌,引起钠水潴留,血容量增加,心肌重塑等作用如Fig1。
但pitt[1]1995年观察临床使用ACEI的HF患者发现,起初患者体内的ALD浓度随时间推移而降低,但3月之后,ALD的水平又回复如初,甚至高过原有水平。
这种现象称为“ALD逃逸”。
尽管目前它的机制仍不清楚,但已有研究[2]表明除了RAAS 外,还存在如包括组织蛋白酶G、组织纤溶酶原激活物、弹性蛋白酶、糜蛋白酶途径等ALD生成途径。
Silvestre[3]发现心内的ALD合成。
研究[4,5]表明,有两个因子在ALD的心内合成起限速作用,一是传统的在肾内催化11-去氧皮质酮(11-deoxycorticosterone)合成ALD的线粒体P-450ALD合成酶(mitochondrial P-450aldosterone synthase),另一是类固醇急性调节蛋白(steroidogenic acute regulatory protein)如Fig2。

醛固酮拮抗剂治疗充血性心力衰竭研究进展标签:醛固酮拮抗剂;心力衰竭充血性心力衰竭(简称心衰)是各种不同病因的严重心脏病发展到最后的共同结局,严重威胁心脏病人的生命和生活质量。
降低心衰的发病率及死亡率、提高远期疗效具有重要意义,而近年来对心衰的病理生理改变及发生机制的研究取得很大进展。
心衰时心脏要启动一系列代偿机制来维持泵血功能,主要表现为交感神经兴奋;肾素-血管紧张素-醛固酮系统(RAAS)被激活,血管紧张素及醛固酮水平升高;一些血管活性物质释放增加。
所有这些均可造成心衰进行性恶化。
在血管紧张素转换酶抑制剂(ACEI)阻断肾素-血管紧张素系统(RAS)的作用被广泛认可后,醛固酮的病理生理作用及醛固酮拮抗剂的临床应用也受到了关注和重视。
本文就此作一综述:1醛固酮与充血性心力衰竭醛固酮是一种重要的盐皮质激素,是RAAS中的一个重要成分,在人体心血管系统的调节中具有重要的作用。
近年来的研究发现,除了肾上腺皮质球状带以外,血管、心、脑、肾、肺等器官也具有合成并分泌醛固酮的功能。
在心力衰竭时,由于肾灌注压降低和肾灌注量减少,交感神经兴奋,血中儿茶酚胺增加,以及限制钠摄入和使用利尿剂等,使肾小球旁器细胞分泌肾素增加,裂解血管紧张素原产生血管紧张素Ⅰ再经过血管紧张素转换酶的作用变为血管紧张素Ⅱ,刺激肾上腺皮质球状带合成并释放醛固酮。
醛固酮升高以后,作用于远曲小管及集合管醛固酮受体,增加管腔膜Na+、K+通道及Na+-K+-ATP酶活性,促进钠再吸收及钾排泄,引起水、钠潴留和低钾、低镁血症,增加心脏负荷及心电的不稳定性,导致冠脉痉挛、心律失常,使心力衰竭进一步恶化;长期的醛固酮升高,还可因细胞内钾的耗竭导致心肌细胞的坏死;醛固酮升高对心力衰竭患者产生的不良影响还表现为致内皮细胞功能紊乱、抑制压力感受器、收缩全身性血管及降低具有保护作用的血清高密度脂蛋白等。
研究表明,醛固酮还是血管损伤的一个重要的调节因子,可直接作用于血管系统,与血管平滑肌细胞肥大、内皮功能异常、心肌纤维化、蛋白尿和肾血管损伤等有关。


心衰治疗新四联——醛固酮受体拮抗剂(MRA)醛固酮的病理和生理作用◆ 醛固酮的合成•醛固酮(Aldosterone Antagonists )是肾素﹣血管紧张素﹣醛固酮系统( RAAS )的重要组成部分。
•醛固酮是一种甾体类盐皮质激素,其分泌来自两条途径:◆ 醛固酮的生理功能◆ 醛固酮的病理机制•心肌细胞摄取儿茶酚胺可很快将其代谢,使儿茶酚胺失活,醛固酮可阻断心肌对儿茶酚胺的摄取,从而使细胞外儿茶酚胺增多,有致心律失常、促心肌缺血作用。
•总之,RAAS 激活,醛固酮合成和释放增加,短时间内可增加心排量,起到代偿作用;长期增高,可引起水钠潴留、电解质紊乱、心肌及血管间质发生胶原沉积、纤维化,导致心血管疾病进行性加重。
MRA的药理作用及药代动力学◆醛固酮受体拮抗剂•醛固酮受体拮抗剂又称盐皮质受体激素拮抗剂(mineralcorticoid recept antagonist , MRA ),目前临床上主要的两种 MRA 为螺内酯和依普利酮。
•MRA 与细胞内的受体结合后,影响醛固酮受体复合物的形成,进而影响醛固酮发挥其作用,发挥心血管保护作用。
★ 螺内酯◇ 药理作用1.排钠、保钾利尿作用•具有保钾、排钠的利尿作用,能够减轻心脏负担,改善心功能。
2.防止心肌、血管纤维化与重塑•醛固酮可引起心肌和血管重塑,导致心功能的下降、血管的顺应性降低。
•螺内酯可阻断醛固酮这种作用,防止心肌、血管的重塑。
3.参与抗心律失常作用•螺内酯通过抗心肌纤维化、逆转心脏重塑而使室壁张力减轻、减少血浆儿茶酚胺的浓度等作用发挥抗心律失常作用。
4.纠正低钾低镁血症•螺内酯醛固酮具有排钾、排镁作用,导致血钾、血镁的降低。
•低钾、低镁血症可导致致命性心律失常、甚至猝死。
螺内酯通过拮抗醛固酮的这种作用,减少猝死的发生。
◇ 药代动力学•螺内酯口服吸收较好,生物利用度>90%,口服1日左右起效,经2-3d药效达到高峰,停药后药效仍可持续2-3d。

史国塞旦医药!Q!Q笙!旦筮§鲞筮!魍£!i塑塑璺璺丛型:』翌垫!Q,!丛:i:№:!外光灯(365rllll)下检视。
供试品色谱中,在与对照药材色谱和对照品色谱相应的位置上,显相同颜色的荧光斑点。
(见图lC)图1薄层色谱图1.阴性对照品溶液2.对照品溶液3.对照药材溶液4缶.供试品A大黄B.姜黄C.黄柏3.3检查3.3.1相对密度按《中国药典))2005年版一部附录ⅦA相・149・对密度测定法比重瓶法检验…,相对密度应不低于1.01。
3.2.2pH值按《中国药典)2005年版一部附录ⅦGpH测定法测定…,pH值应为3.5.5.5。
3.2.3装量差异、微生物限度应符合洗剂项下有关的各项规定(中国药典2005年版一部附录IV)¨]。
4讨论本文通过实验,确定了金黄洗剂中主要中药大黄、姜黄、黄柏的薄层色谱方法,供试品溶液与对照品溶液在色谱相对应位置显相同颜色斑点,而阴性对照溶液不显相应主斑点,检出成份不受处方中其他药材干扰,该鉴别重现性好,专属性强,结果可靠,故该法可以定性地控制该制剂的质量。
参考文献[1]中华人民共和国药典委员会.中国药典(一部)化学工业出版杜,2005.附录ⅥB.醛固酮拮抗剂在治疗心力衰竭中的进展研究刘岚【摘要】目的探讨醛固酮拮抗剂在治疗心力衰竭中的应用。
方法通过螺内酯评价试验来解决“醛同酮逃逸”问题。
结果安慰剂组死亡386例(46%),螺内酯组死亡284例(35%)。
结论BALES试验的结果令为醛周酮拮抗剂进入心衰的一线用药提供了理论依据。
【关键词】醛固酮拮抗剂;心力衰竭;进展近年来慢性心衰的发病率呈上升趋势,已成为严重危害老年人健康的疾病。
传统观点认为:心衰产生的机制是以钠水潴留和泵功能衰竭为表现的血流动力学异常。
与此相应的治疗措施为利尿、强心、扩血管。
80年代之后,随着对心衰机制的研究逐步深入,人们发现神经内分泌的过度激活是心衰产生的更本质的原因。
据此,可以拮抗肾素一血管紧张素一醛固酮系统(RAAS)的ACEI和可以拮抗交感肾上腺素系统的B阻滞剂在心衰的治疗中被提到了一个较高的位置。
摘要摘要目的:本研究主要采用Meta分析的方法科学评价醛固酮受体拮抗剂对射血分数保留的心衰疗效和安全性以及研究质量的总体水平,为今后的临床应用提供依据。
方法:计算机检索PubMed,EMBASE,Cochrane Library,EBSCO,clinical trials databases、中国知网、万方医学、中国生物医学文献数据库,收集2002年1月-2017年1月醛固酮受体拮抗剂与射血分数保留的心衰治疗相关的临床随机对照研究文献。
由2名研究者分别按照纳入标准与排除标准选择文献,对纳入文献进行质量评价并提取有关数据,采用Rev Man5.2软件进行Meta分析。
根据文献异质性检验结果,进行固定效应模型或随机效应模型的Meta分析。
用漏斗图评估发表偏倚。
结果:本次Meta分析纳入7个研究,共计922例患者,其中醛固酮受体拮抗剂组461例,对照组461例。
Meta分析结果显示:(1)与对照组相比,醛固酮受体拮抗剂对心脏舒张功能影响:MRA能显著降低患者E/e'比值[WMD=-1.5,95%CI(-2.12,-0.89),P<0.00001]、增大二尖瓣环最大流速(e')[WMD=0.33,95%CI(0.11,0.55),P=0.003],有缩短E峰减速时间[WMD=-17.07,95%CI(-34.29,0.16),P=0.05]、降低舒张性心衰患者左室质量指数[WMD=-2.81,95%CI(-5.77,0.16),P=0.06]的趋势,但不能显著提高患者左室射血分数水平[WMD=0.95,95%CI(-2.15,4.05),P=0.55]、改善HF-PEF患者E/A比值[WMD=0.09,95%CI(-0.14,0.31),P=0.45]、缩小左室舒张末径[WMD=-0.12,95%CI(-0.35,0.10),P=0.29]、减小左房容积指数[WMD=-0.77,95%CI(-2.19,0.65),P=0.29]。
醛固酮拮抗剂螺内酯在治疗心力衰竭患者中的临床疗效观察目的:探究醛固酮拮抗劑螺内酯在治疗心力衰竭患者中的临床效果。
方法:选取2016年2月-2017年2月来本院治疗并且确诊为心力衰竭的患者130例。
按照随机数字表法将其分为研究组和对照组,各65例。
对照组采用常规治疗方法,研究组在对照组基础上加用醛固酮拮抗剂螺内酯,两组治疗时间均为6个月。
比较两组治疗前后的血钾、肌酐水平及心功能指标,包括心率(heart rate,HR)、左心室舒张末期内径(left ventricular end diastolic diameter,LVEDD)、心排出量(cardiac output,CO)、左心室收缩末期内径(left ventricular end-systolic dimension,LVESD)、左室射血分数(left ventricular ejection fractions,LVEF);比较两组治疗效果。
结果:研究组患者治疗总有效率为93.85%,显著高于对照组的76.92%(P<0.05)。
治疗前,两组患者血钾水平均处于正常范围内,肌酐水平均超过正常值,比较差异均无统计学差异(P>0.05);治疗后,研究组血钾水平显著高于对照组(P<0.05),但两组患者肌酐水平比较差异无统计学意义(P>0.05)。
治疗前,两组患者CO、LVEF、LVESD、LVEDD比较差异均无统计学意义(P>0.05);治疗后,研究组患者CO、LVEF显著高于对照组(P<0.05),且研究组LVESD、LVEDD均显著小于对照组(P<0.05)。
结论:醛固酮拮抗剂螺内酯能够有效治疗心力衰竭,恢复心脏功能,值得在临床上推广。
心力衰竭(heart failure)简称心衰,是指由于心脏的收缩功能或者舒张功能发生障碍,导致回流入心脏的静脉血不能充分泵出,心房所受压力增大,进而会引起静脉血管发生淤积,会导致心脏循环障碍症候群,主要临床表现为肺淤血以及腔静脉淤血[1-2]。