分子原子离子元素化学式物质构成
- 格式:pdf
- 大小:423.76 KB
- 文档页数:13

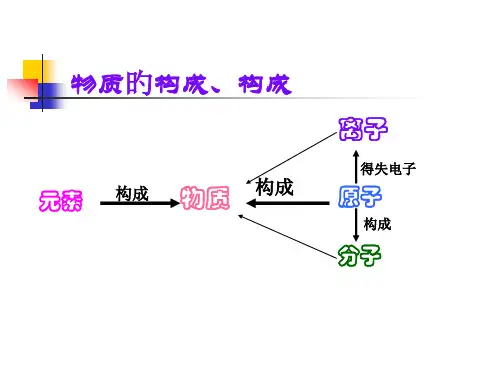
物质由分子.原子.离子组成.分子由原子核.核外电子组成.原子核由质子中子组成.离子表示得到或失去了电子的粒子(粒子表示原子.分子等).原子一般是金属和惰性气体.比如铜只有说铜原子.没有说铜分子的.分子由原子"构成"(只能说构成),原子由原子核(带正电)和核外电子(带负电)构成,原子核由质子(带正电)和中子(不带电)构成,物质由原子(金属和某些非金属)或分子(一般是气体)或离子构成物质中能够独立存在的相对稳定并保持该物质物理化学特性的最小单元。
分子由原子组成,原子通过一定的作用力,以一定的次序和排列方式结合成分子。
以水分子为例,将水不断分割下去,直至不破坏水的特性,这时出现的最小单元是由两个氢原子和一个氧原子组成的水分子。
它的化学式写作 H2O。
水分子可用电解法或其他方法再分为两个氢原子和一个氧原子,但这时它们的特性已和水完全不同了。
有的分子只由一个原子组成,称单原子分子,如氦和氩等分子属此类,这种单原子分子既是原子又是分子。
由两个原子组成的分子称双原子分子,例如氧分子(O2),由两个氧原子组成,为同核双原子分子;一氧化碳分子(CO),由一个氧原子和一个碳原子组成,为异核双原子分子。
由两个以上的原子组成的分子统称多原子分子。
分子中的原子数可为几个、十几个、几十个乃至成千上万个。
例如二氧化碳分子(CO2)由一个碳原子和两个氧原子组成。
一个苯分子包含六个碳原子和六个氢原子(C6H6),一个猪胰岛素分子包含几百个原子,其分子式为C255H380O78N65S6。
物质中能独立存在并保持其组成和一切化学特性的最小微粒。
分子是由原子用化学键结合在一起而构成的,原子之间的作用力比较强,但分子之间的作用力却相当弱,这种力称为范德华力,所以分子在一定程度上表现出独立粒子的行为。
分子可以由同种原子组成,也可以由不同种类的原子组成。
最简单的分子只含有一个原子,如稀有气体的分子。
大多数非金属构成的分子为双原子分子,如氮、氧等分子。

中考化学复习之原子分子离子构成的物质有的物质是由原子构成总结:金属(Fe、Cu、Ag)、大多数固态非金属单质(C、S、P)、稀有气体(He、Ne、Ar)等由原子构成。
例如很多看不见的微观的铁原子构成了铁这种可以看得见的物质、很多看不见的微观的碳原子构成了碳这种可以看得见的物质,即黑色粉末,再者,很多看不到的微观的汞原子构成了液态的汞这种物质。
有的物质是由分子构成首先要了解,分子是由原子构成的。
比如一个氢气分子(H2)是由2个氢原子构成的,一个氧气分子(O2)是由2个氧原子构成的,一个二氧化碳分子(CO2)是由1个碳原子和2个氧原子构成的,一个水分子(H2O)是由2个氢原子和1个氧原子构成。
很多的水分子构成了流动的水这种物质,即水由水分子构成。
很多的二氧化碳分子构成了二氧化碳这种无色无味、产生温室效应的气体,即二氧化碳由二氧化碳分子构成。
总结:由分子构成的物质包括:气态的非金属单质(O2、H2、N2、O3)和由非金属元素组成的化合物(H2O、NH3、CO2、SO2、NO2、H2SO4等)。
有的物质是由离子构成元素的化学性质由最外层电子数决定,当最外层电子数小于4时,易失电子。
如钠最外层电子数为1,失去最外层1个电子形成Na+。
当最外层电子数大于等于4时,易得电子。
如氯最外层电子数为7,最外层得到1个电子形成Cl-。
于是Na+和Cl-友好地通过静电作用结合在一起形成氯化钠。
所以氯化钠由Na+和Cl-构成。
总结:由离子构成的物质包括:一般是含有金属元素和非金属元素的化合物(氯化钠、氧化铜、氧化铁、硫酸钠、氢氧化钠、硝酸铜、碳酸钙等),或NH4+和酸根离子形成的化合物(如NH4Cl、NH4NO3)。


分子、原子、离子区别分子是由原子构成的微观原子是原子核和核外电子构成的. 微观离子是带电的原子,是原子得或者失去核外电子时形成的.离子是带电的原子或原子团。
微观一、、原子指化学反应中的最小微粒;元素指拥有相同核电荷数的一类原子的总称;分子是保持物体化学性质的最小微粒;质子是带电的原子二、原子:1、原子内通常存在质子、中子、电子。
其数量级大约是10^-10m。
因此,与常见物体相比,原子是一个极小的物体,即使把一亿个氧原子排成一排,其长度仍不足1cm,人们只能通过一些特殊的仪器才能间接观测到单个的原子。
2、原子内中子和质子的质量相近且远大于电子,原子核由质子与中子组成,因此原子的质量极小,且99.9%集中在原子核。
3、原子核外分布着电子,电子占据一组稳定的轨道。
当它们吸收和放出光子的时候,电子也可以在不同能级之间跃迁,此时吸收或放出光子的能量与轨道之间的能量差相等。
电子决定了一个元素的化学性质,并且对原子的磁性有着很大的影响。
三、离子:1、离子是指原子由于自身或外界的作用而失去或得到一个或几个电子使其达到最外层电子数为8个或2个(氦原子)或没有电子(四中子)的稳定结构。
这一过程称为电离。
电离过程所需或放出的能量称为电离能。
2、在化学反应中,金属元素原子失去最外层电子,非金属原子得到电子,从而使参加反应的原子或原子团带上电荷。
带电荷的原子叫做离子,带正电荷的原子叫做阳离子,带负电荷的原子叫做阴离子。
阴、阳离子由于静电作用而形成不带电性的化合物。
四、元素:元素(element)又称化学元素,指自然界中一百多种基本的金属和非金属物质,它们只由几种有共同特点的原子组成,其原子中的每一核子具有同样数量的质子,用一般的化学方法不能使之变得更为简单,并且单独地或组合地构成一切物质。
一些常见元素的例子有氢,氮和碳。
到2007年为止,总共有118种元素被发现,其中94种是存在于地球上。
拥有原子序数大于82(即铋Bi及之后的元素)都是不稳定,并会进行放射衰变。

初中化学判断物质是由原子分子离子构成Hessen was revised in January 2021如何判断物质是由原子、分子还是离子构成的一、先说,物质是由原子直接构成的,还是分子构成的,或者是离子构成的(下面没有注明的,默认为只考虑初中阶段的学习)。
(1)原子直接构成的物质:内部是由连接构成的一个巨大的整体,没有很小的重复单元(可以认为单一的一个原子是最小重复单元)。
常见的由原子直接构成的物质有:金属,,某些固态非金属如C,Si ,以后判断一种物质是不是由原子直接构成,最直观的办法是看能不能用中的单个直接表示该种物质,能直接用表示的就是原子直接构成的,反之,则不是。
就是说原子直接构成的物质一定是单质,并且化学式没有下标数字,只有。
(这里要提到P和S,这两种不是原子直接构成的,因为它们都是有最很小重复单元的,P真正的化学式是P4,P4是P的最小重复单元,就是说P单质是由无数个P4分子构成的饿,所以P是分子构成的。
初中简写了,还有S真正的化学式是S2,S4,S8,等)(只限初中,到高中有SiO2,它虽不是单质,并且有数字下标,但它还是原子直接构成的,与它内部结构有关,SIO2的结构是SI和O原子交替以共价单键连接并向空中无限制发展的网状结构,不存在分子,没有最小重复单元。
在这里就不解释了,高中会学)(2)分子构成的物质:内部有最小的重复单元,最小重复单元是分子,物质是由无数个这些相同的最小重复单元通过构成的,这中分子间力很小,就是说由分子构成的物质并不是一个很牢固的整体。
(3)由离子构成的物质:内部没有重复的最小单元,本身是通过连接成的一个整体,但是我们为了研究它的结构,往往会人为的划定出它的最小重复单元,就是。
要注意的是它每个最小的重复单元内部是由连接的,和的区别开,这就是为什么界定它是由离子都成的原因。
在初中很难把它和分子构成的物质区别开,其实有一个很直观的判断方法,有或的化合物就是离子构成的,没有这两种东西的物质就是分子构成的。

物质的微观组成—原子、分子、离子一、物质的微观组成1.宏观上物质是由元素组成的,微观上物质是由分子、原子或离子构成的。
2.元素:具有相同核电荷数(即质子数)的一类原子的总称。
地壳中含量前四位的元素是氧、硅、铝、铁。
3.元素符号的意义:表示_______________该元素,表示_____该元素的一个原子____________。
要求:能默写出原子序数1~20的元素符号及其名称。
二、原子1.原子结构:原子由___________(带正电)和_____________(带负电)组成。
2.原子结构示意图:3.原子的质量集中在__________上,原子核由_________(带正电)和__________(不带电)组成。
原子的质量数=_________+____________。
注:原子的质量数≠原子的相对原子质量。
4.原子的大小是纳米级(nm)的,原子核的大小占原子本身大小的_________之一(填“十分”、“百分”、“万分”或“亿万”)。
5.在原子中,质子数=__________=__________ =__________。
注意:(1)不是所有原子都有中子,如____________。
(2)原子是化学变化中最小的微粒。
原子在化学变化中不可再分,只是发生重新组合。
6.同位素:_________相同________不同的原子,如___________________________。
7.同位素原子的化学性质_________(填“相同”或“不同”),物理性质_________(填“相同”或“不同”)。
8.同素异形体:同种元素形成的不同___________。
如___________________________。
9.同素异形体的化学性质_________(填“相同”或“不同”),物理性质_________(填“相同”或“不同”)。
三、分子1.原子构成分子,分子聚集成为物质,如H2O分子由H、O原子构成,无数的H2O分子汇聚成了聚集态的水(H2O分子肉眼不可见,聚集态的水可见)。

初中化学重要知识:分子、原子、离子知识总结必考知识点一原子:化学变化中的最小微粒。
(1)原子也是构成物质的一种微粒。
例如少数非金属单质(金刚石、石墨等);金属单质(如铁、汞等);稀有气体等。
(2)原子也不断地运动着;原子虽很小但也有一定质量。
对于原子的认识远在公元前5世纪提出了有关“原子”的观念。
但没有科学实验作依据,直到19世纪初,化学家道尔顿根据实验事实和严格的逻辑推导,在1803年提出了科学的原子论。
分子:保持物质化学性质的最小粒子。
(1)构成物质的每一个分子与该物质的化学性质是一致的,分子只能保持物质的化学性质,不保持物质的物理性质。
因物质的物理性质,如颜色、状态等,都是宏观现象,是该物质的大量分子聚集后所表现的属性,并不是单个分子所能保持的。
(2)“最小”不是绝对意义上的最小,而是保持物质化学性质的最小。
分子的性质(1)分子质量和体积都很小。
(2)分子总是在不断运动着的。
温度升高,分子运动速度加快,如阳光下湿衣物干得快。
(3)分子之间有间隔。
一般说来,气体的分子之间间隔距离较大,液体和固体的分子之间的距离较小。
气体比液体和固体容易压缩,不同液体混合后的总体积小于二者的原体积之和,都说明分子之间有间隔。
(4)同种物质的分子性质相同,不同种物质的分子性质不同。
我们都有这样的生活体验:若口渴了,可以喝水解渴,同时吃几块冰块也可以解渴,这就说明:水和冰都具有相同的性质,因为水和冰都是由水分子构成的,同种物质的分子,性质是相同的。
必考知识点二质子:1个质子带1个单位正电荷原子核(+)。
中子:不带电原子不带电。
电子:1个电子带1个单位负电荷。
(1)构成原子的粒子有三种:质子、中子、电子。
但并不是所有的原子都是由这三种粒子构成的。
如有一种氢原子中只有质子和电子,没有中子。
(2)在原子中,原子核所带的正电荷数(核电荷数)就是质子所带的电荷数(中子不带电),而每个质子带1个单位正电荷,因此,核电荷数=质子数,由于原子核内质于数与核外电子数相等,所以在原子中核电荷数=质子数=核外电子数。

一、物质的组成:物质都是由元素组成的。
例:水由氢元素和氧元素组成
羟基磷酸钙Ca10(PO4)6(OH)2是由钙、磷、氧、氢四种元素组成的。
二、构成物质的微粒有三种:分子、原子和离子。
也就是说有的物质是由分子构成;有的物质是由原子构成;有的物质是由离子构成。
1由分子构成的物质一般有以下特点:
①元素符号右下角标有数字的;如O2O3C60
②不同的非金属元素符号写在一起的;如HCl、H2O P2O5H2SO4
③部分金属氧化物如氧化汞是由氧化汞分子构成的。
2由原子直接构成的物质:金属、稀有气体、金刚石、石墨等
3由离子直接构成的物质:碱、盐
一般来说金属与非金属相结合所形成的化合物;金属与原子团相结合所形成的化合物是离子化合物。
如氯化钠是由Na+、和Cl-构成的硫酸铜是由铜离子(Cu2+)和硫酸根离子(SO42-)构成的等。
三、分子都是由原子构成的。
可以有两种描述方法:以H2SO4为例:
法一:硫酸分子是由氢原子、硫原子和氧原子构成。
(都不
说数)
法二:一个硫酸分子是由2个氢原子、1个硫原子和4个氧原子构成。
(都说数)。

原子分子离子质子电子的区别原子由原子核和在原子核和带负电的电子组成。
(原子核一般由带正电荷的质子和不带电的中子构成。
)量子是一个比较宽泛的概念~应该是指量子力学中研究的各种粒子,包括质子,中子,电子……粒子也是比较宽泛的概~泛指各种微粒。
离子是带电微粒~因为量子,粒子范围太大,没法比较。
能确定大小的最小的是电子吧~1、分子是保持物质化学性质的最小粒子(原子、离子也能保持物质的化学性质)。
原子是化学变化中的最小粒子。
例如:保持氯气化学性质的最小粒子是D(氯分子)(A、Cl B、Cl- C、2Cl D、Cl2)。
保持CO2化学性质的最小粒子是CO2分子;保持水银的化学性质的最小粒子是汞原子。
在电解水这一变化中的最小粒子是氢原子和氧原子。
原子中:核电荷数(带正电)=质子数=核外电子数相对原子质量=质子数+中子数原子是由原子核和核外电子构成的,原子核是由质子和中子构成的,构成原子的三种粒子是:质子(正电)、中子(不带电)、电子(带负电)。
一切原子都有质子、中子和电子吗?(错!一般的氢原子无中子)。
某原子的相对原子质量=某原子的质量/C原子质量的1/12。
相对原子质量的单位是“1”,它是一个比值。
相对分子质量的单位是“1”。
由于原子核所带电量和核外电子的电量相等,电性相反,因此整个原子不显电性(即电中性)。
2、①由同种元素组成的纯净物叫单质(由一种元素组成的物质不一定是单质,也可能是混合物,但一定不可能是化合物。
)②由一种分子构成的物质一定是纯净物,纯净物不一定是由一种分子构成的。
③由不同种元素组成的纯净物一定是化合物;由不同种元素组成的物质不一定是化合物,但化合物一定是由不同种元素组成的。
纯净物与混合物的区别是物质的种类不同。
单质和化合物的区别是元素的种类不同。
④由两种元素组成的,其中一种是氧元素的化合物叫氧化物。
氧化物一定是含氧化合物,但含氧化合物不一定是氧化物。
⑤元素符号的意义:表示一种元素,表示这种元素的一个原子。

如何判断物质是由原子、分子还是离子构成的?一、先说,物质是由原子直接构成的,还是分子构成的,或者是离子构成的?(下面没有注明的,默认为只考虑初中阶段的学习)。
(1)原子直接构成的物质:内部是由化学键连接构成的一个巨大的整体,没有很小的重复单元(可以认为单一的一个原子是最小重复单元)。
常见的由原子直接构成的物质有:金属,稀有气体,某些固态非金属如C,Si ,以后判断一种物质是不是由原子直接构成,最直观的办法是看能不能用元素周期表中的单个元素符号直接表示该种物质,能直接用元素符号表示的就是原子直接构成的,反之,则不是。
就是说原子直接构成的物质一定是单质,并且化学式没有下标数字,只有元素符号。
(这里要提到P和S,这两种不是原子直接构成的,因为它们都是有最很小重复单元的,P真正的化学式是P4,P4是P的最小重复单元,就是说P单质是由无数个P4分子构成的饿,所以P是分子构成的。
初中简写了,还有S真正的化学式是S2,S4,S8,等)(只限初中,到高中有SiO2,它虽不是单质,并且有数字下标,但它还是原子直接构成的,与它内部结构有关,SIO2的结构是SI和O原子交替以共价单键连接并向空中无限制发展的网状结构,不存在分子,没有最小重复单元。
在这里就不解释了,高中会学)(2)分子构成的物质:内部有最小的重复单元,最小重复单元是分子,物质是由无数个这些相同的最小重复单元通过分子间作用力构成的,这中分子间力很小,就是说由分子构成的物质并不是一个很牢固的整体。
(3)由离子构成的物质:内部没有重复的最小单元,本身是通过离子键连接成的一个整体,但是我们为了研究它的结构,往往会人为的划定出它的最小重复单元,就是晶胞。
要注意的是它每个最小的重复单元内部是由离子键连接的,和分子晶体的共价键区别开,这就是为什么界定它是由离子都成的原因。
在初中很难把它和分子构成的物质区别开,其实有一个很直观的判断方法,有金属元素或铵根离子的化合物就是离子构成的,没有这两种东西的物质就是分子构成的。
知识点一原子:化学变化中的最小微粒。
(1)原子也是构成物质的一种微粒。
例如少数非金属单质(金刚石、石墨等)、金属单质(如铁、汞等)、稀有气体等。
(2)原子也不断地运动着;原子虽很小但也有一定质量。
对于原子的认识远在公元前5世纪提出了有关“原子”的观念。
但没有科学实验作依据,直到19世纪初,化学家道尔顿根据实验事实和严格的逻辑推导,在1803年提出了科学的原子论。
分子:保持物质化学性质的最小粒子。
(1)构成物质的每一个分子与该物质的化学性质是一致的,分子只能保持物质的化学性质,不保持物质的物理性质。
因物质的物理性质,如颜色、状态等,都是宏观现象,是该物质的大量分子聚集后所表现的属性,并不是单个分子所能保持的。
(2)“最小”不是绝对意义上的最小,而是保持物质化学性质的最小。
分子的性质(1)分子质量和体积都很小。
(2)分子总是在不断运动着的。
温度升高,分子运动速度加快,如阳光下湿衣物干得快。
(3)分子之间有间隔。
一般说来,气体的分子之间间隔距离较大,液体和固体的分子之间的距离较小。
气体比液体和固体容易压缩,不同液体混合后的总体积小于二者的原体积之和,都说明分子之间有间隔。
(4)同种物质的分子性质相同,不同种物质的分子性质不同。
我们都有这样的生活体验:若口渴了,可以喝水解渴,同时吃几块冰块也可以解渴,这就说明:水和冰都具有相同的性质,因为水和冰都是由水分子构成的,同种物质的分子,性质是相同的。
知识点二质子:1个质子带1个单位正电荷原子核(+)。
中子:不带电。
(原子不带电。
)电子:1个电子带1个单位负电荷。
(1)构成原子的粒子有三种:质子、中子、电子。
但并不是所有的原子都是由这三种粒子构成的。
如有一种氢原子中只有质子和电子,没有中子。
(2)在原子中,原子核所带的正电荷数(核电荷数)就是质子所带的电荷数(中子不带电),而每个质子带1个单位正电荷,因此,核电荷数=质子数,由于原子核内质于数与核外电子数相等,所以在原子中核电荷数=质子数=核外电子数。