2017,一轮化学平衡常数及计算
- 格式:ppt
- 大小:521.00 KB
- 文档页数:21


第25讲化学平衡常数及其计算【考纲要求】1.了解化学平衡常数(K)的含义,能利用化学平衡常数进行相关计算。
2.了解化学反应速率和化学平衡的调控在生活、生产和科学研究领域中的重要作用。
考点1 化学平衡常数及其应用[知识整合]1.化学平衡常数(1)概念:在一定温度下,当一个可逆反应达到时,生成物与反应物的比值是一个常数,用符号表示。
(2)表达式:对于反应m A(g)+n B(g)p C(g)+q D(g),K=c p(C)·c q(D)c m(A)·c n(B)。
(3)意义:化学平衡常数的大小反映了化学反应进行的程度。
K 正反应进行的程度平衡时生成物浓度平衡时反应物浓度反应物转化率越大越小一般地说,当K>105时,就认为反应基本进行完全了,当K<10-5时,认为反应很难进行。
2.平衡常数的影响因素对于确定的化学反应,平衡常数K只与有关,与浓度、压强无关。
(1)对于吸热反应,升高温度,K值。
(2)对于放热反应,升高温度,K值。
[应用体验]1.书写下列化学平衡的平衡常数表达式。
①Cl2+H2O HClO+Cl-+H+②C(s)+H2O(g)CO(g)+H2(g)③CH3COOH+C2H5OH CH3COOC2H5+H2O④CO2-3+H2O HCO-3+OH-⑤CaCO3(s)CaO(s)+CO2(g)⑥4NH3+5O24NO+6H2O(g)2.(1)对于N2(g)+3H2(g)2NH3(g)K1 2NH3(g)N2(g)+3H2(g)K2NH3(g)12N2(g)+32H2(g)K3则K1与K2的关系为________,K2与K3的关系为________,K3与K1的关系为________。
(2)已知A+B2C K1,C+D E K2,则A+B+2D2E的K3=________(用K1、K2表示)[多维探究]角度1化学平衡常数的含义及影响因素1.在某温度下,可逆反应m A+n B p C+q D的平衡常数为K,下列说法正确的是() A.K越大,达到平衡时,反应进行的程度越大B.K越小,达到平衡时,反应物的转化率越大C.K随反应物浓度的改变而改变D.K随温度和压强的改变而改变2.已知制备甲醇的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:①2H2(g)+CO(g)CH3OH(g),K1,2.5,0.15②H2(g)+CO2(g)H2O(g)+CO(g),K2,1.0,2.50③3H2(g)+CO2(g)CH3OH(g)+H2O(g),K3,(1)据反应①与②可推导出K1、K2与K3之间的关系,则K3=________(用K1、K2表示)。


化学平衡的相关计算化学平衡是指在化学反应中,反应物转化为产物的速度与产物转化为反应物的速度达到平衡的状态。
在化学平衡中,反应物和产物的浓度以及温度都是重要的因素,通过这些因素可以进行相关的计算。
本文将介绍化学平衡的相关计算方法。
一、化学平衡常数的计算方法化学平衡常数是描述化学平衡位置的物理量,用K表示。
对于一般的化学反应:aA+bB↔cC+dD反应物的浓度的分子数乘积除以产物的浓度的分子数乘积的比值,即可得到化学平衡常数K:K=([C]^c[D]^d)/([A]^a[B]^b)其中,[C]、[D]、[A]、[B]分别表示产物C、D和反应物A、B的浓度。
二、反应浓度的计算反应物和产物的浓度是进行化学平衡计算的重要因素。
根据反应物和产物的摩尔化学计量关系以及它们在平衡状态下的浓度,可以计算出平衡反应物和产物的浓度。
三、平衡常数的影响因素与计算1.温度:随着温度的升高,化学反应速率会增加,使得平衡位置发生变化。
根据反应热力学原理,可以利用反应焓变和温度的关系,计算出在不同温度下的平衡常数。
ΔG=ΔH-TΔS其中,ΔG表示反应的标准自由能变化,ΔH表示反应的标准焓变,T表示温度,ΔS表示反应的标准熵变。
2.压力:对于涉及气体的反应,可以通过改变压力来影响平衡位置。
根据Le Chatelier原理,当反应物和产物中有气体参与反应时,压力增大会使平衡位置向低压方向移动,反之亦然。
根据反应物和产物的分压与平衡常数的关系,可以计算出平衡常数与压力之间的关系。
3.浓度:根据浓度与平衡常数之间的关系,可以计算出化学平衡位置与浓度之间的关系。
当反应物或产物的浓度发生变化时,根据Le Chatelier原理,平衡位置会发生变化,使得浓度变化的方向尽量减小。
四、平衡计算实例以下为一个平衡计算的实例:反应为:2SO2(g)+O2(g)↔2SO3(g)假设在其中一温度下,反应物SO2和O2的初始浓度分别为0.2mol/L,产物SO3的初始浓度为0.1mol/L,求平衡浓度以及平衡常数。

高考化学一轮复习讲义—化学平衡常数的计算[复习目标]1.掌握平衡常数和平衡转化率计算的一般方法。
2.了解速率常数与化学平衡常数的关系并能进行有关计算。
考点一化学平衡常数与平衡转化率的计算1.常用的四个公式公式备注反应物的转化率n 转化n起始×100%=c 转化c起始×100%①平衡量可以是物质的量、气体的体积;②某组分的体积分数,也可以是物质的量分数生成物的产率实际产量理论产量×100%平衡时混合物组分的百分含量平衡量平衡时各物质的总量×100%某组分的体积分数某组分的物质的量混合气体总的物质的量×100%2.平衡常数的计算步骤(1)写出有关可逆反应的化学方程式,写出平衡常数表达式。
(2)利用“三段式”(见化学反应速率及影响因素),确定各物质的起始浓度、转化浓度、平衡浓度。
(3)将平衡浓度代入平衡常数表达式。
(4)注意单位的统一。
3.压强平衡常数(1)以a A(g)+b B(g)c C(g)+d D(g)为例,K p =p c C ·p d D p a A ·p b B[p (X):X 在平衡体系中物质的量分数(或体积分数)×总压强]。
(2)计算方法①根据“三段式”法计算平衡体系中各物质的物质的量或物质的量浓度。
②计算各气体组分的物质的量分数或体积分数。
③根据分压计算公式求出各气体物质的分压,某气体的分压=气体总压强×该气体的体积分数(或物质的量分数)。
④根据平衡常数计算公式代入计算。
例一定温度和催化剂条件下,将1mol N 2和3mol H 2充入压强为p 0的恒压容器中,测得平衡时N 2的转化率为50%,计算该温度下的压强平衡常数(K p )。
答案163p 20解析N 2(g)+3H 2(g)2NH 3(g)起始/mol 130变化/mol 0.5 1.51平衡/mol0.51.51平衡时p (N 2)=0.53p 0、p (H 2)=1.53p 0、p (NH 3)=13p 0。

高中化学一轮复习有关化学平衡常数的计算夯实基础知识1.一个模式——“三段式”如m A(g)+n B(g)p C(g)+q D(g),令A 、B 肇始物质的量浓度分别为a mol·L -1、b mol·L -1,抵达均衡后消耗A 的物质的量浓度为mx mol·L -1。
m A(g)+n B(g)p C(g)+q D(g) c 始/mol·L -1 a b 0 0c 转/mol·L -1 mx nx px qxc 平/mol·L -1 a -mx b -nx px qxK =(px )p ·(qx )q(a -mx )m ·(b -nx )n。
2.明确三个量的干系(1)三个量:即肇始量、变化量、均衡量。
(2)干系①敷衍联合反响物,肇始量-变化量=均衡量。
②敷衍联合生成物,肇始量+变化量=均衡量。
③各转化量之比即是各反响物的化学计量数之比。
3.掌握四个公式(1)反响物的转化率=n (转化)n (肇始)×100%=c (转化)c (肇始)×100%。
(2)生成物的产率:实际产量(指生成物)占理论产量的百分数。
一般来讲,转化率越大,原料利用率越高,产率越大。
产率=实际产量理论产量×100%。
(3)均衡时混合物组分的百分含量=均衡量均衡时各物质的总量×100%。
(4)某组分的体积分数=某组分的物质的量混合气体总的物质的量×100%。
深度思考将固体NH4I置于密闭容器中,在一定温度下产生下列反响:①NH4I(s)NH3(g)+HI(g),②2HI(g)H2(g)+I2(g)。
抵达均衡时:c(H2)=0.5 mol·L-1,c(HI)=4 mol·L-1,则此温度下反响①的均衡常数为___________________________________________________________。

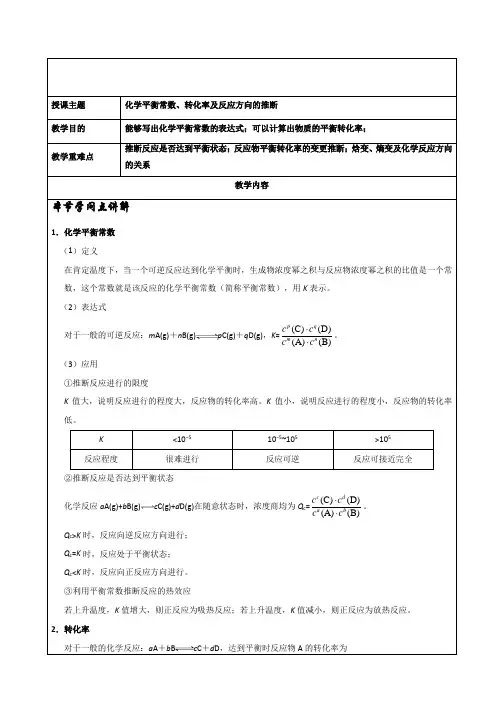
授课主题化学平衡常数、转化率及反应方向的推断教学目的能够写出化学平衡常数的表达式;可以计算出物质的平衡转化率;教学重难点推断反应是否达到平衡状态;反应物平衡转化率的变更推断;焓变、熵变及化学反应方向的关系教学内容本节学问点讲解1.化学平衡常数(1)定义在肯定温度下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与反应物浓度幂之积的比值是一个常数,这个常数就是该反应的化学平衡常数(简称平衡常数),用K表示。
(2)表达式对于一般的可逆反应:m A(g)+n B(g)p C(g)+q D(g),K=(C)(D) (A)(B)p qm nc cc c⋅⋅。
(3)应用①推断反应进行的限度K值大,说明反应进行的程度大,反应物的转化率高。
K值小,说明反应进行的程度小,反应物的转化率低。
K <10−510−5~105>105反应程度很难进行反应可逆反应可接近完全②推断反应是否达到平衡状态化学反应a A(g)+b B(g)c C(g)+d D(g)在随意状态时,浓度商均为Q c=(C)(D) (A)(B)c da bc cc c⋅⋅。
Q c>K时,反应向逆反应方向进行;Q c=K时,反应处于平衡状态;Q c<K时,反应向正反应方向进行。
③利用平衡常数推断反应的热效应若上升温度,K值增大,则正反应为吸热反应;若上升温度,K值减小,则正反应为放热反应。
2.转化率对于一般的化学反应:a A+b B c C+d D,达到平衡时反应物A的转化率为α(A)=A AA的初始浓度-的平衡浓度的初始浓度×100%=0(A)(A)(A)c cc×100%[c0(A)为起始时A的浓度,c(A)为平衡时A的浓度]反应物平衡转化率的变更推断推断反应物转化率的变更时,不要把平衡正向移动与反应物转化率提高等同起来,要视详细状况而定。
常见有以下几种情形:反应类型条件的变更反应物转化率的变更有多种反应物的可逆反应m A(g)+n B(g)p C(g)+q D(g) 恒容时只增加反应物A的用量反应物A的转化率减小,反应物B的转化率增大同等倍数地增大(或减小)反应物A、B的量恒温恒压条件下反应物转化率不变恒温恒容条件下m+n>p+q反应物A和B的转化率均增大m+n<p+q反应物A和B的转化率均减小m+n=p+q反应物A和B的转化率均不变只有一种反应物的可逆反应m A(g)n B(g)+p C(g) 增加反应物A的用量恒温恒压条件下反应物转化率不变恒温恒容条件下m>n+p反应物A的转化率增大m<n+p反应物A的转化率减小m=n+p反应物A和B的转化率不变3.化学反应进行的方向一、自发过程1.含义在肯定条件下,不须要借助外力作用就能自动进行的过程。


化学反应的平衡常数与浓度化学反应平衡常数是描述化学反应体系平衡状况的一个重要指标,它与反应物和生成物的浓度之间存在着密切的关系。
本文将探讨化学反应的平衡常数与浓度的关系,并解释浓度对平衡常数的影响。
一、化学反应平衡常数的定义与计算化学反应平衡常数(记为 K)是指在一定温度下,在平衡状态下,反应物浓度与生成物浓度之比的一个恒定值。
对于一般的化学反应:aA + bB ↔ cC + dD其平衡常数表达式为:K = [C]^c[D]^d / [A]^a[B]^b其中,方括号表示物质的浓度,上标表示该物质的组成物的个数。
通过浓度的计量单位,可以获得平衡常数的数值。
并且在一定温度下,平衡常数是固定不变的。
二、浓度对平衡常数的影响浓度是化学反应平衡常数的一个重要影响因素。
一方面,反应物浓度的增加会导致平衡常数的改变,另一方面,生成物浓度的变化也会引起平衡常数的变化。
下面将分别对这两种情况进行讨论。
1. 反应物浓度的影响当反应物初始浓度增加时,反应向生成物的方向进行。
这是因为增加反应物浓度会提高反应物浓度的分子碰撞频率,增大反应速率。
为了消除这种失衡,反应会向生成物的方向移动,此时平衡常数(K)增大。
2. 生成物浓度的影响当生成物初始浓度增加时,反应向反应物的方向进行。
这是因为增加生成物浓度会减少生成物浓度的分子碰撞频率,降低反应速率。
为了恢复平衡,反应会向反应物的方向移动,此时平衡常数(K)减小。
三、浓度与平衡常数的定量关系浓度与平衡常数之间存在着一定的定量关系。
根据化学反应平衡常数的定义可以推导出如下关系:K = (C/C_0)^c(D/D_0)^d / (A/A_0)^a(B/B_0)^b其中,C_0、D_0、A_0、B_0表示反应物及生成物的初始浓度,C、D、A、B表示反应物及生成物的平衡浓度。
以上公式说明了在已知反应物和生成物初始浓度的情况下,通过平衡时物质浓度的变化情况,可以计算出平衡常数的值。
这种关系为我们理解化学反应平衡过程中浓度的变化提供了有益的线索,对分析化学反应的平衡状态具有重要意义。

一、速率方程平均速率:瞬时速率:对于无固体和纯液体参加的反应:aA+bB=cC+dDK:速率常数,受温度影响。
阿伦尼乌斯方程阿伦尼乌斯方程推论:1.活化能Ea 、A、R为常数,T增大,k变大,反应变快。
2.温度一定A相近,Ea与k成反比,即活化能越大反应越慢3.不同反应温度对速率影响程度不同,由于lnk与1/T呈直线关系斜率为-Ea/R,则在温度变化相同时,Ea越大的反应k的变化越大。
m和n为各反应物反应级数由实验测得,反应级数不同对应速率方程中速率常数单位不同。
反应级数可以为整数,分数,0,或负数。
级数为0的物质的浓度对反应速率无影响,级数为负数说明该物质对反应起阻滞作用。
基元反应:人们将能够再一次化学行为中完成的反应(一次碰撞就完成)称为基元反应。
如:C2H5Cl→C2H4+HClNO2+CO→NO+CO2非基元反应也称为总和反应:当总和反应只包含一个基元反应时,为简单反应。
不止一个基元反应的称为复杂反应,一个复杂反应要经过若干个基元反应才能完成。
例如:2NO+2H2=N2+2H2O2NO+H2=N2+H2O2 (慢)H2O2+H2=2H2O (快)两个步骤完成,而总反应速率由较慢的一个过程决定注意:总速率方程不等同于慢反应的速率方程,两式中K值不同。
速率方程表达式有一化学反应aA +bB=C ,根据影响化学反应速率的因素可得v (C )=kc m (A)c n (B)。
其中k 是与温度有关的常数,为测k 、m 、n 的值,在298 K 时,将A 、B 溶液按不同的浓度混合,得到下列实验数据:(1)根据上表可求得:m =_______,n =______,k =________。
(2) 当c(A)=c(B)=2.0mol/L 时,用B 表示的初始反应速率为___________________。
答案:(1)1 2 1.2×10-2L 2mol -2s -2 (2) 0.144molL -1s -11.【2017江苏卷】温度为T 1时,在三个容积均为1 L 的恒容密闭容器中仅发生反应:2NO 2(g)2NO(g)+O 2 (g) (正反应吸热)。
考纲要求 1.了解化学平衡常数(K )的含义。
2.能利用化学平衡常数进行相关计算。
考点一 化学平衡常数1.概念在一定温度下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与反应物浓度幂之积的比值是一个常数,用符号K 表示。
2.表达式对于反应m A(g)+n B(g)p C(g)+q D(g),K =c p ?C ?·c q ?D ?c m ?A ?·c n ?B ?(固体和纯液体的浓度视为常数,通常不计入平衡常数表达式中)。
3.意义及影响因素(1)K 值越大,反应物的转化率越大,正反应进行的程度越大。
(2)K 只受温度影响,与反应物或生成物的浓度变化无关。
(3)化学平衡常数是指某一具体反应的平衡常数。
4.应用(1)判断可逆反应进行的程度。
(2)利用化学平衡常数,判断反应是否达到平衡或向何方向进行。
对于化学反应a A(g)+b B(g)c C(g)+d D(g)的任意状态,浓度商:Q c =c c ?C ?·c d ?D ?c a ?A ?·c b ?B ?。
Q <K ,反应向正反应方向进行; Q =K ,反应处于平衡状态; Q >K ,反应向逆反应方向进行。
(3)利用K 可判断反应的热效应:若升高温度,K 值增大,则正反应为吸热反应;若升高温度,K 值减小,则正反应为放热反应。
深度思考1.正误判断,正确的打“√”,错误的打“×” (1)平衡常数表达式中,可以是物质的任一浓度( ) (2)催化剂能改变化学反应速率,也能改变平衡常数( ) (3)平衡常数发生变化,化学平衡不一定发生移动( ) (4)化学平衡发生移动,平衡常数不一定发生变化( ) (5)平衡常数和转化率都能体现可逆反应进行的程度( )(6)化学平衡常数只受温度的影响,温度升高,化学平衡常数的变化取决于该反应的反应热()2.书写下列化学平衡的平衡常数表达式。
(1)Cl2+H2O HCl+HClO(2)C(s)+H2O(g)CO(g)+H2(g)(3)CH3COOH+C2H5OH CH3COOC2H5+H2O(4)CO2-3+H2O HCO-3+OH-(5)CaCO3(s)CaO(s)+CO2(g)3.一定温度下,分析下列三个反应的平衡常数的关系①N2(g)+3H2(g)2NH3(g)K1②12N2(g)+32H2(g)NH3(g)K2③2NH3(g)N2(g)+3H2(g)K3(1)K1和K2,K1=K22。