燃料电池分类及简述
- 格式:pdf
- 大小:533.80 KB
- 文档页数:11

燃料电池分类
燃料电池技术是一种运用自然能量将化学能转化为电能的新型可再生能源技术。
它是由多层构成的,分为燃料电池堆、燃料及电催化剂三大部分,可将燃料激发出电子并放出氧气,从而产生电能。
燃料电池可以分为多种类型,其中最常见的有燃料电池堆,它由阳极、阴极和
电解质组成,主要是电极反应转化化学能为电能,常用的燃料物质有高可挥发性燃料,如氢气、乙醇、甲醇、醇酸和乙撑胺等。
另外还有一些现成的燃料电池,由一个固定的燃料电池堆和一个燃料源所组成,燃料源有碳素,如煤、汽油、柴油、石油焦和天然气等。
另外,还有高效率燃料电池,它们可将氢气或碳氢气用加热或催化使用,化学
反应产生水蒸气,可给燃料电池提供电能,其高效率非常适合用于工程机械、轨道交通电气车辆和家用器具等。
而燃料电池堆是燃料电池系统中的基本组成部分,由催化剂、材料和化学反应剂组成,是将太阳能转化为电能的关键环节。
总之,燃料电池技术能有效的利用可再生的自然能源,助力可持续发展,是人
们推进清洁能源进步的有效手段。
各种不同类型的燃料电池都有其相应的特点,用以给人们的生活和社会发展增添活力,今后,燃料电池技术可期待更多的应用面。

燃料电池分类及其工作原理《燃料电池分类及其工作原理》燃料电池(Fuel Cell)是一种新型的能源转换装置,通过将燃料与氧气的化学反应转化为电能,实现能源的高效利用。
燃料电池被广泛运用于交通工具、移动电源、以及工业生产中等各个领域。
本文将介绍燃料电池的分类及其工作原理。
燃料电池可以根据其工作温度和所采用的电解质种类进行分类。
按照工作温度分,燃料电池主要分为低温燃料电池和高温燃料电池两大类。
低温燃料电池是在100°C以下工作温度下运行的,常见的低温燃料电池有质子交换膜燃料电池(Proton Exchange Membrane Fuel Cell,PEMFC)和直接甲醇燃料电池(Direct Methanol Fuel Cell,DMFC)。
高温燃料电池则是在800°C以上工作温度下运行的,其中最常见的是磷酸燃料电池(Phosphoric Acid Fuel Cell,PAFC)和碳酸盐燃料电池(Carbonate Fuel Cell,MCFC)。
质子交换膜燃料电池是一种基于质子导电机制工作的燃料电池。
它由质子交换膜、阳极、阴极和电子导电材料等组成。
当燃料流经阳极时,发生氧化反应,产生质子和电子。
质子通过质子交换膜传输到阴极一侧,而电子则通过外部电路传输,形成电流。
在阴极侧,氧气和质子发生还原反应,生成水和热。
这些反应产生的电能可以用于驱动电动车或供电其他设备。
直接甲醇燃料电池是一种将甲醇直接转化为电能的燃料电池。
它与质子交换膜燃料电池类似,但在阳极上加入了甲醇转化催化剂。
甲醇在阳极上被氧化成二氧化碳和水,并释放出质子和电子。
质子穿过质子交换膜到达阴极一侧,电子则通过外部电路传输,产生电流。
在阴极侧进行还原反应,生成水和热。
直接甲醇燃料电池可直接使用液态甲醇作为燃料,具有简单、方便的优势。
磷酸燃料电池是高温燃料电池的一种,它采用磷酸作为电解质。
它由贵金属催化剂的阳极和阴极,以及磷酸电解质组成。
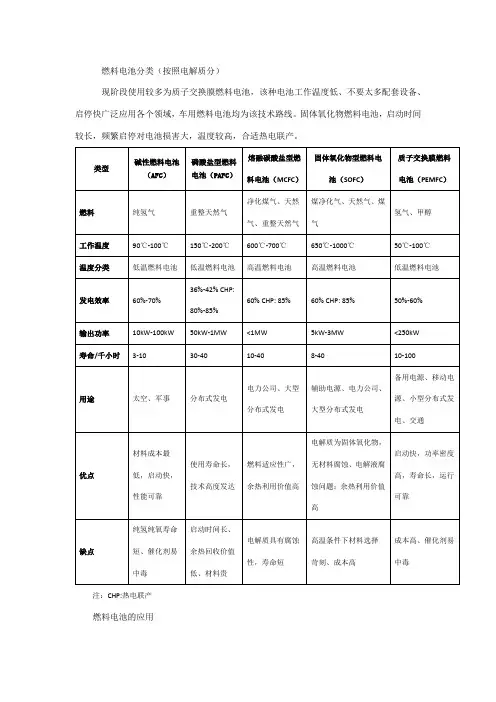


氢燃料电池的分类及特点
氢燃料电池是一种利用氢气作为燃料来产生电能的装置。
根据不同的电解质、反应物和反应方式的不同,氢燃料电池可以分为多种类型。
以下是一些常见的氢燃料电池类型及其特点:
1. PEMFC(质子交换膜燃料电池):使用薄膜作为电解质,电解质中的质子(H+)与氢气在阳极处反应,经过电解质膜运动到阴极处,与氧气反应,产生水和电能。
这种电池具有高效率、快速启动、可控性好等优点。
2. SOFC(固体氧化物燃料电池):使用固体氧化物作为电解质,需要高温(800-1000℃)下运行。
它能够利用各种燃料,包括氢气、天然气、煤气等,在氧化物阳极处产生电子和氧离子,氧离子经过电解质膜运动到阴极处,与燃料反应产生水和电能。
它具有高效率、长寿命、低排放等优点。
3. AFC(碱性燃料电池):使用碱性电解液作为电解质,需要高纯度氢气供应。
它的反应速度快,低温下运行,但稳定性较差,容易受到污染物的影响。
4. DMFC(直接甲醇燃料电池):使用甲醇水溶液直接作为燃料,无需氢气和外部燃料处理系统。
它具有简单、轻便、易于携带等优点,但需要高浓度甲醇才能达到较高效率。
总的来说,氢燃料电池具有高效、环保、零排放等优点,但目前其在成本、供氢等方面还存在一些挑战,需要进一步发展。

燃料电池的分类与应用前景探析燃料电池(Fuel Cell)是一种将化学能转化为电能的新型能源转换技术,其原理是利用氢气和氧气在阳极和阴极之间的化学反应产生电能,同时还会释放出水和阴离子。
燃料电池的应用日益广泛,比如用于汽车、船舶、航空等交通工具的动力系统、家庭和商业用电等。
本文将探索燃料电池的分类和应用前景,并分析其优缺点、未来发展方向等问题。
一、燃料电池的分类按照不同的工作原理,燃料电池可以被分为不同的类型,包括质子交换膜燃料电池(PEMFC)、碱性燃料电池(AFC)、固体氧化物燃料电池(SOFC)等。
其中,PEMFC和SOFC是应用最广泛的两种类型。
质子交换膜燃料电池(PEMFC)是基于质子交换膜技术的一种燃料电池,其工作原理是通过水解反应将储存的氢气分解成质子和电子,然后在PEMFC中将质子和电子重新结合产生水和电能。
PEMFC具有体积小、重量轻、输出功率高、启动快速等优点,适用于车辆和便携设备等领域。
固体氧化物燃料电池(SOFC)是一种基于氧离子导体的高温燃料电池,其工作原理是将氢气和氧气在高温条件下反应产生电能和水,其输出电压高、效率高,适用于大型发电设备、军事应用等高能耗场合。
除此之外,还有直接甲醇燃料电池(DMFC)和间接甲醇燃料电池(IMFC)等其他类型的燃料电池。
不同类型的燃料电池因其工作原理和特点不同,在不同领域具有不同的应用优势。
二、燃料电池的应用前景燃料电池具有高效、环保、灵活等优点,其应用前景广泛,涉及包括能源、交通、环保等多个领域。
1. 汽车行业燃料电池汽车是燃料电池应用最具代表性的领域之一。
与传统内燃机车相比,燃料电池汽车具有零排放、高效、安静等优点。
目前已有多个汽车生产商推出了燃料电池汽车,如丰田、本田等。
2. 发电设备燃料电池发电设备也是应用广泛的燃料电池领域之一,其可以用于城市能源供应,为城市提供更加环保、高效、安全的电力。
另外,其也可以应用于军事设备、船舶、飞机等领域。


燃料电池种类、原理及研究进展一.燃料电池简介1.定义燃料电池(Fuel Cells)是一种不需要经过卡诺循环的电化学发电装置,能量转化率高。
燃料和空气分别送进燃料电池,电就被奇妙地生产出来。
它从外表上看有正负极和电解质等,像一个蓄电池,但实质上它不能“储电”而是一个“发电厂”。
由于在能量转换过程中,几乎不产生污染环境的含氮和硫氧化物,燃料电池还被认为是一种环境友好的能量转换装置。
由于具有这些优异性,燃料电池技术被认为是21世纪新型环保高效的发电技术之一。
随着研究不断地突破,燃料电池已经在发电站、微型电源等方面开始应用。
2.基本结构燃料电池的基本结构主要是由四部分组成,分别为阳极、阴极、电解质和外部电路。
通常阳极为氢电极,阴极为氧电极。
阳极和阴极上都需要含有一定量的电催化剂,用来加速电极上发生的电化学反应,两电极之间是电解质。
图1.燃料电池基本结构示意图3.分类目前燃料电池的种类很多,其分类方法也有很多种。
按不同方法大致分类如下:(1)按运行机理来分类:可分为酸性燃料电池和碱性燃料电池;(2)按电解质的种类来分类:有酸性、碱性、熔融盐类或固体电解质;图2.燃料电池分类详细介绍(3)按燃料的类型来分类:有直接式燃料电池和间接式燃料电池;(4)按燃料电池工作温度分:有低温型(低于200℃);中温型(200-750℃);高温型(高于750℃)。
4.原理燃料电池的工作原理相对简单,主要包括燃料氧化和氧气还原两个电极反应及离子传输过程。
早期的燃料电池结构相对简单,只需要传输离子的电解质和两个固态电极。
当以氢气为燃料,氧气为氧化剂时,燃料电池的阴阳极反应和总反应分别为:阳极:H2→2H++2e-阴极:1/2O2+2H++2e-→H2O总反应:H2+1/2O2→H2O其中,H2通过扩散达到阳极,在催化剂作用下被氧化成和e-,此后,H+通过电解液到达阴极,而电子则通过外电路带动负載做功后也到达阴极,从而与O2发生还原反应(ORR)。

燃料电池的工作原理和分类燃料电池(Fuel Cell,FC)是一种将氢气与氧气反应产生电能的化学电源,它通过将燃料(如氢气、甲醇、乙醇等)与氧气经过电化反应产生电能,是一种高效、清洁、无污染的能源转换技术。
燃料电池的工作原理是将氢气通过阳极从燃料电池进入电解质层,同时让氧气通过阴极接触电解质层,这样氢气经过堆中催化剂的作用与氧气氧化反应形成水,同时释放出电子,从而产生电能。
燃料电池的分类主要有以下几种:1、聚合物电解质膜燃料电池(PEMFC)聚合物电解质膜燃料电池是燃料电池中使用最广泛的一种类型,也是最具有商业化前景的燃料电池。
它采用一种聚合物电解质膜作为电解质,在膜中间为阳极和阴极分别分布两边,并在两面贴合有催化剂的电极,由于聚合物电解质膜可以通过水分子进行质子传输,所以也称为质子交换膜燃料电池。
PEMFC 的优点是启动快、反应迅速、效率高,具有能量密度高、容量大、重量轻等特点,可以在低温下运行,所以被广泛应用于汽车动力系统等领域。
2、固体氧化物燃料电池(SOFC)固体氧化物燃料电池是一种以固态材料作为电解质的燃料电池,其电解质层一般采用氧离子传递材料,电极上面涂有催化剂,将氢气从阳极侧注入,氧气从阴极侧流入,反应时释放出电子和氧离子。
SOFC 的优点是电池效率高、燃料适应性强、发电环境友好等。
缺点是启动时间较长,高温下稳定性难以保证,体积较大,制造成本高等。
3、碳酸盐燃料电池(MCFC)碳酸盐燃料电池是将燃料和氧气通过催化剂反应产生电能,并且在电解质层内引入一些碳酸盐,通过扭曲形成碱性环境来促进反应的进行,同时能够达到能量的高效利用。
DMFC 的优点是可以直接使用常温常压的甲醇溶液作为燃料,体积小,重量轻,但功率输出低,效率低。
缺点是甲醇的毒性大,制造成本高等。
总的来说,不同类型的燃料电池各有特点,在不同的应用领域可以灵活选择,燃料电池的应用前景十分广阔。


燃料电池常见分类方式
燃料电池常见分类方式
燃料电池是一种把化学能转换成电能的能源转换器。
特别是采用氢和氧的燃料
电池具有高效率,清洁和可持续的特点,受到了越来越多的关注和发展。
燃料电池可以分为三个类别,即电化学燃料电池,金属氧化物燃料电池和直接燃料电池。
第一类是电化学燃料电池,其基本原理是将化学能直接转换成电能。
它具有较
高的效率和可靠性,可以用于无污染发电。
典型的电化学燃料电池分为阴极反应型和阳极反应型,常见的有燃料电池、燃料堆和锂-空气电池。
第二类是金属氧化物燃料电池,它比电化学燃料电池技术更发达。
它通常由阳极,阴极和电解质构成,利用金属氧化物和氧气反应来发电。
它是一种低温(低温)电池,热释电性能好,但制作和维护成本较高,有一定的安全隐患。
典型的金属氧化物燃料电池包括燃料电池膜电池,空气电池,锂空气电池,铅-酸电池。
第三类是直接燃料电池,它可以自发的直接将固体燃料转变为电能。
它可以实
现高效的热解,没有污染,回收率高,抗腐蚀性能好。
任何一种以有机物为原料的直接燃料电池都有一定的安全性舆广泛使用,典型的直接燃料电池有木颗粒电池、生物柴油电池、气体燃料电池和甲醇燃料电池等。
综上所述,燃料电池可以从多个方面来分类,它们可以分为电化学燃料电池,
金属氧化物燃料电池和直接燃料电池三大类。
在实际的应用中,应根据实际的需要来选择正确的类型,以便更好地发挥燃料电池的优势。
燃料电池高一相关知识点燃料电池是一种能将氢气、天然气、甲醇等燃料与氧气反应产生电能的装置。
燃料电池具有高效、环保、静音等特点,被广泛应用于电动汽车、无人机和家用电力系统等领域。
在高中化学学科中,燃料电池也是一个重要的知识点。
本文将介绍燃料电池的原理、分类以及应用等相关知识。
一、燃料电池的原理燃料电池的基本原理是利用电化学反应转化化学能为电能。
其中最常见的燃料电池是氢气燃料电池,反应方程式如下:2H2 + O2 → 2H2O该反应产生的电子通过外部电路流动,从而产生电能。
同时,氢气和氧气在燃料电池中通过电解质层交流,氢气被氧化为氧化剂(如氧气中的O2-),氧气被还原为还原剂(如氢气中的H+)。
二、燃料电池的分类燃料电池可以根据不同的电解质材料、工作温度和燃料类型进行分类。
1.根据电解质材料的不同,燃料电池可以分为以下几类:(1)质子交换膜燃料电池(PEMFC):采用固体高分子质子交换膜作为电解质。
(2)碱性燃料电池(AFC):采用碱性电解质溶液作为电解质。
(3)磷酸燃料电池(PAFC):采用磷酸溶液作为电解质。
(4)固体氧化物燃料电池(SOFC):采用固体氧化物作为电解质。
2.根据工作温度的不同,燃料电池可以分为以下几类:(1)低温燃料电池(LTFC):工作温度在100℃以下。
(2)中温燃料电池(MTFC):工作温度在100℃-300℃之间。
(3)高温燃料电池(HTFC):工作温度在500℃以上。
3.根据燃料类型的不同,燃料电池可以分为以下几类:(1)氢气燃料电池(HFC):以氢气为燃料。
(2)甲醇燃料电池(MFC):以甲醇为燃料。
(3)乙醇燃料电池(EFC):以乙醇为燃料。
(4)天然气燃料电池(NGFC):以天然气为燃料。
三、燃料电池的应用目前,燃料电池在多个领域得到广泛应用。
1.交通工具:燃料电池被用于电动汽车以及无人机等交通工具中,取代传统的燃油发动机,以实现零排放和低噪音运行。
2.家用电力系统:燃料电池被应用于家庭能源系统中,可以为家庭供应电力和热能,提供清洁而稳定的能源。
燃料电池工作原理分类及组成燃料电池是一种利用化学能直接转化为电能的设备,其工作原理是将氢气和氧气在电化学反应过程中进行氧化还原反应,从而产生电流和水。
燃料电池通常由电极、电解质和催化剂组成。
根据电解质的不同,燃料电池可分为酸性燃料电池、碱性燃料电池、固体氧化物燃料电池等。
酸性燃料电池以氢气作为燃料,通过氢气在电解质中的氧化还原反应来产生电流。
常见的酸性燃料电池有质子交换膜燃料电池(PEMFC)和直接甲醇燃料电池(DMFC)。
质子交换膜燃料电池将质子(氢离子)通过质子交换膜传递,利用钯和白金等催化剂催化氢气和氧气的反应来产生电流,主要用于汽车和小型电子设备。
直接甲醇燃料电池将甲醇直接反应产生电流,由于甲醇的可液化性和储存性能较好,可以直接使用甲醇作为燃料,常用于小型便携式电子设备。
碱性燃料电池以氢气或氢氧化钠溶液作为燃料,通过氢气和氧气的氧化还原反应来产生电流。
碱性燃料电池广泛应用于航空航天领域和舰船动力系统中。
碱性燃料电池的主要特点是反应速度较快,能够在较低温度下工作,具有较高的电化学效率和较长的寿命。
固体氧化物燃料电池(SOFC)是一种高温燃料电池,以氢气、天然气或其他可燃气体作为燃料,并通过固体氧化物电解质传递氧分子来进行反应。
该类型的燃料电池工作温度高达800-1000摄氏度,具有较高的转化效率和多燃料适应性。
由于高温运行,SOFC需要较长的预热时间和多种复杂材料,因此用途受限,主要用于工业领域的发电和电力系统。
无论是哪一种类型的燃料电池,其组成主要包括两个电极和一个电解质。
电极分为阳极和阴极,阳极与燃料接触,阴极与氧气接触。
阳极上通常采用负载有催化剂的多孔材料,催化剂能够促进燃料的氧化反应。
阴极上也采用催化剂,通常是负载有白金等贵金属的碳载体。
电解质通常是一种特殊的膜或固体材料,用于阻止电子通过,只允许离子通过,实现阳离子和阴离子之间的传导。
电解质的选择和设计对于燃料电池性能至关重要。
除了以上组成部分,燃料电池还需要辅助部件,如电流收集器、冷却系统、气体输送系统等。
燃料电池常见的分类方式
燃料电池是一种低碳、高效的新能源,它们可以有效将化学能转化为电能,而
且还具有多重优势,受到了越来越多的关注。
根据燃料电池的不同原理和结构,可以将其分为几类。
首先,根据电池使用的
可燃物和可用氧化剂,可以分为有机燃料电池和非有机电池。
有机燃料电池通常使用石油或天然气作为燃料,搭配氧来产生电能;而非有机燃料电池则指一类通过使用金属(含水硫化物)作为燃料来产生电能的电池。
其次,根据反应的结构特征,可以分为液态燃料电池和固体燃料电池。
前者是将燃料和氧溶于液体中,再将其反应,而固态燃料电池则是使用固体燃料(如固体氧化物)形式来进行反应产生电能。
除此之外,还可以根据燃料电池的技术特点来分类,如根据电池的温度水平的
高低,可以分为高温燃料电池、中温燃料电池和低温燃料电池;根据燃料电池的功率密度可分为低功率燃料电池和高功率燃料电池等。
以上就是燃料电池常见的分类方式,每种分类方式都具有各自特点,使用者可
以根据实际情况使用不同燃料电池以获得最好的性能。
由于燃料电池具有低碳、经济、安全等多重优点,因此在资源利用,环保,节能和污染控制上有着重要的意义,受到了越来越多的关注。
各种燃料电池简述1.碱性燃料电池(AFC)AFC是以碱性溶液为电解质,将存在于燃料和氧化剂中的化学能直接转化为电能的发电装置,是最早获得应用的燃料电池,由于其电解质必须是碱性溶液,因此而得名碱性燃料电池。
氢氧化钠和氢氧化钾溶液,以其成本低,易溶解,腐蚀性低,而成为首选的电解液。
催化剂主要用贵金属铂、钯、金、银和过渡金属镍、钴、锰等。
在1973年成功地应用于Apollo登月飞船的主电源,使人们看到了燃料电池的诱人前景。
具有启动快、效率高、价格低廉的优点,有一定的发展潜力。
其反应式为:阳极:2H2+4OH-→2 H2O +4e-阴极: 2 H2O +O2→4OH-总反应:2H2+O2→2H2O这种电池常用35%-45%的KOH为电解液,渗透于多孔而惰性的基质隔膜材料中,工作温度小于100℃。
该种电池的优点是氧在碱液中的电化学反应速度比在酸性液中大,因此有较大的电流密度和输出功率,但氧化剂应为纯氧,电池中贵金属催化剂用量较大,而利用率不高。
目前,此类燃料电池技术的发展已非常成熟,并已经在航天飞行及潜艇中成功应用。
国内已研制出200W氨-空气的碱性燃料电池系统,制成了1kW、10kW、20kW的碱性燃料电池,20世纪90年代后期在跟踪开发中取得了非常有价值的成果。
发展碱性燃料电池的核心技术是要避免二氧化碳对碱性电解液成分的破坏,不论是空气中百万分之几的二氧化碳成分还是烃类的重整气使用时所含有的二氧化碳,都要进行去除处理,这无疑增加了系统的总体造价。
此外,电池进行电化学反应生成的水需及时排出,以维持水平衡。
因此,简化排水系统和控制系统也是碱性燃料电池发展中需要解决的核心技术。
2.磷酸型燃料电池(PAFC)PAFC自20世纪60年代在美国开始研究一来,由于操作温度低,耐CO中毒能力强等特点,得到了优先发展,是目前技术成熟、发展最快的燃料电池。
PAFC是一种以磷酸为电解质的燃料电池。
采用重整天然气作燃料,空气做氧化剂,浸有浓磷酸的SIC微孔膜做电解质,PT/C做催化剂,工作温度200℃,是目前单机发电量最大的一种燃料电池。
关键材料包括电极材料,电解质材料,膈膜材料和双极板材料。
结构图如下:PAFC的结构图反应式:阳极:2H2→4 H+ +4e-阴极:4H+ +O2+4e-→2H2O总反应:2H2+O2→2H2O这种电池突出优点是贵金属催化剂用量比碱性氢氧化物燃料电池大大减少,还原剂的纯度要求有较大降低,一氧化碳含量可允许达5%。
该类电池一般以有机碳氢化合物为燃料,正负电极用聚四氟乙烯制成的多孔电极,电极上涂Pt作催化剂,电解质为85%的H3PO4。
在100℃-200℃范围内性能稳定,导电性强。
磷酸电池较其他燃料电池制作成本低,接近供民用的程度。
但是其启动时间较长以及余热利用价值低等发展障碍导致其发展速度减缓目前,PAFC主要用于发电厂,其中分散性发电厂,容量在10-20MW之间,中心电站型发电厂,装机容量可达100MW以上,即使在发电负荷较低时,依然保持高的发电效率。
还可用于现场发电,就是把PAFC直接安装在用户附近,同时提供热和电。
这被认为是PAFC的最佳应用方案。
这种方案的优点是:可根据需要设置装机容量或调整发电负荷,却不会影响装置的发电效率,既使小容量PAFC装置也能达到相当于现代大型热电厂的效率;有效利用电和热,传输损失小。
国际上功率较大的实用燃料电池电力站均用这种燃料的电池。
美国将磷酸型燃料电池列为国家级重点科研项目进行研究开发,向全世界出售200kW级的磷酸型燃料电池,日本制造出了世界上最大的(11MW)磷酸型燃料电池。
到2002年初,美国已在全世界安装测试了200 kW级PAFC发电装置235套,累计发电470万小时,2001年卖出23套。
在美国和日本有几套装置已达到连续发电1万小时的设计目标;欧洲现有5套200kW级PAFC发电装置在运转;日本福日电器和三菱电器已经开发出500 kW级PAFC发电系统。
车用上可以以PAFC作为基本动力电源,配备蓄电池以满足车辆启动和爬坡是峰值用电要求;PAFC可以用作通讯、紧急供电、娱乐等的电源。
与通常的柴油发电系相比,PAFC作为军事上的而通讯电源,其诱人之处在于运行时噪音低和热辐射量极少,有利于隐蔽目标。
另外,许多石油化工厂,如炼油厂、氯碱厂、合成氨厂等,经常排放大量富氢气体。
在现场安装PAFC装置,就可以把排放气体中的氢转化为电能,或者从中分离出纯氢气体,从而减少资源浪费。
3.固体氧化物燃料电池(SOFC)SOFC的开发始于20世纪40年代,但是在80年代以后其研究才得到蓬勃发展。
早期开发出来的SOFC的工作温度较高,一般在800℃-1000℃。
科学家已经研发成功中温SOFC,其工作温度一般在750℃左右。
一些科学家也正在努力开发低温SOFC,其工作温度更可以降低至650℃-700℃。
工作温度的进一步降低,使得SOFC的实际应用成为可能。
电池中的电解质是复合氧化物,在高温(1000℃以下)时,有很强的离子导电功能。
它是由于钙、镱或钇等混入离子价态低于锆离子的价态,使有些氧负离子晶格位空出来而导电。
目前世界各国都在研制这类电池,并已有实质性的进展,但SOFC在高温下工作也给其带来一系列材料,密封和结构上的问题,如电极的烧结,电解质与电极之间的界面化学扩散以及热膨胀系数不同的材料之间的匹配和双极板材料的稳定性等。
这些也在一定程度上制约着SOFC的发展,成为其技术突破的关键方面。
SOFC的结构图和反应式如下:SOFC的原理图阳极:H2→2H++2e-阴极:2H++1/2O2+2e-→H2O总反应:H2+1/2O2→H2O目前国际上,从几十瓦的便携式电源系统到千瓦级的家庭热电联供系统,再到数百千瓦级的分布式电源系统,均已有了相对成熟的产品进入市场。
产品的功能性和适应性也越来越强,它们的发展已经进入了降低成本、提高产品功能以适应具体环境的新阶段。
有西门子-西屋公司的SOFC发电系统长期稳定的成功经验和目前包括Bloom Energy、HEXIS、Kyocera和CFCL等公司的大量SOFC电堆、系统的演示验证,SOFC 的技术可行性毋庸置疑。
现在SOFC发电系统已经入初步量产和成本降低的阶段,有理由相信距离走入千家万户已为时不远。
Bloom Energy SOFC系统安装与eBay数据中心西门子-西屋电力公司的220KW的SOFC/GT联合循环电站4. 熔融碳酸盐燃料电池(MCFC)熔融碳酸盐燃料电池(简称MCFC),是由多孔陶瓷阴极、多孔陶瓷电解质隔膜、多孔金属阳极、金属极板构成的燃料电池。
MCFC工作原理其电解质是熔融态碳酸盐,一般为碱金属Li、K、Na、Cs的碳酸盐混合物,隔膜材料是LiAiO2,正极和负极分别为添加锂的氧化镍和多孔镍。
反应式为:阳极:H2+CO2-3→H2O+CO2+2e-阴极:CO2+1/2 O2+2e-→CO2-3总反应:H2+1/2O2→H2O由上述反应可知,MCFC的导电离子为CO2-3,CO2在阴极为反应物,而在阳极为产物。
实际上电池工作过程中CO2在循环,即阳极产生的CO2返回到阴极,以确保电池连续地工作。
通常采用的方法是将阳极室排出来的尾气经燃烧消除其中的H2和CO,再分离除水,然后将CO2返回到阴极循环使用。
MCFC的优点在于工作温度较高(650-700℃),反应速度加快;对燃料的纯度要求相对较低,可以对燃料进行电池内重整;不需贵金属催化剂,成本较低;采用液体电解质,较易操作。
不足之处在于,高温条件下液体电解质的管理较困难,长期操作过程中,腐蚀和渗漏现象严重,降低了电池的寿命。
MCFC中阴极、阳极、电解质隔膜和双极板是基础研究的4大难点,这4大部件的集成和对电解质的管理是MCFC电池组及电站模块的安装和运转的技术核心。
目前,加压MCFC方面,美国FCE(Full Cell Energy,以前称ERC公司)和日本Melco公司领先;常压MCFC方面,则是美国MCP公司和日本IHI公司领先。
美国FCE公司从20世纪70年代开始研究MCFC,现已实现商业化,从2001年开始进人分布式发电电源市场。
其产品为250kW~3MW内部重整型电站。
电站模块目前销售价格为3500-4000美元/ kW。
日本日立公司2000年开发出1 MMCFC发电装置,三菱公司2000年开发出200kWMCFC发电装置,东芝开发出低成本的10kWMCFC发电装置。
日本“月光计划”从1981年开始研究MCFC,1984年研制成功1kW MCFC 电堆,1986年为10 kW,1991年为30 kW,1992年为50~1000 kW,1997年为01MW。
1987年日本成立MCFC协会。
日立、东芝、富士电机、三菱电机、IHI 分别对5台10 kW级电堆进行发电试验。
在德国,主要是由公司的子公司MTU进行MCFC的开发研究。
从降低费用角度出发,MTU从FCE公司购入了常压内重整型250kW MCFC电池组,在此基础上开放了0.8MPa加压MCFC。
荷兰在中断MCFC研究15年后,于1986年重新开始MCFC开发。
作为荷兰能源组织(NDNEM)和美国IGT合作项目的一部分,荷兰能源研究中心逐渐成为欧洲MCFC、SOFC和PEMFC系统的测试中心。
安装在日本的200 kW MCFC(主要用于工厂废水处理)自20世纪90年代以来,我国多家研究机构开展了MCFC研究工作,上海交通大学和中国科学院大连化学物理研究所都于2001年成功进行了1 kW熔融碳酸盐燃料电池组的发电试验。
目前,上海交通大学与上海汽轮机有限公司合作,已完成50kW MCFC发电外围系统的建设,10kW的MCFC电池组已经制作完成。
5.质子交换膜燃料电池(PEMFC)PEMFC的结构组成如图所示。
PEMFC由膜电极和带气体流动通道的双极板组成。
其核心部件膜电极是采用一片聚合物电解质膜和位于其两侧的两片电极热压而成,中间的固体电解质膜起到了离子传递和分割燃料和氧化剂的双重作用,而两侧的电极是燃料和氧化剂进行电化学反应的场所。
PEMFC结构图PEMFC的工作原理PEMFC通常以全氟磺酸型质子交换膜为电解质,Pt/C或PtRu/C为电催化剂,氢或净化重整气为燃料,空气和纯氧为氧化剂,带有气体流动通道的石墨或表面改性金属板为双极板。
PEMFC工作时,燃料气和氧化剂气体通过双极板上的导气通道分别到达电池的阳极和阴极,反应气体通过电极上的扩散层到达电极催化层的反应活性中心,氢气在阳极的催化剂作用下解离为氢离子(质子)和带负电的电子,氢离子以水合质子H+(nH2O,n约为3-5)的形式在质子交换膜中从一个磺酸基(-SO3H)迁移到另一个磺酸基,最后到达阴极,实现质子导电。