盐酸标准溶液的配制和标定
- 格式:docx
- 大小:32.56 KB
- 文档页数:7


盐酸标准溶液的配置与标定
1.配制
按规定量取盐酸,注入1000ml水中,摇均。
盐酸标准滴定液的浓度[ C(HCl)]1(mol/L)盐酸的体积 90 mL 盐酸标准滴定液的浓度[ C(HCl)]0.5(mol/L)盐酸的体积 45 mL 盐酸标准滴定液的浓度[C(HCl)]0.1(mol/L)盐酸的体积 9 mL 2. 标定
按表4的规定称取于270℃~300℃高温炉中灼烧至恒重的工作基准试剂无水碳酸钠,溶于50mL水中,加10滴溴甲酚绿-甲基红,用配好的盐酸溶液滴定至溶液由绿色变为暗红色,煮沸2分钟,冷却后继续滴定至溶液再呈暗红色。
同时做空白试验。
表 4
盐酸标准滴定液的浓度 C(NaOH) 1mol L工作基准试剂无水碳酸钠的质量1.9g
盐酸标准滴定液的浓度 C(NaOH) 0.5mol L工作基准试剂无水碳酸钠的质量0.95g
盐酸标准滴定液的浓度 C(NaOH) 0.1mol L工作基准试剂无水碳酸钠的质量0.2g
3.计算
盐酸标准滴定液的浓度[ C(HCl)],数值以摩尔每升(mol/L)表示,按式(2)计算:
C(HCl)=m/[v1-v2]*0.05299
式中:m-----无水碳酸钠的质量的准确数值,单位为克(g);
V1---盐酸溶液的体积的数值,单位是毫升(mL);
V2---空白试验盐酸溶液的体积的数值,单位是毫升(mL);。

盐酸标准溶液(0.1 mol·L-1)的配制与标定一、原理市售盐酸为无色透明的HCl水溶液,HCl含量为36%~38%(W/W)。
由于浓盐酸易挥发出HCl气体,若直接配制准确度差,因此配制盐酸标准溶液时需用间接配制法。
采用无水碳酸钠为基准物质标定盐酸,以甲基红-溴甲酚绿混合指示剂指示终点。
用Na2CO3标定时反应为:2HCl + Na2CO3→ 2NaCl + H2O + CO2执行标准:GB/T 601-2002 化学试剂标准滴定溶液的制备二、实验用品分析天平(感量0.1mg/分度),量筒,称量瓶,25mL酸式滴定管,250mL锥形瓶,工作基准试剂无水Na2CO3,浓HCl(浓或0.1mol/L),溴甲酚绿一甲基红指示液(变色点pH=5.1)。
三、实验步骤(1)0.1mol.L-1盐酸溶液的配制:用小量筒取浓盐酸9ml,注入1000 ml,摇匀。
(2) 盐酸标准滴定溶液的标定取在270~300℃干燥至恒重的基准无水碳酸钠约0.2g,精密称定3份,分别置于250ml锥形瓶中,加50ml蒸馏水溶解后,加甲基红-溴甲酚绿混合指示剂10滴,用盐酸溶液(0.1mol·L-1)滴定至溶液又由绿变暗红色,煮沸约2min。
冷却至室温,继续滴定至暗红色,记下所消耗的标准溶液的体积,同时做空白试验四、实验结果(1)数据记录(2)结果计算盐酸标准滴定溶液的浓度[c(HCl)].数值以摩尔每升(mol/L)表示,按下式计算:式中 : m — 无水碳酸钠的质量的准确数值,单位为克(g);V 1— 盐酸溶液的体积的数值,单位为毫升(mL);V 2 — 空白试验盐酸溶液的体积的数值,单位为毫升(mL)M — 无水碳酸钠的摩尔质量的数值,单位为克每摩尔(g/mol),[(1/2Na 2CO 3)=52.994]。
C HCl = M NCO3=105.99计算步骤:V 2=0.00 mL I :MV V m C HCl⨯-⨯=)(100021=994.52)00.060.17(10001241.0⨯-⨯=0.1331(mol/L)同理可得II : c(HCl)=0.1327(mol/L) III :c(HCl)=0.1335(mol/L) 相对平均偏差={()[()()]1331.01331.0-1335.01327.0-1331.01331.0-1331.031++}×100%=0.20%极差(X max -X min )=0.1335-0.1327=0.0008。

实验一盐酸标准溶液的配制与标定一、目的要求1.练习溶液的配制和滴定的准备工作,训练滴定操作,进一步掌握滴定操作。
2.学会用基准物质标定盐酸浓度的方法。
3.了解强酸弱碱盐滴定过程中 pH 的变化。
4.熟悉指示剂的变色观察,掌握终点的控制。
二、实验原理市售盐酸为无色透明的HCl水溶液,HCl含量为36%~38%(W/W),相对密度约为1.18。
由于浓盐酸易挥发出HCl气体,若直接配制准确度差,因此配制盐酸标准溶液时需用间接配制法。
标定盐酸的基准物质常用碳酸钠和硼砂等,本实验采用无水碳酸钠为基准物质,以甲基红-溴甲酚绿混合指示剂指示终点,无水碳酸钠作基准物质的优点是容易提纯,价格便宜。
缺点是碳酸钠摩尔质量较小,具有吸湿性。
因此Na2CO3固体需先在270℃~300℃高温炉中灼烧至恒重,然后置于干燥器中冷却后备用。
计量点时溶液的 pH为3.89,用待标定的盐酸溶液滴定至溶液由绿色变为暗红色后煮沸2 min,冷却后继续滴定至溶液再呈暗红色即为终点。
根据Na2CO3的质量和所消耗的 HCl 体积,可以计算出HCl 的准确浓度。
用Na2CO3标定时反应为:2HCl + Na2CO3→ 2NaCl + H2O + CO2↑反应本身由于产生H2CO3会使滴定突跃不明显,致使指示剂颜色变化不够敏锐,因此,接近滴定终点之前,最好把溶液加热煮沸,并摇动以赶走CO2,冷却后再滴定。
三、实验用品分析天平(感量0.01mg/分度),量筒,称量瓶,25mL酸式滴定管,250mL锥形瓶。
工作基准试剂无水Na2CO3:先置于270℃~300℃高温炉中灼烧至恒重后,保存于干燥器中。
浓HCl(浓或0.1mol/L),溴甲酚绿(3.8-5.4)一甲基红(4.4-6.2)指示液(变色点pH=5.1):溶液Ⅰ: 称取0.1 g 溴甲酚绿,溶于乙醇(95%),用乙醇(95%)稀释至100m L;溶液Ⅱ; 称取0.2 g 甲基红,溶于乙醇(95%),用乙醇(95% )稀释至100m L;取 30 m L溶液I, 10m L溶液Ⅱ,混匀。

盐酸溶液的配制与标定
配制
1. 准备所需试剂:盐酸、去离子水、烧杯、容量瓶等。
2. 确定所需浓度和体积,按比例计算出盐酸和去离子水的用量。
3. 用烧杯将盐酸逐渐加入去离子水中,并不断搅拌,直至完全溶解。
4. 将溶液转移至干净的容量瓶中,加入去离子水至刻度线,摇匀。
标定
1. 取一定体积的盐酸标准溶液,加入少量指示剂(如甲基橙),滴加氢氧化钠溶液,记录消耗的体积和颜色变化。
2. 计算出盐酸溶液的浓度。
3. 多次重复以上步骤,取平均值并计算相对偏差,以确定盐酸标准溶液的浓度。
需要注意的是,在配制和标定的过程中要严格控制实验条件,保证结果的准确性。
同时,为了避免误差,最好使用称量准确、质量好、无杂质的试剂,并用干净的玻璃器皿操作。

实验一盐酸标准溶液的配制与标定一、目的要求 1. 练习溶液的配制和滴定的准备工作,训练滴定操作,进一步掌握滴定操作。
2. 学会用基准物质标定盐酸浓度的方法。
3. 了解强酸弱碱盐滴定过程中pH 的变化。
4. 熟悉指示剂的变色观察,掌握终点的控制。
二、实验原理市售盐酸为无色透明的HCl水溶液,HCl含量为36%~38%(W/W),相对密度约为1.18。
由于浓盐酸易挥发出HCl气体,若直接配制准确度差,因此配制盐酸标准溶液时需用间接配制法。
标定盐酸的基准物质常用碳酸钠和硼砂等,本实验采用无水碳酸钠为基准物质,以甲基红-溴甲酚绿混合指示剂指示终点,无水碳酸钠作基准物质的优点是容易提纯,价格便宜。
缺点是碳酸钠摩尔质量较小,具有吸湿性。
因此Na2CO3固体需先在270℃~300℃高温炉中灼烧至恒重,然后置于干燥器中冷却后备用。
计量点时溶液的pH为3.89,用待标定的盐酸溶液滴定至溶液由绿色变为暗红色后煮沸2 min,冷却后继续滴定至溶液再呈暗红色即为终点。
根据Na2CO3的质量和所消耗的HCl 体积,可以计算出HCl的准确浓度。
用Na2CO3标定时反应为:2HCl + Na2CO3 →2NaCl + H2O + CO2↑反应本身由于产生H2CO3会使滴定突跃不明显,致使指示剂颜色变化不够敏锐,因此,接近滴定终点之前,最好把溶液加热煮沸,并摇动以赶走CO2,冷却后再滴定。
三、实验用品分析天平(感量0.01mg/分度),量筒,称量瓶,25mL酸式滴定管,250mL锥形瓶。
工作基准试剂无水Na2CO3:先置于270℃~300℃高温炉中灼烧至恒重后,保存于干燥器中。
浓HCl(浓或0.1mol/L),溴甲酚绿(3.8-5.4)一甲基红(4.4-6.2)指示液(变色点pH=5.1):溶液Ⅰ: 称取0.1 g 溴甲酚绿,溶于乙醇(95%),用乙醇(95%)稀释至100m L;溶液Ⅱ; 称取0.2 g 甲基红,溶于乙醇(95%),用乙醇(95% )稀释至100m L;取30 m L溶液I, 10m L溶液Ⅱ,混匀。

一.配制:0.02mol/LHCl溶液:虽取1.8毫升盐酸,缓慢注入1000ml水。
O.lmol/LHCI溶液:址取9亳升盐酸.缓慢注入1000ml水°0.2mol/LHCI溶液:址取18毫升盐酸,缓慢注入1000ml水。
0.5mol/LHCI溶液:址取45毫升盐酸,缓慢注入1000ml水。
l.Omol/LHCI溶液:虽取90毫升盐酸,缓慢注入1000ml水。
―、标定:1、反应原理:Na2CO3-+2HCI-*2NaCI+CO2++H2O为缩小批示剂的变色范困,用澳甲酚绿一甲基红混合扌旨示剂•使颜色变化更加明显,该混合抬示剂的喊色为暗绿.它的变色点PH值为5.1,其酸色为暗红色很好判断。
2、仪器:滴定管50ml:三角烧瓶250ml: 135ml:瓷堪如称量瓶。
3、标定过程:基准物处理:取预先在玛瑙研钵中研细之无水碳酸钠适虽.宜入洁净的瓷加圳中,在沙浴上加热•注意使运动览埸中的无水碳酸钠面低于沙浴而.览圳用瓷盖半掩之,沙浴中插一支360C溫度汁.温度讣的水银球与堆竭底平,开始加热.保持27030091小时,加热期间缓缓加以搅拌.防止无水碳酸钠结块•加热完毕后.稍冷,将碳酸钠移入干悚好的称虽瓶中.于干悚器中冷却后称虽。
称収上述处理后的无水碳酸钠(标定0.02mol/L称取0.02-0.03克:O.lmol/L称取0.1-0.12克:0.2mol/L 称取0.2-0.4: 0.5mol/L称取0.5-0.6克:lmol/L称取1.0-1.2克称准至0.0002克)豊于250ml锥形瓶中. 加入新煮沸冷却后的蒸谓水(0.02mol/L加20ml: O.lmol/L 加20ml: 0.2mol/L 加50: 0.5mol/L 加50ml:lmol/L hn looml水)定溶,加10滴渙甲酚绿一甲基红混合指示剂,用待标定洛液滴定至溶液成暗红色,点沸2分钟,冷却后继续滴定至溶液呈暗红色。
同时做空白4、计算:C (HCI)——盐酸标准溶液址浓度mol/Lm—无水碳酸钠的质虽(克)VI——滴定消耗HCI ml数V2——滴定消耗HCI ml数0.05299-一与1.000盐酸标准溶液相十的以克表示的无水碳酸钠的质量。

盐酸标准滴定溶液的配制所需的仪器、材料与试剂:
1、分析天平、酸式滴管、锥形瓶、量筒、吸量管、试剂瓶、烧杯和电炉子。
2、试剂:浓盐酸(分析纯)。
无水碳酸钠(基准物质),甲基橙。
配置步骤:
1、配制:用量筒取浓盐酸4.5ml,加水稀释至500mL混匀,倒入试剂瓶中,密塞。
2、标定:递减质量称量法在分析天平上称取在270~300℃干燥至恒重的基准物无水碳酸钠1.0~1.2g于烧杯中,加入适量的水溶解。
然后定量地转入250mL容量瓶中,用水稀释至刻度,摇匀。
用移液管取碳酸钠溶液25mL,加甲基橙指示剂1-2滴,用HCl溶液滴定至溶液由黄色刚变为橙色,即可得出盐酸标准溶液。
记下所消耗HCl的体积。
平行测定三份,计算盐酸溶液的浓度。

盐酸标准溶液(0.1 mol·L—1)的配制与标定一、原理市售盐酸为无色透明的HCl水溶液,HCl含量为36%~38%(W/W).由于浓盐酸易挥发出HCl气体,若直接配制准确度差,因此配制盐酸标准溶液时需用间接配制法。
采用无水碳酸钠为基准物质标定盐酸,以甲基红-溴甲酚绿混合指示剂指示终点。
用Na2CO3标定时反应为:2HCl + Na2CO3→ 2NaCl + H2O + CO2执行标准:GB/T 601-2002 化学试剂标准滴定溶液的制备二、实验用品分析天平(感量0。
1mg/分度),量筒,称量瓶,25mL酸式滴定管,250mL锥形瓶,工作基准试剂无水Na2CO3,浓HCl(浓或0。
1mol/L),溴甲酚绿一甲基红指示液(变色点pH=5.1).三、实验步骤(1)0.1mol.L—1盐酸溶液的配制:用小量筒取浓盐酸9ml,注入1000 ml,摇匀. (2)盐酸标准滴定溶液的标定取在270~300℃干燥至恒重的基准无水碳酸钠约0。
2g,精密称定3份,分别置于250ml锥形瓶中,加50ml蒸馏水溶解后,加甲基红-溴甲酚绿混合指示剂10滴,用盐酸溶液(0。
1mol·L—1)滴定至溶液又由绿变暗红色,煮沸约2min。
冷却至室温,继续滴定至暗红色,记下所消耗的标准溶液的体积, 同时做空白试验四、实验结果(1)数据记录(2)结果计算盐酸标准滴定溶液的浓度[c (HCl )]。
数值以摩尔每升(mol/L)表示,按下式计算:MV V m C HCl ⨯-⨯=)(100021式中 : m — 无水碳酸钠的质量的准确数值,单位为克(g );V 1— 盐酸溶液的体积的数值,单位为毫升(mL );V 2 — 空白试验盐酸溶液的体积的数值,单位为毫升(mL ) M — 无水碳酸钠的摩尔质量的数值,单位为克每摩尔(g/mol ),[(1/2Na 2CO 3)=52。
994]。
C HCl =? M NCO3=105。
盐酸标准滴定溶液的配制与标定
1、配制
按下表规定量取浓盐酸(AR )注入1000ml 水中,摇匀。
2、标定
按下表规定准确称取经270-300℃灼烧至恒重的基准无水碳酸钠,溶于50ml 水中,加10滴溴甲酚绿-甲基红指示剂,用配好的盐酸溶液滴定至溶液由绿色变成暗红色,煮沸2min ,冷却后继续滴定至溶液再呈暗红色。
同时做空白实验。
3、计算
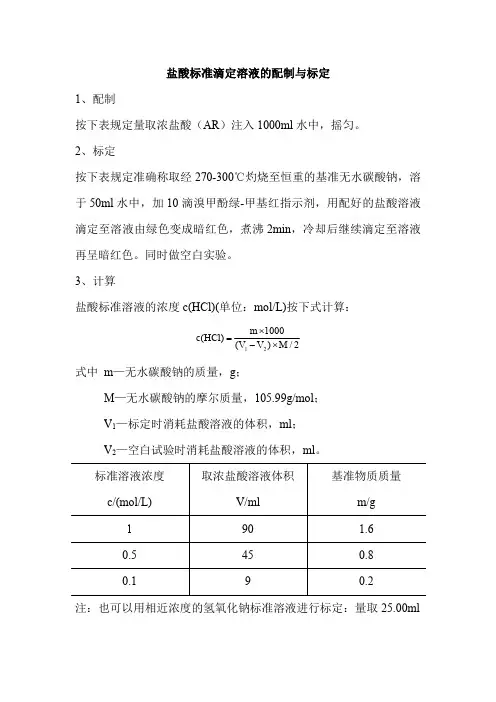
盐酸标准溶液的浓度c(HCl)(单位:mol/L)按下式计算:
2
/M )V V (1000
m )HCl (c 21⨯-⨯=式中m —无水碳酸钠的质量,g ;
M —无水碳酸钠的摩尔质量,105.99g/mol ;
V 1—标定时消耗盐酸溶液的体积,ml ;
V 2—空白试验时消耗盐酸溶液的体积,ml 。
标准溶液浓度
c/(mol/L)
取浓盐酸溶液体积V/ml 基准物质质量m/g 1
90 1.60.5
450.80.190.2
注:也可以用相近浓度的氢氧化钠标准溶液进行标定:量取25.00ml
配制好的盐酸溶液,加50ml 无二氧化碳的水,加2滴酚酞指示剂,用相近浓度的氢氧化钠标准溶液滴定,近终点时加热至80℃,继续滴定溶液至浅粉红色,然后按下式计算:
25C V )HCl (c NaOH NaOH ⨯=。

盐酸标准溶液配制与标定一、配制:0.02mol/LHCl溶液:量取1.8毫升盐酸,缓慢注入1000ml水。
0.1mol/LHCl溶液:量取9毫升盐酸,缓慢注入1000ml水。
0.2mol/LHCl溶液:量取18毫升盐酸,缓慢注入1000ml水。
0.5mol/LHCl溶液:量取45毫升盐酸,缓慢注入1000ml水。
1.0mol/LHCl溶液:量取90毫升盐酸,缓慢注入1000ml水。
二、标定:1、反应原理:Na2CO3-+2HCl→2NaCl+CO2++H2O为缩小批示剂的变色范围,用溴甲酚绿-甲基红混合指示剂,使颜色变化更加明显,该混合指示剂的碱色为暗绿,它的变色点PH值为5.1,其酸色为暗红色很好判断。
2、仪器:滴定管50ml;三角烧瓶250ml;135ml;瓷坩埚;称量瓶。
3、标定过程:基准物处理:取预先在玛瑙研钵中研细之无水碳酸钠适量,置入洁净的瓷坩埚中,在沙浴上加热,注意使运动坩埚中的无水碳酸钠面低于沙浴面,坩埚用瓷盖半掩之,沙浴中插一支360℃温度计,温度计的水银球与坩埚底平,开始加热,保持270-300℃1小时,加热期间缓缓加以搅拌,防止无水碳酸钠结块,加热完毕后,稍冷,将碳酸钠移入干燥好的称量瓶中,于干燥器中冷却后称量。
称取上述处理后的无水碳酸钠(标定0.02mol/L称取0.02-0.03克;0.1mol/L 称取0.1-0.12克;0.2mol/L称取0.2-0.4;0.5mol/L称取0.5-0.6克;1mol/L称取1.0-1.2克称准至0.0002克)置于250ml锥形瓶中,加入新煮沸冷却后的蒸馏水(0.02mol/L加20ml;0.1mol/L加20ml;02mol/L加50;0.5mol/L 加50ml;1mol/L加100ml水)定溶,加10滴溴甲酚绿-甲基红混合指示剂,用待标定溶液滴定至溶液成暗红色,煮沸2分钟,冷却后继续滴定至溶液呈暗红色。
同时做空白4、计算:C(HCl)——盐酸标准溶液量浓度mol/Lm——无水碳酸钠的质量(克)V1——滴定消耗HCl ml数V2——滴定消耗HCl ml数0.05299--与1.000盐酸标准溶液相当的以克表示的无水碳酸钠的质量。
在实验室中,配制和标定盐酸标准溶液是一项非常重要的实验操作。
盐酸标准溶液既可以用作化学试剂,也可以用于化学分析中的定量分析。
本文将就0.01盐酸标准溶液的配制与标定这一主题展开深入探讨。
1. 0.01盐酸标准溶液的配制在进行0.01盐酸标准溶液的配制时,首先需要准备一定质量分数的盐酸溶液。
通常情况下,我们会选择优质的盐酸固体,并在纯净水中逐渐溶解,直到达到所需浓度。
在配制过程中,需要严格控制盐酸的质量和水的用量,保证最终得到的盐酸溶液质量分数准确。
而后,将稀释后的盐酸溶液定容至标定瓶,摇匀即可得到0.01盐酸标准溶液。
2. 0.01盐酸标准溶液的标定标定是为了确定所配制溶液中准确含量的一种实验操作。
在标定盐酸标准溶液时,首先需要准备一定量的碱基溶液,常用的是氢氧化钠溶液。
借助酸碱滴定法,逐滴加入盐酸标准溶液,直至出现中性反应为止。
通过实验测出所需的盐酸溶液的准确浓度,预先确定好浓度的盐酸溶液才能在实验中准确应用。
3. 个人观点和理解配制和标定盐酸标准溶液是实验室工作中的基础操作之一。
通过合理的实验设计和严谨的操作流程,可以得到准确的实验结果。
在实际操作中,需要严格按照实验步骤进行,并注意配制和标定的各个环节,以免引起误差。
盐酸标准溶液广泛应用于化学实验和分析化学中,因此正确的配制和标定对实验结果的准确性至关重要。
在实验操作中,我们应该不断积累经验,提高操作的准确性和技术水平,保证实验数据的可靠性。
在本文中,我们详细探讨了0.01盐酸标准溶液的配制与标定的操作步骤,并就该主题进行了个人观点和理解的共享。
通过深入的讨论和实际操作,相信读者能对该主题有更深入的理解和掌握。
希望读者在实际操作中能够严格遵守相关实验规范和流程,保证实验数据的准确性和可靠性。
盐酸标准溶液是化学实验室中常用的一种标准物质,它具有已知的浓度和成分,可用于定量分析、标定其他试剂、调节试剂的浓度等多种用途。
配制和标定盐酸标准溶液是实验室工作中非常重要的一环。
盐酸标准溶液的配制、标定和碱灰中总碱度的测定晏明(20096564)(四川农业大学生命科学与理学院,化学生物学09-1,625014)摘要碱灰为不纯的Na2CO3,其中混有少量的NaOH、Na2SO4或NaHCO3杂质。
用酸溶液滴定时,以甲基橙为指示剂,除Na2CO3被中和外,NaOH 、NaHCO3等碱牲杂质也被中和,因此测定的结果是碱的总量,常用Na2O含量来表示。
酸碱滴定法的滴定终点与化学计量点往往不一致,存在终点误差,可通过林邦误差公式进行分析。
关键词碱灰总碱度酸碱滴定终点误差Soda ash is Impure Na2CO3, which mixed with small amounts of NaOH, Na2SO4, or NaHCO3 impurities. Acid droplets with time, with methyl orange as indicator, in addition to being neutralize Na2CO3, NaOH, NaHCO3 and other impurities have been neutralize, so the result is the determination of the amount of alkali, usually expressed in Na2O content. Acid-base titration endpoint is often inconsistent with the stoichiometric point, there is error, and the error can be analyzed by Ringbom formula.1 引言碱灰为不纯的Na2CO3,其中混有少量的NaOH、Na2SO4或NaHCO3杂质。
硫酸、硝酸、盐酸和纯碱(碳酸钠)、烧碱(氢氧化钠)统称为“三酸二碱”,它们是重要的无机化工酸、碱原料。
广东石油化工学院实验报告班级:生物技术08-2 学号:实验者:成绩实验一盐酸标准溶液的配制及标定一、目的要求1.练习溶液的配制和滴定的准备工作,训练滴定操作,进一步掌握滴定操作。
2.学会用基准物质标定盐酸浓度的方法。
3.了解强酸弱碱盐滴定过程中 pH 的变化。
4.熟悉指示剂的变色观察,掌握终点的控制。
二、实验原理市售盐酸为无色透明的HCl水溶液,HCl含量为36%〜38%(W/W),相对密度约为1.18。
由于浓盐酸易挥发出HCl气体,若直接配制准确度差,因此配制盐酸标准溶液时需用间接配制法。
标定盐酸的基准物质常用碳酸钠和硼砂等,本实验采用无水碳酸钠为基准物质,以甲基红-溴甲酚绿混合指示剂指示终点,无水碳酸钠作基准物质的优点是容易提纯,价格便宜。
缺点是碳酸钠摩尔质量较小,具有吸湿性。
因此Na CO固体需先在270°C~300°C高温炉中灼烧至恒重,然后置23 于干燥器中冷却后备用。
计量点时溶液的pH为3.89,用待标定的盐酸溶液滴定至溶液由绿色变为暗红色后煮沸 2 min,冷却后继续滴定至溶液再呈暗红色即为终点。
根据Na CO的质量和所消耗的HCl体积,可以计算出HCl的准确浓度。
23用 Na CO 标定时反应为:2HCl + Na CO - 2NaCl + HO + CO t2 3 2 3 2 2反应本身由于产生H CO会使滴定突跃不明显,致使指示剂颜色变化不23够敏锐,因此,接近滴定终点之前,最好把溶液加热煮沸,并摇动以赶走CO ,冷却后再滴定。
2三、实验用品分析天平(感量O.Olmg/分度),量筒,称量瓶,25mL酸式滴定管,250mL 锥形瓶。
工作基准试剂无水NaCO :先置于270°C~300°C高温炉中灼烧至恒重后,保存于干燥器中。
浓HC1(浓或O.lmol/L),溴甲酚绿(3.8-5.4) —甲基红(4.4-6.2)指示液(变色点pH=5.1):溶液I:称取0.1 g溴甲酚绿,溶于乙醇(95%),用乙醇(95%)稀释至100mL;溶液II;称取0.2 g甲基红,溶于乙醇(95%),用乙醇(95% )稀释至 100m L;取30 m L溶液I, 10m L溶液II,混匀。
实验一盐酸标准溶液的配制与标定一、目的要求1.练习溶液的配制和滴定的准备工作,训练滴定操作,进一步掌握滴定操作。
2.学会用基准物质标定盐酸浓度的方法。
3.了解强酸弱碱盐滴定过程中 pH 的变化。
4.熟悉指示剂的变色观察,掌握终点的控制。
二、实验原理市售盐酸为无色透明的HCl水溶液,HCl含量为36%~38%(W/W),相对密度约为1.18。
由于浓盐酸易挥发出HCl气体,若直接配制准确度差,因此配制盐酸标准溶液时需用间接配制法。
标定盐酸的基准物质常用碳酸钠和硼砂等,本实验采用无水碳酸钠为基准物质,以甲基红-溴甲酚绿混合指示剂指示终点,无水碳酸钠作基准物质的优点是容易提纯,价格便宜。
缺点是碳酸钠摩尔质量较小,具有吸湿性。
因此Na2CO3固体需先在270℃~300℃高温炉中灼烧至恒重,然后置于干燥器中冷却后备用。
计量点时溶液的 pH为3.89,用待标定的盐酸溶液滴定至溶液由绿色变为暗红色后煮沸2 min,冷却后继续滴定至溶液再呈暗红色即为终点。
根据Na2CO3的质量和所消耗的 HCl 体积,可以计算出HCl的准确浓度。
用Na2CO3标定时反应为:2HCl + Na2CO3→ 2NaCl + H2O + CO2↑反应本身由于产生H2CO3会使滴定突跃不明显,致使指示剂颜色变化不够敏锐,因此,接近滴定终点之前,最好把溶液加热煮沸,并摇动以赶走CO2,冷却后再滴定。
三、实验用品分析天平(感量0.01mg/分度),量筒,称量瓶,25mL酸式滴定管,250mL锥形瓶。
工作基准试剂无水Na2CO3:先置于270℃~300℃高温炉中灼烧至恒重后,保存于干燥器中。
浓HCl(浓或0.1mol/L),溴甲酚绿(3.8-5.4)一甲基红(4.4-6.2)指示液(变色点pH=5.1):溶液Ⅰ: 称取0.1 g 溴甲酚绿,溶于乙醇(95%),用乙醇(95%)稀释至100m L;溶液Ⅱ; 称取0.2 g 甲基红,溶于乙醇(95%),用乙醇(95% )稀释至100m L;取 30 m L溶液I, 10m L溶液Ⅱ,混匀。
盐酸标准溶液的标定一.仪器与试剂仪器:全自动电光分析天平1台(1)称量瓶1只(2)试剂瓶1000ml 1个(3)锥形瓶250ml 3个(4)酸式滴定管50ml 1支(5)量筒50mL 1只试剂:(1)0.1mol/L盐酸待标定溶液(2)无水碳酸钠(固基准物)(3)溴甲酚绿-甲基红混合指示剂二、步骤0.1mol/L盐酸标准溶液的标定1.标定步骤用称量瓶按递减称量法称取在270~300℃灼烧至恒重的基准无水碳酸钠0.15~0.22g(称准至0.0002g),放入250ml锥形瓶中,以50ml蒸馏水溶解,加溴甲酚绿-甲基红混合指示剂10滴(或以25ml蒸馏水溶解,加甲基橙指示剂1~2滴),用0.1mol/L盐酸溶液滴定至溶液由绿色变为暗红色(或由黄色变为橙色),加热煮沸2分钟,冷却后继续滴定志溶液呈暗红色(或橙色)为终点。
平行测定3次,同时做空白实验。
以上平行测定3次的算术平均值为测定结果。
2.计算式中:m—基准无水碳酸钠的质量,g;V1—盐酸溶液的用量,ml;V0—空白试验中盐酸溶液的用量,ml;52.99—1/2 Na2CO3摩尔质量,g/molC HCL—盐酸标准溶液的浓度,mol/L.氢氧化钠溶液的标定1、试剂:(1)0.1000mol/L 氢氧化钠待标定溶液(2)酚酞指示剂2、仪器:(1)全自动电光分析天平 1台(2)称量瓶 1只(3)碱式滴定管 (50mL ) 1支(4)锥形瓶 (250mL ) 3支(5)烧杯 (250mL ) 2只(6)洗瓶 1只(7)量筒 (50mL ) 1只3、测定步骤:准确称取在110℃~120℃准确称取在110~120℃烘至恒重的基准邻苯二甲酸氢钾0.5~0.6g(称准至0.0002g),放入250ml 三角瓶中,加入250ml 的蒸馏水溶解,加酚酞指示剂2滴,用0.1mol/LNaOH 溶液滴定至由无色变为红色30秒不褪色为终点,平行测定3次,同时作空白试验。
4、计算:C (NaOH)=22.204)(100001⨯-⨯V V m 式中:m —邻苯二甲酸氢钾的质量,g1V —NaOH 溶液的用量,ml0V —空白试验NaOH 溶液的用量,ml204.22 —邻苯二甲酸氢钾的摩尔质量,g/molNaOH C —NaOH 标准溶液的浓度,mol/L混合碱的组成及其含量的测定一、仪器和试剂1.仪器(1)全自动电光分析天平 1台(2)酸式滴定管 50ml 1根(3)称量瓶 1只(4)锥形瓶 250mL 2只(5)洗瓶 1只(6)容量瓶 250mL 1只(7)烧杯 250mL 2只2.试剂0.1%甲基橙指示剂;0.1%酚酞指示剂;混合碱试样、 0.1mol/LHCI 标准溶液。
二、实验步骤1.准确称取混1.8000~2.0000g 合碱试样于烧杯中,溶解并定量转移于250ml 容量瓶中,用蒸馏水稀释到刻度,摇匀。
2.用处理好的移液管准确移取25.00ml 试液于锥形瓶中,加入酚酞指示剂1~2滴,用0.1mol/LHCI 标准溶液滴定至红色刚刚褪去,记录消耗0.1mol/LHCI 标准溶液体积记为V1ml ,然后加入甲基橙指示剂1滴,继续用0.1mol/LHCI标准溶液滴定至溶液由黄色变为橙色为终点,记录消耗HCl标准溶液的总体积V总,平行测定3次。
根据两次消耗0.1mol/LHCI标准溶液的体积,计算出V1和V2,判断出此混合碱是由哪两种物质组成。
另:准确称取混混合碱0.1800~0.2000g试样于锥形瓶中,加入50mL蒸馏水溶解,加入酚酞指示剂1~2滴,用0.1mol/LHCI标准溶液滴定至红色刚刚褪去,记录消耗0.1mol/LHCI标准溶液体积记为V1ml,然后加入甲基橙指示剂1滴,继续用0.1mol/LHCI标准溶液滴定至溶液由黄色变为橙色为终点,记录消耗HCl标准溶液的总体积V总,平行测定3次。
根据两次消耗0.1mol/LHCI标准溶液的体积,计算出V1和V2,判断出此混合碱是由哪两种物质组成。
3、结果计算1、若V1<V2,则:2、若V1>V2,则:式中:HCLC——盐酸标准溶液的浓度,mol/L;V1——以酚酞为指示剂,滴定至终点时盐酸标准溶液的用量,mL;V2——以甲基橙为指示剂,滴定至终点时盐酸标准溶液的用量,mL;0.05300——碳酸钠的毫摩尔质量,g/mmol/L;0.08400——碳酸氢钠的毫摩尔质量,g/mmol/L;0.04000——氢氧化钠的毫摩尔质量,g/mmol/L;高锰酸钾溶液的标定一、仪器和试剂1、仪器(1)全自动电光分析天平 1台(2)称量瓶 1只(3)棕色酸式滴定管 50mL 1根(4)锥形瓶 250mL 3只(5)量筒 50mL 1只2、试剂(1)0.1mol/L 高锰酸钾待标定溶液(2)草酸钠(基准试剂)(3)3mol/L 的硫酸溶液二、步骤1、准确称取于105~110℃烘干至恒重的基准试剂草酸钠0.18~0.22g (准确至0. 0002g ),于锥形瓶中,加入50ml 蒸水溶解后,再加入3mol/L 的硫酸溶液15mL ,加热到75~85℃,趁热用待标定的0.1mol/L 高锰酸钾待标定溶液滴定至溶液呈粉红色,并保持30S 不褪色,平行测定3次,同时做空白试验。
2、结果计算式中:322O C Na M ——基准试剂草酸的质量,g ;V1——高锰酸钾标准溶液的消耗量,mL ;V2——空白试验高锰酸钾标准溶液的用量,mL ;67.00——草酸钠⎪⎭⎫⎝⎛32221O C Na 的摩尔质量,g/mol/L ; 451KMnO C ——高锰酸钾标准溶液的浓度,mol/L ;铵盐中氮含量的测定一、仪器和试剂1、仪器(1)全自动电光分析天平1台(2)碱式滴定管50mL 1根(3)容量瓶250mL 1只(4)锥形瓶250mL 3只(5)移液管25mL 1支(6)吸量管5mL 1只(7)吸耳球1只(8)称量瓶1只(9)烧杯250mL 1只2、试剂(1)0.1mol/L氢氧化钠标准溶液(2)硫酸铵试样(3)18%甲醛溶液(4)酚酞指示剂二、步骤1、准确称取1.20~1.40g(精确至0.0002g)的硫酸铵试样,于250mL烧杯中,加入约50mL的蒸馏水溶解试样,定量移入250mL容量瓶中,用少量的水洗涤烧杯2~3次,洗涤液并入容量瓶中,平摇,稀释至刻度,摇匀。
2、准确移取25mL硫酸铵试液,于锥形瓶中,加入5mL18%的中性甲醛试液,放置5分钟后,加入1~2滴酚酞指示剂,用0.1mol/L氢氧化钠标准溶液滴定至溶液呈浅粉红色,并保持30S不褪色,记录氢氧化钠溶液的消耗量(V),平行测定3次。
3、结果计算C——氢氧化钠标准溶液的摩尔浓度,mol/L;式中:N a O HV——氢氧化钠标准溶液的消耗量,mL;NaOH0.01401——氮的毫摩尔质量,g/mmol/L;m——硫酸铵试样的质量,g;总碱含量的测定1、试剂:(1)0.1000mol/LHCl标准溶液(2)甲基橙指示剂2、仪器:(1)全自动电光分析天平1台(2)称量瓶1只(3)容量瓶(250mL)1只(4)称液管(25mL)1支(5)酸式滴定管(50mL)1支(6)锥形瓶(250mL)3支(7)烧杯(250mL)2只(8)洗瓶1只3、测定步骤:准确称取1.3~1.5克工业碳酸钠试样(准确至0.0001g)于250mL烧杯中,加入蒸馏水溶解后(可适当加热溶解完全),称入250mL 容量瓶中,稀释至刻度。
用称液管吸取25.00mL 试液于锥形瓶中,加入1~2滴甲基橙指示剂,用0.1000mol/LHCl 标准溶液滴定至溶液由黄色变为橙色。
平行测定3次。
4、计算:总碱的质量分数,以Na 2CO 3表示。
式中:()L mol HCl HCl c /,标准溶液的量浓度→ ()HCl V ——消耗HCl 标准溶液的体积,mLm ——试样的质量,g混合物中草酸和草酸钠含量的测定一、 试剂和材料:硫酸 8+92酚酞指示剂 10g/L氢氧化钠标准溶液 0.1000mol/L高锰酸钾标准溶液 0.1000mol/L二、分析步骤准确称取1.8~2.0(精确至0.0002g ),于250mL 的烧杯中,加入50mL 水溶解,转移至250mL 的容量瓶中,用水稀释至刻度,摇匀。
此为溶液A 。
(1)草酸含量的测定用移液管吸取样品溶液(A )25.00mL 于250mL 锥形瓶中,加入50mL 水,加2滴酚酞指示剂,用0.1000mol/LNaOH 标准溶液滴定至溶液呈粉红色为终点,记下V 1(2)草酸钠含量的测定用移液管吸取样品溶液(A )25.00mL 于250mL 烧杯中,加入100mL 硫酸溶液(8+90),加热至75℃,立即用用0.1000mol/LKMnO 4标准溶液滴定至溶液呈粉红色,并保持30S 不褪色为终点,记下V 2二、 数据的记录与结果的处理(1)混合物中草酸质量分数X 1(%)按下式计算:(2)混合物中草酸钠质量分数X 2(%)按下式计算 工业用水中微量铁含量的测定(邻菲啰啉法)1、仪器(1)721或723分光光度计 1台(2)容量瓶(50mL ) 6只(3)烧杯(100mL ) 2只(4)刻度吸量管(10mL ) 1支(5mL ) 3支(1mL ) 1支(5)吸耳球 1只2、试剂(1)0.01mg/mL 铁标准溶液(2)10%盐酸羟胺溶液(3)0.1%邻菲啰啉溶液(4)乙酸—乙酸钠缓冲溶液3、步骤(1)标准曲线的绘制依次吸取铁标准溶液0.00;1.00;3.00;5.00;7.00于50ml容量瓶中,加入1mL10%盐酸羟胺溶液、5mL乙酸—乙酸钠缓冲溶液及5mL0.1%邻菲啰啉溶液,加蒸馏水稀释至刻度,摇匀,静置15分钟。
即组成铁标准系列,用721或723分光光度计选择波长在510nm处测定吸光度。
(2)根据测定出的吸光度及溶液的浓度,绘制出标准曲线。
(3)样品的配制及测定准确移取5.00mL的待测试样,于50ml容量瓶中,加入1mL10%盐酸羟胺溶液、5mL乙酸—乙酸钠缓冲溶液及5mL0.1%邻菲啰啉溶液,加蒸馏水稀释至刻度,摇匀,静置15分钟。
用721或723分光光度计选择波长在510nm处测定吸光度(以空白试液作参比液)。
4、计算5、数据记录与结果计算。