高中化学竞赛辅导---晶体结构
- 格式:ppt
- 大小:2.23 MB
- 文档页数:45

郴州市二中高一化奥班辅导资料——晶体结构(2008-05-28)【涉及概念和内容】根据《化学课程标准》和中学化学教材以及《物质结构与性质》选修教材,晶体结构涉及的内容包括:(1)基本概念:周期性有序排列、晶胞及晶胞类型、晶胞中粒子数的计算、配位数、空隙、堆积方式、晶格能、并置碓砌;(2)堆积方式:面心立方、六方、体心立方和简单立方堆积;(3)晶体种类和性质:金属晶体、离子晶体、分子晶体、原子晶体,自范性、各向异性、金属晶体的导电导热和延展性、X-射线衍射。
这些内容看似零碎,实际上它们有着密切的内在联系,了解和建立它们的关系,对于晶体结构的教与学,深刻理解晶体结构和性质,掌握核心、突出重点都是很重要的。
它们的联系可以用下面的结构表示,其中堆积类型是联系晶体基本概念、基本结构与不同晶体类型的结构和性质的桥梁。
面心立方最密堆积(A1)最密堆积六方最密堆积(A3)体心立方密堆积(A2)简单立方堆积金刚石型堆积(四面体堆积)(A4)一、晶体的结构1、晶体的概念晶体是质点(原子、分子、离子)在空间有规律周期性地重复排列,是具有规则的多面体固体物质。
2自范性:在一定条件下晶体能自动地呈现具有一定对称性的多面体的外形(晶体的形貌)。
非晶体不能呈现多面体的外形。
晶态石英的谱图非晶态石英的谱图3、晶体的点阵结构概念:在晶体内部原子或分子周期性地排列的每个重复单位的相同位置上定一个点,这些点按一定周期性规律排列在空间,这些点构成一个点阵。
点阵是一组无限的点,连结其中任意两点可得一矢量,将各个点阵按此矢量平移能使它复原。
点阵中每个点都具有完全相同的周围环境。
晶体结构= 点阵+ 结构基元结构基元:在晶体的点阵结构中每个点阵所代表的具体内容,包括原子或分子的种类和数量及其在空间按一定方式排列的结构。
(1)直线点阵(2)平面点阵(3)晶胞(晶胞是人为划定的,为平行六面体)空间点阵必可选择3个不相平行的连结相邻两个点阵点的单位矢量a,b,c,它们将点阵划分成并置的平行六面体单位,称为点阵单位。

第五章晶体结构§5-1晶体的点阵理论1. 晶体的结构特征人们对晶体的印象往往和晶莹剔透联系在一起。
公元一世纪的古罗马作家普林尼在《博物志》中,将石英定义为“冰的化石”,并用希腊语中“冰”这个词来称呼晶体。
我国至迟在公元十世纪,就发现了天然的透明晶体经日光照射以后也会出现五色光,因而把这种天然透明晶体叫做"五光石"。
其实,并非所有的晶体都是晶莹剔透的,例如,石墨就是一种不透明的晶体。
日常生活中接触到的食盐、糖、洗涤用碱、金属、岩石、砂子、水泥等都主要由晶体组成,这些物质中的的晶粒大小不一,如,食盐中的晶粒大小以毫米计,金属中的晶粒大小以微米计。
晶体有着广泛的应用。
从日常电器到科学仪器,很多部件都是由各种天然或人工晶体而成,如,石英钟、晶体管,电视机屏幕上的荧光粉,激光器中的宝石,计算机中的磁芯等等。
晶体具有按一定几何规律排列的内部结构,即,晶体由原子(离子、原子团或离子团)近似无限地、在三维空间周期性地呈重复排列而成。
这种结构上的长程有序,是晶体与气体、液体以及非晶态固体的本质区别。
晶体的内部结构称为晶体结构。
晶体的周期性结构,使得晶体具有一些共同的性质:(1) 均匀性晶体中原子周期排布的周期很小,宏观观察分辨不出微观的不连续性,因而,晶体内部各部分的宏观性质(如化学组成、密度)是相同的。
(2) 各向异性在晶体的周期性结构中,不同方向上原子的排列情况不同,使得不同方向上的物理性质呈现差异。
如,电导率、热膨胀系数、折光率、机械强度等。
(3) 自发形成多面体外形无论是天然矿物晶体还是人工合成晶体,在一定的生长条件下,可以形成多面体外形,这是晶体结构的宏观表现之一。
晶体也可以不具有多面体外形,大多数天然和合成固体是多晶体,它们是由许多取向混乱、尺寸不一、形状不规则的小晶体或晶粒的集合。
(4) 具有确定的熔点各个周期内部的原子的排列方式和结合力相同,到达熔点时,各个周期都处于吸热溶化过程,从而使得温度不变。


全国化学竞赛初赛讲义——晶体结构晶体结构是化学竞赛中的重要内容之一、晶体是指由具有有序排列的原子,分子或离子组成的固态物质,具有规则的几何形状。
晶体结构的了解对于理解物质的性质和反应机理非常重要。
下面是晶体结构的讲义。
一、晶体结构的基本概念晶体的结构由最小的重复单元所组成,这个最小重复单元称为晶胞。
晶体结构中的重复单元之间的关系是平移关系,即晶胞通过平移操作得到整个晶体。
晶体结构可以分为离子晶体结构、共价晶体结构和金属晶体结构三种。
离子晶体由阳离子和阴离子组成,通常具有高熔点和硬度,如NaCl、CaF2等。
共价晶体由原子通过共价键相连形成,通常具有高熔点和硬度,如钻石、石墨等。
金属晶体由金属离子通过金属键相连形成,通常具有良好的导电性和延展性,如Cu、Al等。
二、晶体结构的表示方法1.点阵表示法:用数学点阵表示晶体中原子的相对位置关系。
有三种常见的点阵表示方法:简单立方点阵、面心立方点阵和体心立方点阵。
(1)简单立方点阵:晶胞内只含一个原子,每个原子都在晶体的角落上。
(2)面心立方点阵:晶胞内含有4个原子,每个原子都在晶体的角落和晶胞的中心。
(3)体心立方点阵:晶胞内含有2个原子,其中一个原子在晶体的角落上,另一个原子在晶胞的中心。
2.坐标表示法:用坐标系表示晶体中原子的位置。
在二维平面上,可以使用直角坐标系或斜坐标系表示晶体中原子的位置。
直角坐标系中,原子的位置可以用x和y两个坐标表示;斜坐标系中,原子的位置可以用a和b两个坐标表示。
在三维空间中,晶体中原子的位置通常用直角坐标系表示,即通过x、y和z三个坐标来确定原子的位置。
三、晶体的常见缺陷与晶体的生长晶体中常见的缺陷有点缺陷、线缺陷和面缺陷。
1.点缺陷:晶体中原子在其位置上发生的缺失、置换、插入或附加等现象。
(1)缺失缺陷:晶体中缺少一个原子。
(2)置换缺陷:晶体中一个原子被其他原子所替代。
(3)插入缺陷:晶体中多了一个原子。
(4)附加缺陷:晶体中多了一个原子,同时缺少一个原子。

高中化学竞赛经典讲义——晶体结构晶体结构是高中化学竞赛中一个非常重要的知识点。
晶体是由一定数量的离子、分子或原子按照一定的几何排列方式所组成的固体,其最具有代表性的性质就是具有规则的几何形状。
晶体结构的了解对于理解晶体的性质、结构与合成具有重要意义。
晶体结构的揭示是通过实验技术以及理论研究来实现的。
其中最重要的实验手段是X射线衍射。
当X射线穿过晶体时,会产生衍射现象,出现一系列亮斑,这些亮斑的位置和强度依赖于晶体结构。
通过对衍射图像的解析,可以确定晶胞参数,揭示出晶体内部的几何排列。
理论上,可以使用动力学理论计算晶体的结构,得出一系列理论結构参数。
实验与理论的比较可以验证理论的正确性,并进一步完善理论模型。
晶体结构是有一定规律的,可以分为离子晶体和共价晶体两种类型。
离子晶体是由正离子和负离子通过离子键结合而成的晶体。
离子晶体的结构稳定,离子之间的排列有一定的规则。
若正离子与负离子的离子半径比较接近,离子晶体的结构会较紧密,例如氯化钠、氟化钙等。
若离子半径比差异较大,离子晶体的结构则会较为散松,例如氧化银、氧化铅等。
共价晶体是由原子通过共价键结合而成的晶体。
共价晶体的原子之间的键长和键角与几何排列有密切关系。
晶体结构可以通过晶胞参数来描述。
晶胞是晶体的最小重复单元,其正六面体的两边长度为a,与该边垂直的四棱面间的夹角为90°,而与该边相邻的两棱面间的夹角为120°。
晶胞参数a、b、c分别代表了晶体沿三个坐标轴方向的长度,而α、β、γ代表了晶体坐标轴之间的夹角。
晶体结构的描述还需要引入晶体结构中的间隙。
间隙是晶胞中没有原子、离子或分子占据的空隙,可以是正交的,也可以是六角形的。
晶胞中间隙的存在对于许多晶体性质有着重要影响,例如导电性、光学性质等。
为了更好的理解晶体结构,可以引入晶体结构分类的一些基本概念。
首先是晶格点的概念,晶格点是描述晶体排列的重要参考点。
晶格参数是晶体中两个晶格点之间的最短距离,而晶格的基元则是指两个相邻晶格点之间的最短距离。

高中化学奥林匹克竞赛辅导离子键与晶体结构【学习要求】离子键。
晶胞。
原子坐标。
晶格能。
晶胞中原子数或分子数的计算及化学式的关系。
分子晶体、原子晶体、离子晶体和金属晶体。
配位数。
晶体的堆积与填隙模型。
常见的晶体结构类型,如NaCl、CsCl、闪锌矿(ZnS)、萤石(CaF2)、金刚石、石墨、硒、冰、干冰、尿素、金红石、钙钛矿、钾、镁、铜等。
点阵的基本概念。
一、晶体简介:晶体是原子、分子或离子在结晶过程中形成的具有规则几何外形的固体。
自然界中的固体大多是晶体,气体、液体或非晶体在一定条件下也可转化为晶体。
食盐晶体单质铋晶体1.晶体与非晶体相比,具有以下特性:(1)晶体具有规则的几何外形。
晶体外形的对称性是晶体内部结构对称性的表现。
(2)晶体具有固定的熔点。
晶体在熔化过程中,温度保持不变,而非晶体在熔化过程中温度保持上升,所以通过测定熔点来判断晶体的纯度。
(3)晶体具有各项异性,而非晶体各项同性。
晶体的各项异性是指晶体内部不同方向,原子或离子排列的周期性、疏密程度不同导致晶体在不同方向上的物理化学特性不同。
晶体在不同方向具有不同的硬度、导热性、导电性、折射率等。
如石墨在与层平行的方向上具有导电性,而在与层垂直的方向上就不具有导电性。
又如在水晶的柱面上涂一层蜡,用红热的针接触蜡面中央,蜡熔化呈椭圆形而不呈圆形,这是由于水晶柱面长轴方向与短轴方向传热速度不同。
再如从不同方向观察红宝石或蓝宝石,会发现宝石的颜色不同,这是由于方向不同,晶体对光的吸收性质不同。
2.晶格:晶体的结构通常用X射线进行研究。
X射线研究表明,晶体的组成质点(分子、原子或离子)以确定位置的点在空间作有规则的排列,这些点群具有一定几何形状,称为晶格。
3.晶胞:晶体结构中具有代表性的基本重复单位称为晶胞,它反映了晶体的组成和晶体的对称性。
相当大数量的晶胞“无隙并置”起来构成晶体。
“无隙”是指相邻晶胞之间没有缝隙。
“并置”是指所有晶胞平行排列、取向相同。


化学竞赛——晶体结构化学竞赛,晶体结构晶体结构是化学竞赛中的一个重要知识点,它涉及到晶体的组成、结构、性质等方面。
下面我将详细介绍晶体结构的相关知识。
晶体是由原子、离子或分子按照一定的几何规律排列而形成的具有固定形状和结构的物质。
晶体的结构可以分为晶格和晶胞两个层面。
晶格是指晶体中的原子、离子或分子的排列方式。
晶格可以分为三种类型:点阵、空间点阵和布拉维格子。
点阵是指晶体中原子、离子或分子的周期性排列形式,可以分为平面点阵、体心点阵、面心点阵等。
空间点阵是三维空间中具有平移对称性的点的集合,它可以由平面点阵通过添加一个垂直于平面的平移矢量得到。
布拉维格子是指空间中按照一定的几何规律分布的点,它由空间点阵通过移动原点所得到。
晶胞是晶体中一个最小的、具有完整晶体结构的单位。
晶胞可以分为简单晶胞、面心立方晶胞、体心立方晶胞等。
简单晶胞是指由一个或多个原子组成,没有原子在晶体内的重合部分的晶胞。
面心立方晶胞是指在体心立方晶胞的基础上,在每个体心加入了一个原子的晶胞。
体心立方晶胞是指在每个面心和一个体心分别加入一个原子的晶胞。
晶体结构可以通过X射线衍射、电子衍射等实验手段进行研究。
通过这些实验可以确定晶体中原子、离子或分子的位置和排列方式,从而揭示晶体的结构和性质。
晶体结构还可以用来解释化学反应的发生过程。
例如,固态反应与气态反应相比,通常速度较慢。
原因是固态反应需要克服晶体结构的稳定性,使反应物分子能够进入晶体内部,而气态反应则不受晶体结构的限制。
除了晶体结构,晶体中还存在一些缺陷,如点缺陷、线缺陷和面缺陷。
点缺陷是晶体中原子或离子位置的缺陷,如空位、空隙等。
线缺陷是晶体中原子或离子位置的缺陷,如缺陷线、螺旋线等。
面缺陷是晶体中晶面的缺陷,如晶界、孪晶等。
总之,晶体结构是化学竞赛中的一个重要知识点。
它涉及到晶体的组成、结构、性质等方面,对于理解物质的性质和变化过程具有重要意义。
同时,晶体结构的研究也为合成新材料、开发新技术提供了重要的理论基础。
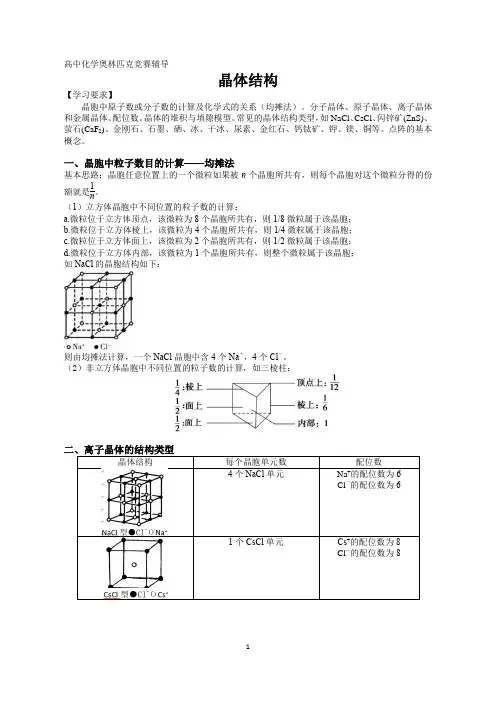
高中化学奥林匹克竞赛辅导晶体结构【学习要求】晶胞中原子数或分子数的计算及化学式的关系(均摊法)。
分子晶体、原子晶体、离子晶体和金属晶体。
配位数。
晶体的堆积与填隙模型。
常见的晶体结构类型,如NaCl 、CsCl 、闪锌矿(ZnS)、萤石(CaF 2)、金刚石、石墨、硒、冰、干冰、尿素、金红石、钙钛矿、钾、镁、铜等。
点阵的基本概念。
一、晶胞中粒子数目的计算——均摊法基本思路:晶胞任意位置上的一个微粒如果被n 个晶胞所共有,则每个晶胞对这个微粒分得的份额就是1n。
(1)立方体晶胞中不同位置的粒子数的计算:a.微粒位于立方体顶点,该微粒为8个晶胞所共有,则1/8微粒属于该晶胞;b.微粒位于立方体棱上,该微粒为4个晶胞所共有,则1/4微粒属于该晶胞;c.微粒位于立方体面上,该微粒为2个晶胞所共有,则1/2微粒属于该晶胞;d.微粒位于立方体内部,该微粒为1个晶胞所共有,则整个微粒属于该晶胞; 如NaCl 的晶胞结构如下:则由均摊法计算,一个NaCl 晶胞中含4个Na +,4个Cl -。
(2)非立方体晶胞中不同位置的粒子数的计算,如三棱柱:晶体结构离子的电子组态在一定程度上也会影响它的晶体结构,这三个性质综合起来还会决定离子键的共价性成分,后者过分强烈时,将使离子晶体转变为原子晶体,其间存在离子晶体到原子晶体的过渡型。
+-堆积方式简单立方堆积体心立方堆积面心立方最密堆积六方最密堆积四、原子晶体1.金刚石、晶体硅的结构:金刚石的晶体结构如下图所示,每个碳原子以sp3杂化与相邻的4个碳原子形成4个共价键,把晶体内所有的C原子连结成一个整体,形成空间网状结构,这种结构使金刚石具有很大的硬度和熔沸点。
由金刚石晶胞得,在一个金刚石晶胞中,含有8个C原子。
晶体硅具有金刚石型的结构。
只需将金刚石中的C原子换成Si原子即得到硅的结构。
常见的原子晶体有:金刚石(C)、晶体硅(Si)、SiO2、SiC、Si3N4、晶体硼(B)、晶体锗(Ge)、氮化硼(BN)等。


第五章晶体结构§5-1晶体的点阵理论1. 晶体的结构特征人们对晶体的印象往往和晶莹剔透联系在一起。
公元一世纪的古罗马作家普林尼在《博物志》中,将石英定义为“冰的化石”,并用希腊语中“冰”这个词来称呼晶体。
我国至迟在公元十世纪,就发现了天然的透明晶体经日光照射以后也会出现五色光,因而把这种天然透明晶体叫做"五光石"。
其实,并非所有的晶体都是晶莹剔透的,例如,石墨就是一种不透明的晶体。
日常生活中接触到的食盐、糖、洗涤用碱、金属、岩石、砂子、水泥等都主要由晶体组成,这些物质中的的晶粒大小不一,如,食盐中的晶粒大小以毫米计,金属中的晶粒大小以微米计。
晶体有着广泛的应用。
从日常电器到科学仪器,很多部件都是由各种天然或人工晶体而成,如,石英钟、晶体管,电视机屏幕上的荧光粉,激光器中的宝石,计算机中的磁芯等等。
晶体具有按一定几何规律排列的内部结构,即,晶体由原子(离子、原子团或离子团)近似无限地、在三维空间周期性地呈重复排列而成。
这种结构上的长程有序,是晶体与气体、液体以及非晶态固体的本质区别。
晶体的内部结构称为晶体结构。
晶体的周期性结构,使得晶体具有一些共同的性质:(1) 均匀性晶体中原子周期排布的周期很小,宏观观察分辨不出微观的不连续性,因而,晶体内部各部分的宏观性质(如化学组成、密度)是相同的。
(2) 各向异性在晶体的周期性结构中,不同方向上原子的排列情况不同,使得不同方向上的物理性质呈现差异。
如,电导率、热膨胀系数、折光率、机械强度等。
(3) 自发形成多面体外形无论是天然矿物晶体还是人工合成晶体,在一定的生长条件下,可以形成多面体外形,这是晶体结构的宏观表现之一。
晶体也可以不具有多面体外形,大多数天然和合成固体是多晶体,它们是由许多取向混乱、尺寸不一、形状不规则的小晶体或晶粒的集合。
(4) 具有确定的熔点各个周期内部的原子的排列方式和结合力相同,到达熔点时,各个周期都处于吸热溶化过程,从而使得温度不变。
全国化学竞赛初赛讲义——晶体结构一、晶体结构的概念和基本特点1.晶体结构的定义:晶体是由重复排列的原胞构成的固体。
2.晶体结构的基本特点:(1)有序性:晶体具有一定的有序性,原子、离子或分子排列有规律。
(2)三维性:晶体结构在三个维度上都有周期性重复性。
(3)稳定性:晶体结构对外界条件的变化具有较高的稳定性。
二、晶体结构的描述和表示方法1.晶胞:晶胞是由原胞重复平移所得到的一个最小重复单元,可以完全描述晶体的结构。
2.原胞:原胞是晶体中重复出现的、具有最简单结构的单元。
3.晶体参数:晶体参数包括晶胞的长度和夹角,用来描述晶体的形状和结构特征。
4.晶格:晶格是由原胞构成的、具有无限重复的空间点阵。
晶格可以用晶面和晶轴来表示。
三、晶体的结构类型和晶系分类1.结构类型:晶体的结构类型有离子晶体、共价晶体、金属晶体和分子晶体等。
2.晶系:晶系是根据晶格的对称性将晶体分为不同的类型。
晶系包括立方系、四方系、单斜系、正交系、斜方系、菱方系和三斜系。
四、晶体的基本结构单元1.离子晶体的基本结构单元是离子。
(1)离子晶体的特点:离子晶体由正、负离子通过电荷吸引力相互结合而成。
(2)离子晶体的类型:离子晶体包括简单离子晶体和复式离子晶体。
2.共价晶体的基本结构单元是原子。
(1)共价晶体的特点:共价晶体由共享电子键结合而成,键强较大。
(2)共价晶体的类型:共价晶体包括晶体分子、网络共价晶体和金刚石型晶体。
3.金属晶体的基本结构单元是金属离子。
(1)金属晶体的特点:金属晶体由金属阳离子和自由移动的电子云组成。
(2)金属晶体的类型:金属晶体包括简单金属晶体和合金。
4.分子晶体的基本结构单元是分子。
(1)分子晶体的特点:分子晶体由分子之间的相互作用力相互结合而成。
(2)分子晶体的类型:分子晶体包括极性分子晶体和非极性分子晶体。
五、晶体的性质与应用1.晶体的性质:晶体具有各向异性、光学性、热学性、电学性等特点。
2.晶体的应用:(1)光学应用:晶体在光学领域有着广泛的应用,如光学仪器、激光技术等。
极性增大非极性共价键 极性共价键 离子键 第6讲 晶体结构【竞赛要求】晶胞。
原子坐标。
晶格能。
晶胞中原子数或分子数的计算及化学式的关系。
分子晶体、原子晶体、离子晶体和金属晶体。
配位数。
晶体的堆积与填隙模型。
常见的晶体结构类型,如NaCl 、CsCl 、闪锌矿(ZnS )、萤石(CaF 2)、金刚石、石墨、硒、冰、干冰、尿素、金红石、钙钛矿、钾、镁、铜等。
点阵的基本概念。
晶系。
宏观对称元素。
十四种空间点阵类型。
分子的极性。
相似相溶规律。
分子间作用力。
范德华力。
氢键。
其他分子间作用力的一般概念。
【知识梳理】一、离子键理论1916 年德国科学家Kossel(科塞尔)提出离子键理论。
(一)离子键的形成1、形成过程 以 NaCl 为例:(1)电子转移形成离子 Na -e ˉ= Na + Cl + e ˉ= Cl ˉ相应的电子构型变化:2s 22p 63s 1 → 2s 22p 6 ;3s 23p 5 → 3s 23p 6分别达到 Ne 和 Ar 的稀有气体原子的结构,形成稳定离子。
(2)靠静电吸引,形成化学键,体系的势能与核间距之间的关系如图所示:注:横坐标——核间距r 。
纵坐标——体系的势能 V 。
纵坐标的零点——当 r 无穷大时,即两核之间无限远时,势能为零。
下面来考察 Na + 和 Cl ˉ彼此接近时,势能V 的变化。
图中可见:r >r 0时,随着 r 的不断减小,正负离子靠静电相互吸引,V 减小,体系趋于稳定。
r = r 0 时,V 有极小值,此时体系最稳定,表明形成了离子键。
r < r 0 时,V 急剧上升,因为 Na + 和 Cl ˉ彼此再接近时,相互之间电子斥力急剧增加, 导致势能骤然上升。
因此,离子相互吸引,保持一定距离时,体系最稳定,即为离子键。
2、离子键的形成条件(1)元素的电负性差要比较大△X > 1.7,发生电子转移,形成离子键;△X < 1.7,不发生电子转移,形成共价键。
高中化学竞赛——常见金属晶体的结构金属是一种特殊的物质,不像非金属那样具有明确的原子、分子结构,而是由大量的金属离子组成的。
金属晶体是由金属离子通过静电力相互吸引、排列而成的有序三维排列结构。
金属晶体具有许多独特的性质,如良好的导电性、导热性、延展性和机械性能等。
以下是几种常见金属的晶体结构的介绍。
1.面心立方结构(FCC)面心立方结构是一种常见的金属晶体结构,也称为充分面心立方结构。
在FCC晶体中,金属离子位于一个面心立方格子的顶点和面心上,形成四方紧密堆积的结构。
银(Ag)、铝(Al)、铜(Cu)和金(Au)都具有FCC结构。
2.体心立方结构(BCC)体心立方结构是另一种常见的金属晶体结构,也称为充分体心立方结构。
在BCC晶体中,金属离子位于一个体心立方格子的顶点和体心上,形成六方紧密堆积的结构。
铁(Fe)、钴(Co)、钨(W)和钠(Na)都具有BCC结构。
3.紧密堆积结构(HCP)紧密堆积结构是一种相对稳定的金属晶体结构。
在HCP晶体中,金属离子位于六方密排的顶点和六角面上,形成堆积的结构。
锌(Zn)、钛(Ti)和镁(Mg)都具有HCP结构。
4.单斜结构单斜结构是一种稀有的金属晶体结构,通常在少数金属中存在。
在单斜结构中,金属离子位于不同的位置上,形成不规则的结构。
例如,铬(Cr)和钽(Ta)具有单斜结构。
5.其他结构除了上述常见的金属晶体结构外,还存在一些特殊的金属晶体结构。
例如,钻石(C)具有金刚石结构,锌矿石(ZnS)具有闪锌矿结构。
这些结构更加复杂,但仍然是由金属离子有序排列而成的。
总结起来,金属晶体的结构多种多样,常见的包括面心立方结构、体心立方结构和紧密堆积结构。
每种结构都具有不同的特点和性质,这些特点和性质决定了金属的物理、化学性质和用途。
通过研究和了解金属晶体结构,可以更好地理解金属材料的性质和应用。
高中化学竞赛专题辅导(三晶体结构一.(9分下图所示为HgCl 2和不同浓度NH 3-NH 4Cl反应得到的两种含汞的化合物A和B的微观结构重复单元图。
1.写出A、B的化学式和B的生成反应方程式;2.晶体A中,NH 3、Cl的堆积方式是否相同,为什么?3.晶体A中Hg占据什么典型位置,占有率是多少?4.指出B中阴阳离子组成特点;5.比较A和B在水溶液中溶解性的大小。
二.(14分钛酸锶是电子工业的重要原料,与BaTO 3相比,具有电损耗低,色散频率高,对温度、机械应变、直流偏场具有优良稳定性。
因此可用于制备自动调节加热元件、消磁元器件、陶瓷电容器、陶瓷敏感元件等。
制备高纯、超细、均匀SrTiO 3的方法研究日益受到重视。
我国研究者以偏钛酸为原料常压水热法合成纳米钛酸锶,粒子呈球形,粒径分布较均匀,平均22nm。
已知SrTiO 3立方晶胞参数a=390.5pm。
1.写出水热法合成纳米钛酸锶的反应方程式;2.SrTiO 3晶体的结构可看作由Sr 2+和O 2-在一起进行(面心立方最密堆积(ccp,它们的排列有序,没有相互代换的现象(即没有平均原子或统计原子,它们构成两种八面体空隙,一种由O 2-构成,另一种由Sr 2+和O 2-一起构成,Ti 4+只填充在O 2-构成的八面体空隙中。
(1画出该SrTiO 3的一个晶胞(Ti 4+用小球,O 2-用大○球,Sr 2+用大球(2容纳Ti 4+的空隙占据所有八面体空隙的几分之几?(3解释为什么Ti 4+倾向占据这种类型的八面体空隙,而不是占据其他类型的八面体空隙?(4通过计算说明和O 2-进行立方密堆积的是Sr 2+而不是Ti 4+的理由(已知O 2-半径为140pm3.计算22nm(直径粒子的质量,并估算组成原子个数。
三.(10分NH 4Cl为CsCl型结构,晶胞中包含1个NH 4+和1个Cl-,晶胞参数a=387pm。
把等物质的量的NH 4Cl和HgCl 2在密封管中一起加热时,生成NH 4HgCl 3晶体,晶胞参数a=b=419pm、c=794pm(结构如右图。