20160809产品包材改版通知
- 格式:xlsx
- 大小:23.72 MB
- 文档页数:20

1.目的(PURPOSE)规范药品生产所用包装材料的变更管理,确保符合法规要求。
2.适用范围(SCOPE)适用于本公司药品生产所用包装材料和容器的变更,如增加或减少包装及附属物(如药棉、干燥剂)、改变包装材料的材质、尺寸和形状。
3.职责(RESPONSIBILITY)3.1 购销部、固体车间、针剂车间、研发部、质量保证部负责提出变更申请。
3.2 法规注册部负责评估法规对变更要求进行的研究验证工作;递交及跟踪直接接触药品的包装材料变更补充申请。
3.3 研发部负责组织实施变更涉及的研究验证工作;提供试验/验证报告、补充申请所需的药学研究资料。
3.4 各生产车间、质量控制部、质量保证部负责配合研发部进行变更相关的研究验证工作。
3.5 质量保证部负责评估包装材料变更产生的影响,审核变更申请和报告。
3.6 质量副厂长负责变更申请的最终审核和批准。
4.关键词(KEY WORDS)包装材料、变更5.定义(DEFINITION)包装材料——药品包装所用的任何材料和容器,如西林瓶、胶塞、铝塑组合盖、铝箔、复合膜、铝袋、标签、说明书、纸盒、纸箱等。
内包装材料——指任何可能与药品直接接触的包装材料,简称内包材。
在《直接接触药品的包装材料和容器管理办法》(局令第13号)中又称为药包材。
外包装材料——指不与药品直接接触的包装材料,简称外包材。
材质——指用于生产包装材料的物质(如玻璃、高密度聚乙烯树脂、金属等)。
6.程序(PROCEDURE)6.1 变更原则:包装材料确定后,一般不进行变更,以确保产品质量的稳定性和可靠性。
有下列情况的之一的,可以进行变更:➢相关产品质量不稳定,经试验确认原因来自于包装材料;➢包装材料属于落后产品,被国家发文建议停止使用;➢包装材料不符合使用要求;➢替代包装材料能更好地保证产品质量和稳定性,或方便患者使用。
6.2 变更申请6.2.1 当购销部、各生产车间、研发部、质量保证部等部门因各种原因需要变更生产所用包装材料时,应到文档制作室领用填写《包装材料变更申请单》,并说明拟变更情况和理由,经申请部门经理审核确认后,送法规注册部。

附件化学药品新注册分类申报资料要求(试行)第二部分注册分类4、5.2类申报资料要求(试行)一、申报资料项目(一)概要1.药品名称。
2.证明性文件。
2.1注册分类4类证明性文件2.2注册分类5.2类证明性文件3.立题目的与依据。
4.自评估报告。
5.上市许可人信息。
6.原研药品信息。
7.药品说明书、起草说明及相关参考文献。
8.包装、标签设计样稿。
(二)原料药19.(2.3.S,注:括号内为CTD格式的编号,以下同)原料药药学研究信息汇总表。
10.(3.2.S)原料药药学申报资料。
10.1.(3.2.S.1)基本信息10.2.(3.2.S.2)生产信息10.3.(3.2.S.3)特性鉴定10.4.(3.2.S.4)原料药的质量控制10.5.(3.2.S.5)对照品10.6.(3.2.S.6)包装材料和容器10.7.(3.2.S.7)稳定性(三)制剂11. (2.3.P)制剂药学研究信息汇总表。
12.(3.2.P)制剂药学申报资料。
12.1.(3.2.P.1)剂型及产品组成12.2.(3.2.P.2)产品开发12.3.(3.2.P.3)生产信息12.4.(3.2.P.4)原辅料的控制12.5.(3.2.P.5)制剂的质量控制12.6.(3.2.P.6)对照品12.7.(3.2.P.7)稳定性13.(2.4.P)制剂非临床研究信息汇总表。
14. 制剂非临床研究申报资料。
214.1.(4.2.2)药代动力学14.2.(4.2.3)毒理学15. (2.5.P.)制剂临床试验信息汇总表。
16.制剂临床试验申报资料。
16.1.(5.2)临床试验项目汇总表16.2.(5.3)生物等效性试验报告16.2.1.(5.3.1.2.1)空腹生物等效性试验报告16.2.2.(5.3.1.2.2)餐后生物等效性试验报告16.2.3.(5.3.1.4) 方法学验证及生物样品分析报告16.3.(5.3.5.4)其他临床试验报告16.4.(5.4)参考文献二、申报资料项目说明(一)概要部分1.药品名称:包括通用名、化学名、英文名、汉语拼音,并注明其化学结构式、分子量、分子式等。

国家认监委关于发布2016年第三批两项认证认可行业标准的通知
正文:
----------------------------------------------------------------------------------------------------------------------------------------------------
国家认监委关于发布2016年第三批两项认证认可行业标准的通知
国认科〔2016〕60号
各相关认证机构、检验检测机构,研究所、认可中心、认证认可协会:
经审查,现将《食品微生物定量检测的测量不确定度评估指南》和《出口作物类农产品监管链评价要求》等两项认证认可行业标准予以发布。
国家认监委
2016年9月22日
2016年第三批认证认可行业标准目录
序号
标准编号
标准名称
实施日期
1
RB/T151-2016
食品微生物定量检测的测量不确定度评估指南
2017-4-1
2
RB/T152-2016
出口作物类农产品监管链评价要求2017-4-1
——结束——。
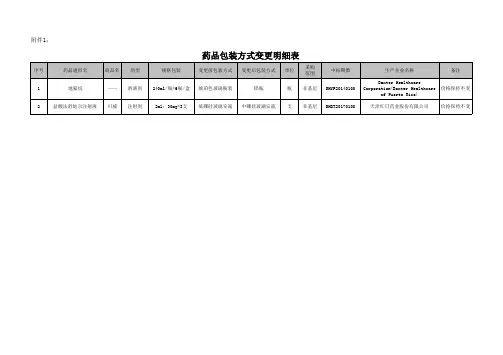


产品包装形式更换通知
应公司销售及生产需求,公司将部分产品作包装形式的更换。
更换的具体内容为:
凡之前涉及的需用打包带打包的产品,即日起更换为统一用公司黄色专用封箱胶带全封四边“工字号”型包装样式。
封箱过程中特别注意“工字号”的平整度,上封口与下封口需要连接到位。
公司弘扬“多劳多得”的计件理念,在增加工序的同时按照对应的标准给予报酬,经公司高层研究决定执行方案如下:
封“工字号”的产品,以件为单位,给予0.03元/件的单价给予支付(含贴合格证和进仓)。
其他不再另行补贴。
特此通知
生产部
2011-9-6
[此文档可自行编辑修改,如有侵权请告知删除,感谢您的支持,我们会努力把内容做得更好]
可编辑范本。

变更直接接触药品的包装材料或者容器申报资料1、目的本指引的制订旨在指导申请人规范药品变更直接接触药品的包装材料或者容器补充申请药学研究资料的撰写,引导申请人关注药品研究的科学性和系统性,提高申报质量。
2、范围适用于《药品注册管理办法》的“药品补充申请注册事项及申报资料要求”第21项:变更直接接触药品的包装材料和容器(除进口药品、国产注射剂、眼用制剂、气雾剂、粉雾剂、喷雾剂及使用新型包材外)注册申请事项;适用于变更直接接触药品的包装材料或者容器(按照国家食品药品监督管理总局办公室关于加强药用玻璃包装注射剂监督管理的通知(食药监办注[2012]132号)。
3、依据3.1《中华人民共和国药品管理法》(中华人民共和国主席令第四十五号)3.2《中华人民共和国药品管理法实施条例》(国务院令第360号)3.3《药品注册管理办法》(国家食品药品监督管理局令第28号)3.4《关于加强药用玻璃包装注射剂监督管理的通知》(食药监办注[2012]132号)3.5《关于印发药品注册现场核查管理规定的通知》(国食药监注[2008]255号)3.6《原料药与药物制剂稳定性试验指导原则》(《中国药典》2010年版二部附录XIX C)3.7《化学药物稳定性研究技术指导原则》(国食药监注[2005]106号)3.8《中药、天然药物稳定性研究技术指导原则》(国食药监注[2006]678号)3.9《中华人民共和国药典》附录3.10《已上市化学药品变更研究的技术指导原则》(国食药监注[2008]242号)3.11《已上市中药变更研究技术指导原则》(国食药监注[2011]472号)3.12《药品包装材料与药物相容性试验指导原则》(YBB00142002)3.13国家其他有关规定4、申报资料的相关要求4.1药品批准证明文件及其附件的复印件包括与申请事项有关的本品各种批准文件,如药品注册批件(或药品再注册批件)、补充申请批件、药品标准颁布件、药品标准修订批件等,并提供药品质量标准、说明书等上述批件的附件。


国家食品药品监管总局公告2016年第108号――关于实施化妆品安全技术规范(2015年版)有关事宜的公告
【法规类别】卫生综合规定
【发文字号】国家食品药品监管总局公告2016年第108号
【发布部门】国家食品药品监督管理总局
【发布日期】2016.05.26
【实施日期】2016.05.26
【时效性】现行有效
【效力级别】XE0303
国家食品药品监管总局公告
(2016年第108号)
关于实施化妆品安全技术规范(2015年版)有关事宜的公告
《化妆品安全技术规范(2015年版)》(食品药品监管总局公告2015年第268号,以下简称《规范》)已于2015年12月23日发布。
为保证《规范》的顺利实施,现就实施《规范》有关事宜公告如下:
一、自2016年12月1日起,禁止生产或进口不符合《规范》规定的化妆品,相关产品可销售至其保质期结束。
其中,仅涉及标签上必须标印的使用条件和注意事项等相关要
求发生改变的,原产品包装可使用至2017年6月30日止,相关产品可销售至其保质期结束。

药品产品更换包装通知范文
为规范公司市场行为,方便对公司产品形象进行统一管理,经开会决定,对药品部分产品包装进行更换。
具体如下:
1、UT-201/2211/等无源转换头采用原彩盒风格新规小包装(规格105*80*35)减小包装体积。
具体包装如下:由原有的包装1变为包装
2、之前包装亚当模块(2506/5209/55等变更用)160*105*55牛皮盒,具体包装如下:由原有的包装1变更为包装2。
3、所有变更后标准包装盒上面印刷xx服务号二维码。
以上所有变更将于通知下发日开始执行,原有库存包装使用完即开始更换,已出售到市面上的产品包装不受影响。
特此公告
xx有限公司
xx月xx8日。

《印刷包装材料设计及改版程序控制图》发布通知通知各部门:为了进一步规范并加强新上市产品包装材料印制及旧产品包装改版的管理,现结合国家政策、我公司现行GMP文件“印刷包装材料设计及改版程序”对有关制度进行重申,望有关部门能够严格执行。
1、新上市产品包装材料印制及旧产品包装改版必须由各承包人或申请变更部门提出书面申请,说明原因或需变更的内容及要求,经销售部经理审核签字,常务副经理或其授权人批准后,书面申请原件存档于质量管理部包装样稿的产生、备案、印制2、各产品承包人提供样稿同时必须标明建议使用的尺寸、材质。
3、所有样稿均应有产品承包人、各审核部门负责人签字认可。
4、各产品承包人均为销售部成员。
附:包装样稿审核流程图质量部2004年9月8日包装样稿审核流程图包装样稿的产生、备案、印制包装样稿的提出按要求修改并确认包装样稿负责:销售部负责:销售部注:样稿须包1份含文字、图案、一式二份尺寸、材质及设计样稿确认后~另外相关说明提供备案样稿一式四份国家相关规定、文字、图案确认进行包装变更文字、图案审核备案手续负责:质量部负责:质量部一式二份 1份尺寸、材质审核尺寸、材质确认负责:生产部负责:生产部供应部注:样稿不符合要求时~供应部返还质量部1份确认包装并联系印刷厂试制注:会签部门为销售、质量、生产及主管经理调研市场成本清样3份并会签会签完毕交质量部、供应部、印刷厂各1份负责:供应部负责:供应部注:提供相关数据注:须经质量部书面确认已备案无误~才能印刷。
预算成本印制负责:财务部负责:供应部1 目的:建立一个印刷包装材料的设计及改版的标准操作程序。
2 范围:公司印刷包装材料的设计及改版的管理。
3 职责:质量部、销售部、生技部、供应部SOP的实施负责。
4 内容:4.1 设计原则:4.1.1 药品的包装标签、说明书应与药品监督管理部门批准的内容相一致。
4.1.2 标签:4.1.2.1 标签印刷内容至少应包括:注册商标、批准文号、品名、产品批号、规格、有效期、生产单位等。
2016年第134号公告附件1.docx
附件1
实行关联审评审批的药包材和药用辅料范
围(试行)
注:
1.高风险药包材一般包括:用于吸入制剂、注射剂、眼用制剂的药包材;新材料、新结构、新用途的药包材;国家食品药品监督管理总局根据监测数据特别要求监管的药包材。
2.鼓励按照包装系统进行申请,如果因为一些技术原因不能按照完整的包装系统进行申请,也可以按照包装组件进行申请。
第二部分药用辅料
一、境内外上市制剂中未使用过的药用辅料;
二、境外上市制剂中已使用而在境内上市制剂中未使用过的药用辅料;
三、境内上市制剂中已使用,未获得批准证明文件或核准编号的药用辅料;
四、已获得批准证明文件或核准编号的药用辅料改变给药途径或提高使用限量;
五、国家食品药品监督管理总局规定的其他药用辅料。
注:
1.高风险药用辅料一般包括:动物源或人源的药用辅料;用于吸入制剂、注射剂、眼用制剂的药用辅料;国家食品药品监督管理总局根据监测数据特别要求监管的药用辅料。
境内外上市制剂中未使用过的药用辅料按照高风险药用辅料进行管理。
2.已在批准上市的药品中长期使用,且用于局部经皮或口服途径风险较低的辅料,如矫味剂、甜味剂、香精、色素等执行相应行业标准,不纳入本目录。
产品包装变更说明精选
文档
TTMS system office room 【TTMS16H-TTMS2A-TTMS8Q8-
外包装系统化升级通知
----暨中国云试剂平台系列产品新包装上市通知
尊敬的用户:
首先再次感激广大用户对乔科系列品牌产品一如既往的支持与厚爱!
化学试剂或关联产品的品类品种包罗万象,目前市面多达十几万种!而做为行业领先的品牌试剂一站式易购平台---中国云试剂平台,体系内商品自然纷繁复杂!
现为更好地进行品牌的宣传与推广,更为能实现交易体验更加快捷系统化,公司在经过多次激烈交流沟通后,特将乔科化学公司目前之包装做统一调整,并同时自2016年3月起,新包装开始陆续面市.具体包装形象见乔科化学官网及
中国云试剂官网相关模块信息报道.
新包装涵盖乔科化学后续出品的多个高性价比品牌产品。
包装形象统一美观大方,同时新增了不少更加人性化的内容,包括包装的材质与印刷质量,以确保公司一直以来所坚持的高标准要求!
为了树立公司更加良好的企业形象,提升品牌效应,并让客户实时了解公司动态,公司一并升级了官方网站、中国云试剂商城及微信公众号,统一化的外包装也增添了相应的网址及二维码,您只要输入网址或扫描二维码便可登录我司官方网站包括商城在内的PC端,触摸屏,移动端,APP等多个切入口!真正实现一站式易购的真实体验!
原乔声品牌外包装形象同时有效,后续停止使用时间请以官方通知为准.
在此,我司保证,外包装变了,但是我们的产品始终如一,符合该产品的质量要求及质量标准,产品生产工艺及质量与既往一致,无任何改动。
改善无止境,今日为起点!给您带来的不便,敬请谅解!
*****
2016年3月18日。
《药包材专项整治工作实施方案》的通知为了加强药品包装材料的专项整治工作,保护患者用药安全,维护公
众健康,我公司决定开展药品包装材料专项整治工作,现将有关事项通知
如下:
一、组织机构
我公司负责组织、协调、密切跟踪和监督有关部门开展药品包装材料
专项整治工作,负责综合组织和协调政策、法规和技术对药包材控制的实
施情况,组建药品包装材料质量监督检测中心;
二、职责设置
(1)组织实施药品包装材料质量监督检测,包括对应用的组合材料、外表标示、催乳剂及添加剂等和安全性进行检测,确保产品质量稳定;
(2)开展药品包装材料的技术和新品种的开发,多渠道推广和推介
优质的药品包装材料和服务;
(3)不断强化药品包装材料质量管理,加强对从事药品包装材料生
产等相关企业的检查,并对符合质量要求的企业给予奖励;
(4)及时宣传药品包装材料的法律法规及风险,对有违法行为的包
装材料经营企业加强管理和监督;
三、工作措施
(1)加强与相关部门的协作,对药包材采购企业管理,强化审核每
一步操作,保证所有药品包装材料安全;
(2)组织包装材料检测,确保材料质量符合标准;。
旧版图片1扬州FA 低聚果糖沙棘茶FA商标yPA013b1081、修改备案号2、“食品方法及用量”改为“食用方法及食用量”3、“本品是以低聚果糖、沙棘粉、红茶粉、柠檬酸、苹果酸、罗汉果甜甙、维生素C、三氯蔗糖、柠檬香精、茶香精、乙基麦芽酚为主要原料制成的保健食品,经动物功能和人体试食试验证明,具有调节肠道菌群的保健功能。
”改为“本品是以低聚果糖、沙棘粉、红茶粉、柠檬酸、苹果酸、罗汉果甜甙、维生素C(抗坏血酸)、三氯蔗糖、柠檬香精、茶香精、乙基麦芽酚为主要原料制成的保健食品,经动物和人体试食功能试验证明,具有调节肠道菌群的保健功能。
”4、主要原料里的维生素C改为维生素C(抗坏血酸)生产日期:20160613批号:162216TPN软管+盖yPB009c1041、修改备案号 2、去掉完美logo右上角“R”生产日期:20160530批号:106016ATPM软管+盖yPB008c1041、修改备案号 2、去掉完美logo右上角“R”生产日期:20160613批号:142216A3中山MLF602双色粉底霜(自然色)MLF602花盒zPD045a2061、喷码位置由侧面改为底部2、修改备案号生产日期:20160608批号:101206-01B4中山MLF603双色粉底霜(深色)MLF603花盒zPD045a3061、喷码位置由侧面改为底部2、修改备案号生产日期:20160608批号:121815-01B尊敬的服务中心负责人,您好:近期,公司有部分产品包材将要改版或已经改版。
此次改版仅针对产品包装,产品内容物不变,详见下表。
请知悉并请相互转告!完美销售室 2016-8-9产品包材改版通知扬州TPP2完美芦荟牙膏套装产品首批生产日期/批号新旧版图片序号产地产品代码产品名称改版包材名称本次新版备案号改版内容5中山MA901玛丽艳俏丽女士香水MA901瓦楞箱zPD033f1061、删除瓦楞箱中文面印制“保质期:五年”中的“五年”2、删除瓦楞箱英文面印制“EXP.DATE:FIVE YEARS”中“FIVE YEARS”3、完美logo红更改为PANTONE201C,地址信息文字更改为黑色4、在顶部增加产品代码5、修改雨滴标示图案生产日期:20160626批号:16050无6中山MA902玛丽艳经典女士香水MA902瓦楞箱zPD035f1051、删除瓦楞箱中文面印制“保质期:五年”中的“五年”2、删除瓦楞箱英文面印制“EXP.DATE:FIVE YEARS”中“FIVE YEARS”3、完美logo红更改为PANTONE201C,地址信息文字更改为黑色。
4、在顶部增加产品代码5、修改雨滴标示图案生产日期:20160627批号:16050无7中山M5033活肤眼霜M5033花盒zPD016a1101、修改备案号2、修改文内容为:“产品标准号:QB/T1857”“生产批号及限期使用日期:见喷码”生产日期:20160619批号:163216-01D8扬州AMPN 完美牌芦荟王浆矿物粉AMPN瓦楞箱yPA023f2061、备案号由yPA023f205修改为yPA023f2062、修改怕雨标志3、英文版面更换为中文版面4、增加最大承受压力:130KG5、完美标志修改为红色,地址信息改为黑色生产日期:20160704批号:1804169扬州FVR09芦荟蔬果洁净剂FVR09标签yPC003b1081、修改备案号 2、修改产品标准号文字内容:由“产品标准号:GB/T 24691”更改为“产品标准号:GB/T 24691 A类,可直接接触食品”生产日期:20160704批号:160416C10中山AMT 完美牌芦荟王浆矿物片AMT瓦楞纸箱zPA024f1031、增加“最大承受压力:100kg”2、英文版面更换为中文版面3、修改怕雨标志4、完美标志修改为PANTONE 201C红色,地址信息改为黑色5、修改备案号生产日期:20160701批号:206216-03A11中山PSG完美牌沙蒜软胶囊PSG商标zPA007b1101、修改备案号;2、“功效成分及含量”改为“功效成份及含量”生产日期:20160626批号:184216-01AFA30花盒zPA013a1101、修改备案号2、“本品是以低聚果糖、沙棘粉、红茶粉、柠檬酸、苹果酸、罗汉果甜甙、维生素C、三氯蔗糖、柠檬香精、茶香精、乙基麦芽酚为主要原料制成的保健食品,经动物功能和人体试食试验证明,具有调节肠道菌群的保健功能。
”改为“本品是以低聚果糖、沙棘粉、红茶粉、柠檬酸、苹果酸、罗汉果甜甙、维生素C(抗坏血酸)、三氯蔗糖、柠檬香精、茶香精、乙基麦芽酚为主要原料制成的保健食品,经动物功能和人体试食试验证明,具有调节肠道菌群的保健功能。
”3、主要原料里的:维生素C改为维生素C(抗坏血酸)生产日期:20160614批号:182216FA30铝膜zPA013d1091、修改备案号2、“本品是以低聚果糖、沙棘粉、红茶粉、柠檬酸、苹果酸、罗汉果甜甙、维生素C、三氯蔗糖、柠檬香精、茶香精、乙基麦芽酚为主要原料制成的保健食品,经动物功能和人体试食试验证明,具有调节肠道菌群的保健功能。
”改为“本品是以低聚果糖、沙棘粉、红茶粉、柠檬酸、苹果酸、罗汉果甜甙、维生素C(抗坏血酸)、三氯蔗糖、柠檬香精、茶香精、乙基麦芽酚为主要原料制成的保健食品,经动物功能和人体试食试验证明,具有调节肠道菌群的保健功能。
”3、主要原料里的:维生素C改为维生素C(抗坏血酸)生产日期:20160614批号:182216-0113扬州AMPN30完美牌芦荟王浆矿物粉AMPN30瓦楞箱yPA023f1041、备案号由yPA023f103修改为yPA023f1042、修改怕雨标志3、英文版面更换为中文版面4、增加最大承受压力:100KG5、完美标志修改为红色,地址信息改为黑色生产日期:20160705批号:101416完美牌低聚果糖沙棘茶(固体饮料)中山12FA3014扬州FD30完美牌高纤乐冲剂FD30瓦楞箱yPA005f1071、备案号由yPA005f106修改为yPA005f1072、修改怕雨标志3、英文版面更换为中文版面4、增加:最大承受压力:100KG5、完美标志修改为PANTONE 201C红色,地址信息改为黑色生产日期:20160706批号:12141615扬州FM30完美高纤餐FM30瓦楞箱yPA002f1071、备案号由yPA002f106修改为yPA002f1072、修改怕雨标志3、英文版面更换为中文版面4、增加:最大承受压力:100KG5、完美标志修改为PANTONE 201C红色,地址信息改为黑色生产日期:20160704批号:10841616中山PSN 完美餐牌肽藻营养粉PSN瓦楞箱yPA008f2081、备案号由yPA008f207修改为yPA008f2082、修改怕雨标志3、英文版面更换为中文版面4、增加:最大承受压力:100KG5、完美标志修改为PANTONE 201C红色,地址信息改为黑色生产日期:20160705批号:101416完美标志修改为PANTONE201C红色,地址信息改为黑色 3、增加:最大承受压力:140kg 4、英文版面更换为中文版面 5、修改怕雨标志批号:180416P银耳芦笋汁ASP标签yPA044b103改变打码方式,增加流水线号生产日期:20160705批号:101416批01A101416批01B银耳芦笋汁ASP花盒yPA044a103改变花盒喷码方式,增加流水线号生产日期:20160705批号:101416批01A101416批01B银耳芦笋汁ASP瓦楞箱——改变瓦楞箱喷码方式,增加流水号生产日期:20160705批号:101416批01A101416批01B17扬州FAPO3完美健康食品礼盒FAPO3瓦楞箱yPE011f1051、修改备案号,备案号由“yPE011f104”改为“yPE011f105” 2、完美标志修改为PANTONE201C红色,地址信息改为黑色 3、增加:最大承受压力:140kg 4、英文版面更换为中文版面 5、修改怕雨标志生产日期:20160711批号:180416P扬州18ASP19扬州FA低聚果糖沙棘茶FA三层裹包式瓦楞箱yPA013f2071、修改备案号2、英文版面换为中文版面3、增加最大承受压力:120KG生产日期:20160712批号:14241620中山MA3041敏感修护面膜MA3041花盒zPD005a1111、修改备案号2、成分后“与上一代配方相比:***”替换为:(升级配方产品)生产日期:20160706批号:106016-182C21中山WP1022金伟连牌WP-102型净水机WP1022瓦楞箱——1、在WP1022外箱上加印“WP1022”字样生产日期:20160707批号:14141622中山MA3032敏感修护乳MA3032花盒zPD003a1121、修改备案号2、成分后“与上一代配方相比:***”替换为:(升级配方产品)生产日期:20160711批号:182216-127D23中山MA5011柔和洁肤乳MA5011花盒zPD006a2081、成分后“与上一代配方相比:***”替换为:(升级配方产品)2、修改前言为:本产品所用原料从法国进口,并严格按其配方及生产工艺制成。
3、修改备案号生产日期:20160707批号:121416-06A24中山MA3021敏感柔肤水MA3021花盒zPD002a1141、修改备案号2、成分后“与上一代配方相比:***”替换为:(升级配方产品)3、引言更改为:“本产品是从德国直接进口主原料,并按其提供的生产工艺配制而成。
”生产日期:20160714批号:182416-01A25中山MA6012清爽洁面乳MA6012花盒zPD011a1111、修改备案号2、成分后“与上一代配方相比:***”替换为:(升级配方产品)生产日期:20160713批号:162416-157B26扬州NB30营养餐NB铝膜yPA003d1091、修改备案号2、【配料】中“麦片、麦精、南瓜粉”改为“复合麦片、麦精(大麦、麦芽)、南瓜粉(南瓜、麦芽糊精)”生产日期:20160718批号:16341627扬州NB30完美营养餐NB30花盒yPA003a1101、修改备案号2、【配料】中“麦片、麦精、南瓜粉、“改为”复合麦片、麦精(大麦、麦芽)、南瓜粉(南瓜、麦芽糊精)、”3、取消QS标志4、“(食品生产许可号)QS321006010853”“改为“生产许可证号:SC10232100300178”生产日期:20160718批号:16341628中山WP101212号颗粒活性炭滤芯2#花盒zPG001a2051、2号单支滤芯花盒已删除“保质期”,更改为喷印,即在生产批号及二维码下喷印“在****年**月**日前开封使用为佳”2、增加“企业通过ISO9001认证生产日期:20160714批号:18241629中山WP101313号颗粒活性炭+KDF滤芯3#花盒zPG001a3061、3号单支滤芯花盒已删除“保质期”,更改为喷印,即在生产批号及二维码下喷印“在****年**月**日前开封使用为佳”2、增加“企业通过ISO9001认证生产日期:20160714批号:182416一生糖套装OLS礼盒zPE023a1101、更改备案号2、生产许可证号:“QS4407 2302 0147”改为“SC13144070400178”3、取消QS标志生产日期:20160717批号:126016-051一生糖套装OLS商标zPA016b1111、更改备案号2、生产许可证号:“QS4407 2302 0147”改为“SC13144070400178”3、取消QS标志生产日期:20160717批号:126016-05131中山M7037美白精华露M7037花盒zPD022a1091、成分后“与上一代配方相比:***”替换为:(升级配方产品)2、修改前言为:本产品所用原料从法国进口,并严格按其配方及生产工艺制成3、修改备案号生产日期:20160720批号:123416-01D32中山MA5041润肤面膜MA5041花盒zPD010a1111、成分后“与上一代配方相比:***”替换为:(升级配方产品)2、修改引言为:本产品所用原料从法国进口,并严格按其配方及生产工艺制成。