肝脏毒理学
- 格式:doc
- 大小:39.50 KB
- 文档页数:2

名词解释1、酶老化(enzyme aging):神经性毒剂中毒后形成的膦酰酶烷氧基上的烷基脱掉,从能被活化的状态变为不能活化的状态。
2、化学复合伤和毒剂混合伤:糜烂性毒剂中毒合并各种创伤,称为糜烂性毒剂复合伤或化学复合伤。
两种糜烂性毒剂混合使用造成的损伤(中毒)称毒剂混合伤。
(化学战剂中毒合并其他损伤称化学复合伤,两种战剂混合使用造成的损伤(中毒)称毒剂混合伤)3、外源性化学物或外源性化合物:是存在于外界环境中,而能被机体接触并进入体内的化学物,它不是人体的组成部分,也不是人体所需的营养成分。
4、化学武器(chemical weapon):是化学战剂、化学弹药及其施放器材的合称。
应用各种兵器,如步枪、各型火炮、火箭或导弹发射架、飞机等将毒剂施放至空间或地面,造成一定的浓度或密度用以攻击敌方,从而发挥其战斗作用。
5、毒物(toxicant):在一定条件下,以较小剂量进入机体就能干扰正常的生化过程或生理功能,引起暂时或永久性的病理改变,甚至危及生命的化学物质。
6、突变(mutation):遗传结构本身的变化及其引起的变异。
7、失能性毒剂:是一类使人暂时丧失战斗能力的化学物质,中毒后主要引起精神活动异常和躯体功能障碍,一般不会造成永久性伤害或死亡。
(按其毒理效应不同,失能剂可分为精神性失能剂和躯体性失能剂。
)8、生物转运与转化:化学毒物在体内的吸收、分布和排泄过程称为生物转运,化学毒物的代谢变化过程称为生物转化。
指外源性化学物质在不同酶系的催化下,发生一系列生物化学反应,物质化学结构发生变化,转变成衍生物及其代谢产物的过程。
9、一般毒性:外源化学物质在一定的剂量、一定的接触时间和一定的接触方式下对实验动物产生综合毒效应的能力称为化学毒物的一般毒性,又称为化学毒物的基础毒性或一般毒性作用。
10、蓄积作用:当化学毒物反复多次给动物染毒,化学毒物进入机体的速度(或总量)超过代谢转化的速度和排泄的速度(或总量)时,化学毒物或其代谢产物就有可能在机体内逐渐增加并贮留,这种现象称为化学毒物的蓄积作用。




第十六章肝脏毒理学卫生毒理学教研室 卫生毒理学教研室徐培渝徐培渝肝脏毒理学(toxicology of the liver)是利用毒理学的基本方法和技术,研究外源化学物对肝的损害作用特点及其机制的学科,它是靶器官毒理学的一个重要研究领域。
主要内容一、肝脏作为毒作用靶器官三、肝对外源化学物的毒性反应与机制三、肝损害所致的生物功能障碍四、化学性肝损伤的检测与评价基础知识•肝结构肝腺泡•肝功能代谢酶人肝脏大鼠肝脏肝损害的程度与类型因素:☻化学物质的种类☻时间长短☻物种差异主要内容一、肝脏作为毒作用靶器官三、肝对外源化学物的毒性反应与机制三、肝损害所致的生物功能障碍四、化学性肝损伤的检测与评价二、肝 毒 物肝毒物(hepatotoxicant):凡是能引起肝损害的化学物质二、肝 毒 物(一)肝毒物的分类(按毒作用机制)�体质依赖性肝毒物�真性肝毒物�直接肝毒物�间接肝毒物二、肝 毒 物(1)体质依赖性肝毒物在具有特异体质(idiosyncrasy)如存在某种遗传特异性或处于某种特殊生理状态的机体中发生毒作用,潜伏期长短不一,其损害作用不易通过动物实验模型复制,亦无剂量依赖性。
多见于药物主要表现:肝细胞坏死与胆汁淤积。
二、肝 毒 物(2)真性肝毒物在接触人群中发生率高,肝损害程度一般有剂量-效应或剂量-反应关系,潜伏期短,造成的肝损害能在动物实验模型中复制。
真性肝毒物可分为- - 直接肝毒物- - 间接肝毒物二、肝 毒 物①直接肝毒物�直接作用于肝细胞膜、细胞器膜或生物大分子的化学毒物;�机制:导致膜脂质过氧化、膜蛋白质变性,最后肝细胞死亡;�例:CCl4、CHCL3、四溴化碳、四氯乙烷、碘仿。
二、肝 毒 物②间接肝毒物�指进入肝细胞内具有干扰细胞酶活性从而导致细胞内物质代谢紊乱的化学毒物或指经代谢转化后其代谢产物能与细胞内生物大分子结合,使细胞功能发生改变的化学毒物;�例:乙硫氨酸、乙醇肝毒物按毒作用机制分类肝毒物类别发生率实验复制剂量依赖性组织学表现毒物实例体质依赖性肝毒物过敏反应低——胆汁瘀积、细胞坏死磺胺、氟烷代谢异常低——胆汁瘀积、细胞坏死异烟碱、异丙嗪真性肝毒物直接肝毒物高++细胞坏死、脂肪变性CCL4、CHCL3间接肝毒物高++脂肪变性、细胞坏死乙硫氨酸、乙醇二、肝 毒 物(二)肝毒物的分类(按毒物的化学性质)�无机肝毒物包括砷、铬、镉、汞、铅、铜及四氯化碳等;�有机肝毒物包括天然毒素如黄曲霉毒素、细菌内毒素和人工合成的医用有机药物与化学物如氯丙嗪、保泰松等。

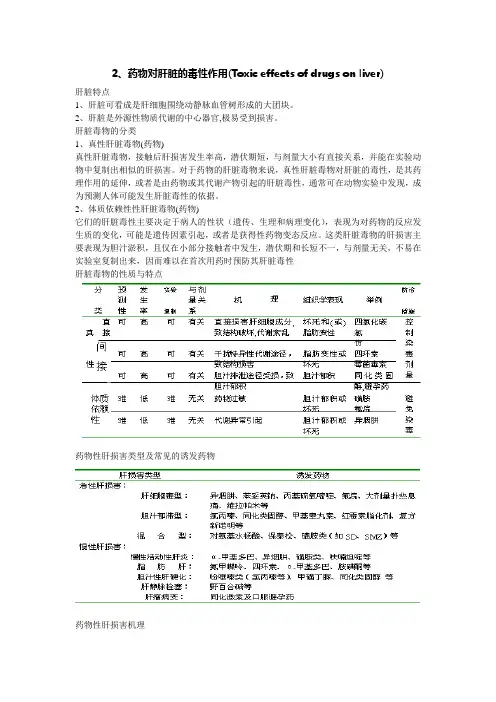
2、药物对肝脏的毒性作用(Toxic effects of drugs on liver)肝脏特点1、肝脏可看成是肝细胞围绕动静脉血管树形成的大团块。
2、肝脏是外源性物质代谢的中心器官,极易受到损害。
肝脏毒物的分类1、真性肝脏毒物(药物)真性肝脏毒物,接触后肝损害发生率高,潜伏期短,与剂量大小有直接关系,并能在实验动物中复制出相似的肝损害。
对于药物的肝脏毒物来说,真性肝脏毒物对肝脏的毒性,是其药理作用的延伸,或者是由药物或其代谢产物引起的肝脏毒性,通常可在动物实验中发现,成为预测人体可能发生肝脏毒性的依据。
2、体质依赖性性肝脏毒物(药物)它们的肝脏毒性主要决定于病人的性状(遗传、生理和病理变化),表现为对药物的反应发生质的变化,可能是遗传因素引起,或者是获得性药物变态反应。
这类肝脏毒物的肝损害主要表现为胆汁淤积,且仅在小部分接触者中发生,潜伏期和长短不一,与剂量无关,不易在实验室复制出来,因而难以在首次用药时预防其肝脏毒性肝脏毒物的性质与特点药物性肝损害类型及常见的诱发药物药物性肝损害机理1、肝细胞毒作用药物肝细胞毒作用,是指某些药物本身具有原浆毒性质,通过干扰肝细胞正常代谢,或抑制酶的活性,或阻滞胆汁分泌,损害肝脏。
其肝损害严重程度与用药量有关,且潜伏期短,发病率高。
/2、特异体质性反应特异体质性反应,包括药物过敏反应引起的肝损害和机体对药物异常代谢引起的肝损害,其病变程度与用药量无关,潜伏期长,发病率低。
肝损害的类型肝坏死脂肪肝胆汁淤积纤维化及肝硬变慢性坏死性肝炎(一)肝坏死坏死(necrosis)是指一个或多个细胞或组织器官的一部分由于不可逆的损害引起的病理性死亡。
许多肝脏毒物能引起肝坏死,根据其范围及严重程度可分为局部性和弥漫性,局部性多见。
⏹多数引起肝小叶中央区坏死,如对乙酰氨基酚(扑热息痛)即可引起;⏹有些也可出现在中间区,如大剂量利尿药呋噻米可引起大鼠肝小叶中间区坏死;⏹少数可引起周边区坏死,如硫酸亚铁。

毒理学的名词解释|有哪些分类毒理学的名词解释:毒理学(toxicology)是一门研究外源因素(化学、物理、生物因素)对生物系统的有害作用的应用学科。
是一门研究化学物质对生物体的毒性反应、严重程度、发生频率和毒性作用机制的科学,也是对毒性作用进行定性和定量评价的科学。
是预测其对人体和生态环境的危害,为确定安全限值和采取防治措施提供科学依据的一门学科。
毒理学的分类:从研究内容上可分为:描述性毒理学、机制性毒理学和管理毒理学(也有称为法规毒理学)三部分。
从依照标准学科划分可分为:法医毒理学、临床毒理学、管理毒理学或法规毒理学、研究毒理学等。
从应用毒理学可分为:食品毒理学、工业毒理学、农药毒理学、军事毒理学、放射毒理学、环境毒理学、生态毒理学等分支。
从研究对象可分为:昆虫毒理学、兽医毒理学、人体毒理学和植物毒理学。
从研究领域可分为:药物毒理学、环境毒理学、食品毒理学、工业毒理学、临床毒理学、法医毒理学、分析毒理学、军事毒理学、管理毒理学等。
从研究的靶器官或系统可分为:器官毒理学、肝脏毒理学、肾脏毒理学、眼毒理学、耳毒理学、神经毒理学、生殖毒理学、免疫毒理学等。
毒理学的作用:目前公认的毒理学定义是研究外源性化学物质对生物体的危害的科学。
由于毒理学的研究目的是为保护生物体的健康或安全提供科学依据的一门学科,因此从学科性质上毒理学属于预防医学,贯穿了预防为主的思想。
由于毒理学的研究对象广泛,包括化学因素、物理因素、生物因素,而生物体包括人、动物、植物,因此毒理学与药理学、生理学、病理学、化学、生物化学、生物学有联系;与工业、农业、经济有联系;与法医学、临床医学、生态学及环境保护有联系;可以说,它与地球上生命的整个未来有联系。
因而,毒理学在临床医学、药学、环境保护、动物学、优生优育、职业劳动保护和食品卫生等领域中均有广泛用途。
也因此毒理学的分类非常复杂,可从不同角度分类,并不完全一致。

毒理名词解释大全毒理学是一门研究毒物对生物体产生的影响的科学。
毒物是指那些会对生物体产生有害作用的物质,包括化学物质、放射性物质、生物毒素等。
在毒理学中,有一些特殊的术语和名词,下面是一份毒理名词解释大全。
1. 毒性(Toxicity):指毒物对生物体的伤害程度。
毒性可以分为急性毒性和慢性毒性。
急性毒性指短期接触或者一次给药所引起的毒性反应,而慢性毒性则是长期暴露于毒物所产生的毒性反应。
2. 毒理作用(Toxicokinetics):指毒物在生物体内的吸收、分布、代谢和排泄的过程。
了解毒物的毒理作用有助于研究其对生物体的影响和毒性机制。
3. 毒理代谢(Toxicant metabolism):毒物在生物体内被代谢的过程。
毒理代谢可以将毒物转化为更容易被排出体外的代谢产物,也可以转化为更具毒性的代谢产物。
4. 毒物动力学(Pharmacokinetics):研究毒物在体内的吸收、分布、代谢和排泄的过程。
毒物动力学有助于揭示毒物与生物体之间的相互作用机制。
5. 毒物相互作用(Toxicant interaction):当两种或更多的毒物同时存在时,它们可能会产生相互增强或者相互抵消的效应。
毒物相互作用的研究对毒物的风险评估和预防具有重要意义。
6. LD50:半数致死剂量(Lethal Dose 50)的缩写,表示在实验条件下,给予一定数量的动物致死的毒物剂量。
7. NOAEL:无观察不良效应水平(No-Observed-Adverse-Effect Level)的缩写,表示在实验条件下,最高剂量或浓度下无毒性反应。
8. 毒作用靶标(Target organ):指毒物在生物体内作用的特定器官或组织。
毒物可以对多个器官产生毒性影响,也可以对特定器官产生选择性毒性。
9. 突变原性(Mutagenicity):指物质对DNA或染色体的遗传物质造成突变的能力。
突变原性是评估物质是否具有致癌风险的重要指标。
10. 致癌性(Carcinogenicity):指物质对生物体产生致癌作用的能力。

药物对肝脏的毒理作用一.研究目的毒理学是一门研究外源性毒物对生物体的毒性作用的学科,而作为人体重要解毒排毒的器官,肝脏当然是毒理学研究的一个重点。
二.肝脏结构肝脏是身体内以代谢功能为主的一个器官,并在身体里面扮演着去氧化,储存肝糖,分泌性蛋白质的合成等等。
肝脏也制造消化系统中之胆汁。
在医学用字上,常以拉丁语字首hepato-或hepatic来描述肝脏。
肝脏是人体内脏里最大的器官,位于人体中的腹部位置,在右侧横隔膜之下,位于胆囊之前端且于右边肾脏的前方,胃的上方。
肝脏是人体消化系统中最大的消化腺,成人肝脏平均重达1.5公斤(约在1-2.5公斤之间;另一说1-1.6公斤),为一红棕色的V 字形器官。
肝脏又是新陈代谢的重要器官三.肝脏的解毒原理肝脏常为毒物作用的靶器官,大多数毒物经胃肠道吸收进入机体后循门静脉携入肝脏。
肝脏有高密度的结合点,该处外源性物质代谢酶的浓度较高,它使多数毒物降低毒性,且更易水溶,而有利于排出,但在一些毒物可被活化而毒力加强,可致肝产生局部损伤。
肝损伤常发生在小叶中央,因该处细胞色素P4 o较高,而谷胱甘肽浓度却相对较低的缘故。
四.肝脏损伤的类型及引发原因毒物可引起肝脏细胞内不同细胞器的各种毒性作用,出现不同肝脏损伤的类型:1.脂肪肝:指含脂量超过5 肝重的肝脏。
组织化学显示肝内有过着染的脂肪存在。
这种肝损伤可以是急性的,如由乙基硫氨酸、磷、四环索引起的损伤。
一些毒物如四环素在细胞内形成许多小的脂肪滴,而其它化学物如乙醇则可形成大的脂肪滴而将核挤向一侧。
虽然肝脂质沉积是这些毒物作用常见的结局,但形成的机理各异。
最常见的机理可能是肝脏的甘油三醣释放入血的过程发生障碍而致。
因为甘油三酯只有与脂蛋白结合后形成极低密度脂蛋白才能分泌。
引起肝脏脂质堆积的机理如下:①抑制脂蛋白的蛋白部分的合成(四氯化碳;乙基硫氨酸);②阻止甘油三酯与脂蛋白的结合(四氯化碳);③肝细胞缺钾而干扰了VLDL经细胞膜的转运(乙基硫氨酸):④损伤了线粒体氧化脂质的功能(乙醇);⑤抑制VLDL的重要活性成份磷脂的合成(缺乏胆碱和乳清酸);2.肝坏死:肝坏死与肝细胞的死亡有关。
毒理大鼠内脏病理
毒理学研究中,大鼠常被用作实验动物来评估药物、化学物质或其他环境因素对生物体的潜在毒性。
这些研究可能涉及观察和分析大鼠内脏器官的病理变化。
内脏病理变化可能因暴露于不同的毒性物质而异,但通常可能包括以下几种类型的变化:
1. 肝细胞变化:肝细胞可能会出现肥大、功能增强的情况。
这可能是由于药物或化合物引起大鼠肝细胞内质网增生和药物代谢酶(DME)表达上调所导致的。
这些变化可能会导致主要通过肝细胞代谢分解的循环甲状腺激素(如T3、T4)的清除率升高。
2. 甲状腺变化:在某些情况下,大鼠可能会出现甲状腺腺泡细胞肥大或增生的情况。
这可能是由于循环血液中的甲状腺激素降低,从而反馈性引起下丘脑促甲状腺素释放激素(TRH)和垂体促甲状腺激素(TSH)上调所导致的。
值得注意的是,啮齿类动物(如大鼠)缺乏与T4结合的球蛋白(TBG),这使得大鼠甲状腺激素的半衰期相比其他种属而言非常短。
3. 其他内脏器官变化:除了肝脏和甲状腺之外,其他内脏器官如心脏、肾脏、肺等也可能受到毒性物质的影响而发生病理变化。
这些变化可能包括细胞坏死、炎症反应、纤维化等。
需要指出的是,以上所述仅为一些可能的病理变化示例,并不涵盖所有情况。
具体的病理变化取决于毒性物质的种类、暴露剂量
和暴露时间等因素。
在进行毒理学研究时,通常会通过组织病理学检查来详细观察和评估内脏器官的病理变化,并结合其他实验数据和临床表现进行综合分析。
鲶鱼的肝脏毒理学研究引言鲶鱼是一种广泛分布于淡水和咸水中的鱼类,被广泛用作食品来源。
然而,随着环境污染和人类活动的增加,鲶鱼肝脏毒理学研究备受关注。
本文将探讨鲶鱼肝脏的结构、功能以及其对环境污染物的敏感性,以期能够更好地了解鲶鱼肝脏的毒理学反应和保护机制。
1.鲶鱼肝脏的结构和功能鲶鱼肝脏是一个重要的器官,承担着多种功能。
首先,它是脂质代谢和能量储存的关键组织。
鲶鱼肝脏中含有大量的脂类物质,包括甘油三酯、胆固醇等,这些物质在能量不足时能够释放出来,满足鲶鱼的能量需求。
其次,鲶鱼肝脏还参与了解毒作用。
肝脏是体内毒物代谢和解毒的主要场所,通过一系列的代谢酶和化学反应,肝脏能够将有毒物质转化为无毒物质或者进行排泄,保护身体免受毒物的侵害。
鲶鱼肝脏作为重要代谢器官,在这方面起到了至关重要的作用。
2.鲶鱼肝脏对环境污染物的敏感性随着现代社会的发展,环境污染物越来越多地存在于自然环境中。
鲶鱼作为底层食物链的重要成员,其肝脏尤为容易受到环境污染物的影响。
研究表明,鲶鱼肝脏对金属污染物、有机污染物以及其他化学物质的敏感性较高。
首先,鲶鱼肝脏对金属污染物的敏感性很高。
金属污染物,如汞、铅等,通过进食或者直接吸收进入鲶鱼体内,由于肝脏是代谢和解毒的主要场所,因此污染金属会在肝脏中积累,并导致肝脏损伤。
研究发现,汞等金属污染物可以影响鲶鱼肝脏的结构和功能,甚至导致肝脏病变。
其次,鲶鱼肝脏对有机污染物的敏感性也很高。
有机污染物,如多氯联苯(PCBs)、氯化汞等,往往通过食物链逐级积累至鲶鱼体内。
这些有机污染物在鲶鱼肝脏中容易引起氧化应激反应,并且可能对肝脏组织结构和代谢功能产生不可逆的影响。
研究表明,有机污染物的长期暴露与鲶鱼肝脏肿瘤的发生有关。
最后,鲶鱼肝脏对其他化学物质的敏感性也受到关注。
如饲料添加剂、抗生素等,这些物质通过饵料进入鲶鱼体内,会积累在肝脏中并产生潜在的毒理作用。
因此,在鲶鱼养殖和捕捞过程中,应注意合理使用这些化学物质,以减少其对鲶鱼肝脏的潜在损害。
heparg细胞肝脏不仅是外源化合物吸收、消化、代谢的场所,也是体内一些必需物质的吸收、贮存、代谢的器官。
由于外源性化合物体内代谢过程中可致肝脏损伤,因此肝脏也是毒理学研究的主要器官之一。
因遗传、环境及病理生理的不同,外源性化合物在不同种属和同一种属的不同个体间的代谢存在差异,故以动物试验来验证药物的肝毒性有时会出现与人体内迥异的状况,需寻找适合于体外肝毒性研究的体外肝细胞模型。
此外,人肝细胞虽可长期冻存,但冻存复苏后的肝标志性的生物学活性会受到影响。
HepaG2 缺乏肝标志性的生物学活性,CYP 相关酶系诱导表达量少,即使采取质粒转染 CYP 酶或肝特异性转录因子的方式,转染的细胞株也不适合研究正常肝细胞的基因表达调控。
尽管原代人肝细胞在运用中受限颇多,但它仍然是体外研究化合物代谢和药物毒性的细胞模型的金标准。
人肝细胞株——HepaRG 细胞,是从慢性丙型肝炎病毒感染的肝癌患者体内非瘤组织分离而得的细胞株,能表现人肝细胞的大多数功能,包括药物代谢所涉及的主要 CYP 酶系。
本文对 HepaRG 细胞的生长形态、与药物代谢、毒理学相关的特性和应用综述如下:一、生长形态学特性HepaRG 细胞有其独特生物学特性:低密度接种时(2.6x104 个细胞/cm2),起初表现为狭长的未分化形态,1周内缓慢融合,积极分化形成两种不同形态学特征的细胞:一种为准肝细胞样的粒状上皮细胞,另一种仍为扁平的胞质透明细胞包围前者。
可进一步分化为明显的肝细胞形态和胆管样结构。
未分化的狭长 HepaRG 细胞能表达肝祖细胞的标志,而分化的两种类型细胞能分别表达肝细胞和胆管细胞的生物学标志,其中,肝样细胞占 50%~55% 的增殖水平。
这种从同一祖细胞向肝细胞样和胆管样两种细胞类型分化的特性及其罕见,与既往报道的肝瘤细胞株大不相同,和 25年前用肝细胞和未分化胆管细胞共培养所建立的细胞模型有些相似,且能更长更好的保持肝细胞的肝特异性功能特性。
肝脏毒理学
1.什么是肝脏毒理学和化学性肝损伤?
肝脏毒理学(toxicology of the liver):是利用毒理学的基本方法和技术,研究外源化学物对肝的损害作用特点及其机制的学科,它是靶器官毒理学的一个重要研究领域。
化学性肝损害(chemically induced liver injury):化学物引起的各种急性和慢性肝损害。
短期暴露:肝细胞内脂质蓄积、肝细胞坏死、肝胆功能障碍
长期暴露:肝硬化、瘤样改变
2.为什么肝脏是外源化学物作用的重要靶器官?
a.在机体内肝脏具有特殊的解剖位置、组织结构和生理生化特性。
肝脏最易作为外来化学物的毒作用靶器官。
b.肝脏是一个被血液充盈的器官,与血液循环密切相关,由于肝脏存在两套入肝血管,分别接受来自胃肠道血液与体循环的动脉血液,化学物质无论从何种途径进入机体,均可通过血液循环达到肝脏,尤其从消化道吸收的毒物,在进入血液循环以前毒物首先与肝脏接触。
c.肝脏作为化学毒物的生物转化器官,在一定条件下,化学毒物极易对肝脏造成损害作用,特别是经体内代谢增毒的外源化学物质在肝脏代谢转化后其有毒代谢产物可首先损害肝脏。
d.由胆汁排泄的有毒化学物质或代谢产物,可通过肝-肠循环系统再次进入肝脏发挥毒作用。
3.肝脏对外源性化学物的毒性反应有哪些?
肝脏对外源化学物的毒性反应依赖于化学物性质、受损细胞群种类、接触剂量与方式等。
化学性肝损伤按其损伤发生的快慢可分为急性肝损伤与慢性肝损伤。
急性肝损伤(acute liver injury)一般是短期接触较大剂量肝毒物或肝脏功能不全时接触某种肝毒物引起,病理改变常见于肝细胞坏死、脂肪变性、胆汁淤积等。
慢性肝损伤(chronic liver injury)可因长期接触低剂量肝毒物引起,也可由一次急性坏死引起的后遗症,病理改变包括纤维化、硬变、癌变等。
一.肝细胞死亡(hepatocyte death)
化学毒物引起肝细胞死亡有两种情况:细胞坏死(necrosis);细胞凋亡(apoptosis)二.脂肪变性(steatosis)
三、胆汁淤积(cholestasis)胆汁淤积较脂肪肝和肝坏死少见,它常常是肝脏对化学毒物的一种急性毒性反应,其出现频率较脂肪肝与肝细胞坏死低,有时可傍有轻微的胆道炎症和肝细胞坏死。
红霉素、氯丙嗪、雌激素等可引起。
四、肝窦状隙损害(sinusoidal damage)窦状隙的内腔阻塞或扩张、肝窦内皮细胞壁的进行性损害可影响窦状隙功能的完整性。
达那唑、硫唑嘌呤、氯乙烯砷制剂等可引起。
五、肝纤维化(hepatic fibrosis)与肝硬化(cirrhosis)毒性机制:①肝细胞坏死后,细胞被分解、吸收,成纤维细胞增生,合成胶原增多,胶原沉积形成纤维化②激活Ito细胞,胶原合成增多③肝星形细胞被活化,导致细胞外基质合成增多,收缩力增强,纤维化介质分泌。
六、肝癌变(hepatocarcinogenesis)
毒性机制:①毒物及其代谢产物对生物大分子(DNA)造成损害②与生物大分子共价结合③活化肝细胞癌基因④抑制肝细胞抑癌基因
4.化学毒物诱导肝细胞死亡的可能机制有哪些?
化学毒物引起肝细胞死亡的可能机制有:①肝细胞膜脂质过氧化,如CCl4等化学毒物在细胞色素P-450系统作用下,产生三氯甲烷自由基,后者可使细胞质膜或亚细胞结构膜脂质发生过氧化,引起膜通透性增加,最终导致细胞死亡。
②毒物及其代谢产物与生物大分子发生结合,使生物大分子功能丧失,导致细胞死亡。
③损伤肝细胞线粒体,影响肝细胞呼吸链中酶蛋白的合成,导致肝细胞呼吸链中酶蛋白的合成发生障碍,肝细胞内呼吸停止,细胞死亡。
④细胞骨架损伤,细胞膜通透性改变,钙稳态失调,引起肝细胞死亡。
5.化学毒物引起肝脂肪变性的机制有哪些?
①脂肪酸氧化减少;如四氯化碳②甘油三酯合成增加;如异丙嗪、巴比妥类③运脂蛋白合成减少,如四环素、甲氨蝶呤等能抑制运脂蛋白的合成,从而使甘油三酯从肝细胞排出减少,导致脂肪变性;④肝外游离脂肪酸入肝过多,如DDT、尼古丁、肼类等化学毒物可通过刺激垂体-肾上腺,导致脂肪组织释放游离脂肪酸过多地进入肝脏。
6.引起胆汁淤积的作用机制有哪些?
①损伤肝细胞膜的功能;②胆管壁上皮细胞通透性降低,使胆汁流降低,发生胆汁淤积;③化学物在胆管内沉淀,胆栓形成,阻塞胆管,胆汁排泄障碍,胆汁淤积。
7.实验性肝损伤的体内试验检测方法有哪些?具体内容是什么?
肝损伤的体内试验评价(evaluation of hepatic injury in vivo)采用整体动物试验。
整体动物试验由于能较为全面反映化学毒物对人体的毒作用,并能长期动态观察生物机体对毒物的反应,故可用于肝脏毒物的危险度评价。
(一)实验动物:在肝脏毒理学实验中,不论是急性或慢性动物实验或化学性肝损伤动物模型试验,最常用的受试动物为大鼠和小鼠,其次为仓鼠、豚鼠、兔、狗等。
(二)染毒途径:动物染毒应尽量选择与人接触化学毒物相同的途径。
常用腹腔注射与经口途径染毒等。
1 血清酶学检测:肝脏损伤时血清中许多酶的活性异常。
其基本的原理在于肝损伤时,肝酶(hepatic enzymes)释放到血液中。
因此,检测血液肝酶的活性是目前肝脏毒性研究中最有用的工具之一。
根据血清酶对不同类型肝脏损伤的特殊性与敏感性,可将血清酶分为四组(表4):
●第一组酶在血清中活性增高能较好地反映胆汁淤积型肝损伤,
●第二组酶能敏感地反映细胞毒性肝损伤,根据酶在其他部位的存在它可被进一步分为三类:
◆A类为肝内外组织细胞均可存在,
◆B类主要存在于肝脏,
◆C类几乎只存在于肝脏内。
●第三组酶对肝损伤相对不敏感,而对肝外器官组织细胞损伤敏感,如肌酐磷酸激酶(CPK)。
●第四组酶与前三种酶相反,肝细胞损伤时酶活性降低,如胆碱酯酶(ChE)。
2 肝脏排泄功能检测:进入体循环的化学物质可经肝脏以原形或者在肝细胞内转化后排泄。
根据胆汁/血浆浓度比可将随胆汁分泌的化合物分为A、B、C三类。
A类物质包括钠、钾、氯离子以及葡萄糖,这些物质的胆汁/血浆浓度比约为1。
B类物质随胆汁分泌的过程涉及多个转运系统即有机酸转运系统如胆红素和BSP的分泌、有机碱转运系统如乙基溴化普鲁卡因酰胺(PAEB)、中性有机分子转运系统如哇巴因。
胆汁/血浆浓度比约为10~1000之间。
C类物质是一些大分子物质,如菊粉、磷脂、粘蛋白和白蛋白,其胆汁/血浆浓度比小于1。
胆汁/血浆浓度比越大的物质越易通过胆汁分泌和排泄。
肝脏排泄功能检测试验:1)血清磺溴酞钠(BSP)排泄试验2)靛青绿(ICG)试验
肝脏化学组成成分改变的检测:化学性肝毒物除了能引起血清酶活性和肝脏分泌排泄功能的改变以外,还可使肝脏化学组成成分的结构和功能发生变化。
因此,检测肝脏化学组成成分的改变可以定量地评价肝脏损伤的程度,并可有利于阐明化学毒物产生肝损伤的机制。
肝脏组织病理学检查:(1)一般检查:整体动物实验结束,解剖受试动物,肉眼观察肝脏颜色和外观,可发现脂肪肝与肝硬化等改变。
肝脏的脏器系数是一个较为敏感的观察指标。
(2)光镜检查:光镜检查是确定肝损害的传统方法。
(3)电镜检查:电镜检查能提供肝细胞早期损伤的形态学改变依据。
8.肝脏的主要生理生化功能有哪些?
肝脏具有多种生理生化功能:
1.它可作为消化腺分泌胆汁促进肠道脂肪和脂质的消化和吸收;
2.它具有内分泌腺作用,能合成清蛋白、纤维蛋白原、凝血酶原以及多种载脂蛋白等,释放入血液,影响和调节机体的各种生理活动
3. 它是体内最大的物质代谢与生物转化器官,体内糖、脂类、蛋白质、维生素、激素等物质代谢主要在肝脏,由于肝脏富含代谢转化酶,它参与许多化学物质包括营养物质、药物与化学毒物的氧化、还原与结合反应过程;
4. 肝内有极其丰富的血窦,是人体内最大的贮血器官之一,血窦内含大量的巨噬细胞,能吞噬和清除血液中的异物。
胚胎期的肝脏有造血功能,正常成年人的肝脏不参与造血,但在某些病理情况下,肝可恢复一定的造血能力。