第六章 难溶强电解质的沉淀
- 格式:ppt
- 大小:650.00 KB
- 文档页数:18


第六章 沉淀—溶解平衡∙教学基本要求∙⑴熟悉难溶电解质的沉淀溶解平衡,掌握标准溶度积常数及其与溶解度间的关系和有 关计算。
⑵掌握溶度积规则,能用溶度积规则判断沉淀的生成和溶解。
熟悉 PH 对难溶金属氢氧 化物和金属硫化物沉淀溶解平衡的影响及有关计算。
熟悉沉淀的配位溶解及其简单计算。
⑶了解分步沉淀和两种沉淀间的转化及有关计算。
∙重点概要∙1.溶度积常数⑴沉淀溶解平衡与溶度积在一定条件下,难溶电解质与其饱和溶液中的相应阴、阳离子之间达到沉淀溶解平衡:A nB m (s) ƒnA m+ (aq) +mB n(aq)沉淀溶解平衡属于多相离子平衡,其标准平衡常数的表达式为:( ) ( ) ( ) mm n sp n m K A B c A c c B c +- éùéù = ëûëû(61)sp K 称为溶度积常数,简称为溶度积。
⑵溶度积与溶解度的关系溶度积和溶解度都可以表示难溶电解质的溶解性,它们之间可以相互换算。
对于同类型的电解质, sp K 小者,其溶解度(以 mol ∙L -1 为单位)也小。
对于不同类型的难溶电解质,不能直接用 sp K 的大小来比较其溶解度的大小,必须通 过计算比较。
⑶溶度积规则对于难溶电解质 A n B m ,通过比较任意状态时的反应商J 与溶度积 sp K 的大小,可以判 断沉淀的生成和溶解,即溶度积规则。
J > sp K ,沉淀从溶液中析出。
J = sp K ,溶液为饱和溶液,系统中有固相(沉淀)存在,溶液与固相相处于平衡状态。
J < sp K ,溶液为不饱和溶液,无沉淀析出;若原来有沉淀,则沉淀溶解。
⑷同离子效应和盐效应在难溶电解质溶液中加入含有系统相同离子的易溶强电解质,可使难溶电解质的溶解 度降低,这种现象称为同离子效应。






《难溶电解质的沉淀溶解平衡》讲义一、什么是难溶电解质的沉淀溶解平衡在一定温度下,当难溶电解质溶于水形成饱和溶液时,溶解速率和沉淀速率相等的状态,就叫做沉淀溶解平衡。
比如说,把一定量的氯化银固体放入水中,氯化银会在水中溶解,同时溶解的银离子和氯离子又会结合生成氯化银沉淀。
开始时,溶解速率较大,沉淀速率较小。
随着时间的推移,溶解的氯化银逐渐增多,溶液中的银离子和氯离子浓度也逐渐增大,沉淀速率就会随之加快。
最终,溶解速率和沉淀速率相等,达到了一种动态平衡。
这就好像是一个拔河比赛,溶解和沉淀两边的力量相等,谁也无法战胜谁。
二、沉淀溶解平衡的特征1、动态平衡沉淀溶解平衡是一种动态平衡,溶解和沉淀这两个过程仍在不断进行,只是速率相等,看起来好像没有变化。
2、等速溶解速率和沉淀速率相等,这是平衡状态的重要标志。
3、定态平衡时,溶液中各离子的浓度保持不变,但不是绝对不变,而是在一定范围内波动。
4、同条件沉淀溶解平衡的建立与温度、浓度等条件有关。
在相同条件下,无论溶液中固体的量有多少,平衡状态下离子的浓度都是一定的。
三、沉淀溶解平衡的表达式以 AgCl 为例,其沉淀溶解平衡的表达式为:AgCl(s) ⇌ Ag+(aq) + Cl(aq)这里的“s”表示固体,“aq”表示在水溶液中。
四、影响沉淀溶解平衡的因素1、内因难溶电解质本身的性质是决定沉淀溶解平衡的主要内因。
不同的难溶电解质在相同条件下溶解度不同,溶解度越小,越难溶解。
2、外因(1)温度大多数难溶电解质的溶解过程是吸热的,升高温度,平衡向溶解的方向移动,溶解度增大;少数难溶电解质的溶解过程是放热的,升高温度,平衡向生成沉淀的方向移动,溶解度减小。
(2)浓度加水稀释,平衡向溶解的方向移动,但溶解度不变。
(3)同离子效应向平衡体系中加入相同的离子,平衡向生成沉淀的方向移动。
例如,在 AgCl 的饱和溶液中加入氯离子,会使平衡向左移动,生成更多的AgCl 沉淀。
(4)化学反应若加入能与体系中某些离子发生反应的物质,平衡会向溶解的方向移动。


关于难溶电解质的沉淀溶解平衡●沉淀溶解平衡与电离平衡的区别:比如氢氧化铁:Fe(OH)3(s)Fe3++3OH-是沉淀溶解平衡;而Fe(OH)3(aq)Fe3++3OH-是电离平衡。
注意括号中的s、aq。
通常,(aq)可以省略不写,而(s)却不能省略不写。
当然,难溶强电解质只有沉淀溶解平衡,没有电离平衡。
●*难溶电解质的溶度积:一定温度下,难溶电解质的饱和溶液中,(难溶电解质的饱和溶液是极易获得的,只要有沉淀,就一定是饱和溶液!!)阳离子的浓度以其化学计量数(在溶解平衡的方程式中)为指数的幂与阴离子的浓度以其化学计量数(在溶解平衡的方程式中)为指数的幂的乘积为一常数,叫做溶度积常数,(不叫离子积常数!)简称为溶度积。
【参见课本p65.】记作Ksp 。
Ksp的几点用法:【以下计算是为了加深对于一些结论的理解,因为计算一般地都很麻烦,估计高考不会出现。
】1、与摩尔溶解度(用难溶电解质的饱和溶液中的溶质的物质的量浓度来表示的溶解度)互相换算。
(当然也可以与每100g水中,最多能够溶解的溶质质量g表示的溶解度继续换算。
)例1:已知常温下,硫酸钡的溶解度为0.000242g/100g水,求硫酸钡的溶度积。
解:先换算为摩尔溶解度。
硫酸钡这类难溶电解质的饱和溶液极稀,密度基本上仍然是1g/mL。
所以100g水形成的溶液认为是0.100L。
0.000242g硫酸钡的物质的量是0.000242g/233g·mol-1=1.039×10-6mol.所以摩尔溶解度为1.039×10-6mol/0.100L=1.039×10-5mol/L.那么,硫酸钡饱和溶液中C(Ba2+)= C(SO42-)=1.039×10-5mol/LKsp (BaSO4)=1.039×10-5×1.039×10-5=1.08×10-10【对于不同类型的难溶电解质,不能直接根据Ksp 的大小,来推断溶解度的大小。
难溶电解质的沉淀溶解平衡【热点思维】【热点释疑】1、怎样判断沉淀能否生成或溶解?通过比较溶度积与非平衡状态下溶液中有关离子浓度幂的乘积——离子积Q c的相对大小,可以判断难溶电解质在给定条件下沉淀生成或溶解的情况:Q c>K sp,溶液有沉淀析出;Q c=K sp,溶液饱和,沉淀的生成与溶解处于平衡状态;Q c<K sp,溶液未饱和,无沉淀析出。
2、如何理解溶度积(K sp)与溶解能力的关系?溶度积(K sp)反映了电解质在水中的溶解能力,对于阴阳离子个数比相同的电解质,K sp的数值越大,难溶电解质在水中的溶解能力越强;但对于阴阳离子个数比不同的电解质,不能通过直接比较K sp数值的大小来判断难溶电解质的溶解能力。
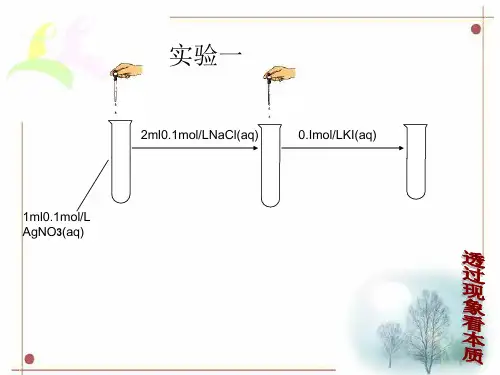
3、沉淀溶解平衡有哪些常考的知识点?沉淀生成的两大应用①分离离子:对于同一类型的难溶电解质,如向含有等浓度的Cl-、Br-、I-的混合溶液中滴加AgNO3溶液,AgCl、AgBr、AgI中溶度积小的物质先析出,溶度积大的物质后析出。
②控制溶液的pH来分离物质,如除去CuCl2中的FeCl3就可向溶液中加入CuO 或Cu(OH)2等物质,将Fe3+转化为Fe(OH)3而除去。
【热点考题】【典例】实验:①0.1 mol·L-1 AgNO3溶液和0.01 mol·L-1 NaCl溶液等体积混合得到浊液a,过滤得到滤液b和白色沉淀c;②向滤液b中滴加0.1 mol·L-1 KI溶液,出现浑浊;③向沉淀c中滴加饱和KI溶液,沉淀变为黄色。
下列分析正确的是()A.通过实验①②证明浊液a中存在沉淀溶解平衡:AgCl(s) Ag+(aq)+Cl-(aq) B.滤液b中不含有Ag+C.③中颜色变化说明AgCl转化为AgID.实验可以证明AgI比AgCl更难溶【答案】C【对点高考】【2014年高考上海卷第11题】向饱和澄清石灰水中加入少量CaC2,充分反应后恢复到原来的温度,所得溶液中()A.c(Ca2+)、c(OH-)均增大B.c(Ca2+)、c(OH-)均保持不变C.c(Ca2+)、c(OH-)均减小D.c(OH-)增大、c(H+)减小【答案】B【解析】试题分析:碳化钙溶于水与水反应生成氢氧化钙和乙炔,反应的化学方程式为CaC2+2H2O→Ca(OH)2+HC≡CH↑。