实验二 凯氏定氮法测定牛奶中蛋白质的含量知识讲解
- 格式:doc
- 大小:18.47 KB
- 文档页数:4
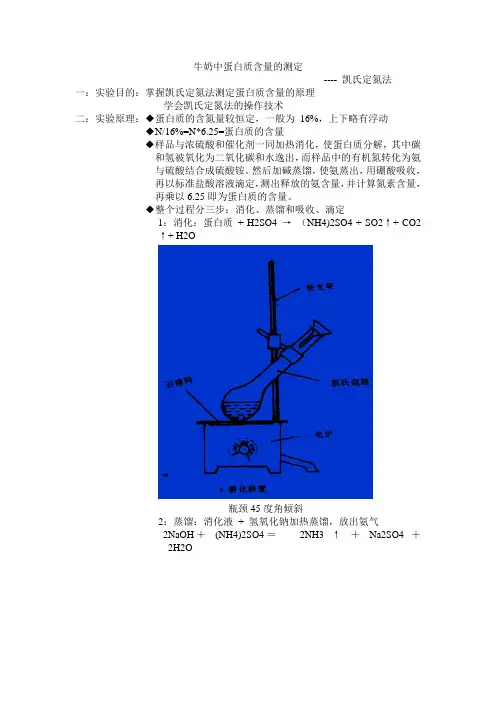
牛奶中蛋白质含量的测定---- 凯氏定氮法一:实验目的:掌握凯氏定氮法测定蛋白质含量的原理学会凯氏定氮法的操作技术二:实验原理:◆蛋白质的含氮量较恒定,一般为16%,上下略有浮动◆N/16%=N*6.25=蛋白质的含量◆样品与浓硫酸和催化剂一同加热消化,使蛋白质分解,其中碳和氢被氧化为二氧化碳和水逸出,而样品中的有机氮转化为氨与硫酸结合成硫酸铵。
然后加碱蒸馏,使氨蒸出,用硼酸吸收,再以标准盐酸溶液滴定,测出释放的氨含量,并计算氮素含量,再乘以6.25即为蛋白质的含量。
◆整个过程分三步:消化、蒸馏和吸收、滴定1:消化:蛋白质+ H2SO4 →(NH4)2SO4 + SO2↑+ CO2↑+ H2O瓶颈45度角倾斜2:蒸馏:消化液+ 氢氧化钠加热蒸馏,放出氨气2NaOH+(NH4)2SO4=2NH3 ↑+Na2SO4 +2H2O3:吸收与滴定(1)用4%硼酸吸收(2)用盐酸标准溶液滴定(3)混合指示剂(甲基红—溴甲基酚绿混合指示剂)指示剂:红色———→绿色———→红色(酸)吸收(碱)滴定(酸)3NH3 + H3BO3→(NH4)3BO3(NH4)3BO3+ 3HCl →3NH4Cl + H3BO3三:实验步骤1、消化:准确量取牛奶0.5mL,移入干燥的凯氏烧瓶中(勿粘附在瓶壁上),加入0.2g硫酸铜、0.3g硫酸钾、10mL浓硫酸,小心摇匀,于通风橱内消化(先小火,待炭化完全后,加大火力至溶液呈蓝绿色),冷却至室温,定容至25mL。
同时消化一份空白试剂为对照。
2、蒸馏、吸收◆取40mL硼酸溶液于锥形瓶中,加2d混合指示剂,置于冷凝管下端,为接受瓶。
◆量取5mL样品消化液由加料口加入反应室,用5mL蒸馏水冲洗加料口,再加入40%NaOH10mL(溶液呈蓝褐色),不要摇动,立即封口。
◆夹紧缓冲管下口,开始蒸馏,当接收瓶溶液颜色变化时,继续蒸馏3-5min,下降接收瓶,使硼酸液面离开冷凝管口,继续蒸馏1min,用蒸馏水淋洗浸入硼酸的管外壁,移出接收瓶,滴定。

实验二_蛋白质含量的测定-凯氏定氮法1一、实验原理蛋白质是生物体内重要的营养成分,因此测定样品中蛋白质含量是生物学领域中的一项基础性工作。
凯氏定氮法是测定蛋白质含量的一种常用方法。
由于蛋白质中氮元素的含量较高,因此凯氏定氮法以氮元素计算蛋白质含量,具有简便、准确、重现性好等特点,广泛应用于蛋白质含量的测定中。
该法的基本原理是:将待测样品中蛋白质水解后,将产生的氨基酸再通过氧化还原反应以生成气态氨,利用碱性铜离子氧化氨生成蓝色化合物,蓝色化合物的浓度与样品中氮的含量成正比,从而计算出样品中蛋白质的含量。
二、实验仪器和试剂1. 仪器:水浴器、移液器、分析天平。
2. 试剂:包括0.1mol/L NaOH、1% CuSO4、1% KNaC4H4O6、1% Na2SO4、 Na2CO3和测定氯离子的盐酸铵铁Ⅲ溶液等。
三、实验步骤1. 准备样品:首先将待测样品去除水分,将10mg的样品放入烘箱中加热到60℃,持续4h使其干燥。
取出后冷却,称取约10mg-20mg样品,转移到干净、干燥的燃烧器中。
2. 水解:加入3ml的6mol/L HCl,进行加热水解。
将燃烧器放到水浴器中,加入适量的水,然后用酒精灯或燃气灯加热至沸腾。
持续水解1h,注意不要使燃烧器干燥,需要时加入适量的水。
3. 去除氨:过滤水解液,将滤液倒入容量瓶中,并加入足量的NaOH溶液,使pH值达到9-10。
再加入10ml的Na2SO4溶液,混匀。
然后将瓶口拔开,将瓶口放在水浴器中并加入适量的NaOH溶液,使瓶内的氨气完全挥发,待液面稳定后用盖子盖好。
4. 确定还原态铜离子的数量:取一定量的0.1mol/L NaOH溶液,加入CuSO4和KNaC4H4O6,混匀后加入约1g的Na2CO3,加水定容,制成标准CuSO4溶液。
5. 滴定:取出约5ml水解液,放入锥形瓶中加清水至刻度线,加入50μl的盐酸铵铁Ⅲ溶液,混匀。
用标准CuSO4溶液滴定至液体颜色由黄变蓝。

凯氏定氮法检测奶粉中蛋白质质量控制及注意事项
凯氏定氮法是一种常用的检测蛋白质含量的方法,也被广泛应用于奶制品行业。
在奶粉生产中,蛋白质的含量是影响奶粉品质的重要因素之一。
因此,采用凯氏定氮法对奶粉中蛋白质含量进行检测和质量控制非常必要。
本文将介绍凯氏定氮法在奶粉中检测蛋白质的应用以及注意事项。
一、凯氏定氮法原理
凯氏定氮法是以蛋白质中的亮氨酸和脯氨酸为基础,通过催化剂作用使蛋白质中的氮原子被氧化成氨,进而转化为氨基氮,再以铜离子为催化剂,将氨基氮还原成亚铜离子。
通过比色法或电位滴定法测定亚铜离子的含量,计算出蛋白质含量。
该方法具有准确、简单、灵敏等特点,被广泛应用于生物化学、食品科学等领域。
二、凯氏定氮法在奶粉中的应用
1. 样品处理要彻底。
奶粉在生产过程中易受到各种污染,应保持样品卫生和细心处理样品。
2. 操作要规范。
操作过程中要注意按操作规程处理,仪器设备要经过严格的校准。
3. 标准品的准备要充分。
标准品的准备要求较高,必须通过标准品验证后再进行蛋白质含量分析。
4. 良好的实验室管理。
合理的实验室布局、管理及仪器设备养护、维护是保持精度可靠性的前提。
5. 实验操作人员要熟练掌握相关技术,具备一定的实验经验和操作技能。
总之,凯氏定氮法是目前奶粉制造工业中广泛采用的一种检测蛋白质含量的方法。
在奶粉制造和质量控制中,准确、快速、准确的测定奶粉中蛋白质含量是保证产品质量的一个重要环节。
同时,操作规范、维护仪器设备、常规检验、标准品准备以及实验室管理都是确保实验结果准确可靠的必要前提。

凯氏定氮法测定食品中蛋白质含量一、目的与要求1.学习凯氏定氮法测定蛋白质的原理2.掌握凯氏定氮法的操作技术,包括样品的消化处理、蒸馏、滴定及蛋白质含量计算等。
二、实验原理蛋白质是含氮的化合物。
食品与浓硫酸和催化剂共同加热消化,使蛋白质分解,产生的氨与硫酸结合生成硫酸铵,留在消化液中,然后加碱蒸馏使氨游离,用硼酸吸收后,再用盐酸标准溶液滴定,根据酸的消耗量乘以蛋白质换算系数,即得蛋白质含量。
因为食品中除蛋白质外,还含有其他含氮物质,所以此蛋白质称为粗蛋白。
三、仪器与试剂1.仪器微量定氮蒸馏装置2.试剂硫酸铜;硫酸钾;硫酸;硼酸溶液(20g/L);氢氧化钠溶液(400g/L);0.01mol/L 盐酸标准溶液;混合指示剂:0.1%甲基红乙醇溶液1份,与0.1%溴甲酚绿乙醇溶液5份临用时混合;黄豆粉四、实验步骤1.样品消化称取大豆粉约1.0g,加入0.2g硫酸铜和3g硫酸钾,移入干燥的100ml凯氏烧瓶中,稍摇匀加入20ml浓硫酸,将瓶置于石棉网上使用电炉,在通风橱中加热消化,开始时用低温加热,待内容物全部炭化,泡沫停止后,再升高温度保持微沸,消化至液体呈蓝绿色澄清透明后,继续加热0.5h,取下放冷,小心加20ml水,放冷后,无损地转移到100ml容量瓶中,加水定容至刻度,混匀备用,即为消化液。
2.定氮装置的检查与洗涤检查微量定氮装置是否装好。
在蒸汽发生瓶内装水约三分之二,加甲基红指示剂数滴及数毫升硫酸,以保持水呈酸性,加入数粒玻璃珠或沸石以防止暴沸。
测定前定氮装置洗涤2~3次:从样品进入口加水适量通入蒸汽煮沸,产生的蒸汽冲洗冷凝管,数分钟后关闭上方的螺旋夹,使反应管中的废液倒吸流到反应室外层,打开下方的夹子由橡皮管排除,如此数次,即可使用。
3.碱化蒸馏量取硼酸试剂20ml于锥形瓶,加入混合指示剂2~3滴,并使冷凝管的下端插入硼酸液面下,在上方螺旋夹关闭,下方夹子开启的状态下,准确吸取10.0ml样品消化液,由小漏斗流入反应室,并以1适量蒸馏水洗涤样口流入反应室,塞紧棒状玻璃塞。

凯氏定氮法检测奶粉中蛋白质质量控制及注意事项凯氏定氮法是一种常用于检测食品中蛋白质含量的方法,它的原理是通过测定样品中的氮含量来间接推断样品中的蛋白质含量。
以下是凯氏定氮法在奶粉中蛋白质质量控制及注意事项方面的相关内容。
奶粉是常见的婴幼儿奶制品,其中的蛋白质含量对于婴儿的健康发育至关重要。
通过凯氏定氮法检测奶粉中的蛋白质含量,可以有效控制奶粉的质量,确保其符合国家标准和婴儿的营养需求。
1. 样品的准备:首先需将奶粉样品充分研磨,以保证样品的均匀性和颗粒的细小化。
2. 氮元素的提取:将研磨后的样品与适量的硫酸和硫酸钠混合,并进行消解(加热),使样品中的有机氮转化为无机氮。
3. 滴定反应:将消解后的样品用硫酸前水稀释稀释,加入硼酸作为缓冲剂,然后滴定加入的标准硝酸钠溶液。
4. 数据计算:用滴定所用标准硝酸钠溶液的体积减去空白对照的滴定体积,得到滴定值。
根据标准曲线或计算公式,将滴定值转化为样品中的蛋白质含量。
1. 样品的选择与保存:应从各个部位采样,以保证样品的代表性。
样品应保存在干燥、密封的容器中,避免阳光直射和潮湿环境。
2. 操作条件的控制:在凯氏定氮法的操作中,控制样品的消解温度、滴定剂的浓度和滴定速度等条件,以免对结果产生干扰。
3. 校准曲线的制备:为了准确反应样品中的蛋白质含量,需要制备标准样品并建立校准曲线。
4. 实验仪器的校准与维护:定期对实验所需的仪器进行校准和维护,以保证仪器的精确度和准确性。
5. 重复测试与结果验证:为了提高结果的可靠性,建议对同一个样品进行多次测试,并与其他方法进行结果验证。
总结:通过凯氏定氮法检测奶粉中的蛋白质含量,可以确保奶粉的质量符合标准和需求。
在进行凯氏定氮法测试时,应注意样品的选择、保存和处理条件的控制,同时要建立校准曲线、校准仪器,并进行结果的重复测试和验证。

凯氏定氮法测定蛋白质的含量一、原理:有机含氮化合物与浓硫酸共热消化,氮转化为氨,再与硫酸结合成硫酸铵。
硫酸铵与强碱反应,放出氨。
将氨蒸馏到过量的标准无机溶液中,再用标准碱溶液进行滴定。
根据测得的氨量,计算样品的总氮量。
二、试剂与材料:浓硫酸、硫酸钾-硫酸铜粉末(称取80g硫酸钾和20g硫酸铜(五水),0.3g二氧化硒研细混合)、30%氢氧化钠溶液、2%硼酸溶液、0.01M标准盐酸、混合指示剂(田氏指示剂)储存液(取50ml0.1%甲烯蓝乙醇溶液与200ml0.1%甲基红溶液混合,储存于棕色瓶中备用。
此指示剂在PH5.2为紫色;PH为5.4为暗灰色或灰色;PH5.6为绿色;变色点为PH5.4)、硼酸-田氏指示剂混合液(100ml2%硼酸溶液,滴加约1ml田氏指示剂,摇匀后,溶液呈紫红色)、蛋白质样品、容量瓶、吸管、凯氏烧瓶、凯氏定氮蒸馏装置、微量滴定管、电炉浓硫酸500ml硫酸钾200g硫酸铜200g硼酸50g盐酸200ml甲基红0.5g溴甲酚绿0.5g三、操作方法1、样品处理:固体样品,应在105℃干燥至恒重。
液体样品可直接吸取一定量,也可经适当稀释后,吸取一定量进行测定,使每一样品的含氮量在0.2-1.0mg范围内。
2、消化:取一定量样品,于50ml干燥的凯氏烧瓶内。
加入300mg硫酸钾-硫酸铜混合粉末,再加入3ml浓硫酸。
用电炉加热,在通风厨中消化,瓶口加一小漏斗。
先以文火加热,避免泡沫飞溅,不能让泡沫上升到瓶颈,待泡沫停止发生后,加强火保持瓶内液体沸腾。
时常转动烧瓶使样品全部消化完全,直至消化液清澈透明。
另取凯氏瓶一个,不加样品,其它操作相同,作为空白试验,用以测定试剂中可能含有的微量含氮物质,以对样品进行校正。
3、蒸馏:将微量凯氏蒸馏装置洗涤(先用水蒸气洗涤)干净。
将凯氏烧瓶中的消化液冷却后,全部转入100ml的容量瓶,用蒸馏水定容至刻度。
吸取20ml稀释消化液,置于蒸馏装置的反应室中,加入10ml30%氢氧化钠溶液,将玻璃塞塞紧,于漏斗中加一些蒸馏水,作为水封。

凯氏定氮法测定蛋白质含量简介凯氏定氮法(Kjeldahl method)是一种常用的测定蛋白质含量的方法,它通过将样品中的有机氮转化为氨,然后将氨转化为氨基氮,再由氨基氮计算得出蛋白质的含量。
这个方法的优点是稳定可靠,适用于各种类型的样品。
实验原理凯氏定氮法的实验原理如下:1.样品预处理:将待测样品进行预处理,去除样品中的非氮有机物。
这样可以确保凯氏定氮方法只测定到蛋白质中的氮。
2.消化反应:将预处理后的样品与硫酸相结合,加热至沸腾。
在这个过程中,有机氮将被转化为氨。
3.碱化反应:将消化后的样品中的硫酸中和,加入过量的氢氧化钠溶液,使样品呈碱性。
4.蒸馏捕收:将碱化后的样品进行蒸馏,捕集捕集样品中的氨。
5.滴定:将捕集到的氨溶液与酸反应,使用盐酸或硫酸等强酸进行滴定,直至中和反应结束,测定出反应过程中消耗的酸的体积。
6.计算:根据滴定所消耗的酸的体积,计算出样品中的氨的量,再根据氨和蛋白质含氮的摩尔比例,计算出样品中蛋白质的含量。
实验步骤以下是凯氏定氮法测定蛋白质含量的实验步骤:1.准备样品:根据实验需要,准备待测样品。
样品的选择应根据实验目的和样品的特性进行。
2.样品预处理:将样品经过细碎、研磨等处理,去除样品中的非氮有机物。
3.消化反应:将预处理后的样品与浓硫酸相结合,加热至沸腾。
消化时间一般为2小时。
4.碱化反应:将消化后的样品中的硫酸中和,加入过量的氢氧化钠溶液,使样品呈碱性。
5.蒸馏捕收:将碱化后的样品进行蒸馏,捕集捕集样品中的氨。
6.滴定:将捕集到的氨溶液与酸反应,使用盐酸或硫酸等强酸进行滴定,直至中和反应结束。
7.计算:根据滴定所消耗的酸的体积,计算出样品中的氨的量,再根据氨和蛋白质含氮的摩尔比例,计算出样品中蛋白质的含量。
实验注意事项1.在进行样品消化时,必须控制好加热温度,避免样品的溢出和烧焦。
2.在进行滴定时,应注意控制滴液的速度,避免过量的酸滴入。
3.实验过程中需注意个人安全,避免触及强酸和强碱。

【读者园地】〔文章编号〕100428685(2004)032373202凯氏定氮法测定牛奶中蛋白质的不确定度分析陈辉,刘振林,张忠义(南京市疾病预防控制中心,江苏 210003)〔中图分类号〕R155.5+7 〔文献标识码〕C 采用凯氏定氮法测定消毒牛奶中蛋白质的含量,其测量不确定度来源于样品称量、消化、定容、蒸馏、稀释标准溶液及滴定等过程。
通过对各个不确定度分量的计算合成,找出影响测量不确定度的因素,并对各个不确定度分量进行评估,最终给出样品中蛋白质含量的标准不确定度及扩展不确定度。
1 原理消毒牛奶与硫酸和催化剂一同加热消化,使蛋白质分解的氨与硫酸结合成硫酸铵。
然后加碱蒸馏使氨游离,用硼酸吸收后,再以盐酸标准溶液滴定,根据盐酸的消耗量乘以换算系数,即为蛋白质的含量。
2 测定方法简述取样5g左右消化,消化完全后加入蒸馏水至100m l定容,取5.00m l蒸馏,用0.01m olΠL盐酸标准溶液滴定馏出液至反应终点。
3 测量数学模型 根据公式:X=(V-V0)×C HC L×V10V100×0.014×6.38m×V5V100×100(1)其中:X-样品中蛋白质的含量,gΠ100g;V-样品消耗盐酸标准溶液的体积,ml;V0-试剂空白消耗盐酸标准溶液的体积,ml;C H L-盐酸标准溶液的浓度,m olΠL;V10-用10ml移液管移取盐酸标准溶液的体积,ml;V100-100ml容量瓶的体积,ml;V5-用5ml移液管移取样品消化液的体积,ml;m-样品的质量,g;0.014-1m olΠL盐酸标准溶液1ml相当于氮的克数;6.38-乳制品由氮转化成蛋白质的系数。
由于各分量相互独立,由(1)式得X的相对合成标准不确定度的估算为:u c(X) X =u(rep)rep2+u(V-V0)V-V02+u(C HC L)C HC L2+u(V10)V102+2u(V100)V1002+u(V5)V52+u(m)m2(2)其中:u c(X)-X的合成标准不确定度,gΠ100g;u(rep)-重复实验的标准不确定度;u(V-V0)-样品扣除试剂空白后消耗盐酸标准溶液带来的标准不确定度,ml;u(C HC L)-盐酸标准溶液浓度的标准不确定度,m olΠL;u(V10)-用10ml移液管移取盐酸标准溶液带来的标准不确定度,ml;u(V100)-用100ml容量瓶定容带来的标准不确定度,ml;2--使用两次100ml容量瓶定容;u(V5)-用5ml移液管移取样品消化液带来的标准不确定度,ml;u(m)-样品称量带来的标准不确定度,g。

凯氏定氮法检测奶粉中蛋白质质量控制及注意事项凯氏定氮法是一种常用的方法,用于检测奶粉中蛋白质的质量。
在奶制品行业中,蛋白质是非常重要的营养成分,对于奶粉生产厂家来说,保证奶粉中蛋白质的质量是至关重要的。
对于凯氏定氮法检测奶粉中蛋白质质量控制及注意事项,我们需要做好相关的工作。
我们需要了解凯氏定氮法的原理和步骤。
凯氏定氮法是通过测定样品中氮的含量来间接计算出样品中蛋白质的含量。
其原理是利用硝化亚氮还原为氨氮,然后和酚酞反应生成氧化还原指示剂。
然后利用标准溶液中的已知氨氮含量和还原后的氨氮含量进行对比,计算出蛋白质的含量。
在进行凯氏定氮法检测奶粉中蛋白质质量控制时,我们需要注意以下几点:1. 样品的选取:在进行凯氏定氮法检测时,需要注意样品的选取。
样品应该是代表性的,可以代表整个批次的奶粉产品。
还需注意样品的保存和处理,避免样品受到外界因素的影响。
2. 实验操作规范:在进行实验操作时,需要做好实验记录和实验操作规范。
实验过程中需要准确计量药剂和溶液,避免因为操作不规范导致的误差。
还需要注意实验环境的洁净,避免外界因素的干扰。
3. 标准品的使用:在进行凯氏定氮法检测时,需要使用标准品来建立标准曲线。
标准品的质量和纯度对于结果的准确性是至关重要的。
在使用标准品时,需要仔细核对其相关参数,并严格按照标准操作规范进行使用。
4. 仪器设备的维护和校准:在进行凯氏定氮法检测时,需要保证所使用的仪器设备的良好状态。
仪器设备的维护和校准对于实验结果的准确性有较大影响。
需要定期对仪器设备进行维护,并严格按照标准程序进行校准。
5. 结果的解析和判定:在进行凯氏定氮法检测后,需要对实验结果进行解析和判定。
需要注意的是,实验结果可能受到外界因素的影响,因此需要将实验结果结合其他相关因素综合分析,得出最终的结论。
以上就是关于凯氏定氮法检测奶粉中蛋白质质量控制及注意事项的相关内容。
正确的操作规范和良好的质量控制是保证实验结果准确性的关键。

一、概述蛋白质是生命活动中不可或缺的重要物质,其含量的测定在生物化学研究和食品加工领域具有重要意义。
针对蛋白质含量的测定方法有许多种,其中凯氏定氮法是一种经典且常用的测定方法,本文将就凯氏定氮法测定蛋白质的原理及操作进行详细介绍。
二、凯氏定氮法原理1. 基本原理凯氏定氮法是通过测定样品中氨基氮的含量来间接测定蛋白质含量的方法。
蛋白质是由氨基酸构成的,而氨基酸中含有氮元素,故可以通过测定样品中氮元素的含量来推算出样品中蛋白质的含量。
2. 操作步骤(1)样品的预处理:将待测样品进行适当的预处理,通常是将样品中的有机物燃烧成气体,从而将其中的氮元素转化为氮气。
(2)氮气的收集:收集样品燃烧产生的氮气,通常是通过化学吸收剂的吸收来将氮气纯化。
(3)氮气的测定:将纯化后的氮气进行定量测定,得出氮气的含量。
(4)蛋白质含量的计算:根据氮气的含量,通过一定的计算公式来推算出样品中蛋白质的含量。
三、凯氏定氮法操作注意事项1. 样品的选择选择代表性好的样品进行测定,避免样品中含有其他干扰物质,影响测定结果的准确性。
2. 仪器的使用严格按照仪器的操作说明进行操作,保证测定过程的准确性和精确度。
3. 数据的处理对测定得到的数据进行严格的处理,计算过程中不应出现错误,以确保蛋白质含量的测定结果准确可靠。
四、凯氏定氮法测定蛋白质的优缺点1. 优点(1)测定范围广:凯氏定氮法可以适用于各种类型的样品,包括食品、饲料、生物组织等。
(2)测定结果可靠:经过严格的样品预处理和操作步骤,测定结果具有较高的准确性和精确度。
2. 缺点(1)操作繁琐:凯氏定氮法的操作步骤相对繁琐,需要较长的操作时间。
(2)不适用于含氮杂质的样品:如果样品中含有其他氮元素化合物的干扰物质,则可能影响凯氏定氮法的测定结果。
五、结语凯氏定氮法作为一种经典且常用的蛋白质测定方法,其原理和操作步骤相对简单明了,但需要严格遵守操作规范,以确保测定结果的准确性和可靠性。

凯氏定氮法测定蛋白质含量【凯氏定氮法测定蛋白质含量】引言:蛋白质是生物体中非常重要的一类有机物质,它在细胞结构、代谢调节、酶催化等方面都起到至关重要的作用。
因此,准确测定蛋白质的含量对于研究生物体的生理功能和代谢过程十分重要。
凯氏定氮法是一种常用的测定蛋白质含量的方法,它利用蛋白质中的氮元素与含氮化合物反应,通过测定反应生成物中的氨基氮含量来确定蛋白质的含量。
本文将一步一步地介绍凯氏定氮法测定蛋白质含量的原理、实验步骤以及注意事项。
一、原理:凯氏定氮法的原理基于蛋白质是含有较高比例的氮元素的化合物。
测定蛋白质的含量可以通过测定样品中氨基氮的含量来实现,其中氨基氮与蛋白质的含量呈线性关系。
凯氏定氮法的核心步骤是将蛋白质样品与含有氧化剂的酸溶液一起加热,使蛋白质中的氮元素被氧化转化为氨基氮,然后用氨盐指示剂反应形成带有颜色的化合物,最后通过比色分析来测定蛋白质中氮元素的含量。
二、实验步骤:1. 实验前准备:根据实验需求准备蛋白质样品、凯氏试剂、氨盐指示剂等。
2. 样品制备:将蛋白质样品称取适量,加入酸性溶液中溶解,使其完全溶解。
注意保持溶液的酸性,并避免样品中的氨基酸被过度氧化。
3. 氮元素的氧化:将样品溶液与凯氏试剂混合,在适当的温度下加热,使样品中的氮元素被氧化转化为氨基氮。
反应时间根据样品的性质而定,一般为1-2小时。
4. 反应结束:冷却样品溶液,使其达到室温。
反应结束后,样品中的蛋白质会被转化为氨基氮。
5. 比色分析:将反应溶液与氨盐指示剂进行反应,形成带有颜色的化合物。
然后使用分光光度计测定化合物的吸光值。
通过与标准曲线进行比较,可以确定样品中氨基氮的含量,进而计算出蛋白质的含量。
三、注意事项:1. 样品的选择:样品的选择取决于实验的目的,可以是纯蛋白质样品,也可以是含有蛋白质的复杂混合物。
样品的含量和浓度应该适当,以保证实验结果的准确性。
2. 温度和时间的控制:样品与凯氏试剂的加热温度一般为75-105摄氏度,反应时间根据样品的性质而定。
凯氏定氮法检测奶粉中蛋白质质量控制及注意事项凯氏定氮法是一种常用的分析化学方法,它是测定样品中蛋白质含量的一种准确方法。
在奶粉中,蛋白质是最重要的组分之一,因此,对于奶粉生产厂家来说,凯氏定氮法检测奶粉中蛋白质质量控制是非常重要的。
本文将介绍凯氏定氮法的原理、操作步骤、质量控制及注意事项,以便于生产厂家合理使用和掌握该方法。
一、凯氏定氮法的原理凯氏定氮法是一种测定有机物中氮元素含量的方法。
其原理是将样品中的有机物完全燃烧成气体,然后用化学方法测定氮气中的氮含量,从而计算出原样品中氮元素的含量。
由于蛋白质分子中氮元素的含量非常高,因此,凯氏定氮法可以用来测定蛋白质的含量。
根据凯氏定氮法测定的氮元素含量,可以通过一定的计算方法计算出样品中蛋白质的含量。
总的来说,凯氏定氮法是一种可靠的用来测定样品中蛋白质含量的方法。
二、凯氏定氮法操作步骤凯氏定氮法的具体操作步骤如下:1. 样品的处理首先,需要将奶粉样品中脂肪、碳水化合物等组分除去,以便于准确测定蛋白质含量。
具体方法有以下两种:(1)加入去脂牛奶粉:将样品加入5%的去脂牛奶粉中并充分搅拌,然后检测。
(2)加入乙醇:将样品加入80%乙醇中并充分搅拌,然后离心、除去液体,再用烘干器烘干,最后检测。
2. 样品的燃烧样品需要在燃烧炉中燃烧,使样品中的有机化合物被氧化成氮气。
3. 氮的测定用一定的化学方法测定氮气中的氮含量。
4. 计算蛋白质含量通过计算方法计算出样品中蛋白质的含量。
1. 样品的存储储存奶粉需要避免与空气、氧及水分接触,避免样品变质。
必要时,可以对样品进行干燥过程,以保持样品的原始含量。
2. 样品的前处理减少杂质对检测结果的干扰,按照所选分析方法进行适当样品的处理。
如在凯氏定氮法中,应将奶粉样品中的脂肪、碳水化合物等组分除去。
3. 校准和控制实验误差稳定的标准品和复制实验等方法,最大程度地降低实验误差。
4. 样品量的控制样品量必须保证稳定且符合所选择的方法的要求。
谈凯氏定氮法测定牛乳中蛋白质含量的方法作者:韩昱瑾来源:《科学与财富》2011年第05期[摘要] 牛奶中的含氮的物质最多的是蛋白质,蛋白质含氮量为95%,其中脂肪球膜蛋白质的含量非常少,主要包括乳清蛋白和酪蛋白。
牛奶中的肌酸、嘌呤、尿素、游离氨基酸等也含有少量的非蛋白质氮。
当前我国对牛奶中蛋白质含量的所采用的检测方法是凯氏定氮法。
这种方法具有非常大的优越性,它不但能够准确地检测出蛋白质中的氮含量,也能够有效地给出非蛋白质氮含量的准确数据,这就遏制并杜绝了不法经销商在牛奶中添加三聚氰胺或尿素等物质来制作牛奶中含氮数据的现象发生。
可见,凯氏定氮法测定牛乳中蛋白质含量的方法对规范生产、加强牛奶行业的管理机制都具有特殊的意义。
[关键词] 牛乳蛋白氮测定牛奶中的含氮的物质最多的是蛋白质,蛋白质含氮量为95%,其中脂肪球膜蛋白质的含量非常少,主要包括乳清蛋白和酪蛋白。
牛奶中的肌酸、嘌呤、尿素、游离氨基酸等也含有少量的非蛋白质氮。
当前我国对牛奶中蛋白质含量的所采用的检测方法是凯氏定氮法。
这种方法具有非常大的优越性,它不但能够准确地检测出蛋白质中的氮含量,也能够有效地给出非蛋白质氮含量的准确数据,这就遏制并杜绝了不法经销商在牛奶中添加三聚氰胺或尿素等物质来制作牛奶中含氮数据的现象发生。
可见,凯氏定氮法测定牛乳中蛋白质含量的方法对规范生产、加强牛奶行业的管理机制都具有特殊的意义。
一、材料与方法1、原理牛奶中的蛋白质需要乙醇来进行沉淀,经过离心分离而获得蛋白质的沉淀,这时候蛋白质中所含氮元素经过转化形成了氨,氨与硫酸产生反应生成硫酸氨。
然后加氢氧化钠溶液蒸馏,用硼酸吸收后再以标准盐酸溶液滴定,根据标准盐酸消耗量计算样品中纯蛋白质的含量。
2、所采用的仪器与试剂KDY-04A凯氏定氮仪(金坛市盛蓝仪器制造有限公司);TDL-5-A低速台式大容量离心机(无锡建议实验器材有限公司);FA2004分析天平(上海高精度电子天平生产厂);LNK-882多功能快速消化仪(宜兴市科教仪器研究所);DK-98-1型电热恒温水浴锅(天津泰斯特仪器有限公司)。
凯氏定氮法测定牛奶中的蛋白质含量摘要:为了检测不同品牌牛奶的蛋白含量及与其标注是否相符,本文用凯氏定氮法测定了光明,蒙牛,伊利牛奶中蛋白质的含量,结果发现三种牛奶蛋白含量基本相同目前蛋白质测定最常用的方法是凯氏定氮法。
凯氏定氮法是通过测出样品中的总含氮量再乘以相应的蛋白质系数而求出蛋白质的含量,此法的结果称为粗蛋白质含量。
由于样品中含有少量非蛋白质含氮化合物,如核酸、生物碱、含氮类脂、卟啉以及含氮色素等非蛋白质的含氮化合物,所以凯氏定氮不能分辨蛋白质与其他含氮化合物。
凯氏定氮法是测定总有机氮量较为准确、操作较为简单的方法之一,可用于所有动、植物食品的分析及各种加工食品的分析,可同时测定多个样品,故国内外应用较为普遍,是个经典分析方法。
至今仍被作为标准检验方法。
凯氏定氮法可分为全量法、微量法及经改进后的改良凯氏定氮法。
目前通常以硫酸铜作催化剂的常量、半微量、微量凯氏定氮法样品质量及试剂用量较少,且有一套微量凯氏定氮器,所以选用微量凯氏定氮法介于目前市场售卖的许多产品存在虚假宣传等现象,我们决定检测目前国产牛奶三大品牌的蛋白含量,并作横向和纵向(与其标注)的比较,旨在为消费者选择牛奶品牌时提供参考。
接下来以试验来比较不同品牌牛奶的蛋白含量的大小。
材料与方法1.1实验材料1.1.1实验样品光明牛奶,蒙牛牛奶,伊利牛奶1.1.2试验药品和试剂所有试剂均为分析纯,水为蒸馏水。
硫酸铜、硫酸钾、浓硫酸;2%硼酸溶液:称取10g硼酸溶于500ml蒸馏水中0.1mol/l盐酸标准滴定溶液;混合指示液:0.1%溴甲酚绿酒精溶液5体积和0.2%甲基红酒精溶液1体积混合而成,贮于棕色瓶内1.1.3仪器与设备7支消化管,凯氏定氮仪,消化炉,酸式滴定管1支,量筒,移液管,烧杯,滴管1.2试验方法1.2.1微量凯氏定氮法微量凯氏定氮法的原理:样品与浓硫酸和催化剂一同加热消化,使蛋白质分解。
其中碳和氢被氧化为二氧化碳和水逸出,而样品中的有机氮转化为氨与硫酸结合成硫酸铵。
实验二凯氏定氮法测定牛奶中蛋白质的含实验二凯氏定氮法测定牛奶中蛋白质的含量一、实验目的与要求1. 掌握半微量凯氏定氮法的原理.2. 熟悉利用半微量凯氏定氮法测定干酵母片中蛋白质含量的操作方法.二、实验原理蛋白质是含一定量氮的有机化合物,蛋白质样品在凯氏烧瓶中经过浓H2SO4消化后,有机物炭化生成碳,碳将硫酸复原为了SO2,本身那么变成CO2,SO2使N复原为了NH3,本身那么氧化为了S2O3而消化过程中生成H2, 乂加速了NH3 的形成.在反响过程中,生成的H2O和S2O3溢出,而NH3那么与H2SO4结合成(NH4) 2SO4存在溶液中,参加NaOH并蒸僻,使NH3溢出,用H3PO3吸收后,以标准酸溶液滴定,根据标准酸溶液消耗的量计算样品中的含氮量,从而可以折算出蛋白质含量.三、实验材料、试剂与仪器1. 材料与试剂浓H2SO4、K2SO4、CuSO45H2O、NaOH、HCl、H3PO4、甲基红、乙醇、漠甲酚绿、牛奶、定量滤纸等.40 %NaOH 溶液:40 g NaOH 溶于100 mL 水中;0.05 mol/LHCl标准液:4.2 mL HCl溶丁1000 mL水中,碳酸钠法标定盐酸;2 % H3BO3溶液:H3BO3 2 mL 溶丁100 mL 水中;加速剂:K2SO4 150 g , CuSO4 5H2O 10 g仔细混匀研磨.甲基红一漠甲酚绿混合指示剂:甲基红溶丁乙醇配成0.1 %乙醇溶液,漠甲酚绿溶丁乙醇配成0.5 %乙醇溶液,两种溶液等体积混合,阴凉处保存(保存期三个月以内).2. 仪器消化管、小漏斗、研钵、玻璃珠、酸式滴定管、锥形瓶、天平、凯氏定氮仪等.四、实验方法与步骤1. 样品消化1)牛奶5 mL置丁消化管内,参加加速剂5 g,并沿烧瓶壁缓缓参加20 mL 浓硫酸,参加玻璃珠2~3粒,摇动烧瓶使全部样品浸没丁硫酸.2) 消化管放在消化炉支架上,套上蠹气罩,压下蠹气罩锁住二面拉钩.3) 把支架连同装有试样的消化管一起移至电热炉上保持消化管在电炉中 心,设定温度在420 C 保持消化管中液体连续沸腾,沸酸在瓶颈部下冷凝回 流.待溶液消煮至无微小碳粒、呈蓝绿色时继续消煮 5 min 左右.4) 消化结束,将支架连同消化管一同移回消化管托底上,冷却至室温.注 意,在冷却过程中,蠹气罩必须保持吸气状态(切忌放入冷水中冷却)放置, 预防废气溢出.2. 样品蒸僻1)翻开自来水给水龙头,使自来水经过给水口进入冷凝管.注意水流量以保 证冷凝管起到冷却作用为了止.2) 开总电源开关,待红色指示灯亮起,按一下汽按钮待蒸汽导出管放出蒸 汽,按消除按钮停止加热.3) 在蒸僻导出管托架上,放上已经参加适量(15 mL 左右)的接受液(硼 酸和混合指示剂)的锥形瓶.抬起锥形瓶支架使蒸僻导出管的末端浸入接受液内.4) 在消化完全冷却后的消化管内,逐个参加 10 mL 左右蒸僻水稀释样品.5) 向下压左侧手柄,将消化管套在防溅管密封圈上,稍加旋转使其保持接 口密封,拉下防护罩.6) 按一下蒸汽按钮,开始蒸僻,到时或到量时自动停止.用洗瓶将蒸僻水 冲洗接收,取下锥形瓶.7) 加碱:按一下碱按钮,NaOH 溶液量必须至蒸僻液碱性颜色变黑为了止.3. 滴定与计算吸收氨后的吸收液,用标定后的盐酸溶液进行滴定,溶液由蓝绿色变为了灰 紫色为了滴定终点.式中:V2——样品时消耗酸标准溶液的体积, mL;V1——滴定空白时消耗酸标准溶液的体积, mL;V'——试样消解液蒸僻用体积,mL;V ——样品分解液总体积,mL;C ——酸标准溶液浓度,mol/L;K ——氮换算成粗蛋白质的系数,牛奶为了 ;粗蛋白质ZEC t .14 K 100 %W ---- 样品水平,g;0.0140——氮的毫克当量数.五、思考题1. 能否使用碱溶液进行滴定,应如何设计实验?2. 凯氏定氮法是否适合丁所有含氮化合物的测定?3. 何谓样品消化?在定氮仪的反响室内将发生什么化学反响?。
2009年5月第30卷第5期食品研究与开发沈文,陈均志,代春吉(陕西科技大学化学与化工学院,陕西西安710021)微波消解—凯式定氮法测定牛奶中蛋白质含量基金项目:国家“十五”重大科技专项(2002BA518A17);陕西科技大学B 类科研创新团队资助(SUST -B04)作者简介:沈文(1982—),男(汉),硕士研究生,主要从事药物新型材料及分析检测技术研究。
摘要:建立微波消解—凯式定氮法测定牛奶中蛋白质含量的方法,采用密闭微波消解样品,优化微波消解条件。
方法的相对标准偏差RSD 为1.82%,回收率在98.8%~101.7%之间。
关键词:微波消解;凯式定氮;牛奶;蛋白质DETERMINATION OF PROTEIN CONTENT IN MILK BY MICROWAVE DIGESTION-KJELDAHLSHEN Wen,CHEN Jun-zhi,DAI Chun-ji(College of Chemistry and Chemical engineering ,Shaanxi University of Science &Technology,Xi'an 710021,Shaanxi,China )Abstrac t:A method of microwave digestion -kjeldahl for the determination of protein content in milk was developed.Microwave digestion conditions were optimized.The RSD is 1.82%,the recovery is 98.8%-101.7%.Key words:microwave digestion;kjeldahl;milk;protein凯式定氮法是测定蛋白质含量的法定方法[1],测定结果稳定、准确,但此方法存在消解时间长,使用消解溶剂用量大,易造成环境污染等缺点。
实验二凯氏定氮法测蛋奶定牛白质的含中量
精品文档
实验二凯氏定氮法测定牛奶中蛋白质的含量
一、实验目的与要求
1. 掌握半微量凯氏定氮法的原理。
2. 熟悉利用半微量凯氏定氮法测定干酵母片中蛋白质含量的操作方法。
二、实验原理
蛋白质是含一定量氮的有机化合物,蛋白质样品在凯氏烧瓶中经过浓HSO消化后,有机物炭化生成碳,碳将硫酸还原为SO,本身则变成CO,2422SO使N还原为NH,本身则氧化为SO而消化过程中生成H,又加速了NH332232O和SO溢出,而NH则与HSO结合成H的形成。
在反应过程中,生成的432223)SO存在溶液中,加入NaOH并蒸馏,使NH溢出,用HPO吸收NH(334423后,以标准酸溶
液滴定,根据标准酸溶液消耗的量计算样品中的含氮量,从而可以折算出蛋白质含量。
三、实验材料、试剂与仪器
1. 材料与试剂
SO、KSO、CuSO·5HO、NaOH、HCl、HPO、甲基红、乙醇、H浓44244232溴甲酚绿、牛奶、定量滤纸等。
40 %NaOH 溶液:40 g NaOH 溶于100 mL水中;
0.05 mol/LHCl标准液:4.2 mL HCl 溶于1000 mL 水中,碳酸钠法标定盐酸;
2 % HBO溶液:HBO 2 mL 溶于100 mL 水中;3333SO 150 g ,CuSO·5HO 10 g 仔细混匀研磨。
K加速剂:2442甲基红—溴甲酚绿混合指示剂:甲基红溶于乙醇配成0.1 % 乙醇溶液,溴甲酚绿溶于乙醇配成0.5 % 乙醇溶液,两种溶液等体积混合,阴凉处保存(保存期三个月以内)。
2. 仪器
消化管、小漏斗、研钵、玻璃珠、酸式滴定管、锥形瓶、天平、凯氏定氮仪等。
四、实验方法与步骤
1. 样品消化
1)牛奶5 mL置于消化管内,加入加速剂5 g,并沿烧瓶壁缓缓加入20 mL浓硫酸,加入玻璃珠2~3粒,摇动烧瓶使全部样品浸没于硫酸。
收集于网络,如有侵权请联系管理员删除.
精品文档
2)消化管放在消化炉支架上,套上毒气罩,压下毒气罩锁住二面拉钩。
3)把支架连同装有试样的消化管一起移至电热炉上保持消化管在电炉中心,设定温度在420 ℃保持消化管中液体连续沸腾,沸酸在瓶颈部下冷凝回流。
待溶液消煮至无微小碳粒、呈蓝绿色时继续消煮5 min左右。
4)消化结束,将支架连同消化管一同移回消化管托底上,冷却至室温。
注意,在冷却过程中,毒气罩必须保持吸气状态(切忌放入冷水中冷却)放置,防止废气溢出。
2. 样品蒸馏
1)打开自来水给水龙头,使自来水经过给水口进入冷凝管。
注意水流量以保证冷凝管起到冷却作用为止。
2)开总电源开关,待红色指示灯亮起,按一下汽按钮待蒸汽导出管放出蒸汽,按消除按钮停止加热。
3)在蒸馏导出管托架上,放上已经加入适量(15 mL左右)的接受液(硼酸和混合指示剂)的锥形瓶。
抬起锥形瓶支架使蒸馏导出管的末端浸入接受液内。
4)在消化完全冷却后的消化管内,逐个加入10 mL左右蒸馏水稀释样品。
5)向下压左侧手柄,将消化管套在防溅管密封圈上,稍加旋转使其保持接口密封,拉下防护罩。
6)按一下蒸汽按钮,开始蒸馏,到时或到量时自动停止。
用洗瓶将蒸馏水冲洗接收,取下锥形瓶。
7)加碱:按一下碱按钮,NaOH溶液量必须至蒸馏液碱性颜色变黑为止。
3. 滴定与计算
吸收氨后的吸收液,用标定后的盐酸溶液进行滴定,溶液由蓝绿色变为灰紫
色为滴定终点。
(V?V)?C?0.014?K12粗蛋白质%=?%100'V?W?V
——样品时消耗酸标准溶液的体积,mL;V式中:2V——滴定空白时消耗酸标准溶液的体积,mL;1V'——试样消解液蒸馏用体积,mL;
V——样品分解液总体积,mL;
收集于网络,如有侵权请联系管理员删除.
精品文档
C——酸标准溶液浓度,mol/L;
K——氮换算成粗蛋白质的系数,牛奶为;
W——样品质量,g;
0.0140——氮的毫克当量数。
五、思考题
1. 能否使用碱溶液进行滴定,应如何设计实验?
2. 凯氏定氮法是否适用于所有含氮化合物的测定?
3. 何谓样品消化?在定氮仪的反应室内将发生什么化学反应?
收集于网络,如有侵权请联系管理员删除.精品文档
收集于网络,如有侵权请联系管理员删除.。