葡聚糖凝胶 LH-20使用说明(恒辉)
- 格式:rtf
- 大小:40.99 KB
- 文档页数:2

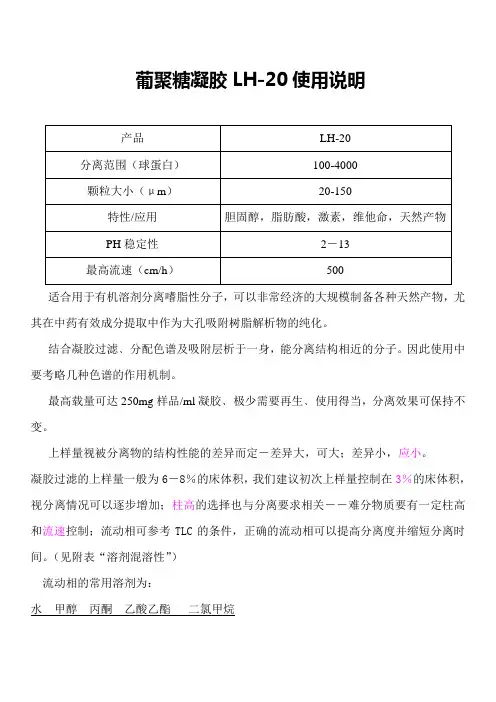
葡聚糖凝胶LH-20使用说明
适合用于有机溶剂分离嗜脂性分子,可以非常经济的大规模制备各种天然产物,尤其在中药有效成分提取中作为大孔吸附树脂解析物的纯化。
结合凝胶过滤﹑分配色谱及吸附层析于一身,能分离结构相近的分子。
因此使用中要考略几种色谱的作用机制。
最高载量可达250mg样品/ml凝胶﹑极少需要再生﹑使用得当,分离效果可保持不变。
上样量视被分离物的结构性能的差异而定-差异大,可大;差异小,应小。
凝胶过滤的上样量一般为6-8%的床体积,我们建议初次上样量控制在3%的床体积,视分离情况可以逐步增加;柱高的选择也与分离要求相关――难分物质要有一定柱高和流速控制;流动相可参考TLC的条件,正确的流动相可以提高分离度并缩短分离时间。
(见附表“溶剂混溶性”)
流动相的常用溶剂为:
水甲醇丙酮乙酸乙酯二氯甲烷
上述溶剂的极性依次降低,对带有极性的被分离物而言,保留值和分离度依次递增;同理选用的凝胶柱高可依次降低,流速可以增大(或上样量可以增加)。
使用方法:将干粉浸泡于60—70%乙醇中过夜(充分搅拌),洗去可能存在的残留物,抽干然后湿态装柱,动态用一倍柱体积的60—70%乙醇淋洗,再用水洗净乙醇即根据自己选用的流动相体系平衡、上样
LH-20在不同溶剂中的溶胀性能:
溶剂混溶性表。

【实验目的】1.掌握葡聚糖凝胶的特性及凝胶层析的原理。
2.学习葡聚糖凝胶层析的基本操作技术。
【实验原理】凝胶层析又称分子排阻层析或凝胶过滤,是以被分离物质的分子量差异为基础的一种层析分离技术,这一技术为纯化蛋白质等生物大分子提供了一种非常温和的分离方法。
层析的固定相载体是凝胶颗粒,目前应用较广的是:具有各种孔径范围的葡聚糖凝胶(Sephadex)和琼脂糖凝胶(Sepharose)。
葡聚糖凝胶是由直链的葡聚糖分子和交联剂3—氯1,2—环氧丙烷交联而成的具有多孔网状结构的高分子化合物。
凝胶颗粒中网孔的大小可通过调节葡聚糖和交联剂的比例来控制,交联度越大,网孔结构越紧密;交联度越小,网孔结构就越疏松,网孔的大小决定了被分离物质能够自由出入凝胶内部的分子量范围。
可分离的分子量范围从几百到几十万不等。
葡聚糖凝胶层析,是使待分离物质通过葡聚糖凝胶层析柱,各个组分由于分子量不相同,在凝胶柱上受到的阻滞作用不同,而在层析柱中以不同的速度移动。
分子量大于允许进入凝胶网孔范围的物质完全被凝胶排阻,不能进入凝胶颗粒内部,阻滞作用小,随着溶剂在凝胶颗粒之间流动,因此流程短,而先流出层析柱;分子量小的物质可完全进入凝胶颗粒的网孔内,阻滞作用大,流程延长,而最后从层析柱中流出。
若被分离物的分子量介于完全排阻和完全进入网孔物质的分子量之间,则在两者之间从柱中流出,由此就可以达到分离目的。
本实验以葡聚糖凝胶G—25作为固定相载体,来分离蓝色葡聚糖—2000和溴酚蓝。
蓝色葡聚糖—2000分子量接近2×106,而溴酚蓝分子量为670,二者分子量相差较大,前者完全排阻,而后者则可完全进入凝胶颗粒网孔内,二者通过层析柱的时间不同而分开。
【实验材料】1.实验器材层析柱(1×20cm)附有一小段乳胶管及螺旋夹;洗脱液瓶(带下口的三角瓶,250m1);试管及试管架;量筒10m1;721型分光光度计2.实验试剂(1) Tris—醋酸缓冲液(pH7.0):取0.0lmol/L Tris溶液(含0.1mol/L KCl)900ml,用浓醋酸调pH至7.0,加蒸馏水至1000m1。

葡聚糖凝胶LH-20使用说明书货号:S8111规格:25g/50g/100g保存:室温存储产品简介:适合用于有机溶剂分离嗜脂性分子,天然产物在有机溶剂中的纯化。
可以非常经济的大规模制备各种天然产物,尤其在中药有效成分提取中作为大孔吸附树脂解析物的纯化。
结合凝胶过滤﹑分配色谱及吸附层析于一身,能分离结构相近的分子,因此使用中要考略几种色谱的作用机制。
最高载量可达250mg样品/ml凝胶﹑极少需要再生﹑使用得当,重复使用分离效果可保持不变。
上样量视被分离物的结构性能的差异而定:差异大,则大;差异小,则小。
凝胶过滤的上样量一般为5-7%的床体积,我们建议初次上样量控制在1-2%的床体积,视分离情况可以逐步增加;柱高的选择也与分离要求相关——难分物质要有一定柱高和流速控制;流动相可参考TLC的条件,正确的流动相可以提高分离度并缩短分离时间。
流动相的常用溶剂为:水、甲醇、丙酮、乙酸乙酯、二氯甲烷。
这些溶剂的极性依次降低,对极性的被分离物而言,保留值和分离度依次递增;同理选用的凝胶柱高可依次降低,流速可以增大(或上样量可以增加,树脂体积在低极性溶剂中明显收缩)。
溶剂的溶解性,极性,沸点,毒性都是要考虑到的,二氯甲烷通常在被分离物质间的极性和碱性差异比较小时采用。
甲醇通常对带环状(包括苯环)物质分离适用,葡聚糖凝胶对环状物质有强烈吸附。
LH-20同时具备亲水和亲脂双重性质,且被分离物质的极性在分离过程中起着重要作用。
使用说明:1葡聚糖凝胶LH-20的原理葡聚糖凝胶LH-20的分离原理主要有两方面:以凝胶过滤作用为主,兼具反相分配的作用(在反相溶剂中)。
因为凝胶过滤作用,所以大分子的化合物保留弱,先被洗脱下来,小分子的化合物保留强,最后出柱。
如果使用反相溶剂洗脱,葡聚糖凝胶LH-20对化合物还起反相分配的作用,所以极性大的化合物保留弱,先被洗脱下来,极性小的化合物保留强,后出柱。
如果使用正相溶剂洗脱,主要靠凝胶过滤作用来分离。

葡聚糖凝胶柱的使用方法:(1) 预处理称取Sephadex G-25(50-100目)约5g,加入蒸馏水100ml,置室温下3h进行溶胀。
(2) 装柱凝胶层析柱的直径与柱长之比一般为1:15。
柱的底部用装有细玻璃管的橡皮塞塞紧,用洗净的玻璃丝(约200目尼龙布)垫底或购买类似规格的商品柱。
然后将柱垂直安装好,先加入1/3柱体积蒸馏水,接着将溶胀好的凝胶边搅匀边连续装入,使它们在柱内自然沉降。
同时大开下口慢速流出蒸馏水。
装柱后的凝胶必须均匀,不能有气泡或明显条纹。
否则,必须到出重装,装好后,用蒸馏水平衡2-3h即可加样品分离。
(3) 加样加样前,首先把柱内凝胶上面多余的蒸馏水放出,直到柱内液面与凝胶表面相齐(或留一极薄液层)为止。
然后,由柱的上端加水解液2ml,注意不要让溶液把凝胶冲松浮起,加完样品后,打开下口缓慢放出液体至液面与凝胶面相齐,再用少量蒸馏水冲洗原来盛样品的容器2-3次,待全部进入层析柱后,即可进行洗脱。
(4) 洗脱与收集洗脱时,用蒸馏水作洗脱剂,并且要连续不断地进行,使凝胶柱上端保持一定的液层,防止凝胶柱表面的液体流干。
本实验洗脱液流出的速度应控制在0.8-1.0ml/min。
洗脱液的收集采用分管连续顺序收集,每管收集3ml,共收集10管。
据经验,4或5号管核苷酸浓度最大,可作为层析鉴定的样品液。
但因层析柱长度的差异,管号会有变化,必要时可用紫外检测A260nm,找出浓度最大的管号。
(5) 凝胶的再生和回收凝胶柱使用一次后,必须反冲疏松一次,平衡后再使用。
若使用数次,就需要再生处理。
用0.1mol/L NaOH-0.5mol/L NaCl溶液浸泡,然后用蒸馏水洗至中性备用。
若实验完毕,将再生后的凝胶在布氏漏斗上用蒸馏水洗涤抽干,再用95%乙醇洗两次,在60℃烘箱中烘干,回收保存。
实验五. 葡聚糖凝胶层析【实验目的】1.掌握葡聚糖凝胶的特性及凝胶层析的原理。
2.学习葡聚糖凝胶层析的基本操作技术。

葡聚糖凝胶柱的使用方法一、准备工作:1.准备好葡聚糖凝胶柱和所需的缓冲液,如PBS(磷酸盐缓冲液)、TBS(三甲基氨基甲烷缓冲液)等。
2.将葡聚糖凝胶柱放入柱层析设备中,并根据设备的要求进行调整和固定。
3.预冲柱层析设备和葡聚糖凝胶柱,以去除可能的污染和杂质。
二、样品处理:1.将待纯化的生物大分子样品先进行预处理,如去除悬浮物、离心沉淀等。
2.将样品溶液以适当的缓冲液进行稀释,以达到最佳的样品浓度和适合葡聚糖凝胶柱操作的样品体积。
三、样品加载:1.将处理好的样品溶液缓慢地倒入柱顶,让样品从柱顶进入柱内。
避免产生气泡。
2.分子在葡聚糖凝胶柱中会根据分子大小和亲疏水性质的不同而发生分离和吸附。
较大分子会在柱上层析,而较小分子会透过凝胶层均匀流出。
因此,样品会在柱内逐渐被分离和纯化。
四、缓冲液流动:1.样品完成加载后,使用适当的缓冲液进行柱洗涤,以洗掉非特异结合的杂质。
2.缓冲液的选择应根据样品的性质而定,具体的选择和流动条件可以参考相关的文献或经验。
五、洗脱纯化:1.在用于洗脱纯化的缓冲液中,调整适当的条件以实现目标分子的洗脱。
如调整pH值、离子浓度、添加洗脱剂等。
2.根据分子的亲疏水性质,选择适当的缓冲液浓度梯度进行洗脱。
一般来说,较强亲疏水性的分子需要更高浓度的洗脱缓冲液。
六、收集洗脱液:1.将洗脱液通过柱底收集,收集不同时间点或不同分析目的的洗脱液。
2.根据实验需要,将洗脱液分为不同部分进行后续的分析或纯化处理。
七、重复使用:1.柱层析后,葡聚糖凝胶柱可以进行再生,以重复使用。
具体的再生方法可以参考柱层析设备和葡聚糖凝胶柱的说明书。
总结:葡聚糖凝胶柱是一种常用的生物大分子纯化方法,通过分子在柱内的分离和纯化来实现样品纯化的目的。
使用葡聚糖凝胶柱时,需要根据样品的特性和需求进行适当的样品处理、缓冲液选择、洗脱纯化条件的优化等。
如操作规范且配合适当的实验条件,葡聚糖凝胶柱可以快速、高效地纯化和富集生物大分子。


葡聚糖凝胶柱使用及注意事项1 Sephadex G型葡聚糖凝胶只适合在水中使用,Sephadex G-25羟丙化后就是Sephadex LH-20。
其既有分子筛作用,在由极性与非极性溶剂组成的溶剂中还有反相层析效果。
虽然价位很高,但由于性能颇佳,可再生利用,所以倍受亲睐。
此外上柱样品损失很少,对处理小样品较好,这也是我们实验室常用的原因之一。
2 Sephadex LH20的原理。
Sephadex LH20的分离原理主要有两方面:以凝胶过滤作用为主,兼具反相分配的作用(在反相溶剂中)。
因为凝胶过滤作用,所以大分子的化合物保留弱,先被洗脱下来,小分子的化合物保留强,最后出柱。
如果使用反相溶剂洗脱,Sephadex LH20对化合物还起反相分配的作用,所以极性大的化合物保留弱,先被洗脱下来,极性小的化合物保留强,后出柱。
如果使用正相溶剂洗脱,这主要靠凝胶过滤作用来分离。
3 Sephadex LH20洗脱溶剂。
看完第2点后,就应该清楚Sephadex LH20洗脱溶剂因分为两类:反相和正相两种。
用得最多的是反相溶剂洗脱,以甲醇--水系统最为常见,先用水,逐渐增加甲醇比例,最后用100%甲醇冲柱。
正相系统以氯仿--甲醇最为常见,先用50%氯仿--甲醇,逐渐增加甲醇比例,最后用100%甲醇冲柱。
4 Sephadex LH20样品的处理和洗脱溶剂的选择。
如果样品极性大,这选用反相溶剂洗脱(甲醇--水),样品用最少体积的甲醇--水(尽可能甲醇少一些)溶解,过滤后,湿法上样(一定要滤喔!要是把Sephadex LH20堵啦,就得将Sephadex LH20的柱头部分弃去,很心痛呀)。
如果样品极性小,这选用正相溶剂洗脱(氯仿--甲醇),样品用最少体积的氯仿--甲醇溶解,过滤后,湿法上样。
5 Sephadex LH-20的步骤。
(1)选择条件:梯度洗脱在Sephadex使用中并不象在正相柱层析中那么重要。
首先你的样品须要能溶解在尽量少量的洗脱剂中。

页眉内容1. Sephadex LH-20简介羟丙基葡聚糖凝胶LH-20是一种Sephadex G-25的羟丙基衍生物,字母LH的含义是这种凝胶骨架在亲脂溶剂中或在水溶剂中都能溶胀。
在G-25分子中引入羟丙基以代替分子中羟基上的氢,葡聚糖凝胶分子的葡萄糖部分将与羟丙基形成醚键连接:R—OH――→R—O—CH2CH2CH2OH与Sephadex G相比,Sephadex LH-20分子中-OH总数虽无改变,但碳原子所占比例却相对增加了,从而使葡聚糖的亲脂性增大。
这种凝胶既有亲水性,又有亲脂性,不仅可在水中应用,也可在极性有机溶剂或它们与水组成的混合溶剂中膨润使用,如丁醇、氯仿、四氢呋喃、二氧六环等,应用范围增大,对黄酮、蒽醌、香豆素等成分也能分离。
SephadexLH-20除保留有Sephadex G-25原有的分子筛特性,可按分子量大小分离物质外,在有极性与非极性溶剂组成的混合溶剂中常常起到反相分配色谱的效果,适用于不同类型有机物的分离,在天然药物分离中得到了越来越广泛的应用。
使用注意事项:羟丙基葡聚糖凝胶Sephadex LH-20虽然是一种两性凝胶,但由于在不同溶剂中的溶胀因子各不相同(见表1),因此在柱中直接更换溶剂是不允许的,床体积在2.5mL /g干胶以下的不能用于GPC分析。
这种凝胶在有机溶剂中分离较小分子量的脂溶性化合物是十分有效的。
但在使用时不允许有氧化剂存在。
再生与保存:Sephadex LH-20价格比较昂贵。
用过的Sephadex LH-20可以反复再生使用,而且柱子的洗脱过程往往就是柱子的再生过程。
短期不用时可以水洗→含水醇洗(醇的浓度逐步递增)→醇洗,最后泡在醇中贮于磨口瓶中备用。
如长期不用时,可在以上处理基础上,减压抽干,再用少量乙醚洗净抽干,室温充分挥散至无醚味后,60~80℃干燥后保存。
Sephadex LH-20不仅具有亲水性能,可以吸水膨胀,而且也有一定的亲脂性,可以吸收有机溶剂而膨胀。

Sephadex LH-20使用说明Sephadex LH-20是由葡聚糖G-25羟丙基化加工而成,属于分子筛凝胶,尤其适用于天然产物在有机溶剂中的纯化。
例如:类固醇、萜类、脂类以及小分子多肽等,Pharmadex LH-20同时适用于分子类别非常相似的物质的分离和工业规模的制备,既可用于初步纯化步骤,也可用于最终精制步骤,如非对映同分异构体的分离。
制备凝胶悬浮液Sephadex LH-20在使用之前必须进行溶胀。
在溶胀的过程中,要尽量避免过分搅拌,否则会破坏球形胶粒,且要避免使用磁力搅拌器。
1.在室温下,将凝胶溶胀于层析溶剂中至少三小时,溶胀后胶体积的大小决定于所使用的溶剂系统,请参考后页之干胶溶胀表计算特定柱体积所需要干胶的量。
2.使溶胀胶体积沉淀之后占总体积的75%,上层溶剂占25%,这时,悬浮液从一个容器倒入另一容器时胶粒可移动。
3.将溶胀后的凝胶根据装柱要求均匀倒入柱内,在保证胶粒不变形的前提下,应在尽可能高的压力下装柱,反压不要超过1.5ba。
平衡上样前,用洗脱液平衡层析柱至少两个柱体积直到基线变得平稳为止,如改变溶剂应该注意凝胶在新溶剂中的溶胀性质,并根据性质确定柱高调节器的位置,如使用相同的溶剂,在以后的层析中柱平衡可以省略。
洗脱液为确保延长层析柱的使用寿命,所有的缓冲液都应该离心或经过0.45um的膜过滤以除去杂质。
样品样品体积应该占柱总体积的1-2%,同样在使用之前样品应该离心或经过0.45um 的膜过滤。
洗脱洗脱流速应根据情况而定,最大张性流速约12cm/min(反压1.5ba),建议流速为1-10cm/h。
总体来说,较低的流速,具有较高的分辩率。
再生凝胶再生通常是先用2-3个柱体积的洗脱液进行清洗,如更换洗脱液,则需要重新平衡。
体积流速与线性流速的关系线性流速=体积流速/横截面积溶胀体积由于Pharmadex LH-20的溶胀体积依赖于溶剂,所以对于不同直径的柱可根据比例增加或减少旧柱体积以便计算出新体积。

葡聚糖凝胶的操作方法
1.将葡聚糖凝胶粉末放入1.5ml离心管中,并加入所需的培养基或溶液(通常是0.1M PBS缓冲液)
2.用紫外灯或消毒灯照射管子和粉末,以杀菌消毒。
3.将管子在室温下静置15分钟,使凝胶充分水解。
4.在使用前,用无菌过滤器或离心管转运转移液体中的小颗粒或杂质。
5.将细胞或材料悬浮在凝胶中,并快速转移和组装需要的实验器具(如培养皿、培养板等)。
6.将实验器具放置在37的恒温箱中,使凝胶在液体中固定并形成3D结构。
7.根据实验的需要,可以选择添加细胞营养物质或生长因子等,以促进细胞的生长和分化。
8.在实验结束后,可以用酶解剂将凝胶中的细胞和材料溶解,并收集并分离细胞和其他成分,进行后续的分析和研究。
葡聚糖凝胶柱使用及注意事项葡聚糖凝胶柱是一种常用的色谱柱,其主要由多糖聚合物构成,具有多孔结构以及极高的比表面积。
葡聚糖凝胶柱在生物分离、蛋白质纯化以及分析等方面有重要的应用。
下面将介绍葡聚糖凝胶柱的使用方法以及注意事项,并列举了几种常见溶剂的溶胀系数作为参考。
使用方法:1.预处理:新柱使用前需进行预处理。
首先,在使用前用适当的缓冲液再生柱子,一般推荐使用PBS缓冲液进行再生。
其次,用去离子水进行洗脱,去除缓冲液中的离子。
2.样品准备:准备好带有样品的溶液,可以是蛋白质溶液、核酸溶液或者其他需要分离的溶液。
3.进样:将样品溶液注入到柱子中,可以使用曲线尖管或者注射器进行。
4.溶剂流动:使用适当的流动缓冲液进行柱子的着色,常用的缓冲液有PBS缓冲液、甲醇和乙醇。
5.收集分离的组分:通过收集分离的组分,可以进行后续的实验操作或者分析。
注意事项:1.柱子的平衡:在使用柱子前,将柱子放入合适的缓冲液中,进行平衡处理,通常需要约30分钟。
2.柱子的保管:使用完毕后,需将柱子用适当的缓冲液保存,避免干燥。
3.柱子的温度:柱子的运行温度一般在室温下进行,避免过高温度的使用,以免影响柱子的性能。
4.溶液选择:在选择适当的缓冲液时,应根据样品的性质以及需求进行选择,不同的缓冲液对分离的效果会有影响。
5.柱子的清洗:使用完毕后的柱子需要进行彻底的清洗工作,尤其是对于经常使用的柱子,清洗工作要做得彻底。
下面是几种常见溶剂的溶胀系数参考值:1.水:溶胀系数为1,对于葡聚糖凝胶柱来说,水是适用的溶剂。
2.硫酸:溶胀系数为0.57,硫酸能够完全渗透葡聚糖凝胶柱。
3.乙醇:溶胀系数为0.44,适量的乙醇可以使用,但过高浓度的乙醇可能会影响柱子的性能。
4.甲醇:溶胀系数为0.65,甲醇也可以使用,但同样需要注意控制浓度。
总结:葡聚糖凝胶柱是一种常见的色谱柱,具有广泛的应用。
在使用葡聚糖凝胶柱时,需进行适当的处理以及注意事项,以保证柱子的性能和寿命。
凝胶使用方法及注意事项1原理Sephadex LH-20的分离原理主要有两方面:以凝胶过滤作用为主,兼具反相分配的作用(在反相溶剂中)。
因为凝胶过滤作用,所以大分子的化合物保留弱,先被洗脱下来,小分子的化合物保留强,最后出柱。
如果使用反相溶剂洗脱, Sephadex LH-20对化合物还起反相分配的作用,所以极性大的化合物保留弱,先被洗脱下来,极性小的化合物保留强,后出柱。
如果使用正相溶剂洗脱,这主要靠凝胶过滤作用来分离。
2.前处理及装柱Sephadex LH-20在使用前必须进行溶胀,溶胀过程中必须避免过分搅拌,否则会破坏球形胶粒。
(1)室温下,将凝胶溶胀于层析液(一般为甲醇)中至少三小时(2)使溶胀胶体积沉淀后占总体积的75%,上层溶剂占25%凝胶悬浮液黏度要适宜A.太稠会在搅拌时产生气泡;太稀会导致装柱时沉降时间长,加凝胶悬浮液的次数增加;B.将凝胶悬浮液静止后所得上清液弃去,保留高于凝胶液面约1 cm的液体即可;C 装柱混悬液的浓度以流动性好,搅拌阻力小为宜。
(3)装柱的要点A 装柱前,先在色谱柱中加入约1/4柱高的液体(溶胀时所用的试剂);B 装柱时,将下端活塞打开,流速尽量大,但要保证小于凝胶沉降速度,否则会干柱;C将凝胶悬浮液搅拌均匀,以漏斗倒入柱子中即可;3.流动相1.分子筛作用,常用的是甲醇、甲醇+氯仿混合溶剂。
甲醇:氯仿一般为1:1左右,切不可用氯仿做为流动相!氯仿比重大,用单纯的氯仿做流动相,填料将浮起来,严重影响分离效果!!2.反相分配作用,常用的是甲醇/水,比例可以根据实际情况进行调整,也可以是梯度洗脱(先用水,逐渐增加甲醇比例,最后用100%甲醇冲柱)4.样品的处理及洗脱过程(1).最重要的一点:用尽可能少的溶剂溶解样品,样品可以很浓。
如果溶解体积很大,一定要先进行浓缩,否则基本没有多大的分离效果。
上样体积一般为柱体积的1%~5%。
(2).很重要的一点:尽可能用起始洗脱溶剂溶解样品(很多情况下样品并不能在起始溶剂中很好地溶解)。
葡聚糖凝胶柱的使用方法:1 预处理称取Sephadex G-2550-100目约5g;加入蒸馏水100ml;置室温下3h进行溶胀..2 装柱凝胶层析柱的直径与柱长之比一般为1:15..柱的底部用装有细玻璃管的橡皮塞塞紧;用洗净的玻璃丝约200目尼龙布垫底或购买类似规格的商品柱..然后将柱垂直安装好;先加入1/3柱体积蒸馏水;接着将溶胀好的凝胶边搅匀边连续装入;使它们在柱内自然沉降..同时大开下口慢速流出蒸馏水..装柱后的凝胶必须均匀;不能有气泡或明显条纹..否则;必须到出重装;装好后;用蒸馏水平衡2-3h即可加样品分离..3 加样加样前;首先把柱内凝胶上面多余的蒸馏水放出;直到柱内液面与凝胶表面相齐或留一极薄液层为止..然后;由柱的上端加水解液2ml;注意不要让溶液把凝胶冲松浮起;加完样品后;打开下口缓慢放出液体至液面与凝胶面相齐;再用少量蒸馏水冲洗原来盛样品的容器2-3次;待全部进入层析柱后;即可进行洗脱..4 洗脱与收集洗脱时;用蒸馏水作洗脱剂;并且要连续不断地进行;使凝胶柱上端保持一定的液层;防止凝胶柱表面的液体流干..本实验洗脱液流出的速度应控制在0.8-1.0ml/min..洗脱液的收集采用分管连续顺序收集;每管收集3ml;共收集10管..据经验;4或5号管核苷酸浓度最大;可作为层析鉴定的样品液..但因层析柱长度的差异;管号会有变化;必要时可用紫外检测A260nm;找出浓度最大的管号..5 凝胶的再生和回收凝胶柱使用一次后;必须反冲疏松一次;平衡后再使用..若使用数次;就需要再生处理..用0.1mol/L NaOH-0.5mol/L NaCl溶液浸泡;然后用蒸馏水洗至中性备用..若实验完毕;将再生后的凝胶在布氏漏斗上用蒸馏水洗涤抽干;再用95%乙醇洗两次;在60℃烘箱中烘干;回收保存..实验五. 葡聚糖凝胶层析实验目的1.掌握葡聚糖凝胶的特性及凝胶层析的原理..2.学习葡聚糖凝胶层析的基本操作技术..实验原理凝胶层析又称分子排阻层析或凝胶过滤;是以被分离物质的分子量差异为基础的一种层析分离技术;这一技术为纯化蛋白质等生物大分子提供了一种非常温和的分离方法..层析的固定相载体是凝胶颗粒;目前应用较广的是:具有各种孔径范围的葡聚糖凝胶Sephadex和琼脂糖凝胶Sepharose..葡聚糖凝胶是由直链的葡聚糖分子和交联剂3—氯1;2—环氧丙烷交联而成的具有多孔网状结构的高分子化合物..凝胶颗粒中网孔的大小可通过调节葡聚糖和交联剂的比例来控制;交联度越大;网孔结构越紧密;交联度越小;网孔结构就越疏松;网孔的大小决定了被分离物质能够自由出入凝胶内部的分子量范围..可分离的分子量范围从几百到几十万不等..葡聚糖凝胶层析;是使待分离物质通过葡聚糖凝胶层析柱;各个组分由于分子量不相同;在凝胶柱上受到的阻滞作用不同;而在层析柱中以不同的速度移动..分子量大于允许进入凝胶网孔范围的物质完全被凝胶排阻;不能进入凝胶颗粒内部;阻滞作用小;随着溶剂在凝胶颗粒之间流动;因此流程短;而先流出层析柱;分子量小的物质可完全进入凝胶颗粒的网孔内;阻滞作用大;流程延长;而最后从层析柱中流出..若被分离物的分子量介于完全排阻和完全进入网孔物质的分子量之间;则在两者之间从柱中流出;由此就可以达到分离目的..本实验以葡聚糖凝胶G—25作为固定相载体;来分离蓝色葡聚糖—2000和溴酚蓝..蓝色葡聚糖—2000分子量接近2×106; 而溴酚蓝分子量为670;二者分子量相差较大;前者完全排阻;而后者则可完全进入凝胶颗粒网孔内;二者通过层析柱的时间不同而分开..实验材料1.实验器材层析柱1×20cm附有一小段乳胶管及螺旋夹;洗脱液瓶带下口的三角瓶;250m1;试管及试管架;量筒10m1;721型分光光度计2.实验试剂1 Tris—醋酸缓冲液pH7.0:取0.0lmol/L Tris溶液含0.1mol/L KCl900ml;用浓醋酸调pH至7.0;加蒸馏水至1000m1..2 溴酚蓝溶液:称取溴酚蓝10毫克;溶于5毫升乙醇中;充分搅拌使其溶解;然后逐滴加入Tris—醋酸缓冲液pH7.0至溶液呈深蓝色..3 蓝色葡聚糖—2000溶液:称取蓝色葡聚糖—2000 10毫克;溶于2毫升Tris—醋酸缓冲液pH7.0中即成..4 样品溶液:取溴酚蓝溶液0.1毫升;蓝色葡聚糖—2000溶液0.5毫升混匀后为上柱样品溶液..5葡聚糖凝胶G-25 Sephadex-G-25实验操作1.实验凝胶的制备:商品凝胶是干燥的颗粒;使用时需经溶胀处理;称取4克葡聚糖凝胶G—25;加50毫升蒸馏水;搅拌均匀;在室温溶胀6小时;或沸水浴溶胀 2小时;一般采用后一种方法..再用倾泻法除去凝胶上层水及细小颗粒;用蒸馏水反复洗涤几次;再以缓冲溶液pH7.0的Tris—醋酸溶液洗涤2—3次;使pH和离子强度达到平衡;最后抽去溶液及凝胶颗粒内部气泡;凝胶可保存在缓冲液内..2.装柱:将层析柱洗净;垂直固定在铁支架上;选择有薄膜端作为层析柱下口;将下口接上乳胶管并用螺旋夹夹紧..层析柱中加入洗脱液;打开下口螺旋夹;让溶液流出;排除残留气泡;最后保留约2厘米高度的洗脱液;拧紧螺旋夹..将凝胶轻轻搅动均匀;用玻璃棒沿层析柱内壁缓缓注入柱中;待凝胶沉积到柱床下已超过l厘米时;打开下口螺旋夹;继续装柱至柱床高度达到8厘米;关闭出口..装柱过程中严禁产生气泡;尽可能一次装完;避免出现分层..再用洗脱液平衡l至2个柱床体积;凝胶面上始终保持有一定的洗脱液..平衡后;拧紧下端螺旋夹..3.加样品:打开螺旋夹使柱面上的洗脱液流出;直至床面与液面刚好平齐为止;关闭下端出口..取溴酚蓝及蓝色葡聚糖—2000混合液0.3毫升;小心地加于凝胶表面上;切勿搅动层析柱床表面..打开下端出口;使样品溶液进入凝胶内;并开始收集流出液..当样品溶液恰好流至与凝胶表面平齐时;关闭下端出口..用少量洗脱液清洗层析柱加样区;共洗涤三次;每次清洗液应完全进入凝胶柱内后;再进行下一次洗涤..最后在凝胶表面上加入洗脱液;保持高度为3—4cm..4.洗脱与收集:连接好凝胶柱层析系统;调节洗脱液流速为每分钟1毫升;进行洗脱..仔细观察样品在层析柱内的分离现象;收集洗脱液;每收集3毫升即换一支收集管试管预先编号;收集约20管左右;样品即可完全被洗脱下来..将各收集管中的洗脱液分别用721型分光光度计在波长540nm处测定其光密度..5.凝胶回收处理方法:将样品完全洗脱下来后;继续用三倍柱床体积的洗脱液冲洗凝胶后;将柱下口放在小烧杯中;慢慢打开;再将上口慢慢松开;使凝胶全部回收至小烧杯中;备用..2 Sephadex LH20 的原理..Sephadex LH20的分离原理主要有两方面:以凝胶过滤作用为主;兼具反相分配的作用在反相溶剂中..因为凝胶过滤作用;所以大分子的化合物保留弱;先被洗脱下来;小分子的化合物保留强;最后出柱..如果使用反相溶剂洗脱; Sephadex LH20对化合物还起反相分配的作用;所以极性大的化合物保留弱;先被洗脱下来;极性小的化合物保留强;后出柱..如果使用正相溶剂洗脱;这主要靠凝胶过滤作用来分离..3 Sephadex LH20 洗脱溶剂..看完第2点后;就应该清楚Sephadex LH20 洗脱溶剂因分为两类:反相和正相两种..用得最多的是反相溶剂洗脱;以甲醇--水系统最为常见;先用水;逐渐增加甲醇比例;最后用100%甲醇冲柱..正相系统以氯仿--甲醇最为常见;先用50%氯仿--甲醇;逐渐增加甲醇比例;最后用100%甲醇冲柱..4 Sephadex LH20 样品的处理和洗脱溶剂的选择..如果样品极性大;这选用反相溶剂洗脱甲醇--水;样品用最少体积的甲醇--水尽可能甲醇少一些溶解;过滤后;湿法上样一定要滤喔要是把Sephadex LH20 堵啦;就得将Sephadex LH20 的柱头部分弃去;很心痛呀..如果样品极性小;这选用正相溶剂洗脱氯仿--甲醇;样品用最少体积的氯仿--甲醇溶解;过滤后;湿法上样..5 Sephadex LH-20的步骤..1 选择条件:梯度洗脱在Sephadex使用中并不象在正相柱层析中那么重要..首先你的样品须要能溶解在尽量少量的洗脱剂中..极性在的用甲醇水系统;极性小者一般用不含水的系统..我们实验室常用正己烷二氯甲烷甲醇系统;用了很多年;效果较好..2 饱和层析柱:用洗脱剂将凝胶摇匀;直立柱身;让其自然沉降;此时要防止气泡留在其中..至少半小时打开开关;流出几个柱体种的洗脱剂;目的是使其膨胀在正确比例的洗脱剂中..3 样品处理:用尽量少的洗脱剂溶解样品;常压过滤..4 湿法上柱..这也是要有技巧的步骤..5 洗脱:控制流速;一般1drop/s以下;可参见厂家的一些参数;必要时更改极性很多时一个极性就可以将样品洗脱完毕..再生以备下次使用..6 分离的技巧;最后说说我的使用心得1 流速不可太快;切切不可新急;所谓欲速则不达..2柱子尽可能长; Sephadex LH20 柱长的增加将极大地改善分离;所不要吝惜填料;宁可将填料全装在一根大柱子中;不要将填料装成几根小柱..所谓集中优势兵力;打击敌人..3 馏分一定要接的细;可1/10;或1/20 个保留体积接成一馏分..4 洗脱体积一般为2-3个保留体积;对特殊保留强的化合物;可洗脱5个保留体积..5鞣质成分死吸附严重;如不在乎填料者;可用Sephadex LH20 分鞣质6Sephadex LH20 对黄酮类成分的分离效果极佳;方法很成型;有大量文献参考..7填料反复使用;每次用完;一般可用甲醇将柱子洗干净;然后用下一次分离的起步溶剂将甲醇替换出来;待用..Sephadex LH-20是由葡聚糖G-25羟丙基化加工而成;属于分子筛凝胶;尤其适用于天然产物在有机溶剂中的纯化..例如:类固醇、萜类、脂类以及小分子多肽等;Pharmadex LH-20同时适用于分子类别非常相似的物质的分离和工业规模的制备;既可用于初步纯化步骤;也可用于最终精制步骤;如非对映同分异构体的分离..1.装柱装填的重要原则之一就是需要形成一个稳定均一的柱床..胶颗粒越均一粒径分布越窄;越容易获得稳定均一的柱床..但是对于Sephadex LH-20而言;25~100μm的粒径范围相对于许多用于制备色谱的填料而言;不能说分布均一;也就是说其粒径分布较宽..然而当胶溶胀后就相对容易得到均一的柱床..这对于长柱最高至250cm而言也是同样的..在装柱前;层析柱和储槽都必须进行彻底的清洗..Sephadex LH-20在使用之前必须进行溶胀..在溶胀的过程中;要尽量避免过分搅拌;否则会破坏球形胶粒;且要避免使用磁力搅拌器..在室温下;将凝胶溶胀于层析溶剂中至少三小时;溶胀后胶体积的大小决定于所使用的溶剂系统;请参考后页之干胶溶胀表计算特定柱体积所需要干胶的量..使溶胀胶体积沉淀之后占总体积的75%;上层溶剂占25%;这时;悬浮液从一个容器倒入另一容器时胶粒可移动..将溶胀后的凝胶根据装柱要求均匀倒入柱内;在保证胶粒不变形的前提下;应在尽可能高的压力下装柱;反压不要超过1.5ba..2.平衡上样前;用洗脱液平衡层析柱至少两个柱体积直到基线变得平稳为止;如改变溶剂应该注意凝胶在新溶剂中的溶胀性质;并根据性质确定柱高调节器的位置;如使用相同的溶剂;在以后的层析中柱平衡可以省略..3.洗脱液为确保延长层析柱的使用寿命;所有的缓冲液都应该离心或经过0.45um的膜过滤以除去杂质..4.样品样品体积应该占柱总体积的1-2%;同样在使用之前样品应该离心或经过0.45um的膜过滤..5.洗脱洗脱流速应根据情况而定;最大线性流速约12cm/min反压1.5ba;建议流速为1-10cm/h..总体来说;较低的流速;具有较高的分辩率..。
葡聚糖凝胶使用说明化学和物理性质葡聚糖凝胶是一种珠状的凝胶,含有大量的羟基,很容易在水中和电解质溶液中溶胀。
G型的葡聚糖凝胶有各种不同的交联度,因此它们的溶胀度和分级分离范围也有所不同。
葡聚糖凝胶的溶胀度基本上不因盐和洗涤剂的存在而受影响。
葡聚糖凝胶有不同的粒度。
超细级的葡聚糖凝胶是用于需要极高分辨率的柱色谱和薄层色谱。
粗级和中级的凝胶用于制备性色谱过程,可在较低的压力下获得较高的流速。
另外,粗级也可用于批量工艺。
化学稳定性葡聚糖凝胶不溶于一切溶剂(除非它被化学降解)。
它在水、盐溶液、有机溶剂、碱和弱酸性溶液中都是稳定的,在强酸中凝胶骨架的糖苷键被水解。
长期接触氧化剂将破坏凝胶,因而应避免使用。
物理稳定性葡聚糖凝胶并不熔融,可以在湿态、中性PH进行灭菌或在高压灭菌器120℃、30分钟而不影响它的色谱性质。
干态的凝胶加热至120℃以上将开始焦糖化。
葡聚糖凝胶的机械强度取决于交联度。
产品说明:产品名称分离范围应用葡聚糖凝胶 G-10<700缓冲液交换、脱盐,分离小分子,去除小分子葡聚糖凝胶 G-15<1500缓冲液交换、脱盐,分离小分子,去除小分子葡聚糖凝胶 G-251000-5000工业上脱盐及交换缓冲液葡聚糖凝胶 G-501000-30000多肽分离、脱盐、清洗生物提取液、分子量测定葡聚糖凝胶 G-752000-70000蛋白分离纯化、分子量测定、平衡常数测定葡聚糖凝胶 G-1002000-120000蛋白分离纯化、分子量测定、平衡常数测定葡聚糖凝胶 G-1505000-300000蛋白分离纯化、分子量测定、平衡常数测定葡聚糖凝胶 G-2005000-600000蛋白分离纯化、分子量测定、平衡常数测定使用方法:1. 乙醇浸泡:在室温下,将干粉浸泡于50-60%乙醇中至少24小时,并不断搅拌以保证凝胶溶胀,用无盐水洗去残存的乙醇滤干;2. 无盐水浸泡:室温下,在无盐水中充分溶胀24小时,间隙搅拌,以保证凝胶的完全溶胀,然后;3. 盐酸浸泡:在常温下再用0.2N HCl浸泡12小时,间隙搅拌,滤干,水洗只中性;4. 将溶胀好的凝胶脱气后(真空抽滤或超声波)根据装柱要求一次性置入柱内,注意保持湿态装柱,并避免柱内产生气泡或断层;5. 上样前平衡层析柱至少3-5个柱体积直到记录仪基线变得平稳为止(流出液的PH值等于上柱的Buffer的PH值);6. 凝胶过滤的上样量一般为5%的柱床体积,我们建议初次上样控制在1-2%的床体积,视分离情况可以调整;脱盐时上样量可以达到20%的柱床体积,柱高的选择也与分离要求相关,柱高控制在40-50cm 以下,过高的凝胶层会引起较大的反压,应当尽可能避免。
葡聚糖凝胶使用说明书一、产品名称产品名称:葡聚糖凝胶型号:Ge1-300二、适用范围葡聚糖凝胶适用于生物实验室、化学实验室、制药厂等场所,用于分离、纯化蛋白质、核酸、肽类等生物分子。
三、使用方法1.准备葡聚糖凝胶和缓冲液。
根据所需的分离纯化效果,选择合适的缓冲液类型和浓度。
2.将缓冲液加入玻璃柱或层析柱中,直至填满整个柱子。
3.加入适量的葡聚糖凝胶,使其均匀分布在柱子的底部。
4.将样品溶液缓慢地加入柱子中,注意不要过快,以免影响分离效果。
5.收集洗脱液,并进行分析。
根据分离纯化的目的,可以采用不同的收集方法,如分步收集或集中收集。
6.在每次使用后,及时清洗和保存凝胶柱,以延长其使用寿命。
四、注意事项1.在使用葡聚糖凝胶前,应仔细阅读本说明书并遵守操作规程。
2.避免直接接触皮肤和眼睛,若不慎接触,应立即用清水冲洗。
3.使用过程中要避免剧烈震动或晃动,以免影响分离效果。
4.在使用前应确认所需缓冲液的种类和浓度是否合适,避免浪费和影响分离效果。
5.不要使用已经过期或变质的凝胶和缓冲液。
6.在储存和使用过程中要保持环境干燥,避免潮湿和高温。
7.使用后要及时清洗和保存凝胶柱,以免被污染和变质。
五、常见问题及解决方案1.分离效果不佳:可能是由于凝胶或缓冲液质量问题、操作不当等原因引起的。
解决方法是检查凝胶和缓冲液的质量和浓度是否合适,确认操作规程是否正确。
若问题仍未解决,建议更换新的凝胶柱。
2.柱子压力过高:可能是由于样品溶液中存在杂质或凝胶柱堵塞等原因引起的。
解决方法是检查样品溶液是否含有杂质,或者对样品进行预处理以去除杂质。
同时检查凝胶柱是否堵塞,若堵塞则进行清洗或更换新的凝胶柱。
3.柱子漏液:可能是由于接头松动或密封圈损坏等原因引起的。
解决方法是重新拧紧接头或更换新的密封圈。
若问题仍未解决,建议联系售后服务与支持部门寻求帮助。
4.洗脱液中含有杂质:可能是由于样品溶液中存在杂质或缓冲液不纯等原因引起的。