混合液张力公式
- 格式:doc
- 大小:95.00 KB
- 文档页数:2

HLB值计算
HLB(依凡尼洛夫法)值是一种用于测量表面活性剂(也称为表面活性剂)的极性度的指标。
依凡尼洛夫(HLB)值是一种常用的表面活性剂组合的量化指标,主要是用来确定表面活性剂的最佳组合。
HLB(依凡尼洛夫)值计算过程有以下四步:
第一步:计算组份的HLB值。
HLB值是用来衡量表面活性剂的极性度的指标,可以用来确定每种表面活性剂的组合,确定母液的形成与特性。
每种表面活性剂都有其自身的HLB值,可以简单地通过手册或者互联网等方式获得这个HLB值。
第二步:根据公式计算表面活性剂总体的HLB值。
通过以下公式可以计算表面活性剂的总体HLB值:
总体HLB值=∑[每种表面活性剂的质量分数×每种表面活性剂对应的HLB值]
第三步:根据总体HLB值计算混合液体的表面张力
根据总体HLB值可以计算混合液的表面张力,公式如下:
表面张力= 20 × 总体HLB值(dyn / cm)
第四步:计算和结果报告
最后,将所有步骤的结果汇总在一起,就可以得出总体表面活性剂组合的HLB值和其对应的表面张力。
HLB值是一种定量分析表面活性剂的标准,可以有效地控制表面活性剂的极性和组合,从而得到所需的特性。

在液体治疗中,液体的渗透压与张力是很重要的概念,是我们了解、认识液体特点的基础一.定义1.液体渗透压(Fluid osmolality):当两种不同浓度溶液用一种理想的半透膜隔开时,则溶剂从低浓度溶液向高浓度溶液中渗透,这种溶剂渗透的力,通常称为渗透压,可简单理解为溶质分子对溶剂分子产生的吸引力,反映的是单位体积溶液中溶质微粒的数目液体渗透压的计算摩尔浓度(mmol/L)=1000×ρ×A%÷摩尔质量×1000备注:ρ为溶剂密度(水密度为1);A%为质量百分比浓度;上式计算结果数值与渗透压(单位mOsm/L)的数值相等2. 液体张力(Fluid tonicity):指溶液进入到体内后能够维持渗透压的能力,是指溶液中电解质产生的渗透压与血浆渗透压正常值的比值,是一个没有单位的数值液体张力计算:电解质渗透压/血浆渗透压说明:葡萄糖进入体内后很快被代谢,只剩自由水,渗透液压就消失了。
因此说葡萄糖溶液是无张力的3. 等渗液(iso-osmotic solution):渗透压与血浆相等或相似的溶液是一个物理化学观念4. 等张液(isotonic solution)与红细胞张力相等或相似的溶液是一个生物学概念在等张液中红细胞既不肿胀也不皱缩,维持原有形态等张溶液是由不能自由透过细胞膜的溶质形成的等渗溶液二.一些治疗液体的渗透压与张力液体渗透压(mOsm/L)张力0.45%氯化钠154 1/25%葡萄糖252 00.9%氯化钠308 1复方氯化钠305 1乳酸钠林格273 15%葡萄糖0.9%氯化钠560 12.5%葡萄糖0.45%氯化钠280 1/22.5%葡萄糖1/2张林格278.5 1/22.5%葡萄糖1/2张乳酸林格262.5 1/210%葡萄糖504 03%氯化钠1026 3.45%碳酸氢钠1190 4说明:5%葡萄糖液中的葡萄糖是水合葡萄糖(分子式为C6H12O6·H2O ;分子量为198)。


补液张力计算液体疗法是儿科最常用的治疗方法之一,是儿科学的重要内容,也是每位临床医学生必需掌握的基本技能。
液体张力计算与配制则是液体疗法的基础,如对此不理解、不掌握,则将难以学习和运用液体疗法。
现有多种教材对液体张力的计算与配制,阐述均较为复杂而含糊,教师按教材授课,学生按课本学习,其结果是大多数学生难于理解与掌握。
通过五个步骤,即使所有学生很快便能理解与掌握。
过程如下:1、首先出一道简单的数学算术题例1、将10%NaCL10ml稀释至100ml,请问稀释后溶液百分比浓度。
学生很快便能列出算式:10%×10=X×100,X=1%。
稀释定律:稀释前浓度×稀释前体积=稀释后浓度×稀释后体积。
即:C1×V1=C2×V2。
并且强调但凡涉及物质浓度的换算,均遵循此定律。
2、问题:能够用来表达物质浓度的有A.百分比浓度 B.摩尔浓度 C.张力张力亦是物质浓度的一种表达方式。
3、阐述溶液张力的概念及计算张力是指溶液溶质的微粒对水的吸引力,溶液的浓度越大,对水的吸引力越大。
判断某溶液的张力,是以它的渗透压与血浆渗透压正常值(280~320mosm/L,计算时取平均值300mosm/L)相比所得的比值,它是一个没有单位但却能够反映物质浓度的一个数值。
溶液渗透压=(百分比浓度×10×1000×每个分子所能离解的离子数)/分子量。
如0.9%NaCL溶液渗透压=(0.9×10×1000×2)/58.5=308mosm/L(794.2kPa)该渗透压与血浆正常渗透压相比,比值约为1,故该溶液张力为1张。
又如5%NaHCO3溶液渗透压=(5×10×1000×2)/84=1190.4mosm/L(3069.7kPa)该渗透压与血浆正常渗透压相比,比值约为4,故该溶液张力为4张。


2024补液基本功的液体张力计算某日一位小儿患者因呕吐腹泻3天入院,查体轻度脱水貌,辅助检查暂未出结果。
医生予以IOoml10%葡萄糖溶液+3ml10%NaCI溶液+5ml5%NaHCO3溶液补液,请问这个医嘱正确吗?01这个配比正确吗?为什么?首先,未确定该患儿是什么性质的脱水,所以先按等渗性脱水处理。
IoOml10%葡萄糖溶液+3ml10%NaCl溶液+5ml5%NaHCo3溶液,计算出来的液体张力约为1/2张,符合等渗性脱水情况下适合的液体张力。
所以这个医嘱是可行的。
02什么是液体张力?如何计算?液体张力是指溶质的微粒对水的吸引力,也是指溶液进入人体后能够维持渗透压的能力(葡萄糖进入人体后被吸收代谢,所以葡萄糖溶液不具备张力\计算公式如下[1]:溶液张力二溶液渗透压/血液渗透压(正常值);正常人体血液的渗透压约为285~310mθsmol∕kg o溶液渗透压(mθsmol∕kg)=(每千克溶剂中溶解溶质的克数/分子量)×10OOX该溶质分子解离的粒子数。
比如:10%NaCI溶液渗透压=(10×10/58.5)×1000×2=3418.8mθsmol∕kg≈11倍血浆渗透压,所以10%NaCl溶液约为11张。
03如何运用在临床呢?儿科补液非常精细,液体张力要根据病情选择。
一般而言,低渗性脱水选择2/3张液体,等渗性脱水选择1/2张液体,高渗性脱水选择1/3-1/5张液体,大量失血或严重彳氐血压患儿选择2:1等张含钠液[2]。
临床常用的1/2张液体有1:1液(0.9%NaCI50ml+5%或10%葡萄糖50ml)和2:3:1液(0.9%NaCI33ml+5%或10%葡萄糖50ml+1.4%NaHCO3/1.87%乳酸钠17ml\临床常用的2/3张液体是4:3:2液,你知道0.9%NaCL5%或10%葡萄糖、1.4%NaHCO3/1.87%乳酸钠各占多少比例吗?2:1的等张含钠液溶液配比又是多少?参考文献:[1]《中华人民共和国药典》2015年三部通则.[2]苗凤英.急危重症护理学[M].长春:吉林科学技术出版社.2019.。

液体疗法的计算好方法医学文章2009-04-19 08:20:38 阅读1094 评论5 字号:大中小液体疗法的计算好方法小儿液体疗法小儿各器官发育尚未成熟,对体液的调节能力不如成人,年龄小的婴儿细胞外液相对较成人多,对脱水的耐受能力亦差,因此重视及掌握小儿液体疗法是非常必要的。
临床工作中常要用各种混合液来配制小儿混合液,如何准确、快捷配制如各种张力混合液是进行曲液体疗法的关键。
下面主要介绍小儿常用各种张力混合液的简便制方法。
一、小儿体液分布代谢特点1、小儿体液主要分布在细胞外,年龄越小,细胞间质分布液体越多,对脱水的耐受力越差,尤其是新生儿。
2、小儿肾脏的调节能力差于成人,输入过多的无张力液体及过多的等张液体则引起水中毒或高渗性脱水。
因此小儿脱水时常用1/5张至2/3张各种混合液。
3、小儿液体还经皮肤、呼吸道、消化道额外丢失,因为小儿呼吸频率快,消化道屏障功能差,皮肤相对面积大,因此,患病小儿要重视各系统丢失体液特点,用时补充附合该系统特点的液体。
二、常用溶液1、电解质溶液A 、生理盐水:0.9%N S,为等渗液。
作用:①抗休克(20~30ml/kg);②某药物溶媒;③纠正低钠血症;④与G S或1.4%S B配制混合液。
10%N S是高渗液,不能直接静脉使用,临床用于代替N S配制混合液。
B、1.4%S B;等渗液作用:①抗休克,纠酸,与N S配成2:1等张含钠液20ml/kg;②与N S或G S配制成混合液(如4:3:2,3:2:1。
液)5%S B为高渗液,一般不能直接用于静注,主要用于代替1.4%S B配制混合液(如4:3:2,3:2:1液)。
C、Kcl:0.2~0.3%Kcl可静脉使用,用于纠正低钾血症。
每100ml混合液中可最多加3ml的10%Kcl。
补钾注意:①每日补钾一般为2~3ml/kg。
日②静脉使用时溶液中Kcl浓度小于0.3%③补钾速度不能太快,每日静脉补钾时间大于4~6小时。

小儿补液三部曲来源:穆欢喜的日志一、首先,我们必须先判断孩子的病情到底如何,属于哪种脱水程度,以知道我们下一步的补液计划。
1、程度性脱水判断:轻度脱水:由于身体内水分减少,患儿会稍感到口渴,有尿排出,检查见患儿一般情况良好,两眼窝稍有陷,捏起腹部或大腿内侧皮肤后回缩尚快。
(轻度脱水最重要的判断标准就是:有尿排出,一般情况可,哭时有泪)中度脱水:患儿的出烦躁,易激惹;口渴想喝水,婴儿四处找奶头,如果得到奶瓶,会拼命吸吮;医学教育网原创啼哭时泪少,尿量及次数也减少;检查见患儿两眼窝下陷,口舌干燥,捏起腹壁及大腿内侧皮肤后回缩慢。
(中度脱水主要的判断标准:开始烦躁,易激惹,哭时泪少,眼窝下陷)重度脱水:患儿现为精神极度萎缩、昏睡,甚至昏迷;口喝非常严重,啼哭时无泪流出,尿量及尿次数明显数少。
检查见患儿两眼窝明显下陷,口舌非常干燥;捏起腹壁及大腿内侧皮肤后回缩很慢。
(重度脱水判断标准:精神萎靡,甚至昏睡。
皮肤相当的干燥,甚至出现了花纹,哭时无泪,无尿排出。
)2、渗透性的判断:低渗:血清钠<130mmol/L;(初期并未有口渴症状,但是极易发生脑水肿)等渗:血清钠130-150mmol/L;高渗:血清钠>150mmol/L。
(口渴症状相当的明显,高热,烦躁、肌张力增高.小儿补液三部曲之二先前,我们已经了解判断了小儿脱水的基本判断方法了,那么接下来,我们就应该了解,补什么,补多少,怎么补的问题了。
一、补什么、补多少1、补液总量:轻度失水:90-120ml/kg*d中度失水:120-150 ml/kg*d重度失水:150-180 ml/kg*d补液总量是由三部分组成的:一般需按累积损失量、继续损失量和生理需要量计算。
①累积损失量:指病后(如急性脱水)减轻之体重数量,这部分液体最主要。
这部分液量可根据脱水程度加以估计。
累积损失量也可按体表面积计算,轻度脱水为30-50ml/kg ,中度脱水为50-100ml/kg,重度脱水为100-150ml/kg。


儿科补液张力快速计算法张力是指电解质溶液占总溶液的比值。
只有糖是非电解质溶液,也就是说把糖除去,其他液体的份数除以总溶液的份数就是该液体的张力。
张力越高,液体含的电解质就越多一、4:3:2液4份0.9%NaCl 3份5%GS 2份1.4%NaHCO3电解质溶液是4+2=6份,总溶液是4+3+2=9份,张力=6/9=2/3张二、3:2:1液3份0.9%NaCl 2份5%GS 1份1.4%NaHCO3电解质溶液是2+1=3份,总溶液是3+2+1=6份,张力=3/6=1/2张三、1:1液1份5%GS 1份0.9%NaCl电解质溶液是1份,总溶液是1+1=2份,张力=1/2张四、2:1液2份5%GS 1份0.9%NaCl电解质溶液是1份,总溶液是2+1=3份,张力=1/3张五、4:1液4份5%GS 1份0.9%NaCl电解质溶液是1份,总溶液是4+1=5份,张力=1/5张六、2:1等张含钠液2份0.9%NaCl 1份1.4%NaHCO3不含糖,所以总溶液就是电解质溶液=1张,所以是等张婴幼儿腹泻脱水补液时,电解质溶液与非电解质溶液的比例主要根据脱水性质而定。
(1)等渗性脱水:此型脱水临床最多见,主要为细胞外脱水,但脱水严重的病例细胞内液亦同时损失。
用1∶1液(1份5 %葡萄糖溶液,1份0.9%氯化钠溶液)或3∶2∶1液(3份10%葡萄糖溶液,2份0.9%氯化钠溶液,1份1.87%乳酸钠溶液或1.4%碳酸氢钠溶液),即1/2张液体补给(张力指含晶体的电解质溶液,如含钠液的张力)。
(2)低渗性脱水:用3∶4∶2液(3份10%葡萄糖溶液,4份0.9%氯化钠溶液,2份1.87%乳酸钠溶液或1.4%碳酸氢钠溶液)或6∶7∶5液(一般称5∶6∶7液,6份5 %~10%葡萄液,7份0.9%氯化钠溶液,5份1.87%乳酸钠溶液),即2/3张液体补给。
(3)高渗性脱水:为数较少,用6∶2∶1液(6份5%葡萄糖溶液,2份0.9%氯化钠溶液,1份1.87%乳酸钠溶液或1.4%碳酸氢钠溶液),即1/ 3张液体补给。
护理张力计算公式张力是指溶液在体内维持渗透压的能力。
在医学和护理学中,准确计算溶液的张力对于患者的治疗和护理至关重要。
咱们先来说说为啥要搞清楚这个张力的计算。
你想啊,要是给病人输液,输的液体张力不对,那可就麻烦大啦!比如说,给一个脱水的小朋友补液,要是张力算错了,那不仅不能治病,还可能加重病情呢。
我还记得有一次,在病房里遇到一个小孩子因为腹泻导致脱水。
医生开了补液的医嘱,但是最初计算张力的时候出了点小差错。
我们按照错误的张力配置了液体,结果孩子的脱水症状没有得到及时缓解。
这可把大家急坏了!后来重新仔细计算,调整了补液方案,孩子的情况才慢慢好转。
从那以后,我就对张力的计算格外上心。
那到底怎么算这个张力呢?其实也不难,咱们一步步来。
首先,要明确几个概念。
啥是等渗溶液、低渗溶液和高渗溶液?像0.9%的氯化钠溶液就是等渗溶液,5%的葡萄糖溶液就是无张力的溶液。
然后,咱们来看看张力的计算公式。
张力=(含钠液量总和×相应的电解质浓度)÷总液量。
比如说,有一份 2:1 等张含钠液,其中 0.9%氯化钠溶液的量是 200ml,1.4%碳酸氢钠溶液的量是 100ml,那总液量就是 300ml。
0.9%氯化钠溶液含钠量是 0.9g/100ml,1.4%碳酸氢钠溶液含钠量是 1.67g/100ml。
所以含钠液量总和就是(200×0.9 + 100×1.67)÷300 = 1 张。
再比如说 4:3:2 液,也就是 4 份 0.9%氯化钠溶液、3 份 5%或 10%葡萄糖溶液、2 份 1.4%碳酸氢钠溶液(或 1.87%乳酸钠溶液)混合的溶液。
我们来算算它的张力。
假设各溶液的量分别是 400ml、300ml、200ml。
0.9%氯化钠溶液含钠量是 0.9g/100ml,1.4%碳酸氢钠溶液含钠量是 1.67g/100ml。
那含钠液量总和就是(400×0.9 + 200×1.67)÷(400 + 300 + 200) = 2/3 张。
俩溶液混合后的表面应力计算
表面张力是一个液体表面上单位长度的能量,它是衡量液体与空气或其他介质接触时的相互作用力的一种常见参数。
当两个不同的液体混合时,它们的表面张力也会发生变化。
因此,计算混合后的表面张力是非常有用的,它可以帮助我们更好地理解液体混合的过程。
在计算混合液体表面张力时,需要考虑两个因素:两个液体各自的表面张力和它们混合之后的相互作用力。
通常,这些相互作用力可以通过Young-Laplace公式来计算。
对于一个液滴的表面张力,这个公式可以被写作:
F = T(1/R1 + 1/R2)
其中,F是表面张力,T是张力系数,R1和R2是液滴半径的两个曲率半径。
当液滴混合时,Young-Laplace公式可以通过使用每个液体的表面张力和混合界面上的角度来计算混合后液体的表面张力。
如果液体混合的表面张力是正的,那么混合液体较难形成液滴或泡沫,因为表面张力抵消了任何可能的增加曲率的压力。
如果混合液体的表面张力是负的,那么形成液滴或泡沫会更容易,因为表面张力可以提供向外的力量,使得液滴或泡沫形成。
最终,在计算混合液体表面张力时,需要考虑两个液体的化学性质和比例以及它们混合后形成的物理状态。
通过精确计算液体表面张力,我们可以更好地理解液体混合和相互作用,提高科学家和工程师的实践水平,更好地掌握物质的变化规律。
混合液张力的快速计算公式和配制方法1混合液张力公式混合液张力=溶质产生的张力混合液的体积(或总量)=高渗液的体积×张力系数混合液的体积2公式运用(1)张力是指溶液溶质的微粒对水的吸引力,溶液的浓度越大,对水的吸引力越大。
判断某溶液的张力是以它的渗透压与血浆渗透压正常值(280~320mmol/L)相比所得的比值。
溶液渗透压=(百分比浓度×10×1000×每个分子所能解离的离子数/分子量)。
如0.9%NaCl溶液的渗透压为0.9×10×1000×2/58.5=308mmol/L。
该渗透压与血浆相比比值为1,故该溶液张力为1,即为等张液。
又如5%NaHCO3溶液渗透压为5×10×1000×2/84=1190.4,其张力为1190.4/300≈4。
同样,10%NaCl溶液张力约等于10。
故临床上常把1ml0.9%NaCl产生的张力看成1,那么1ml10%NaCl产生的张力约为10;同样把1ml1.4%NaHCO3产生的张力看成1,那么1ml5%NaHCO3产生的张力约为4。
其换算方法:高渗液的张力=高渗液的体积×换算系数。
例如10%的NaCl10ml溶液产生的张力为10×10=100张力。
临床上常用的几种高渗液与等渗液间的换算系数见表1。
(2)上述公式中溶质产生的张力是指混合液中各电解质所产生的张力之和。
(3)为了计算方便,加入的电解质不计入混合液的总量,临床上常用的混合液的成分及张力见表2。
表1高渗液与等渗液间张力的换算系数(略)表2临床常见溶液成分及张力(略)从上表中可以看出以下规律:①上述混合液(含盐和碱)中,盐∶碱=2∶1②混合液张力=盐+碱盐+碱+糖举例说明:例1:在200ml5%Glucose中加入10ml10%NaCl,该混合液的张力为多少?该溶液的张力=10(高渗液的体积)×10(张力系数)/200=1/2。
二组分表面张力混合规则公式以二组分表面张力混合规则公式为标题,我们来探讨一下表面张力混合规则的概念和应用。
表面张力混合规则公式是用来计算两种液体混合时的表面张力的一种数学公式。
在液体表面,由于分子间的相互作用力,会形成一个薄而坚固的膜,这就是表面张力。
表面张力决定了液体在表面上的形状和性质。
在混合液体的界面处,两种液体分子之间会发生相互作用,这种相互作用会影响混合液体的表面张力。
二组分表面张力混合规则公式可以帮助我们计算混合液体的表面张力。
二组分表面张力混合规则公式可以表示为:γ_mix= x_1 * γ_1 + x_2 * γ_2 + x_1 * x_2 * Δγ其中,γ_mix是混合液体的表面张力,γ_1和γ_2分别是两种纯液体的表面张力,x_1和x_2是两种纯液体的摩尔分数,Δγ是混合液体的表面张力差。
混合液体的表面张力与两种纯液体的表面张力、摩尔分数以及表面张力差之间存在一定的关系。
通过上述公式,我们可以计算出混合液体的表面张力。
二组分表面张力混合规则公式可以应用于许多领域。
在材料科学中,我们可以使用该公式来研究不同材料的表面张力混合行为,从而优化材料的性能。
在化学工程中,我们可以利用该公式来预测混合液体的表面张力,从而指导工艺的设计和优化。
在生物医学领域,我们可以利用该公式来研究生物体内不同液体的相互作用,从而探索生物体的结构和功能。
除了二组分表面张力混合规则公式,还有许多其他的表面张力混合规则公式。
这些公式都是基于对液体分子间相互作用的理论和实验研究的结果。
通过这些公式,我们可以更好地理解液体的表面性质,并应用于实际问题中。
二组分表面张力混合规则公式是一种用于计算混合液体表面张力的数学公式。
通过该公式,我们可以预测混合液体的表面张力,并应用于材料科学、化学工程和生物医学等领域。
通过深入研究表面张力混合规则,我们可以更好地理解液体的性质和行为,为实际应用提供指导和支持。
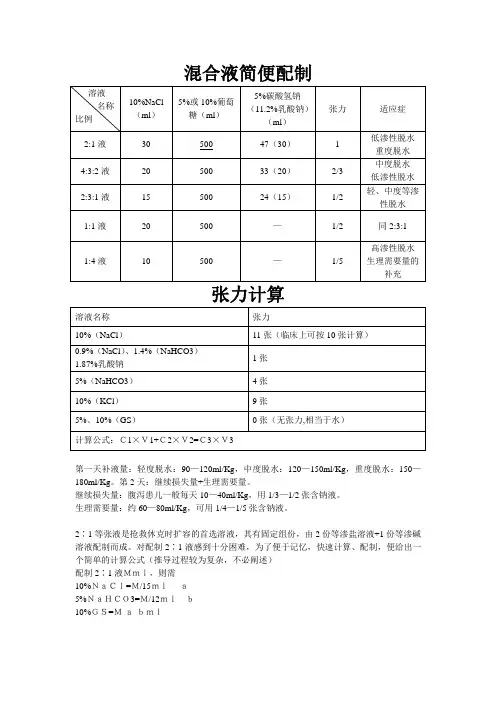
补液,液体张力的计算方法10%(NaCl)11张(临床上可按10张计算): `9 P q% M+ ~4 J- o 0.9%(NaCl)1张5%(NaHCO3)4张& [9 n6 J' _# l1 v- ?& V9 d1 G10%(KCl)9张10%(GS)0张(无张力,相当于水)6 n, J. x5 m. s& u: b x临床上多数情况下就是用以上几种溶液配制成其它所需的液体进行治疗,只需记住此几种溶液的张力,便可灵活自如地进行配制与计算所需溶液及张力;而不必去追究为什么10%NaCl张力是10张这一复杂的计算过程。
0 t4 z: A5 u8 k3 |3.举例说明混合溶液张力的计算某种液体的张力x某种液体的容量ml+另一种液体的张力x另一种液体的容量ml=混合液体的张力?X混合液体的容量ml例1、10%NaCl(10ml)+10%GS(90ml),请问该组溶液张力。
根据C1×V1=C2×V2列出算式:10×10=X×100,X=1张例2、10%NaCl(20ml)+5%NaHCO3(25ml)+10%GS(255ml),请问该组溶液张力。
10×20+4×25=X×300,X=1张。
例3、欲配制一组300ml,2/3张液体,现已使用5%NaHCO3(15ml),还需10%NaCl多少毫升。
10×X+4×15=2/3×300,X=14ml那么,再加入10%GS271(270)ml后即可配制成所需液体(300-15-14=271ml,GS为0张)2∶1等张液是抢救休克时扩容的首选溶液,其有固定组份,由2份等渗盐溶液+1份等渗碱溶液配制而成。
学生对配制2∶1液感到十分困难,为了便于学生记忆,快速计算、配制,便给出一个简单的计算公式(推导过程较为复杂,不必阐述)配制2∶1液Mml,则需. f* [) t9 ]. j0 T3 m0 {' X10%NaCl=M/15ml----a3 L; Q; ]& |% ^3 x8 j9 _6 k& q5%NaHCO3=M/12ml---b& T& F9 U' E- R5 K10%GS=M-a-bml$ o$ m% D. ] w: o+ p. Q 例4、配制2∶1液300ml,需10%NaCl、5%NaHCO3、10%GS各多少毫升。
1 混合液张力公式
混合液张力=溶质产生的张力混合液的体积(或总量)=高渗液的体积×张力系
数混合液的体积
2 公式运用
(1)张力是指溶液溶质的微粒对水的吸引力,溶液的浓度越大,对水的吸引力越大。
判断某溶液的张力是以它的渗透压与血浆渗透压正常值(280~320mmol/L)相比所得的比值。
溶液渗透压=(百分比浓度×10×1000×每个分子所能解离的离子数/分子量)。
如0.9%NaCl溶液的渗透压为0.9×10×1000×
2/58.5=308mmol/L。
该渗透压与血浆相比比值为1,故该溶液张力为1,即为等张液。
又如5%NaHCO3溶液渗透压为5×10×1000×2/84=1190.4,其张力为1190.4/300≈4。
同样,10%NaCl溶液张力约等于10。
故临床上常把1ml0.9%NaCl产生的张力看成1,那么1ml10%NaCl产生的张力约为10;同样把1ml1.4% NaHCO3产生的张力看成1,那么1ml5% NaHCO3产生的张力约为4。
其换算方法:高渗液的张力=高渗液的体积×换算系数。
例如10%的NaCl 10ml溶液产生的张力为10×10=100张力。
临床上常用的几种高渗液与等渗液间的换算系数见表1。
(2)上述公式中溶质产生的张力是指混合液中各电解质所产生的张力之和。
(3)为了计算方便,加入的电解质不计入混合液的总量,临床上常用的混合液的成分及张力见表2。
表1 高渗液与等渗液间张力的换算系数(略)
表2 临床常见溶液成分及张力(略)
从上表中可以看出以下规律:
①上述混合液(含盐和碱)中,盐∶碱=2∶1
②混合液张力=盐+碱盐+碱+糖
举例说明:
例1:在200ml5%Glucose中加入10ml10% NaCl,该混合液的张力为多少?
该溶液的张力=10(高渗液的体积)×10(张力系数)/200=1/2。
例2:如何用5%葡萄糖、5% NaHCO3及10 %NaCl配制2∶1等张含钠液M ml?
根据张力公式则有:
盐产生张力+碱产生张力 M=1
因为盐∶碱=2∶1,则盐产生张力为2/3M,碱产生张力为1/3M,那么2/3M张力需要10%NaCl为2/3M
×1/10,即M/15ml;1/3M张力需要5% NaHCO3为1/3M×1/4,即M/12ml。
即配制2∶1等张含钠液M ml
则需10%NaCl M/15ml、5% NaHCO3 M/12ml。
上例公式可作为配制2∶1等张含钠液简化公式,类推:配制2∶1等张含钠液300ml,则需10%NaCl为300/15=20ml,5% NaHCO3为300/12=25ml。
该混合液张力为(20×10+25×4)/300 = 1。
同理可得出配制3∶2∶1溶液M ml的简化公式为需10%NaCl M/30ml、5% NaHCO3 M/24ml。
例3:如何配制3∶2∶1溶液300ml?
首先该溶液张力为2+1/3+2+1=1/2,又根据张力公式:该混合溶液张力(1/2)=盐生产张力+碱产生张力体积(300ml),则盐和碱产生张力之和为150,其中盐∶碱=2∶1,则盐产生张力为2/3×150=100;碱产生张力为1/3×150=50,故需要10% NaCl为100×1/10=10ml,5% NaHCO3为50×1/4=12.5ml。
也可以这样计算:300ml溶液中0.9%NaCl占2/6,即100ml可产生100个张力,若用10%NaCl只需
100/10=10ml;同样:300ml溶液中1.4% NaHCO3占1/6,即50ml可产生50个张力,若用5% NaHCO3只需50/4=12.5ml。
也可直接代入例2的简化公式得出10% NaCl为300/30=10ml,5% NaHCO3为300/24=12.5ml。