电子监管码赋码解决方案.
- 格式:ppt
- 大小:2.92 MB
- 文档页数:36

电子监管码赋码标准操作与维护保养规程目的:建立药品电子监管码赋码操作与维护标准规程,规范药品电子监管码的申请、赋码、核销等操作程序,确保电子监管码在整个生产过程中的准确、规范。
范围:本规程使用于电子监管码申请、赋码及出库整个过程。
职责:MT950电子监管码赋码操作及维护相关人员执行本规程规程:操作前说明:设备开机:连上电源后,打开设备上方的电源开关,即可开机;设备关机:点击右下角【开始图标】,点击“挂起”,再关闭设备上方电源开关,即可关机。
操作过程:1、电子监管码的申请、下载、解密1.1 由数字证书保管员从中国药品电子监管网系统提出监管码申请,选择需申请监管码的药品通用名、剂型、规则、包装规格,并输入包装比例、申请数量等信息。
1.2 监管码生成后,通过“监管码下载”页面下载已经生产的监管码文件,下载完监管码后,进行确认,点击“监管码解密”菜单,选择监管码加密包文件,然后点击解密进行解密操作。
2、信息导入2.1 产品信息导入,由在线赋码操作系统控制台主菜单“数据文件管理”中点击“产品信息导入”,在打开的窗口中点击“浏览”选择导入路径,找到从中国药品电子监管网下载的产品信息文件(*.xml文件),点击“导入”后,将产品信息导入服务器数据库中。
2.2 监管码导入,由在线赋码操作系统控制台主菜单“数据文件管理”中的“监管码信息导入”,在打开的窗口中点击“浏览”,选择要导入的监管码文件(*.txt文件),文件打开后会在中间的表格中预览要导入的监管码信息,确认无误后,点击下方“导入”按钮导入监管码文件。
2.3 下载后的药监码文件名称和文件格式不能随意更名,否则将无法正常导入赋码系统,由于药监码文件名称中含有系统需要的信息,文件名和格式为国家药监局制定的标准格式不可更改。
3、生产前基础信息设置3.1 点击“生产线管理”点击“添加”建立生产车间,生产线,工位,并可通过“添加”、“修改”和“删除”、和对车间、生产线、工位信息进行相应操作。

药品电子监管码在赋码过程中的常见问题与处理中国药品电子监管码是对药品实施电子监管,为每件最小销售包装单位的药品赋予的电子标识标签。
每件药品的电子监管码唯一,即“一件一码”,好像人的身份证,也就是药品的电子身份证。
“一件一码”,突破了传统一类一码的机制,做到对每件产品唯一识别、全程跟踪,实现了政府监管、物流应用、商家结算、消费者查询的功能统一。
每一盒、每一箱、每一批重点药品生产、经营、库存以及流向情况,遇有问题时可以迅速追溯和召回。
按照药品包装规格对监管码进行分级,常见的有二级(小盒、运输箱)和三级(小盒、中盒、运输箱)两种类型,在一些特殊包装要求下,也有四级、五级等类型,并在包装过程中赋码,形成关联关系。
因为药品每一盒、每一箱之间都要通过扫描包装小盒、中盒、运输箱上的药品监管码,同时在特定的赋码系统软件中建立包装关联关系,在药品生产完成下线后将已经建立包装关系的系统文件上传于《中国药品电子监管网》,以激活监管码。
兰州生物制品研究所药品电子监管码已于2008年10月起进行赋码入网,所使用的系统为中信国检信息技术有限公司指定运营商开发的软件,现已使用一年。
药品电子监管码的赋码过程是一个比较复杂的操作过程。
首先在《中国药品电子监管网》上根据生产的药品品种、规格和实际生产量,申请监管码并且下载,下载的监管码都为一级未使用状态。
在根据生产需要分成已印刷与未使用状态的监管码,再由专人导入赋码软件,进行扫描赋码,于每一级包装建立包装关系。
在扫描建立包装关系的过程中常常会遇到一些问题,现就这些问题及其处理方法介绍如下。
1 监管码的导入在导入监管码时常会出现无法导入、数据存在等问题,解决办法如下:1.1 在导入监管码之前,首先要导入产品码。
具体操作:(1)登陆系统,打开基础信息,选中“产品管理”,点击导入产品,选中所需要的药品信息文件,然后点击打开文件。
如果无法导入,首先查看文件的格式是否正确,药品信息文件的格式必须是(.xml)的文件;(2)导入成功后点击“查询”,此时“查询”旁边的“确认”按钮激活,点击“确认”按钮,便可出现产品码文件当中产品详细的信息。

赋码实施方案一、背景随着信息技术的不断发展,数字化管理已成为企业发展的必然趋势。
而在数字化管理中,赋码技术的应用越来越广泛,可以有效提高数据管理的效率和准确性。
因此,制定赋码实施方案,对于企业的数字化管理具有重要意义。
二、目标制定赋码实施方案的目标是为了实现以下几点:1. 提高数据管理的效率和准确性;2. 规范数据管理流程,降低数据管理成本;3. 保障数据安全,防止数据泄露和篡改。
三、实施步骤1. 赋码技术选择在制定赋码实施方案时,首先需要选择适合企业实际情况的赋码技术。
赋码技术应具备以下特点:易于实施、安全可靠、适应性强。
针对企业的具体需求,可以选择条形码、二维码、RFID等赋码技术。
2. 数据整理和标识在确定赋码技术后,需要对企业的数据进行整理和标识。
这包括对产品、设备、文件等进行赋码标识,确保每个数据都有唯一的标识符,便于管理和追踪。
3. 赋码设备采购和部署根据赋码技术的选择,需要采购相应的赋码设备,并进行部署。
赋码设备的选择应考虑设备的性能、稳定性和兼容性,部署应按照实际情况进行合理的布局和配置。
4. 培训和推广在赋码设备部署完成后,需要对相关人员进行赋码技术的培训,包括设备操作、数据管理流程等内容。
同时,需要进行赋码技术的推广,让更多的员工了解赋码技术的优势和重要性。
5. 监控和维护赋码技术的实施并不是一次性的工作,需要进行持续的监控和维护。
建立赋码技术的监控体系,及时发现和解决问题,确保赋码技术的稳定运行。
四、实施效果通过赋码实施方案的实施,可以实现以下效果:1. 数据管理效率提高:赋码技术可以加速数据的采集和识别,提高数据管理的效率;2. 数据管理成本降低:赋码技术可以简化数据管理流程,降低人力成本和时间成本;3. 数据安全保障:赋码技术可以对数据进行有效的标识和管理,保障数据的安全性和完整性。
五、总结赋码实施方案的制定和实施对于企业的数字化管理具有重要意义。
通过选择适合企业实际情况的赋码技术,对数据进行整理和标识,采购和部署赋码设备,进行培训和推广,建立监控和维护体系,可以实现数据管理效率的提高、成本的降低和数据安全的保障。

电子监管码赋码管理规程文件编号SMP-QA029-00版本号00编制质量管理部审批生效日期电子监管码赋码管理规程1.目的建立药品电子监管码赋码管理规程,规范药品电子监管码的申请、赋码、核注核销等程序,确保电子监管码在整个实施过程的规范及安全有效。
2.适用范围本规程使用于电子监管码实施的整个过程。
3.职责3.1 质量受权人职责:负责电子监管码体系的建立、实施及完善。
3.2 质量部职责:负责电子监管网平台信息的维护、监管码数据申请下载及上传,负责对电子监管码实施过程的监控,废弃码销毁监控。
3.3 生产部职责:负责产品赋码操作及赋码生产线的保管维护。
3.4 物控部职责:负责带有电子监管码包材的保管、发放,赋码产品出库扫码及扫码设备的保管。
3.5 销售部职责:负责赋码产品销售统筹及销售客户信息的维护。
4.定义4.1 电子监管码:电子监管码是国家食品药品监督管理局监管平台所颁发的针对药品监管的编码,每个药品最小包装及上级包装都有一个唯一的编码,是一串由20位数字按照一定规定排序而成的一维码,即电子监管码。
4.2 赋码:就是给每件产品赋予唯一的标识(监管码),每件产品的监管码唯一,即“一件一码”,类似商品的身份证。
4.3 监管码关联关系:在产品赋码过程中,对赋予产品上的电子监管码与包装上的电子监管码建立的内在联系,称为监管码关联关系。
5.规程5.1监管码信息管理5.1.1 由专人(数字证书保管员)负责药品电子监管平台信息的维护,监管码的申请、下载、解密,并保证数据能及时、准确、完整的上传。
5.1.2 电子监管码的申请、保管和使用等操作人员对监管码数据负有保密责任;码和数据不能外泄(包括用过的、没有用过的、报废的、电子的、纸质的、损坏的药盒上的等等)。
5.1.3 监管码委托印刷时需和厂家签订保密协议,承印企业应当保证所印制的监管码标识达到《监管码印刷规范》中所规定的要求,对监管码具有数据保密措施,对印刷残次品销毁制度,不能随意丢弃,以防止被他人利用进行造假。


电子监管码赋码系统验证方案一.目的确认电子监管码赋码系统系统配置齐全,能按照要求采集存储数据,并有权限要求,满足车间的使用要求。
二.适用范围本方案适用于电子监管码赋码系统的验证。
主要验证范围和内容为:计算机系统硬件配置及安装确认,计算机外部设备配置及安装确认,计算机系统软件配置安装确认,计算机启动运行及外部数据链确认,计算机系统的安全权限确认,计算机性能确认。
三.相关责任四、验证条件1.人员培训:灯检机验证方案和相关培训内容的培训情况:2.验证所用的测试仪器仪表已校准并在有效期内。
所涉及到的检验方法已经过验证或为国家法定方法。
五.计算机系统确认1.计算机系统硬件配置及安装确认(1).确认目的确认计算机可以满足运行的条件,保证计算机可以正常运行。
(2).确认方法检查计算机系统各硬件配置,确认计算机的()复合系统运行需求。
(3).确认结果名称:电脑显示屏编号:1.1确认人/日期:复核人/日期:名称:扫码枪编号:1.2确认人/日期:复核人/日期:1.3名称:数据显示器编号:2.计算机系统外部设备配置及安装确认(1).确认目的目视检查电子监管码赋码系统,计算机的外部设备(服务器、工控机、固定光栅扫描器、二级码扫描枪、特殊指令扫描枪、顾客显示屏、条码打印机、手持扫描终端)之间的连接以及计算机与外部设备之间的连接是否符合仪器说明书要求。
服务器、工控机、固定光栅扫描器、二级码扫描枪、顾客显示屏、条码打印机、手持扫描终端。
(2).确认方法检查计算机系统的外部设备,以及安装确认结果。
(3).确认结果确认人/日期:复核人/日期:3.计算机系统软件配置及安装确认(1).确认目的确认计算机系统及运行及检品分析要求。
(2).确认方法检查计算机软件。
(3).确认结果名称:电子监管码赋码系统编号:3.1确认人/日期:复核人/日期:4.计算机系统启动运行及外部数据链确认(1).确认目的确认计算机系统能够正常启动,检测软件能够正常启动,与外部数据链接传输状态正常。

药品电子监管码在赋码过程中的常见问题与处理药品电子监管码的赋码过程是一个比较复杂的操作过程。
首先在《中国药品电子监管网》上根据生产的药品品种、规格和实际生产量,申请监管码并且下载,下载的监管码都为一级未使用状态。
再根据生产需要分成已印刷与未使用状态的监管码,再由专人导入赋码软件,进行扫描赋码,于每一级包装建立包装关系。
在扫描建立包装关系的过程中常常会遇到一些问题,现就这些问题及其处理方法介绍如下。
1.监管码的导入。
在导入监管码时常会出现无法导入、数据存在等问题,解决办法如下:1.1 在导入监管码之前,首先要导入产品码。
具体操作:(1)登陆系统,打开基础信息,选中“产品管理”,点击导入产品,选中所需要的药品信息文件,然后点击打开文件。
如果无法导入,首先查看文件的格式是否正确,药品信息文件的格式必须是“.xml”的文件;(2)导入成功后点击“查询”,此时“查询”旁边的“确认”按钮激活,点击“确认”按钮,便可出现产品码文件当中产品详细的信息。
1.2 导入监管码。
具体操作:在赋码系统中打开“监管码管理”,点击“导入监管码”,导入由《中国药品电子监管网》所下载的药品电子监管码。
在导入过程中如系统提示无法导入,首先需要查看导入文件格式是否正确,监管码文件的格式是“.txt”的文件。
如果还是无法导入,就需要查看文件是否有标头信息,标头信息的格式为(#导入码的级别#导入码所代表的产品编码#无意义#数量)。
例如:#0#13584#00123456#00486666#就代表:#一级#XXX产品#无意义#486666个条码#。
每次下载的标头信息都是不同的,所以在导入前需要查看是否有标头信息,信息格式是否正确。
还有一种情况就是查看文件名是否包含包装规格。
例如:XXX产品一级监管码_盒1支.txt,这“_盒1支”就是包装规格。
如果包装规格不符合,虽然可以导入但是无法扫描,会对包装生产有极大的影响。
1.3 校对经过所有核对,修改后将由《中国药品电子监管网》所下载的药品电子监管码重新导入系统。

电子监管码赋码系统安装、运行、性能确认方案目录1人员职责.................................................. 错误!未定义书签。
2确认背景.................................................. 错误!未定义书签。
3方案培训 (3)4 验证内容 (3)4.1安装确认(IQ) (3)4.2运行确认(OQ) (4)5偏差处理.................................................. 错误!未定义书签。
6附件登记.................................................. 错误!未定义书签。
7总结...................................................... 错误!未定义书签。
8附件...................................................... 错误!未定义书签。
附件1:方案修改申请表...................................... 错误!未定义书签。
1方案培训正式实施此确认方案前,车间副主任应组织电子监管码操作人员、车间相关管理人员、相关QA、相关设备人员开展本确认方案的培训,并评估培训效果,确保本确认方案得到有效实施,将培训记录作为本次确认的附件,设备/计量员将培训检查结果填写于原始记录表12.1安装确认(IQ)2.1.1设备验收设备到厂后设备管理员对照合同、装箱单对该系统的名称、生产厂家、型号、出厂编号、备品备件、主要技术性能参数、文件等进行确认,将验收的详细信息填写于原始记录表2,设备/计量QA员进行复核。
可接受标准:•该系统的外观应无任何损坏、缺失;•备品备件应齐全、完好;•用户说明书或操作手册等技术资料应完整并具有指导性和可操作性;•设备名称、主要技术性能参数信息等应与合同规定一致;2.1.2安装过程确认设备管理员应全程跟进设备的安装过程,整个安装过程符合安装程序要求,将安装过程的检查信息填写在原始记录表3,并得出确认结论,车间副主任进行复核。


中国药品电子监管码赋码操作规程目的:建立药品电子监管码赋码操作规程,规范药品电子监管码的申请、赋码、核销等操作程序,确保电子监管码在整个生产过程中的准确、规范。
范围:本规程使用于电子监管码申请、赋码及出库整个过程。
职责:总工办、生产部、物控部内容1、电子监管码的申请、下载、解密1.1由数字证书保管员从中国药品电子监管网系统提出监管码申请,选择需申请监管码的药品通用名、剂型、规则、包装规格,并输入包装比例、申请数量等信息。
1.2监管码生成后,通过“监管码下载”页面下载已经生产的监管码文件,下载完监管码后,进行确认,点击“监管码解密”菜单,选择监管码加密包文件,然后点击解密进行解密操作。
2、信息导入2.1产品信息导入,由在线赋码操作系统控制台主菜单“数据文件管理”中点击“产品信息导入”,在打开的窗口中点击“浏览”选择导入路径,找到从中国药品电子监管网下载的产品信息文件(*.xml文件),点击“导入”后,将产品信息导入服务器数据库中。
2.2监管码导入,由在线赋码操作系统控制台主菜单“数据文件管理”中的“监管码信息导入”,在打开的窗口中点击“浏览”,选择要导入的监管码文件(*.txt文件),文件打开后会在中间的表格中预览要导入的监管码信息,确认无误后,点击下方“导入”按钮导入监管码文件。
2.3下载后的药监码文件名称和文件格式不能随意更名,否则将无法正常导入赋码系统,由于药监码文件名称中含有系统需要的信息,文件名和格式为国家药监局制定的标准格式不可更改。
3、生产前基础信息设置3.1点击“生产线管理”点击“添加”建立生产车间,生产线,工位,并可通过“添加”、“修改”和“删除”、和对车间、生产线、工位信息进行相应操作。
3.2点击“设备信息管理”添加赋码线所使用的设备信息,扫描枪,固定扫描器属于输入设备,打印机显示牌属于输出设备;点击“设备关联”对已经存在的设备,进行组合关联操作,设置其所在的工位,和其工作包装级别。
电子监管码解决方案随着国家质检总局的大力推进,中国电子监管码整体的应用即将进入一个井喷的状态,对于目前大量的生产企业来说,尽快的使自己的产品能够符合国家电子监管码标准是当务之急~电子监管码的载体,“电子监管码”标签的印刷制作,以及粘贴了电子监管码标签的产品在出厂之前的激活工作,还是让很多企业不知道该如何运作的难点。
如果企业把制作电子监管码的工作全部委托印刷厂来解决,那么又存在如下问题:1、电子监管码数据是企业的机密数据,电子监管码的泄密将使原来赋予电子监管码防伪的主要功效丧失殆尽~2、很难保证印刷企业对电子监管码的浪费,因为印刷企业无法去很好的验证到底打印了多少电子监管码3、企业在粘贴电子监管码的过程中如果出现粘贴失败需要重做一张相同标签将是非常麻烦的事情。
针对上述问题,鑫恒图公司特按照国家标准,结合行业现状推出了一整套针对电子监管码的“制码,激活,追溯”整体软硬件解决方案来满足广大企业的急迫需求。
企业通过部署这套方案完全符合当前的国家标准要求,印刷厂部署这套方案也能有效的满足企业客户的需求。
1、制码硬件:电子监管码采用一品一码原则,也就是说每一件商品都需一个独立的编号,所以就需要采用可变数据制作生成办法,通常有3种办法来进行可变数据的标签的生产:数码印刷机如HP的喷码设备可变数据打印机如北洋BTP-6200I INDIGO系列优速度快,效率高,可整价格相对于数码印刷机便宜成本低廉,单台投资在1万以内,速势体一次印刷很多,约60万人民币度较快,耗材成本低廉,使用简单方价格昂贵,约600万人便,无需专业培训,可以独立使用山劣民币,耗材费用高昂,速度慢,需在生产线上进行组东新北洋生产的条码打印机势需大量教育培训时间合调试较麻烦,耗材较贵 BTP-6200I来实现.才能掌握2、制码软件:赋码工作是企业在中国产品质量电子监管网上获得的电子监管码数据文件,然后应用该文件中的数据制作对应的电子监管码标签。
所以企业除需制码的硬件设备,还需制码的软件,制码软件就是完成自动从监管数据文件中获取数据然后按照国际条码标准控制打印设备打印出符合国家标准的电子监管码标签,这其中涉及到数据的编码,条码的生成,以及图文打印工作。
鼎恒电子监管码赋码印刷解决方案
张文忠
【期刊名称】《印刷技术》
【年(卷),期】2008(000)012
【摘要】在国家大力推行产品电子监管制度的大趋势下,为了更好、更快、更直接地为印刷企业提供优良的设备及服务,帮助解决其中的技术难题,北京鼎恒联合科技有限公司推出以下电子监管码赋码印刷解决方案。
【总页数】1页(P42)
【作者】张文忠
【作者单位】北京鼎恒联合科技有限公司
【正文语种】中文
【中图分类】TS8
【相关文献】
1.药品电子监管码赋码解决方案的选择 [J], 胡泽豪
2.药品电子监管码赋码解决方案探析 [J], 胡建明
3.如何选择合适的电子监管码赋码解决方案 [J], 耿宁辉
4.带中盒包装的自动包装线四级药品电子监管码赋码解决方案 [J], 蒋井明;丁志慧
5.带中盒包装的自动包装线四级药品电子监管码赋码解决方案 [J], 蒋井明;丁志慧因版权原因,仅展示原文概要,查看原文内容请购买。
1 验证目的建立车间药品电子监管码赋码系统验证方案,通过安装确认、运行确认和性能确认,考察确认药品电子监管码赋码系统符合国食药监办【2010】194号文要求,确保系统能正确生成、顺利导出、成功上传生产关联数据、出入库数据至国家监管平台,满足其监管要求。
2 适用范围本方案适用于车间药品电子监管码赋码系统的验证。
3 编写依据国食药监办【2010】194号《关于基本药物进行全品种电子监管工作的通知》4 简述车间药品电子监管码赋码系统是按国食药监办【2010】194号文的统一要求,对公司生产的基本药物XXXX按最小销售包装唯一赋码(监管码附着有生产日期、产品批号、保质期等生产数据),并建立两级包装之间监管码的关联关系,将关联关系上传国家监管平台(对生产数据进行监管);然后在进行出入库业务时扫描外包装监管码,将出入库数据上传国家监管平台(对出入库数据进行监管)。
系统由硬件、软件等部分构成,硬件包括服务器、工控机、固定光栅扫描器、扫描枪、显示器、条码打印机、手持扫描终端等,其中由工控机、固定光栅扫描器、扫描枪、显示器构成的生产线X条,二级码标签打印机1台,系统服务器1台;软件为:XXXX药监赋码系统、系统环境软件等。
XXXX采用两级赋码,一级码由包材供应商直接印刷,抽样后由系统比对复核其状态,二级码由系统条码打印机打印成标签粘贴在外包装箱指定位置;该系统于XXXX年购回、安装、调试验收完毕后投入使用。
根据相关设备验证管理的规定,指定本方案对药品电子监管码赋码系统进行验证。
5 验证计划5.1 安装确认时间安排:5.2 运行确认时间安排:5.3 性能确认时间安排:6 验证职责及小组成员6.1 质保部6.1.1 组织验证方案和报告的审核,负责验证方案和报告的批准。
6.1.2 监督检查整个验证过程实施,处理验证过程中出现的各种问题。
负责对验证过程中出现的偏差进行处理。
6.1.1 验证结束后负责验证结果总结与分析评价。
要求系统/设备满足以下要求(不仅限于)1,电子监管赋码系统整体要求序号要求必需或期望药品监管码赋予系统URS01系统包含电子监管码赋码系统,仓库托盘出入库系统,电子监管码自动线控制系统,条码数据管理服务器系统。
项目范围包括一条瓶装线,一条低速线,三条HSL线,仓库出库,系统配置图见系统回顾部分“系统配置图”。
必需总共5条赋码线吗?都是几级包装几级赋码?URS02数据采集系统为完全独立的 LAN, 不与SFDA和其他外部网络做任何的连接。
但必须保证北京商务部需要在北京进行入库系统操作。
数据采集系统总体架构为:现场控制和数据采集系统,药监码应用服务器。
C/S,B/S架构都能实现,可以满足。
URS03现场控制和数据采集系统包括5条生产线和一个仓库,工厂级药监码服务系统应至少支持 10 台现场控制和数据采集系统。
至少支持URS04对于仓库出库操作,配备至少8套条码扫描终端,条码扫描终端应能够扩充为至少 30 套。
扫描枪(建议无线)必须实现功能:能够实现产品代码(产品名称),产品批号,产品订单数量和出货单及时对应修正,当有唯一条件不符合出库单时系统有明显的警告语出现,并提示详细的出错信息:如订单号码,产品代码,订单数量(多于或少于)出库单需求数量等。
在验证阶段需要对此进行验证。
出入库设备,根据出货量和仓库面积来算的,通过无线来扫描可以实现URS05系统应通过国家药监局“中国药品电子监管网”数据接口测试,符合国家药监局的条码数据库格式的要求,并在两个系统中增加产品代码信息。
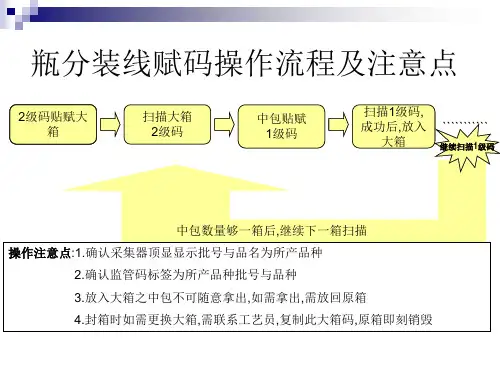
满足URS06小盒条码由小盒供应商变码印刷,条码质量等级为 C 级以上,条码等级由供应方保证; 中包、大箱条码采用集中打印,人工粘贴方式。
中包和大箱都是人工吗?URS07小盒条码一次成功读取率、中包/大箱一次赋码和检测成功率均需达到 99.995%以上。
满足URS08小盒条码读取系统具有自动与系统内已存储数据的比对功能,如有数据重复,系统能够自动提示并剔除。