循环伏安及能级计算
- 格式:ppt
- 大小:2.57 MB
- 文档页数:25




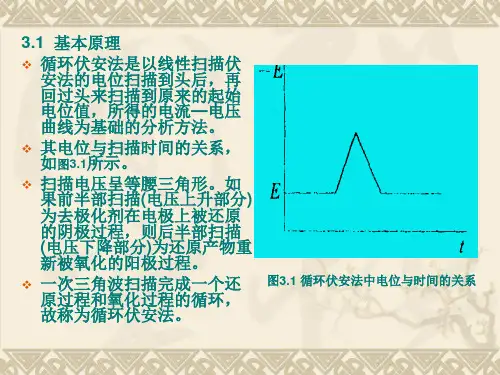

循环伏安法原理及结果分析一、循环伏安法的原理循环伏安法是通过控制工作电极的电位,在一个特定的电位范围内以一定的扫描速率进行循环扫描,同时测量电流随电位的变化。
在典型的循环伏安实验中,工作电极(如铂、金、玻碳等)、参比电极(如饱和甘汞电极、Ag/AgCl 电极等)和辅助电极(通常为铂丝)组成三电极体系,置于含有研究对象的电解质溶液中。
电位扫描通常从起始电位开始,向一个方向扫描到终止电位,然后反向扫描回到起始电位,形成一个完整的循环。
在扫描过程中,电极表面发生氧化还原反应,产生电流。
电流的大小与电极表面发生的电化学反应速率以及反应物和产物的浓度有关。
当电位逐渐增加时,若达到某种物质的氧化电位,该物质就会在电极表面发生氧化反应,产生氧化电流。
反之,当电位逐渐降低时,若达到某种物质的还原电位,该物质就会在电极表面发生还原反应,产生还原电流。
通过测量不同电位下的电流值,可以得到循环伏安曲线。
二、循环伏安曲线的特征循环伏安曲线通常呈现出峰形,包括氧化峰和还原峰。
氧化峰对应于物质的氧化过程,还原峰对应于物质的还原过程。
峰电流(ip)是循环伏安曲线中最重要的参数之一。
峰电流的大小与电活性物质的浓度、扫描速率、电极面积以及电化学反应的速率常数等因素有关。
一般来说,电活性物质的浓度越高,峰电流越大;扫描速率越快,峰电流也越大,但峰形可能会变得更尖锐;电极面积越大,峰电流也越大。
峰电位(Ep)是指峰电流对应的电位值。
氧化峰电位(Epa)和还原峰电位(Epc)之间的差值(ΔEp = Epa Epc)可以反映电化学反应的可逆性。
对于可逆的电化学反应,ΔEp 约为 59/n mV(n 为电子转移数);对于不可逆的电化学反应,ΔEp 通常较大。
此外,还可以通过循环伏安曲线计算出其他参数,如半峰电位(E1/2)、峰宽(W)等,这些参数对于分析电化学反应的性质也具有重要意义。
三、结果分析1、定性分析通过循环伏安曲线的峰电位,可以初步判断发生的电化学反应类型以及参与反应的物质。


循环伏安(fúān)法原理及应用(yìngyòng)小结(xiǎojié) 1 电化学原理(yuánlǐ)1.1 电解池电解池是将电能转化(zhuǎnhuà)为化学能的一个装置,由外加电源,电解质溶液,阴阳电极构成。
阴极:与电源负极相连的电极(得电子,发生还原反应)阳极:与电源正极相连的电极(失电子,发生氧化反应)电解池中,电流由阳极流向阴极。
1.2 循环伏安法1)若电极反应为O+e-→R,反应前溶液中只含有反应粒子O,且O、R在溶液均可溶,控制扫描起始电势从比体系标准平衡电势(φ平)正得多的起始电势(φi)处开始势作正向电扫描,电流响应曲线则如图0所示。
图0 CV扫描电流响应曲线2)当电极电势逐渐负移到(φ平)附近时,O开始在电极上还原,并有法拉第电流通过。
由于电势越来越负,电极表面反应物O的浓度逐渐下降,因此向电极表面的流量和电流就增加。
当O的表面浓度下降到近于零,电流也增加到最大值Ipc,然后电流逐渐下降。
当电势达到(φr)后,又改为反向扫描。
3)随着电极电势逐渐变正,电极附近可氧化的R粒子的浓度较大,在电势接近并通过(φ平)时,表面上的电化学平衡应当向着越来越有利于生成R的方向发展。
于是R开始被氧化,并且电流增大到峰值氧化电流Ipa,随后又由于R的显著消耗而引起电流衰降。
整个曲线称为“循环伏安曲线”1.3 经典三电极体系经典三电极体系由工作电极(WE)、对电极(CE)、参比电极(RE)组成。
在电化学测试过程中,始终以工作电极为研究电极。
其电路原理如图1,附CV图(图2):扫描范围-0.25-1V,扫描速度50mV/S,起始电位0V。
图1 原理图图2 CBZ的循环伏安(fúān)扫描图图2所示CV扫描(sǎomiáo)结果为研究(yánjiū)电极上产生的电流随电位(di àn wèi)变化情况图。

循环伏安法介绍循环伏安法(Cyclic Voltammetry,简称CV)是一种电化学测试方法,广泛应用于表征电化学反应的动力学、电化学过程的机理和电极材料的性质等方面。
该方法通过不断改变电极电位,并测量对应的电流,来获得电化学反应过程中的电化学信息。
原理循环伏安法基于电化学基础理论和法拉第定律,利用电极材料与电解质溶液之间的电化学反应,在电位范围内,通过施加正向和负向扫描电压,观察电流的变化,得到伏安图。
伏安图表示了电流与电极电位之间的关系,反映了电化学反应的动力学与热力学信息。
实验步骤1.准备工作:清洗电极并将其与计量电位仪连接好。
2.准备电解质溶液:根据实验需求,配置适当浓度的电解质溶液,并使用磁力搅拌器搅拌均匀。
3.实验设置:将电解质溶液注入电解池中,并使电极浸入其中。
根据需要,设置施加电压的扫描范围和扫描速率。
4.实验操作:打开计量电位仪,设置初始电位,并开始扫描。
仪器会逐渐改变电极电位,并记录对应的电流值。
5.数据处理:根据实验结果,绘制伏安图,并分析图形特征。
根据法拉第定律,可以计算电极反应的电荷转移系数、反应速率常数等参数。
应用循环伏安法在电化学和材料科学领域有着广泛的应用。
1.电化学催化研究:循环伏安法可以用于表征电化学催化剂的活性和稳定性,评估催化剂对某种电化学反应的催化效率。
2.电极材料研究:通过循环伏安法可以评估电极材料的电活性表面积、电荷传递速率以及与电解质溶液之间的界面反应。
3.电化学反应动力学研究:利用循环伏安法可以确定电极反应的控制步骤和反应机理,并研究电化学反应速率与温度、扫描速率等因素的关系。
优点和局限循环伏安法具有以下优点:•实验步骤简单,容易操作。
•可以快速获取材料的电活性表面积等信息。
•可以在不同电位下观察电化学反应的动力学与热力学变化。
然而,循环伏安法也存在一些局限性:•无法直接获得电化学反应的反应速率常数等定量信息。
•实验数据分析较为复杂,需要依赖理论模型和数学计算。


循环伏安cv 计算电容现今,电容器是电子工程中使用最广泛的一种元件,把它们用到各种电路中,以满足各种应用的需求。
然而,如何准确地确定电容器的容量是一个重要的问题,因为它们的容量决定了电路的性能。
在一些情况下,可以通过实验来测量电容器的容量,但这种方法不够精确,且耗费时间。
因此,开发一种比较准确的方法来测量电容器的容量是十分重要的。
伏安测量技术是计算并确定电容器容量的一种有效方法。
它是一种利用伏安效应来测量电容器容量的方法。
伏安效应指在交流电压下,电容器内电容量随着交流频率的增加而发生改变。
这意味着如果能够测量电容器在不同频率下的伏安值,就能够确定电容器的容量。
这就是伏安cv计算电容的基本原理。
伏安cv计算电容技术是由英国科学家吉尔伯特卢纳尔多夫在1964年发明的。
卢纳尔多夫指出:在给定的范围内,可以测量2个不同频率的伏安值,通过测量的这2个结果,就可以确定电容器的容量。
这也是伏安cv计算电容的基本原理。
伏安cv计算电容技术为循环伏安法,与其他常见的电容容量测量方法相比,更加精确、快捷且稳定可靠,在实际应用中效果较好。
首先,它可以准确测量电容器的容量,因此可以有效控制电路的性能。
此外,由于可以循环使用伏安cv计算电容,因此在不断变化的电容器容量值的情况下,可以获得和伏安cv测量法一致的结果。
从技术上而言,伏安cv计算电容主要包括以下几个步骤:1.置交流电源,并测量电容器一次通过一段时间后的电流和电压;2.置调节器,测量不同频率的电容器一次通过一段时间后的电流和电压;3.过测量第2步中不同频率时的电容器伏安值,计算电容器的容量;4.过调节调节器,不断调整调节器的相位,循环重复第2步和第3步的操作,以获得不同频率下的电容器容量。
最后,伏安cv计算电容技术因其精确、快捷、稳定可靠的特点,在电子工程中应用得越来越广泛,可以有效地缩短电容容量测量的时间,提高电路的性能。
循环伏安法定义+原理+参数设置一、循环伏安法(Cyclic Voltammetry)一种常用的电化学研究方法。
该法控制电极电势以不同的速率,随时间以三角波形一次或多次反复扫描,电势范围是使电极上能交替发生不同的还原和氧化反应,并记录电流-电势曲线。
根据曲线形状可以判断电极反应的可逆程度,中间体、相界吸附或新相形成的可能性,以及偶联化学反应的性质等。
常用来测量电极反应参数,判断其控制步骤和反应机理,并观察整个电势扫描范围内可发生哪些反应,及其性质如何。
对于一个新的电化学体系,首选的研究方法往往就是循环伏安法,可称之为“电化学的谱图”。
本法除了使用汞电极外,还可以用铂、金、玻璃碳、碳纤维微电极以及化学修饰电极等。
1.基本原理如以等腰三角形的脉冲电压加在工作电极上,得到的电流电压曲线包括两个分支,如果前半部分电位向阴极方向扫描,电活性物质在电极上还原,产生还原波,那么后半部分电位向阳极方向扫描时,还原产物又会重新在电极上氧化,产生氧化波。
因此一次三角波扫描,完成一个还原和氧化过程的循环,故该法称为循环伏安法,其电流—电压曲线称为循环伏安图。
如果电活性物质可逆性差,则氧化波与还原波的高度就不同,对称性也较差。
循环伏安法中电压扫描速度可从每秒种数毫伏到1伏。
工作电极可用悬汞电极,或铂、玻碳、石墨等固体电极。
2.循环伏安法的应用循环伏安法是一种很有用的电化学研究方法,可用于电极反应的性质、机理和电极过程动力学参数的研究。
但该法很少用于定量分析。
(1)电极可逆性的判断循环伏安法中电压的扫描过程包括阴极与阳极两个方向,因此从所得的循环伏安法图的氧化波和还原波的峰高和对称性中可判断电活性物质在电极表面反应的可逆程度。
若反应是可逆的,则曲线上下对称,若反应不可逆,则曲线上下不对称。
(2)电极反应机理的判断循环伏安法还可研究电极吸附现象、电化学反应产物、电化学—化学耦联反应等,对于有机物、金属有机化合物及生物物质的氧化还原机理研究很有用。
循环伏安法原理及结果分析循环伏安法(Cyclic voltammetry,CV)是一种电化学分析方法,常用于研究电极上的化学和电化学反应以及物质的电化学行为。
它通过改变电极电位并测量所引起的电流变化,得到一个电流-电压(I-V)曲线,从而分析电化学反应的特性和机理。
CV实验通常使用一个工作电极、一个参比电极和一个辅助电极的电化学电池。
工作电极是用来进行电化学反应的电极,参比电极用来测量工作电极与参比电极之间的电位差,辅助电极用来提供能量以促进电化学反应的进行。
实验中,通过改变工作电极的电位,可以在电化学电池中引起氧化还原反应。
结果是电流的变化,这个变化被记录下来以产生I-V曲线。
CV实验中的结果分析包括几个方面:1.反应的电位范围:通过改变工作电极的电位扫描范围,可以确定反应的电位范围。
通常将电位从一个初始电位线性地扫描到另一个终止电位,然后再返回到初始电位。
扫描速率和电位范围的选择取决于所研究的电化学反应和物质的性质。
2.峰电位和峰电流:CV曲线通常包含多个峰,每个峰对应于一个电化学反应。
峰电位是峰的中心电位,表示氧化和还原反应的临界电位。
峰电流是峰的最大电流值,表示反应速率和物质浓度的关系。
通过测量峰电位和峰电流,可以确定反应的动力学和热力学参数。
3.峰形:CV曲线的峰形可以提供有关反应机理的信息。
对于可逆反应,峰电流正比于扫描速率;对于不可逆反应,峰电流与扫描速率无关。
峰形也可以显示反应的控制步骤,如扩散控制、电极控制或混合控制。
4.电化学反应的类型:通过分析CV曲线的形状和特征,可以确定电化学反应的类型。
例如,CV曲线中的一个峰表示一个氧化还原反应,而CV曲线中的两个峰表示一个两步反应。
5.物质的电化学行为:CV实验也可以用来研究物质在电极上的电化学行为。
通过改变溶液pH、阳离子或阴离子的浓度,可以观察到电化学反应的变化。
此外,还可以测量不同溶液中的CV曲线并进行比较,以了解物质在不同环境中的电化学性质。