分子克隆实验设计
- 格式:ppt
- 大小:1.13 MB
- 文档页数:38

分⼦克隆实验标准步骤分⼦克隆实验标准步骤⼀、常规分⼦克隆实验流程:⼆、分⼦克隆实验标准步骤(含实验编号):1. PCR 扩增⽬的基因(编号Clone SOP-1)以本实验室常⽤酶KOD-Plus-Neo (TOYOBO )为例体系(50ul ):10×KOD buf 5uldNTP(2mM) 5ulMg 2+ 3ulPrimer1 1ulPrimer2 1ulTemplate50-200ngKOD0.5ulddH 2O up to 50ul程序:95℃2min98℃10s58℃30s 35cycle68℃2kb/min68℃7min12℃∞2.PCR产物的琼脂糖凝胶电泳琼脂糖凝胶的制备(编号Clone SOP-2)琼脂糖溶液的制备:称取琼脂糖,置于三⾓瓶中,按1%-1.5%的浓度加⼊相应体积的TBE或TAE缓液,将该三⾓瓶置于微波炉加热⾄琼脂糖溶解。
胶板的制备:①取有机玻璃内槽,洗净、晾⼲;②将有机玻璃内槽置于⼀⽔平位置模具上,安好挡板,放好梳⼦。
在距离底板上放置梳⼦,以便加⼊琼脂糖后可以形成完好的加样孔。
③将温热琼脂糖溶液倒⼊胶膜中,使胶液缓慢地展开,直到在整个有机玻璃板表⾯形成均匀的胶层。
④室温下静置30min左右,待凝固完全后,轻轻拔出梳⼦,在胶板上即形成相互隔开的上样孔。
制好胶后将铺胶的有机玻璃内槽放在含有0.5~1×TAE(Tris-⼄酸)或TBE(Tris-硼酸)⼯作液的电泳槽中使⽤,没过胶⾯1mm以上。
3.试剂盒回收DNA⽚段(编号Clone SOP-3)以本实验室常⽤DNA凝胶回收试剂盒(天根)为例使⽤前请先在漂洗液PW中加⼊⽆⽔⼄醇,加⼊体积请参照瓶上的标签。
①柱平衡步骤:向吸附柱CA2中(吸附柱放⼊收集管中)加⼊500µl平衡液BL,12,000rpm(~13,400×g)离⼼1min,倒掉收集管中的废液,将吸附柱重新放回收集管中。
(请使⽤当天处理过的柱⼦)②将单⼀的⽬的DNA条带从琼脂糖凝胶中切下(尽量切除多余部分)放⼊⼲净的离⼼管中,称取重量。

分子克隆技术实验报告姓名:班级:学号:指导老师:pUC19外源1.5kbDNA片段亚克隆于pUC1301摘要:分别从大肠杆菌菌液中提取质粒pUC19和pUC1301,两种质粒都使用Bam HI+Kpn I两种限制性内切酶进行切割。
回收pUC1301质粒中1.5kb片段,使用连接酶将它与切开的pUC19连接,转化感受态大肠杆菌,利用标记基因amp r、kan r和α—互补筛选阳性克隆。
实验获得了很好的酶切效果,但最后没有筛选出阳性克隆。
关键词:pUC19、pUC1301、亚克隆、限制性内切酶、感受态1前言初始克隆中的外源DNA片段往往较大,含有许多目的基因以外的片段,在诸如表达、序列标签和突变等操作中不变进行,因此必须将目的基因所对应的小片段DNA找出来,这个过程叫做亚克隆。
本实验是将pU1301中一段来自水稻1.5kb的片段亚克隆到pUC19上。
首先需要提取所需的质粒。
在大肠杆菌中质粒又大又小、拷贝数又多又要少,因此分离的方法也多种多样。
在实践中最常见的是通过将裂解法提取高拷贝的小质粒以及基于此方法的纯化技术,其他方法还有试剂盒分离纯化等,本实验通过试剂盒分离纯化E.coil质粒DNA。
将质粒提取出来后需要检测所获质粒的质量,方法有吸光值检测、凝胶电泳检测等。
要获得目的片段然后亚克隆与其他载体上,需使用两种工具酶:限制性内切酶、连接酶。
限制性酶切酶主要有三类,目前使用最多的是Ⅱ型。
限制性内切酶的使用需要在合适的条件下,当条件不合适时往往会出现星星活性。
限制性内切酶产生的黏性末端将导致载体自连,为了防止其自连,可以使用双酶切、去磷酸化、末端补平等方法。
连接酶是将两段核酸连接起来的酶,常用的有T4DNA连接酶、大肠杆菌DNA连接酶、TaqDNA连接酶、T4RNA连接酶。
目的片段和载体在连接酶作用下连接成一个整体,需借助一定方法导入受体细胞,首先需要制备感受态细胞,这类细胞处在易吸收外源DNA 条件下,然后通过电转化、CaCl2转化法将外源DNA导入受体细胞。

一、扩增1、LB培养基5ml;2、抗生素:1000X,即1:1000比例。
种类根据细菌抗性决定;3、菌体:看浑浊度,1%-5%,取500ul于其中;4、37℃摇床220转,过夜,12-16h。
二、纯化质粒DNA1、1.5ml离心管,编号一定要写清楚;2、加满离心管,离心12000xg. 1min,弃上清。
取三次;3、加Buffer S1 200ul,溶解沉淀,5min;4、加S2(用完立刻盖紧瓶盖,以免CO2中和Buffer中的NaOH)200ul,不能剧烈(以免基因组DNA的污染),上下翻转4-6次,直至形成透亮的溶液,时间少于5min。
目的是使蛋白包裹基因组DNA,游离质粒;5、加S3 280ul,温和充分翻转混合6-8次,12000xg,10min(此步呈白色絮状);*备注:S1:S2:S3=5:5:76、取上清加入制备管(置于2ml离心管),12000xg,1min,去滤液;7、加Buffer W1 500ul,12000xg,1min,弃滤液;8、加Buffer W2 700ul,12000xg,1min,弃滤液。
重复一遍;9、空管离心12000xg,1min;10、制备管移入新的1.5ml离心管,管膜中加60-80ul去离子水,静置1min,12000xg,1min。
(将去离子水加热至65度,将提高洗脱效率)四、跑胶回收:sost回收失败1、2%浓度胶,Loading Buffer如是6X,则加10ul到样品,全部加样到胶孔中。
插入:配胶方法大块胶60ml;小块胶25ml;需要配置大块胶、大孔胶;Agarose 0.6g,TAE60ml,微波中火2min;趁热但不烫手时加入gold view 0.5ul/25ml;倒入槽里。
2、跑胶:单位厘米/5-10v。
所以大槽25cm,150v即可。
小槽100v即可。
3、紫外灯下切胶,纸巾吸进液体,计算凝胶重量(1mg=1ul);4、加3个凝胶体积的凝胶结合液DB(0.1ul视为100ul;如凝胶浓度大于2%,则加入6倍体积溶胶液;凝胶块最大不能超过400ul,超过可多个离心柱);5、56℃水浴放置10分钟,至完全溶解;6、每100mg最初的凝胶重量加入150ul的异丙醇,震荡混匀,回收大于4Kb的片段可不加异丙醇,加入反而降低回收效率;7、将上一步所得溶液加入吸附柱AC中(吸附柱放入收集管中),12000rpm,30-60s,弃液体;8、加700ul漂洗液WB,12000rpm,1min,弃废液;9、加500ul漂洗液WB,12000rpm,1min,弃废液;10、空离心2min,弃废液;11、晾干乙醇,以免抑制下游反应;12、将吸附柱放入新的1.5ml离心管,加入50ul(最少30ul)洗脱缓冲液EB或者去离子水(65-70水浴加热效果更好,或将得到的溶液重新加入离心柱可增加洗脱量);五、连接体系:六、转化1、加感受肽:连接产物=10:1,冰浴30min;2、激活:42℃,90s,不能震动;3、加500ul LB培养基;4、37℃,150转摇床,45min;5、铺板子七、检测1、细菌长势良好,对照组不长;2、酶切检测:(1)1ml LB体系:1ml LB培养基+1ul抗生素于1.5mlEP管中;(2)15ul Pcr体系:7.5ul Mix(2X)5.5ul water1ul上游引物1ul下游引物(3)用枪头挑培养皿中的菌体,吹打于1ml LB体系中,再吹打于15ul Pcr体系中;(4)1ml LB体系放入37℃摇床,150rpm;显示4°/4°时,结束。
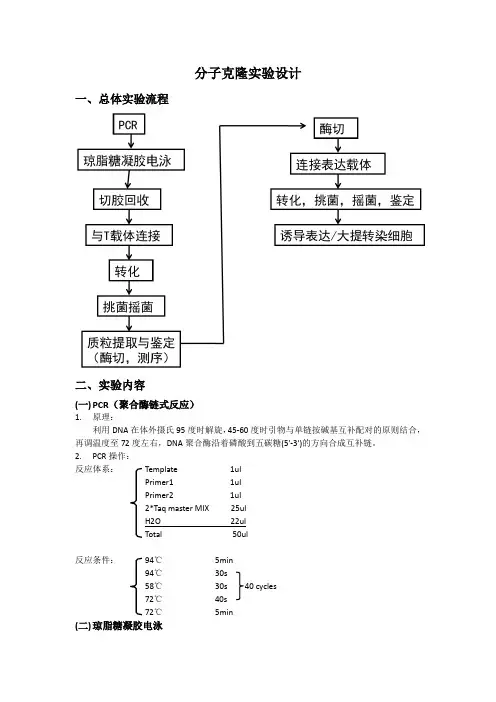
分子克隆实验设计一、总体实验流程二、实验内容(一)PCR(聚合酶链式反应)1.原理:利用DNA在体外摄氏95度时解旋,45-60度时引物与单链按碱基互补配对的原则结合,再调温度至72度左右,DNA聚合酶沿着磷酸到五碳糖(5'-3')的方向合成互补链。
2.PCR操作:反应体系:Template 1ulPrimer1 1ulPrimer2 1ul2*Taq master MIX 25ulH2O 22ulTotal 50ul反应条件:94℃5min94℃30s58℃30s 40 cycles72℃40s72℃5min(二)琼脂糖凝胶电泳1.原理:琼脂糖凝胶具有网络结构,分子通过时会受到阻力,大分子物质在涌动时受到的阻力大,因此在凝胶电泳中,带电颗粒的分离不仅取决于净电荷的性质和数量,而且还取决于分子大小。
2.凝胶电泳步骤:1)称取0.5g琼脂糖至50ml 电泳缓冲液(TAE)中,摇匀;同时装置制胶架。
2)加热至琼脂糖完全融化,期间停止加热摇动3次,即无可见漂浮物,澄清为止。
3)加入1ulEB染液,充分摇匀。
4)缓慢倒入制胶架内,冷却30-60min,至凝胶充分凝固,放入电泳槽中即可使用。
5)使用时,将样品点入相应的加样孔内,即可开始电泳,待指示剂位于整块凝胶2/3位置时,停止电泳,在紫外灯下观察样品条带。
(三)切胶回收(天根生化公司凝胶回收试剂盒)1. 将空小离心管称重。
将回收的带DNA 片段的凝胶放入其中、再次称重,确定凝胶净重。
2. 将离心管中的凝胶捣碎以助于凝胶溶解。
按胶的重量加入三倍体积的Extraction buffer (1mg凝胶加3μl Extraction buffer )。
3. 55℃恒温加热直到凝胶完全融化(5-15 分钟),每隔2-3分钟需将管内混悬液混匀一次。
4. 按照1:1比例加入异丙醇(1mg凝胶加1μl异丙醇),混匀。
5. 将混合液全部移入Spin column、6000rpm离心1分钟,弃去接液管中的液体。

分子克隆技术实验讲义黑龙江大学生命科学学院2016年3月甜菜M14品系BvM14-glyI基因的克隆与鉴定一、实验目的1、熟悉和了解目的基因克隆与鉴定的过程和方法。
2、学习和掌握质粒、T载体的特点。
3、学习和掌握TA克隆的连接体系及操作要点。
4、学习和掌握XcmⅠ酶切制备T载体的过程及方法。
5、学习和掌握CaCl2法制备大肠杆菌感受态细胞的原理和方法。
6、学习并掌握热激法转化技术的原理和操作步骤。
7、学习并掌握重组子鉴定和筛选的原理及蓝白筛选的原理和方法。
8、学习并掌握碱法小量制备质粒DNA的原理及操作步骤。
二、相关知识(一)T载体的制备pMD18-T Vector是一种高效克隆PCR产物(T-A Cloning)的商业化专用载体,由pΜC 18载体改建而成。
在pΜC 18多克隆位点处的XbaⅠ和SalⅠ识别位点之间插入了EcoRⅤ识别位点,用EcoRⅤ进行酶切反应后,再左两侧的3′端添加“T”而成,可以大大提高PCR产物的连接、克隆效率。
相关知识点:(1)质粒的提取;(2)酶切;(3)PCR等。
(二)DNA的重组与连接(PCR产物的克隆)把DNA片段从某一类型的载体无性繁殖到另一类型载体中,例如从某种质粒克隆到另一种质粒,这个过程称为亚克隆。
所谓重组,就是把外源目的基因“装进”载体的过程,即DNA的重新组合。
为了将目的基因重组于载体分子中,需要将载体DNA和目的基因分别进行适当处理,一般采用内切酶法将载体DNA分子切割成可与外源基因连接的线性分子,使其与相同酶切过的载体分子相互连接,彼此成为配伍末端(compatible end),以产生末端连接。
现在一些生物公司也开发了针对不同插入DNA片段的专用载体,如专门用于克隆PCR产物的载体,大大方便了实验操作。
相关知识点:(1)克隆与亚克隆;(2)DNA重组;(3)内切酶;(4)粘性末端与平末端;(5)连接酶;(6)连接酶的分类及功能等。
(三)大肠杆菌感受态细胞的制备外源基因与载体在体外连接成重组体DNA分子后,需将其导入受体细胞进行扩增和筛选,得到大量、单一的重组体分子,这就是外源基因的无性繁殖,或称为克隆。

做了快一年的分子克隆,犯了很多错误,经历了很多坎坷,也学到了很多东西。
分子克隆过程中出现问题最多的大概就是连接了,大家抱怨的也最多,我也陷入在个步骤上很久。
经过长时间的摸索我在连接这个问题上有一些体会,在这里跟大家分享一下我的经验,以供和我一样陷入困境及刚开始做克隆的同学参考。
关于连接的提问多集中在连接的体系、DNA的用量、vector和insert的比例、连接酶等。
但是我认为,连接不成功,问题并不一定出在连接这步上。
有很多环节影响连接的成败,如酶切的好不好、回收的质量好坏、连接时的浓度或比例、感受态等。
以下我详细说明。
1,PCR引物的设计。
通俗的不说,需要指出的是设计引物时一定要考虑切点的甲基化问题。
做普通的克隆会涉及到甲基化形式有两种:dam甲基化和dcm甲基化。
常用的大肠杆菌都有这两种甲基化酶。
dam甲基化酶识别GATC位点并甲基化;dcm甲基化酶识别CCWGG 位点(W是A或T)并甲基化。
如果有这两种位点那么多数情况内切酶是切不开了。
容易受甲基化影响的内切酶有:Dpn1(GA/TC)天生就甲基化;Cla1(A TC/GAT)如果前面加个G或后面加个C那么恭喜你,dam甲基化;Xba1(T/CTAGA)如果前面加个GA或后面加个TC也是dam甲基化,等等有好多。
这些容易甲基化的切点设计引物时一定要注意,避免引入甲基化位点。
如果真是避免不了或者后来才发现问题,那么把甲基化的质粒转化到甲基化酶缺陷型大肠杆菌中再提质粒就没有甲基化,可以切了。
甲基化缺陷型菌有:DM1(Invitrogen)、INV110(invitrogen)、JM110等。
2,PCR产物。
两种方式:一种纯化后直接酶切连接;一种连T载体再往下切连接。
我个人强烈建议第二种,连T载体。
因为PCR产物直接酶切我觉得有两个缺点:①由于两头把手太短,虽说有保护碱基,但我觉得还是不如从质粒上往下切好切,而且容易切坏、切碎;②无法从电泳上看出来切没切开,因为也就切下了几个十几个bp,带形没啥变化。

在大肠杆菌中表达克隆化基因导言方案 1.用IPTG诱导启动子在大肠杆菌中表达克隆化基因方案 2.用T7噬菌体启动子在大肠杆菌中表达克隆化基因方案 3.用λ噬菌体P L启动子在大肠杆菌中表达克隆化基因方案 4.用碱性磷酸酶启动子(pho A)和信号序列在大肠杆菌中分泌表达外源蛋白------附加方案:phoA融合蛋白的亚细胞定位方案 5.谷胱甘肽琼脂糖亲和层析纯化融合蛋白方案 6.直链淀粉树脂亲和层析纯化麦芽糖结合融合蛋白方案7.用固化Ni2+吸收色谱纯化带有组氨酸标签的蛋白------替代方案:用pH递降的缓冲液从金属亲和柱洗脱多聚组氨酸标签蛋白------附加方案:NTA- Ni2+琼脂糖再生方案8.从包涵体中纯化表达蛋白------附加方案:重折叠从包涵体提取的溶解蛋白方案9.9信息栏克隆基因的表达大肠杆菌表达系统LacZ融合离液剂导言方案 1.用IPTG诱导启动子在大肠杆菌中表达克隆化基因(一)引言带异丙基-β-D硫代半乳糖苷(IPTG)诱导启动子的质粒表达外源蛋白的总量可以达到全菌蛋白的30%以上。
这些质粒非常适于实验室小规模操作,但IPTG价格昂贵,不能用于大规模制备外源蛋白。
(二)实验方案A.材料1.缓冲液和溶液a)考马斯亮蓝染色溶液或银染溶液b)IPTG (1mmol/L)c)1*SDS凝胶加样缓冲液d)10% SDS-PAGE2.载体和细菌菌株a)带有lacI q或lacI q1等位基因的适于转化的大肠杆菌菌株带有lacI q等位基因的IPTG诱导表达质粒可以转化实验室的任何大肠杆菌菌株(如JM1, DH5F’,TG1等)。
b)IPTG诱导的表达载体c)阳性对照质粒(表达已知大小的LacZ融合蛋白的IPTG诱导载体)3.培养基(如何配制?---分子克隆附录及科技出版社。
)a)含氨苄(50μg/ml)的LB琼脂平板b)含氨苄(50μg/ml)的LB培养基c)含氨苄(50μg/ml)的LB培养液4.专用设备a)沸水浴b)振荡培养箱5.细胞和组织6.附加试剂B.方法含重组表达载体的大肠杆菌菌株的构建1.PCR2.含3.重组质粒4.通过诱导靶蛋白表达的优化5.对照菌和重组菌分别挑取1~2个菌落,接入1ml含氨苄青霉素(50μg/ml)的LB培养液,适当温度(20~37℃)培养过夜(~16h)。

第1篇一、实验目的本实验旨在学习分子克隆技术的基本原理和操作步骤,掌握目的基因的扩增、克隆及表达,为后续相关研究奠定基础。
二、实验原理分子克隆技术是指将目的DNA片段从供体细胞中分离出来,通过体外重组、转化和转导等方法,将其插入到克隆载体中,再将其引入宿主细胞进行复制和扩增。
本实验采用无缝克隆技术,通过T5核酸外切酶、DNA聚合酶和DNA连接酶三种酶的共同作用,实现单片段或多片段与载体连接。
三、实验材料1. 试剂:限制性内切酶、DNA连接酶、T5核酸外切酶、DNA聚合酶、dNTPs、Taq DNA聚合酶、PCR引物、载体DNA、目的基因DNA、质粒提取试剂盒、琼脂糖凝胶电泳试剂盒等。
2. 仪器:PCR仪、凝胶成像仪、电泳仪、紫外灯、超净工作台、离心机、恒温水浴锅、移液器等。
四、实验步骤1. 目的基因扩增(1)设计引物:根据目的基因的序列设计特异性引物,引物长度一般在18-25bp,5'端添加限制酶切位点。
(2)PCR反应:配制PCR反应体系,加入引物、模板DNA、dNTPs、Taq DNA聚合酶等,进行PCR反应。
2. 载体线性化(1)酶切:使用限制性内切酶对载体DNA进行酶切,获得线性化的载体。
(2)去磷酸化:对单酶切得到的线性化载体进行去磷酸化处理。
3. 目的基因与载体连接(1)同源臂连接:将目的基因PCR产物和线性化载体进行同源臂连接,确保目的基因正确插入载体。
(2)连接反应:配制连接反应体系,加入目的基因PCR产物、线性化载体、DNA连接酶等,进行连接反应。
4. 转化与筛选(1)转化:将连接产物转化至宿主细胞中。
(2)筛选:通过抗生素筛选、酶切鉴定和测序等方法筛选出含有目的基因的克隆。
5. 目的基因表达(1)重组质粒提取:从筛选出的阳性克隆中提取重组质粒。
(2)重组质粒转化:将重组质粒转化至表达宿主细胞中。
(3)表达产物检测:通过Western blot、ELISA等方法检测目的蛋白的表达水平。

分子克隆及细胞培养基本实验方法1.载体构建实用操作技术1.1菌种的保存—20%甘油菌2体积菌液与1体积70%的甘油混合后,储存于-20℃或-70℃备用。
(甘油菌中甘油的浓度为20-30%均可)1.2甘油菌复苏、培养方法一、挑取甘油菌一环,接种在含100ug/ml Amp的LB固体培养基上(活化菌种),37℃培养过夜(约16小时);挑取一个菌落转接在含100ug/ml Amp的LB液体培养基中,37℃振荡过夜(约12~16小时)。
方法二、直接吸取10~20ul甘油菌,接种在含100ug/ml Amp的LB液体培养基中,37℃振荡过夜(约12~16小时)。
1.3小规模制备质粒DNA(QIA miniprep kit )适于从1~5ml 菌液中制备20ug高拷贝质粒⑴收集菌液,离心1000rpm,1分,弃上清⑵以250ul P1重悬细菌(P1中已加RNase)⑶加入250ul P2,颠倒4~6次轻混,约2~3分(轻混以免剪切基因组DNA,并免长时间消化)⑷加入350ul N3,迅速颠倒4~6次轻混;离心10分,13 000rpm⑸上清入QIAprep柱,离心30~60秒,滤液弃之⑹加入0.5ml PB洗,离心30~60秒⑺加入0.75ml PE洗,离心30~60秒,弃滤液,再离心1分⑻换新管,加入50ul EB,静置1分(EB 37℃预热),离心1分。
1.4酶切反应⑴体系构成(反应体系尽可能小!)pGEM3ZF-huCTLA4-Ig(ul)pAdTrack-CMV(ul)①dd.H2O 17 17②10×NEbuff 2 3 3③10×BSA 3 3④底物DNA 5 5⑤内切酶HindⅢ 1 1XbaⅠ 1 1Total : 30 ul 30ul⑵37℃水浴1~2小时,必要时延长酶切时间至12小时⑶酶切2小时后,取5-10ul 电泳观察酶解是否完全⑷65℃灭活内切酶⑸-20℃保存备用1.5回收目的片段(QIAquick Gel extraction Protocol)⑴胶,尽可能去除多余的胶,称重;⑵加入适量buff QG(300ul QG /100mg胶);>2%的胶,应加大QG用量(600ulQG /100mg);⑶水浴50℃,10min,每2-3min混匀一次,使胶完全溶解!必要时延长水浴时间,胶完全溶解后混合物颜色应为黄色,与buff QG 相似;⑷当DNA片段在<500bp或>4kb时,应加入异戊醇100ul/100mg胶,以提高产物量。

分子克隆操作步骤1.RNA提取实验步骤实验前准备:A.用酒精棉将所有物品擦拭干净。
B.准备好蓝枪头、黄枪头、1000ul枪、-20℃冰箱保存的无水乙醇、酒精棉、PE手套、盛有烧碱烧杯、垃圾盒等。
C:紫外照射10分钟左右。
实验步骤1.于-38℃冰箱最上层取出一只1000ul细胞毒液,用冰盒装好。
2.将细胞毒分装入3个无菌管,冰盒上进行操作。
每只无菌管中加入等量的RLT,轻轻摇匀。
3.放入4℃冰箱,变性10min。
4.离心3min,转速大于10000rpm。
5.向三只无菌管中加入等量无水乙醇,混匀,轻轻摇晃5-6次。
6.将3只无菌管溶液分多次装入两只离心柱中,每只离心柱700ul。
7.离心15s,除去下层离出液。
8.取700ulRWI加到离心柱中,离心15s,除去下层离出液。
9.将离心柱转移到新的无菌管中。
10.取500ulRPE加到离心柱中,离心15s,除去下层离出液。
11.取500ulRPE加到离心柱中,离心2min,除去下层离出液。
12.将离心柱转移到新的无菌管中。
取无Rnase水40ul(一般30-50ul左右),离心1min,无菌管标记:一洗,日期。
13.取无Rnase水30ul,离心1min,无菌管标记:“二洗,日期”。
14.将提取好的RNA放于-20℃冰箱保存。
2.反转录常用的反转录体系(按以下体系加完样后,37℃水浴1.5h)A4‘片段反转录体系:5X AMV Buffer : 4 ulAMV : 2 ulE4’: 1 ul20ul RRI :0.5 ul10mM dNTP : 2 ulRNA :10.5ul(注:A4‘片段上游引物:AWW5307 下游引物:E4’)A3‘片段反转录体系:5X AMV Buffer : 4 ulAMV : 2 ulAHN5667(-) : 1 ul20ul RRI :0.5 ul10mM dNTP : 2 ulRNA :10.5ul(注:A3‘片段上游引物:AHNXX502(+)、AHNXX600(+)、下游引物: AHN5667(-)、AHNXX5581(-)。

一、扩增1、LB培养基5ml;2、抗生素:1000X,即1:1000比例。
种类根据细菌抗性决定;3、菌体:看浑浊度,1%-5%,取500ul于其中;4、37℃摇床220转,过夜,12-16h。
二、纯化质粒DNA1、1.5ml离心管,编号一定要写清楚;2、加满离心管,离心12000xg. 1min,弃上清。
取三次;3、加Buffer S1 200ul,溶解沉淀,5min;4、加S2(用完立刻盖紧瓶盖,以免CO2中和Buffer中的NaOH)200ul,不能剧烈(以免基因组DNA的污染),上下翻转4-6次,直至形成透亮的溶液,时间少于5min。
目的是使蛋白包裹基因组DNA,游离质粒;5、加S3 280ul,温和充分翻转混合6-8次,12000xg,10min(此步呈白色絮状);*备注:S1:S2:S3=5:5:76、取上清加入制备管(置于2ml离心管),12000xg,1min,去滤液;7、加Buffer W1 500ul,12000xg,1min,弃滤液;8、加Buffer W2 700ul,12000xg,1min,弃滤液。
重复一遍;9、空管离心12000xg,1min;10、制备管移入新的1.5ml离心管,管膜中加60-80ul去离子水,静置1min,12000xg,1min。
(将去离子水加热至65度,将提高洗脱效率)四、跑胶回收:sost回收失败1、2%浓度胶,Loading Buffer如是6X,则加10ul到样品,全部加样到胶孔中。
插入:配胶方法大块胶60ml;小块胶25ml;需要配置大块胶、大孔胶;Agarose 0.6g,TAE60ml,微波中火2min;趁热但不烫手时加入gold view 0.5ul/25ml;倒入槽里。
2、跑胶:单位厘米/5-10v。
所以大槽25cm,150v即可。
小槽100v即可。
3、紫外灯下切胶,纸巾吸进液体,计算凝胶重量(1mg=1ul);4、加3个凝胶体积的凝胶结合液DB(0.1ul视为100ul;如凝胶浓度大于2%,则加入6倍体积溶胶液;凝胶块最大不能超过400ul,超过可多个离心柱);5、56℃水浴放置10分钟,至完全溶解;6、每100mg最初的凝胶重量加入150ul的异丙醇,震荡混匀,回收大于4Kb的片段可不加异丙醇,加入反而降低回收效率;7、将上一步所得溶液加入吸附柱AC中(吸附柱放入收集管中),12000rpm,30-60s,弃液体;8、加700ul漂洗液WB,12000rpm,1min,弃废液;9、加500ul漂洗液WB,12000rpm,1min,弃废液;10、空离心2min,弃废液;11、晾干乙醇,以免抑制下游反应;12、将吸附柱放入新的1.5ml离心管,加入50ul(最少30ul)洗脱缓冲液EB或者去离子水(65-70水浴加热效果更好,或将得到的溶液重新加入离心柱可增加洗脱量);五、连接体系:六、转化1、加感受肽:连接产物=10:1,冰浴30min;2、激活:42℃,90s,不能震动;3、加500ul LB培养基;4、37℃,150转摇床,45min;5、铺板子七、检测1、细菌长势良好,对照组不长;2、酶切检测:(1)1ml LB体系:1ml LB培养基+1ul抗生素于1.5mlEP管中;(2)15ul Pcr体系:7.5ul Mix(2X)5.5ul water1ul上游引物1ul下游引物(3)用枪头挑培养皿中的菌体,吹打于1ml LB体系中,再吹打于15ul Pcr体系中;(4)1ml LB体系放入37℃摇床,150rpm;显示4°/4°时,结束。
分子克隆与表达实验流程1.选取菌株从保存的海冰细菌中随机选取某几株,挑取其单菌落于发酵培养基(2216)活化培养,1d后将活化的菌株5ml接入70ml发酵培养基中,12℃,100rpm摇床培养,大约4~5d后对菌株在4℃下,12000rpm进行离心,收集菌体,于4℃保存。
2.提取菌株全基因组在超净工作台上取120μl离心后的菌株悬浮于400μl的1×TE缓冲液中,加入10%SDS 100μl和2mg/mL的溶菌酶20μl,混匀后置于37℃保温1h,加入5M 的NaCl 70μl充分混匀,置于65℃水浴10min,加入等体积的苯酚/氯仿/异戊醇(25:24:1)混匀,离心(12000rpm、8min),取上层水相于新离心管中并加入等体积的氯仿/异戊醇(24:1)充分抽提,取上层水相加入两倍体积的无水乙醇沉淀DNA,并用70%的乙醇淋洗两次,倾去乙醇,真空干燥后溶于25μl的1×TE缓冲液。
对全基因组进行电泳检验,其余的置-4℃冰箱保存备用。
3.根据目的蛋白设计引物本实验研究的是小分子蛋白:谷胱甘肽转移酶(GST)、硫氧还蛋白(Trx)和谷氧还蛋白(Grx)。
根据这三种蛋白的基因用Primer5设计引物。
引物名称与序列引物名称引物序列,方向5′——3′合成规格(OD)GST1(1) TTTATGGYGTMCCKCTTTCTC 2GST1(2) CA TGCTSCA TATTSATTAWCTG 2GST2(1) AGTSTCGCCGTTTAATCAACC 2GST2(2) YKCATY AAKYTGCTCRCCMSC 2GST3(1) TTTA TGGCGTACCTCTTTCTCC 2GST3(2) CGGTAA TACCTAACTGCTCAGC 2GST4(1) TCTGTTACCTCGCCTTAT 2GST4(2) AAAGCCA TTATCTTCTGC 2GST5(1) ACTTA TTTGGAGCA TTGAGCGG 2GST5(2) TCGGCGGTTCAAGAAAAG 2Trx1(1) AAGAATTCA TGAGCGAGAAAATAATCC 2Trx1(2) CGCAAGCTTTTAAAGA TTGTTTTCTA 2Trx2(1) AAGAATTCA TGAGCGAGAAAATAATC 2Trx2(2) CTCAAGCTTTTAGA TGTTGTTTTCTA 2Trx3(1) CGGAGAGCCA TA TGAGCGAGAA 2Trx3(2) TTGTTTAAATCTCGAGATTGTTTTCT 2Grx1(1) GTGTTATCTGGTGGTA TGG 2Grx1(2) TTGTGCTGCTGCGTTTTG 24.PCR扩增以菌株的全基因组为模板,对上述引物进行PCR,从中寻找含有目的基因的菌株,对含有目的基因的菌株进行验证并保种。
第1篇一、实验目的1. 学习分子生物学中最基本的技术——分子克隆的操作过程。
2. 掌握基因克隆的概念,了解基因克隆的基本原理和方法。
3. 熟练掌握DNA提取、限制性内切酶切割、DNA连接、转化、筛选和鉴定等分子克隆实验操作。
4. 提高实验操作技能,培养严谨的科学态度。
二、实验原理分子克隆是指将目的基因(或DNA片段)与载体DNA连接,使其在宿主细胞中复制和表达的过程。
本实验采用分子克隆组装技术,将目的基因插入载体中,实现基因克隆。
三、实验材料1. 基因组DNA提取试剂盒2. 限制性内切酶3. DNA连接酶4. 载体DNA5. 目的基因片段6. 转化宿主细胞7. LB培养基、琼脂糖、氨苄青霉素等四、实验步骤1. 提取目的基因片段和载体DNA(1)取适量基因组DNA,按照试剂盒说明书进行提取。
(2)取适量载体DNA,按照试剂盒说明书进行提取。
2. 限制性内切酶切割(1)将目的基因片段和载体DNA分别用限制性内切酶进行切割。
(2)酶切反应体系:10×酶切缓冲液5μl,限制性内切酶1μl,DNA模板5μl,加双蒸水至50μl。
(3)酶切条件:37℃反应2小时。
3. DNA连接(1)将酶切后的目的基因片段和载体DNA进行连接。
(2)连接反应体系:10×连接缓冲液5μl,DNA连接酶1μl,酶切后的目的基因片段5μl,酶切后的载体DNA5μl,加双蒸水至50μl。
(3)连接条件:16℃反应4小时。
4. 转化宿主细胞(1)将连接产物转化大肠杆菌DH5α感受态细胞。
(2)转化条件:42℃热激45秒。
5. 筛选和鉴定(1)将转化后的细胞涂布于含有氨苄青霉素的LB培养基平板上,37℃培养过夜。
(2)挑取单克隆菌落,提取质粒DNA。
(3)对提取的质粒DNA进行PCR扩增,检测目的基因是否插入载体。
(4)对阳性克隆进行测序,验证插入序列的正确性。
五、实验结果1. 成功提取目的基因片段和载体DNA。
2. 目的基因片段和载体DNA经限制性内切酶切割后,酶切图谱与预期相符。
一、实验目的1. 学习并掌握分子克隆实验的基本原理和方法。
2. 通过实验操作,提高分子生物学实验技能。
3. 熟悉DNA提取、限制性内切酶酶切、连接、转化、筛选等实验步骤。
二、实验原理分子克隆是指将目的基因片段从供体DNA中分离出来,并通过体外重组、转化、筛选等步骤,将其插入到载体DNA中,形成重组质粒。
重组质粒再经过扩增、提取等步骤,得到大量的目的基因。
三、实验材料1. E. coli感受态细胞2. pUC19载体3. 目的基因片段4. 限制性内切酶(如HindIII)5. T4 DNA连接酶6. DNA分子量标准7. DNA凝胶电泳试剂盒8. 琼脂糖9. 载体提取试剂盒10. 其他试剂(如DNA模板、PCR引物、Tris-HCl缓冲液、NaCl等)四、实验步骤1. DNA提取:按照试剂盒说明书提取目的基因片段和pUC19载体DNA。
2. 限制性内切酶酶切:将提取的DNA进行HindIII酶切,反应条件按照酶切试剂盒说明书进行。
3. 连接:将酶切后的目的基因片段和载体DNA进行连接,反应条件按照T4 DNA连接酶说明书进行。
4. 转化:将连接产物转化到E. coli感受态细胞中,具体操作按照转化试剂盒说明书进行。
5. 筛选:将转化后的细胞涂布在含有抗生素的琼脂平板上,37℃培养过夜。
6. 提取重组质粒:从平板上挑取白色菌落,按照载体提取试剂盒说明书提取重组质粒。
7. 验证:将提取的重组质粒进行PCR扩增,检测目的基因是否插入载体。
8. 纯化:将PCR产物进行纯化,具体操作按照纯化试剂盒说明书进行。
9. 测序:将纯化后的PCR产物进行测序,验证目的基因序列的正确性。
五、实验结果与分析1. 酶切结果:在DNA凝胶电泳中,目的基因片段和载体DNA在HindIII酶切位点处均出现特异性条带,说明酶切成功。
2. 连接结果:转化后的平板上出现白色菌落,说明连接产物成功转化到E. coli 细胞中。
3. 筛选结果:提取的重组质粒经过PCR扩增,在预期位置出现特异性条带,说明目的基因成功插入载体。
一、实验目的1. 学习分子克隆的基本原理和方法;2. 掌握质粒的提取、纯化、线性化及目的基因的插入等实验操作;3. 熟悉DNA的纯化、鉴定及重组载体的构建等实验技术。
二、实验原理分子克隆是指将目的基因片段从基因组DNA中分离出来,并在宿主细胞中复制和扩增的过程。
实验过程中,利用限制性内切酶切割目的基因和载体,通过连接酶将二者连接形成重组载体,然后转化宿主细胞,筛选出含有目的基因的克隆。
三、实验材料1. 质粒:pET-28a2. 目的基因:EGFP3. 限制性内切酶:BamHI、EcoRI4. DNA连接酶:T4 DNA连接酶5. DNA分子量标准:DL20006. DNA纯化试剂盒7. 转化宿主细胞:大肠杆菌DH5α8. LB培养基、氨苄青霉素9. 等等四、实验步骤1. 质粒提取与纯化(1)按照试剂盒说明书提取质粒DNA;(2)用DNA纯化试剂盒纯化质粒DNA;(3)检测质粒浓度和纯度。
2. 目的基因的线性化(1)用BamHI和EcoRI双酶切目的基因片段和载体;(2)用DNA纯化试剂盒纯化酶切产物;(3)检测酶切产物浓度和纯度。
3. DNA连接(1)将纯化的目的基因片段和载体进行连接反应;(2)将连接产物转化大肠杆菌DH5α;(3)在含有氨苄青霉素的LB培养基中培养转化菌。
4. 阳性克隆的筛选(1)提取转化菌的DNA;(2)用BamHI和EcoRI双酶切提取的DNA;(3)电泳检测酶切产物,筛选出与预期大小相符的重组质粒;(4)将重组质粒进行测序验证。
五、实验结果与分析1. 质粒提取与纯化:质粒浓度约为50ng/μl,纯度大于0.8。
2. 目的基因的线性化:酶切产物浓度约为10ng/μl,纯度大于0.8。
3. DNA连接:转化菌在含有氨苄青霉素的LB培养基中生长良好。
4. 阳性克隆的筛选:电泳结果显示,重组质粒大小与预期相符。
5. 重组质粒测序验证:测序结果与预期序列一致,表明目的基因已成功插入载体。