高中化学必修1:微项目 探秘膨松剂
- 格式:docx
- 大小:563.88 KB
- 文档页数:5


微项目 探秘膨松剂[核心素养发展目标] 1.运用研究物质性质的基本方法(观察、实验、分类、比较等)和基本程序,对碳酸氢钠的蓬松原理进行实验探究,促使“科学探究与创新意识”核心素养的发展。
2.了解复合膨松剂的组成,学会在真实情景中分析、解决实际问题,探究陌生物质的性质,促进“科学态度与社会责任”核心素养的发展。
一、探究碳酸氢钠的蓬松作用原理1.膨松剂及其类别(1)概念膨松剂是在食品加工过程中加入的,能使面胚发起形成多孔组织,从而使食品具有柔软或蓬松特点的一类物质。
(2)分类膨松剂⎩⎨⎧ 生物膨松剂(酵母)化学膨松剂⎩⎪⎨⎪⎧ 单一膨松剂复合膨松剂 (3)化学膨松剂中基本上都含有一种化学物质——碳酸氢钠。
2.观察不同方法蒸出的馒头(1)图①所示过程中产生的气体较少。
(2)图②所示过程中产生的气体较多。
3.实验探究陌生物质(碳酸氢钠)的性质实验装置操作如下图所示:(1)图①所示的实验过程中观察到导管口持续出现气泡,溶液出现浑浊,说明碳酸氢钠受热易分解,化学方程式为2NaHCO 3=====△Na 2CO 3+H 2O +CO 2↑。
(2)图②所示的实验过程观察到试管内有大量气体产生,化学方程式为NaHCO3+HCl===NaCl +H2O+CO2↑。
(1)依据碳酸氢钠的化学性质,进一步解释做馒头过程中产生的现象。
提示碳酸氢钠受热分解,碳酸氢钠与酸反应都能产生二氧化碳气体,所以二者都能使面团蓬松。
由于相同质量的碳酸氢钠与酸反应放出的二氧化碳气体,比受热分解产生的二氧化碳气体多,所以直接在面团中加入碳酸氢钠和醋酸蒸出的馒头更蓬松。
(2)如果面团没有发酵,能否用加入纯碱的方法使其蓬松?提示不能,若面团没有发酵,不能生成乳酸等,且碳酸钠受热不分解,故不能产生CO2气体,不能使面团蓬松。
碳酸氢钠的性质(1)易溶于水,水溶液呈碱性。
(2)不稳定,受热易分解。
(3)能与酸反应,放出二氧化碳。
(4)能与碱溶液反应NaOH+NaHCO3===Na2CO3+H2O,Ca(OH)2+2NaHCO3===CaCO3↓+Na2CO3+2H2O或Ca(OH)2+NaHCO3===CaCO3↓+NaOH +H2O。



微项目 探秘膨松剂[核心素养发展目标] 1.运用研究物质性质的基本方法(观察、实验、分类、比较等)和基本程序,对碳酸氢钠的蓬松原理进行实验探究,促使“科学探究与创新意识”核心素养的发展。
2.了解复合膨松剂的组成,学会在真实情景中分析、解决实际问题,探究陌生物质的性质,促进“科学态度与社会责任”核心素养的发展。
一、探究碳酸氢钠的蓬松作用原理1.膨松剂及其类别(1)概念膨松剂是在食品加工过程中加入的,能使面胚发起形成多孔组织,从而使食品具有柔软或蓬松特点的一类物质。
(2)分类膨松剂⎩⎨⎧ 生物膨松剂(酵母)化学膨松剂⎩⎪⎨⎪⎧ 单一膨松剂复合膨松剂(3)化学膨松剂中基本上都含有一种化学物质——碳酸氢钠。
2.观察不同方法蒸出的馒头(1)图①所示过程中产生的气体较少。
(2)图②所示过程中产生的气体较多。
3.实验探究陌生物质(碳酸氢钠)的性质实验装置操作如下图所示:(1)图①所示的实验过程中观察到导管口持续出现气泡,溶液出现浑浊,说明碳酸氢钠受热易分解,化学方程式为2NaHCO 3=====△Na 2CO 3+H 2O +CO 2↑。
(2)图②所示的实验过程观察到试管内有大量气体产生,化学方程式为NaHCO3+HCl===NaCl +H2O+CO2↑。
(1)依据碳酸氢钠的化学性质,进一步解释做馒头过程中产生的现象。
提示碳酸氢钠受热分解,碳酸氢钠与酸反应都能产生二氧化碳气体,所以二者都能使面团蓬松。
由于相同质量的碳酸氢钠与酸反应放出的二氧化碳气体,比受热分解产生的二氧化碳气体多,所以直接在面团中加入碳酸氢钠和醋酸蒸出的馒头更蓬松。
(2)如果面团没有发酵,能否用加入纯碱的方法使其蓬松?提示不能,若面团没有发酵,不能生成乳酸等,且碳酸钠受热不分解,故不能产生CO2气体,不能使面团蓬松。
碳酸氢钠的性质(1)易溶于水,水溶液呈碱性。
(2)不稳定,受热易分解。
(3)能与酸反应,放出二氧化碳。
(4)能与碱溶液反应NaOH+NaHCO3===Na2CO3+H2O,Ca(OH)2+2NaHCO3===CaCO3↓+Na2CO3+2H2O或Ca(OH)2+NaHCO3===CaCO3↓+NaOH +H2O。

微项目 探秘膨松剂1.膨松剂及化学膨松剂的类型(1)膨松剂 在食品加工过程中加入的,能使面胚发起形成01多孔组织,从而使食品具有02松软或酥脆特点的一类物质。
(2)膨松剂的分类膨松剂⎩⎨⎧ 生物膨松剂酵头化学膨松剂⎩⎪⎨⎪⎧ 单一膨松剂复合膨松剂2.膨松剂的作用原理 (1)食品在加工过程中产生无毒气体使面胚内部形成海绵状结构,根据面粉的组成可知该气体应为CO 2。
(2)单一膨松剂(NaHCO 3)的作用原理 032NaHCO 3=====△Na 2CO 3+CO 2↑+H 2O 。
由此可知Na 2CO 304大于NaHCO 3的。
(3)复合膨松剂[NaHCO 3、柠檬酸(C 6H 8O 7)或食醋(CH 3COOH)]的作用原理3NaHCO 3+C 6H 8O 7―→C 6H 5O 7Na 3+3CO 2↑+3H 2O ,NaHCO 3+CH 3COOH ―→CH 3COONa +H 2O +CO 2↑。
1.下列有关Na 2CO 3和NaHCO 3的叙述正确的是( )A .受热时,NaHCO 3比Na 2CO 3容易分解B .NaHCO 3俗名苏打,Na 2CO 3俗名纯碱C .NaHCO 3溶液显酸性,Na 2CO 3溶液显碱性D .1 mol NaHCO 3和1 mol Na 2CO 3分别与足量盐酸反应,产生CO 2的质量不同 答案 A解析 NaHCO 3不稳定,加热易分解:2NaHCO 3=====△Na 2CO 3+CO 2↑+H 2O ,碳酸钠较稳定,A正确;NaHCO 3俗名小苏打,B 错误;NaHCO 3溶液和Na 2CO 3溶液都显碱性,C 错误;根据碳原子守恒可知,在物质的量相等的条件下,碳酸氢钠、碳酸钠分别与足量盐酸反应生成的CO 2一样多,D 错误。
2.如图是某兴趣小组根据教材实验设计的一个能说明碳酸钠与碳酸氢钠热稳定性的套管实验。
请观察实验装置,分析实验原理,并判断下列说法和做法中不正确的是( )A .甲为碳酸氢钠,乙为碳酸钠B .要证明碳酸氢钠受热能产生水,可在小试管内塞上沾有无水硫酸铜粉末的棉花球C .加热不久就能看到A 烧杯中的澄清石灰水变浑浊D .整个实验过程中都没有出现A 烧杯中的澄清石灰水变浑浊的现象答案 C解析 直接加热大试管,大试管中温度较高,若加热温度较高的物质不分解,而加热温度较低的物质分解,则可判断物质稳定性的强弱,故甲为碳酸氢钠、乙为碳酸钠,A 正确;白色的无水硫酸铜遇水显蓝色,可证明碳酸氢钠受热能产生水,B 正确;碳酸钠较稳定,加热过程中不会分解,则连接A 烧杯的大试管中没有二氧化碳产生,故A 烧杯中的澄清石灰水不会变浑浊,C 错误,D 正确。


微项目探秘膨松剂学业要求1.通过观察、实验、分类、比较等方法,结合研究物质性质的基本程序,对碳酸氢钠作为膨松剂的作用原理进行科学探究,体会研究物质性质的基本方法和基本程序在化学研究中的作用,培养实验探究与创新意识。
2.学习如何在真实情境中分析、解决实际问题,探究陌生物质的性质,提升科学态度和创新意识。
3.强化合理使用化学品的安全意识,能够正确使用食用添加剂,培养科学态度与社会责任。
1.膨松剂:常见的膨松剂有________(酵母)和________,化学膨松剂可分为单一膨松剂和复合膨松剂。
2.NaHCO2的物理性质3.NaHCO3的化学性质写出上述序号①②③④所表示反应的化学方程式:①________________________________________________________________________。
②________________________________________________________________________。
③________________________________________________________________________。
④________________________________________________________________________。
[即学即练]1.下列说法不正确的是( )A.干冰可用于人工降雨B.碘酸钾可用作食盐的添加剂C.碳酸钠是发酵粉的主要成分D.次氯酸钙是漂白粉的有效成分2.下列关于钠及其化合物的说法正确的是( )A.将剩余的金属钠丢弃在废纸篓里B.小苏打可用于制作糕点的膨松剂,苏打可用于治疗胃酸过多C.侯氏制碱法的工艺过程中应用了物质溶解度的差异D.生活中用热的烧碱溶液洗去油污3.下列除去杂质的方法正确的是( )A.Na2CO3溶液(NaHCO3):加热法B.CO2(HCl):先通入饱和NaHCO3溶液再通入碱石灰中,收集气体C.N2(O2):通过足量灼热的铜粉,收集气体D.NaCl溶液(Na2SO4):加入适量氢氧化钡溶液4.在密闭容器中,加热等物质的量的NaHCO3和Na2O2的固体混合物,充分反应后,容器中固体剩余物是( )A.Na2CO3和Na2O2B.Na2CO3和NaOHC.NaOH和Na2O2D.NaOH、Na2O2和Na2CO35.碳酸氢铵是白色固体,在生产、生活中应用广泛。
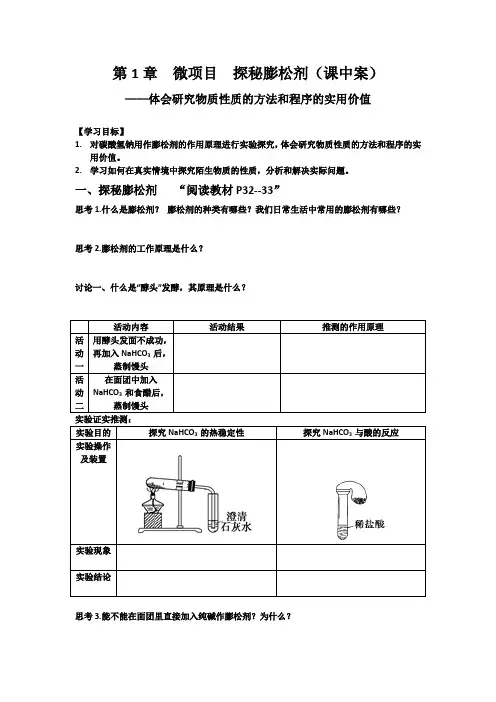
第1章微项目探秘膨松剂(课中案)——体会研究物质性质的方法和程序的实用价值【学习目标】1.对碳酸氢钠用作膨松剂的作用原理进行实验探究,体会研究物质性质的方法和程序的实用价值。
2.学习如何在真实情境中探究陌生物质的性质,分析和解决实际问题。
一、探秘膨松剂“阅读教材P32--33”思考1.什么是膨松剂?膨松剂的种类有哪些?我们日常生活中常用的膨松剂有哪些?思考2.膨松剂的工作原理是什么?讨论一、什么是“酵头”发酵,其原理是什么?活动内容活动结果推测的作用原理活动一用酵头发面不成功,再加入NaHCO3 后,蒸制馒头活动二在面团中加入NaHCO3 和食醋后,蒸制馒头实验证实推测:实验目的探究NaHCO3 的热稳定性探究NaHCO3 与酸的反应实验操作及装置实验现象实验结论思考3.能不能在面团里直接加入纯碱作膨松剂?为什么?例1.一天,小鲁惊奇的发现妈妈蒸馒头时用的不是纯碱,而是小苏打,她好奇的问:“为什么不用纯碱而用小苏打呢?”妈妈说:“面团没发酵,不能用纯碱。
”通过查阅资料小鲁发现小苏打是一种常用的膨松剂,加热后可转化为纯碱。
下列有关推断不合理的是()A.小苏打对人体无害B.小苏打能用作膨松剂是因为能产生二氧化碳C.吃这种馒头可中和过多的胃酸D.小苏打能和酸反应,所以小苏打属于碱讨论二、小鲁妈妈用NaHCO3单独做膨松剂,得到的食品色泽发黄且带有碱味,想解决这一问题,应当加入什么物质?原因是什么?二、碳酸钠和碳酸氢钠的比较(1)热稳定性:思考1:向碳酸钠溶液中逐滴滴加稀盐酸时,一段时间后才有气泡产生,请推测原因:思考2:Na2CO3和NaHCO3分别与足量的盐酸反应,哪个反应产生气体速率更快?为什么?。
思考3:如何不用其它任何试剂鉴别盐酸和碳酸钠溶液?(2)与酸溶液的反应(例如与稀盐酸的反应)Na2CO3 与稀盐酸:。
NaHCO3 与稀盐酸:。
思考4:能否用石灰水鉴别碳酸钠和碳酸氢钠?(3)与碱的反应①NaHCO 3: 与NaOH 溶液: 与足量Ca (OH )2 溶液: ②Na 2CO 3:与NaOH 溶液: 与Ca (OH )2 溶液: (4)与某些盐的反应(例如与CaCl 2或者BaCl 2溶液) Na 2CO 3: NaHCO 3:思考5:在饱和Na 2CO 3 溶液中通入足量的CO 2 ,会有白色的晶体析出,生成了什么? (5)碳酸钠和碳酸氢钠在一定条件下可以相互转化:方程式:例2.除去NaHCO 3溶液中混有的少量Na 2CO 3,下列说法最合理的是( )A.加入稀盐酸B.通入过量的CO 2C.加入适量的NaOHD.加入适量的澄清石灰水 【拓展】碳酸氢钠作为单一膨松剂,可能会造成食品口味不佳、颜色加深等问题。


微项目 探秘膨松剂
[核心素养发展目标] 1.运用研究物质性质的基本方法(观察、实验、分类、比较等)和基本程序,对碳酸氢钠的蓬松原理进行实验探究,促使“科学探究与创新意识”核心素养的发展。
2.了解复合膨松剂的组成,学会在真实情景中分析、解决实际问题,探究陌生物质的性质,促进“科学态度与社会责任”核心素养的发展。
一、探究碳酸氢钠的蓬松作用原理
1.膨松剂及其类别
(1)概念
膨松剂是在食品加工过程中加入的,能使面胚发起形成多孔组织,从而使食品具有柔软或蓬松特点的一类物质。
(2)分类
膨松剂⎩⎨⎧ 生物膨松剂(酵母)化学膨松剂⎩⎪⎨⎪⎧ 单一膨松剂复合膨松剂
(3)化学膨松剂中基本上都含有一种化学物质——碳酸氢钠。
2.观察不同方法蒸出的馒头
(1)图①所示过程中产生的气体较少。
(2)图②所示过程中产生的气体较多。
3.实验探究陌生物质(碳酸氢钠)的性质
实验装置操作如下图所示:
(1)图①所示的实验过程中观察到导管口持续出现气泡,溶液出现浑浊,说明碳酸氢钠受热易分解,化学方程式为2NaHCO 3=====△
Na 2CO 3+H 2O +CO 2↑。
(2)图②所示的实验过程观察到试管内有大量气体产生,化学方程式为NaHCO3+HCl===NaCl +H2O+CO2↑。
(1)依据碳酸氢钠的化学性质,进一步解释做馒头过程中产生的现象。
提示碳酸氢钠受热分解,碳酸氢钠与酸反应都能产生二氧化碳气体,所以二者都能使面团蓬松。
由于相同质量的碳酸氢钠与酸反应放出的二氧化碳气体,比受热分解产生的二氧化碳气体多,所以直接在面团中加入碳酸氢钠和醋酸蒸出的馒头更蓬松。
(2)如果面团没有发酵,能否用加入纯碱的方法使其蓬松?
提示不能,若面团没有发酵,不能生成乳酸等,且碳酸钠受热不分解,故不能产生CO2气体,不能使面团蓬松。
碳酸氢钠的性质
(1)易溶于水,水溶液呈碱性。
(2)不稳定,受热易分解。
(3)能与酸反应,放出二氧化碳。
(4)能与碱溶液反应
NaOH+NaHCO3===Na2CO3+H2O,
Ca(OH)2+2NaHCO3===CaCO3↓+Na2CO3+2H2O或Ca(OH)2+NaHCO3===CaCO3↓+NaOH +H2O。
二、设计并运用复合膨松剂
1.选择合适的物质制取复合膨松剂
(1)酸性物质选择
酸性物质化学式色态气味溶解性挥发性
白醋CH3COOH 无色液体刺激性易溶于水易挥发
柠檬酸C6H8O7·H2O 无色晶体无臭易溶于水难挥发
由上表分析,膨松剂中酸性物质选择柠檬酸。
(2)碳酸盐选择
适合做膨松剂的碳酸盐有:NaHCO3、NH4HCO3等。
2.复合膨松剂的组成
(1)复合膨松剂为什么应在干燥环境中保存?
提示复合膨松剂中的碳酸盐和酸性物质遇水反应产生CO2,故应在干燥的环境中保存。
(2)某复合膨松剂中含碳酸氢钠、焦磷酸二氢二钠、碳酸钙、葡萄糖酸δ内酯、淀粉,其中起酸性作用的是哪种成分?
提示焦磷酸二氢二钠。
1.常用来作为食品制作过程中的膨松剂的小苏打,其化学名称为()
A.氧化钠
B.氢氧化钠
C.碳酸钠
D.碳酸氢钠
[答案] D
[解析]小苏打是碳酸氢钠的俗称,化学式为NaHCO3。
2.在下列膨松剂中,属于复合膨松剂的是()
A.泡打粉
B.碳酸钠
C.碳酸氢钠
D.碳酸氢铵
[答案] A
[解析]泡打粉是由碱性物质、酸式盐和填充物按一定比例混合而成的化学复合膨松剂。
3.下列不属于化学膨松剂的是()
A.碳酸氢钠
B.碳酸氢铵
C.干酵母
D.泡打粉
[答案] C
[解析]碳酸氢钠受热分解生成二氧化碳、水和碳酸钠,碳酸氢铵受热分解生成水、氨、二氧化碳,且二者都与酸反应生成二氧化碳,故都可做膨松剂;干酵母属于一种生物膨松剂。
4.下列化合物与小苏打溶液混合,没有气体或沉淀生成的是()
A.烧碱
B.硫酸
C.氢氧化钡
D.过氧化钠
[答案] A
[解析]A项,NaOH+NaHCO3===Na2CO3+H2O;B项,2NaHCO3+H2SO4===Na2SO4+2H2O
+2CO 2↑;C 项,Ba(OH)2+2NaHCO 3===BaCO 3↓+Na 2CO 3+2H 2O 或Ba(OH)2+NaHCO 3===BaCO 3↓+NaOH +H 2O ;D 项,2Na 2O 2+2H 2O===4NaOH +O 2↑,NaOH +NaHCO 3===Na 2CO 3+H 2O 。
5.下列既能跟NaOH 溶液反应,又能跟盐酸反应的是( )
A.Na 2CO 3溶液
B.CaCO 3
C.NaHCO 3溶液
D.Na 2SO 4溶液 [答案] C
[解析] A 项只能与盐酸反应而不与氢氧化钠反应,错误;B 项只能与盐酸反应而不与氢氧化钠反应,错误;C 项与氢氧化钠反应生成碳酸钠,与盐酸反应生成二氧化碳,正确;D 项既不能与氢氧化钠反应,又不能与盐酸反应,错误。
6.除去混在Na 2CO 3粉末中的少量NaHCO 3,最合理的方法是( )
A.加热
B.加过量氢氧化钠溶液,再蒸发结晶
C.加盐酸
D.加氢氧化钙溶液
[答案] A
[解析] 将固体加热到质量不变,NaHCO 3受热易分解生成Na 2CO 3,A 项合理;加入过量NaOH 溶液,会引入新杂质NaOH ,B 项不合理;加入适量盐酸,与两者均反应,C 项不合理;加入适量氢氧化钙溶液,与两者均反应,D 项不合理。
7.下列试剂能用来鉴别等物质的量浓度的Na 2CO 3溶液和NaHCO 3溶液的是( )
A.盐酸
B.澄清石灰水
C.NaCl 溶液
D.NaOH 溶液
[答案] A
[解析] 由于盐酸与NaHCO 3反应比与Na 2CO 3反应剧烈,A 项可以;澄清石灰水与NaHCO 3、Na 2CO 3溶液均能生成白色沉淀,B 项不可以;Na 2CO 3溶液、NaHCO 3溶液与NaCl 溶液均不反应,C 项不可以;Na 2CO 3溶液与NaOH 溶液不反应,NaHCO 3溶液与NaOH 溶液虽然反应但无明显现象,D 项不可以。
8.已知:NH 4HCO 3=====△NH 3↑+H 2O +CO 2↑,Na 2CO 3比较稳定,加热不分解;碱石灰不与氨反应,常用于吸收水蒸气和二氧化碳。
现有某膨松剂含碳酸氢钠、碳酸氢铵中的一种或两种,某化学兴趣小组对该膨松剂进行如下探究:
在玻璃管中加入该膨松剂,按如图连接好装置(气密性良好,铁架台略去),点燃酒精灯。
(1)关闭止水夹2,打开止水夹1,观察到现象______________________________________,说明产物中有二氧化碳,该反应的化学方程式为______________________________________ __________________________________。
(2)打开止水夹2,关闭止水夹1,观察到的现象:____________________________________,说明产物中有氨。
(3)若想确定该膨松剂的成分是碳酸氢钠和碳酸氢铵的混合物,在上述实验的基础上(不添加其他仪器和试剂)应该继续完成的实验是___________________________________________
________________________________________________________________________
_______________________________________________(具体实验操作及现象)。
[答案](1)澄清石灰水变浑浊Ca(OH)2+CO2===CaCO3↓+H2O
(2)无色酚酞溶液变为红色
(3)打开止水夹1,关闭止水夹2,继续加热至石灰水中不再有气泡产生,玻璃管中仍有固体剩余
[解析](1)碳酸氢钠、碳酸氢铵受热分解都能够生成二氧化碳,关闭止水夹2,打开止水夹1,观察到的现象是澄清石灰水变浑浊,氢氧化钙和二氧化碳反应的化学方程式为Ca(OH)2+CO2===CaCO3↓+H2O。
(2)如果有氨生成,则氨进入酚酞溶液中时,能和水反应生成氨水,氨水显碱性,能使酚酞溶液变红色。
(3)应该继续完成的实验是:打开止水夹1,关闭止水夹2,继续加热至石灰水中不再有气泡产生,玻璃管中仍有固体剩余。