纠正及预防措施表格格式
- 格式:doc
- 大小:37.00 KB
- 文档页数:4

纠正预防措施处理单一、背景介绍在各行各业的工作中,纠正预防措施处理单是一种常见的文档,用于记录和跟踪问题的纠正和预防措施。
该文档的目的是确保问题得到及时处理,并采取适当的措施以防止类似问题再次发生。
本文将详细介绍纠正预防措施处理单的标准格式及其内容要求。
二、标准格式纠正预防措施处理单的标准格式通常包括以下几个部份:1. 标题:在文档的顶部居中位置,用粗体字体写明“纠正预防措施处理单”字样,字号为14号。
2. 单号:在标题下方,居左位置,用正常字体写明单号,格式为“YYYYMMDD-XXX”,其中“YYYYMMDD”表示年月日,XXX表示流水号。
3. 日期:在单号下方,居右位置,用正常字体写明填写该单的日期,格式为“YYYY年MM月DD日”。
4. 发起人:在日期下方,居左位置,用正常字体写明发起该处理单的人员姓名和职位。
5. 受理人:在发起人下方,居右位置,用正常字体写明受理该处理单的人员姓名和职位。
6. 问题描述:在发起人和受理人之间,居左位置,用正常字体写明问题的具体描述,包括问题的发生时间、地点、原因等。
7. 纠正措施:在问题描述下方,用正常字体写明对该问题采取的纠正措施,包括具体的操作步骤、时间计划、责任人等。
8. 预防措施:在纠正措施下方,用正常字体写明为了防止类似问题再次发生所采取的预防措施,包括改进流程、培训人员、加强监督等。
9. 处理结果:在预防措施下方,用正常字体写明问题处理的结果,包括纠正措施的执行情况、预防措施的有效性等。
10. 处理人签名:在处理结果下方,居右位置,用正常字体写明处理该问题的人员姓名和职位,并留出足够的空间供其签名。
11. 审核人签名:在处理人签名下方,居右位置,用正常字体写明审核该处理单的人员姓名和职位,并留出足够的空间供其签名。
12. 备注:在审核人签名下方,用正常字体写明对该处理单的补充说明或者备注信息。
三、内容要求纠正预防措施处理单的内容要求如下:1. 问题描述:准确、清晰地描述问题的发生时间、地点、原因等,以便受理人能够全面了解问题的背景。



版次/改号:C/1 编号:R-P-008
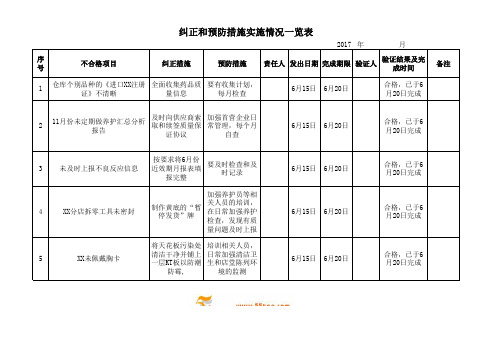
纠正和预防措施通知单
日期:年月日
1.本通知单由品质运营部向责任部门发出,交责任部门负责人/主工签收:“事实描述”栏和“验证意见”栏由归口管理部门填写。
2.“原因”栏由责任人填写“纠正/预防措施”栏由主负责人填写,“评审意见”栏由责任部门负责人填写;若需采取重大纠正/预防措施,须报管理者代表或分管总工评审确定。
3.纠正措施完成后,责任部门责任人应将本通知单及相关整改资料复印留存,原件传递至归口管理部门,由归口管理部门保存。

1 目的建立纠正措施和预防措施(CAPA)程序,纠正与预防不符合、潜在不符合、不期望事件的发生,确保公司持续、有效地执行 GMP 规范及相关法律法规,实现质量管理体系的持续改进。
2 合用范围本规程合用于生产质量管理活动中所有纠正措施和预防措施的制定、实施和控制。
3 定义3.1 纠正措施:为消除已发现的不合格或者其他不期望情况的发生所采取的措施,纠正措施是针对问题的根本原因,减少或者消除问题再发生的措施。
3.2 预防措施:为消除潜在不合格或者其他潜在不期望情况的发生所采取的措施,采取预防措施是为了防止不合格或者其他潜在不期望情况的发生。
3.3 根本原因:通过各种方法和工具,深入分析而确定问题发生的内在根本因素。
4 纠正预防措施(CAPA)的范围来源于客户投诉、产品缺陷、召回、生产偏差、实验室异常检验结果偏差、自检、外部审计(包括政府检查)、工艺性能和产品质量监测趋势、变更控制、产品年度回顾等活动中发现问题所采取的措施。
整改措施的深度和形式应与风险评估的级别相适应。
5 职责5.1 企业所有员工:(1)正确理解纠正和预防措施(CAPA)规程的要求(2)在不合格总是发生时,按要求采取适当的措施,并报告主管或者直接领导5.2 生产部经理、工程部经理、物料供应部经理及车间负责人:(1)根据批准的计划,在规定期限内完成相应的整改措施。
(2) 定期检查整改措施计划的发展,直到所有的整改措施均已完成并最终得到质量部的确认批准。
(3) 因特殊原因,整改措施计划需要进行变更或者延长时,在原计划完成日之前提出申请,并得到部门负责人、质量管理部经理的批准。
5.3 质量部:(1)负责建立和维护纠正和预防措施(CAPA)系统。
(2)批准(CAPA)的执行。
(3)批准(CAPA)的变更、包括完成期限的延长。
(4)跟踪(CAPA)实施发展情况。
(5)确保(CAPA)的合理性、有效期和充分性。
(6)保存纠正和预防措施(CAPA)的记录。

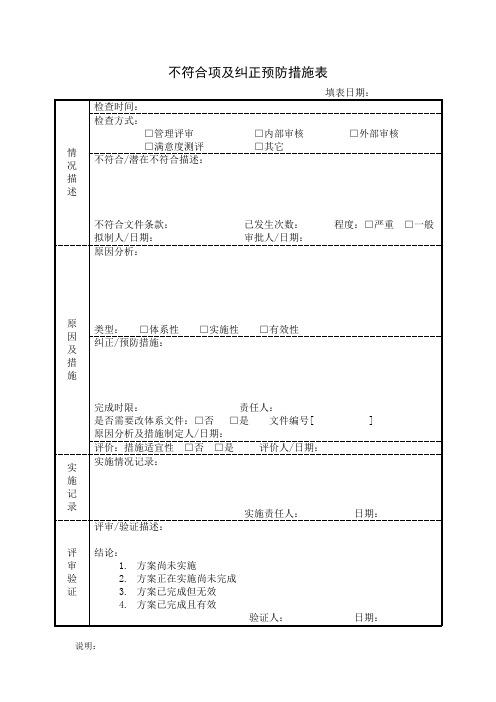
1、目的
1.1制定本程序及责任,清楚界定系统不符项之调查,制定纠正及预防措
施。
2、概述
2.1本程序主要适用于处理来自材料验收、生产中检查、最终检查及客户
品质投诉的不符合项目。
2.2另外,品质系统的不符合项,可通过COP17.1内部品质审核执行处理。
3、职责
3.1品质系统代表(QMR)、QC部负责人及生产部负责人全力推行及维持本
规定。
4、程序
4.1改善要求(Action Request)的发出条件
在以下任何一种情况下,各部门负责人均有权经由QMR向责任部门发
出改善措施要求表(CAR:Corrective Action Request),并要求有关
责任部门作出纠正行动或预防措施。
A.不合格品属于致命缺陷(Cr.)。
B.不合格品属于严重缺陷(MAJ),不良率超过5%。
C.不合格品属于轻微缺陷,不良率为100%。
D.每月FQC合格率低于即定目标。
E.客户投诉(记录于[客户投诉履历表]中)。
F.不符合项可能导致以上情况发生。
4.2纠正或预防措施范围
4.2.1在材料验收过程中出现不合格品/不合格项时,由QC部负责人决定是
否需发行CAR。
4.2.2当生产过程中生产部人员发现不合格品/不合格项时,由生产部负责
人决定是否需发行CAR。
4.2.3 在生产过程中巡回检查发现不合格品/不合格项时,由QC部负责人决
定是否需发行CAR。
4.2.4在FQC最终检查过程中出现不合格品/不合格项时,由QC部决定是否
需发行CAR。
4.2.5 当接到客户投诉时,由QA部负责人决定是否需发行CAR。
4.3纠正或预防措施的处理。
4.3.1 纠正行动
有关部门在收到4.2项所及的CAR时,须研究出现不合格品/不合格
项的原因,并提出纠正方法。
4.3.2 预防措施
当不合格品/不合格项发生的原因属于以下两种潜在性原因时,除作
纠正行动外,还需制定预防措施。
A.不合格品发生的原因会导致其它产品有可能发生同类性质不合格
品的出现(水平
展开预防)。
B.不合格项发生的原因可能会导致不合格品的出现。
4.3.3 纠正或预防措施的内容由责任部门填写在CAR上。
4.3.4 发行CAR的部门负责人应监察纠正或预防措施的执行过程,执行情况
由有关负责人填写在CAR上。
4.3.5 因更改预防行动而涉及到的相关的文件,手册程序等须进行同步更
改,并记录在[新发行/变更通知书]上,工程更改则记录在[工程更改]
上。
4.3.6 QMR应确保:
a)纠正或预防行动真正执行。
b)如遇上同样的问题反复出现,QMR应召开会议检讨其纠正或预防行
动是否有效,是否须作出更改,检讨的内容填写在[会议记录]上。
c)如有需要,QMR可安排内部审核进行监查。
d)有关纠正或预防行动呈交于管理会议上作定期评审(参照
COP1.1)。
4.4CAR跟进行动
4.4.1如果改善措施(纠正或预防)已有效完成,QMR将记录跟进结果完成
日及签署。
CAR即完结,存档。
4.4.2 如果改善措施到期后仍未完成,则记录于[CAR完成状态表]上。
4.4.3 若超过两次承诺日仍未成,则记录于[CAR完成状态表]上。
4.4.4 CAR的编号按顺序及他们的完成状态,记录于[CAR完成状态表]上由
QMR填写及保存。
5记录及表格
5.1改善措施要求表(CAR)。
(FM-MR-1411-01)
5.2 CAR完成状态表。
(FM-MR-1412-02)
5.3 客户投诉履历表。
(FM-MR-1413-01)。