安徽省怀远县包集中学高三化学二轮复习 考点40 高分子化合物
- 格式:doc
- 大小:41.50 KB
- 文档页数:4

安徽省怀远县包集中学2013届高三二轮复习第二轮复习资料第一部分基本概念和基础理论[教材分析]化学基本概念和基础理论是化学知识的基础,是从大量的化学现象和化学事实中抽象概括出来的,是化学现象的本质,它对学习元素及化合物知识有重要的指导意义。
能否准确、深刻地理解基本概念和基础理论,注意分析这些内容之间的联系和区别,形成体系,并能灵活运用这些知识,是学好化学的一个重要标志。
第一部分基本概念和基础理论一、物质的组成和分类1.理解原子、分子、离子、元素等概念的涵义。
熟记常见的元素符号。
2.理解化合物的涵义,能根据化合价书写分子式,并能根据分子式判断元素的化合价。
3.理解单质和化合物、混合物和纯净物的概念,能判断一些易分辨的、典型的混合物和纯净物。
4.理解酸、碱、盐(正盐、酸式盐、碱式盐)氧化物(酸性氧化物、碱性氧化物、两性氧化物)的概念。
二、化学中常用的量1.理解原子量、分子量的涵义。
2.理解物质的量的单位——摩尔、摩尔质量、气体摩尔体积的涵义。
三、物质的性质和变化1.理解物理变化、化学变化的涵义,能判断一些典型的、易分辨的物理变化和化学变化。
2.理解质量守恒定律的涵义,能正确书写化学方程式。
3.能判断化学反应的四种基本类型:化学反应、分解反应、置换反应、复分解反应(包括中和反应)。
能应用复分解反应发生的条件,判断反应能否发生。
4.理解离子方程式的涵义,掌握复分解反应的离子方程式的书写。
5.理解氧化——还原反应、氧化和还原、氧化性和还原性、氧化剂和还原剂等概念。
能判断并配平氧化——还原反应的化学方程式。
6.理解反应热的概念及热化学方程式的写法。
四、物质结构、元素周期律1.了解原子的组成及同位素的概念,理解原子序数、核电荷数、质子数、核外电子数之间的相互关系,以及质量数、中子数、质子数之间的相互关系。
2.理解离子键、共价键(极性键、非极性键)的涵义。
并能用电子式表示典型离子键、共价键的形成过程。
理解离子化合物、共价化合物的涵义。

物质的组成和分类1.掌握分子、原子、离子、原子团、元素等概念。
2.掌握混合物、纯净物、单质、化合物、金属、非金属的概念3.掌握氧化物、酸、碱、盐概念及相互关系。
4.了解同位素和同素异形体。
一、原子、分子、离子、元素、同位素、同素异形体的概念1.原子是。
2.分子是。
思考:是否可理解为分子是保持物质性质的微粒?3.元素是。
思考:质子数相同的微粒一定是同一种元素吗?4. 同位素是。
5.同素异形体是。
二、物质的分类1.将物质分为纯净物与混合物,是依据所含物质种类是不是一种来区分的。
2.将纯净物分为单质和化合物,是依据组成纯净物的元素是不是一种来区分的。
3.将无机物分为氧化物、酸、碱和盐四类,其依据是物质组成和性质上的不同。
氧化物是指由___________种元素组成,且其中一种为__________元素的化合物(注意氧化物与含氧化合物的区别和联系)。
将氧化物分为酸性氧化物、碱性氧化物、两性氧化物、不成盐氧化物,是依据氧化物跟酸或碱反应的情况来区分的。
【例1】下列叙述正确的是A.非金属氧化物都是酸性氧化物 B.碱性氧化物都是金属氧化物C.酸酐都是酸性氧化物 D.酸性氧化物都不能跟酸反应解析非金属氧化物不都是酸性氧化物,如水、一氧化碳、一氧化氮等氧化物就属于不成盐氧化物,所以A不正确。
酸性氧化物也称为酸酐,但多数有机酸的酸酐却不是酸性氧化物,如乙酸酐的结构简式为:,是两分子乙酸脱一分子水的产物,它不属于酸性氧化物。
所以C不正确。
酸性氧化物一般不能和酸反应,但二氧化硅能与氢氟酸反应,生成四氟化硅气体和水:SiO2+4HF=SiF4↑+2H2O D选项也不正确。
只有碱性氧化物都是金属氧化物的说法是正确的。
答案 B【例2】1995年诺贝尔化学奖授予致力于研究臭氧层破坏问题的三位环境化学家。
大气中的臭氧层可滤除大量的紫外光,保护地球上的生物。
氟利昂(如CC2F2)可在光的作用下分解,产生Cl原子,Cl原子会对臭氧层产生长久的破坏作用(臭氧的分子式为O3),有关化学反应为: Cl+O3→ClO+O2ClO+O→Cl+O2总反应:2O3→3O2①在上述反应中臭氧变成氧气的反应过程中,Cl是 ( )A.反应物 B.生成物 C.中间产物 D.催化剂②在叙述中O3和O2是 ( )A.同分异构体 B.氧的同位素 C.同系物 D.氧的同素异形体解析由题中所给的有关的化学反应可知,在上述反应中,氯原子所起的作用是促进臭氧分子转化成氧气分子,而它本身在反应前后并未发生变化。
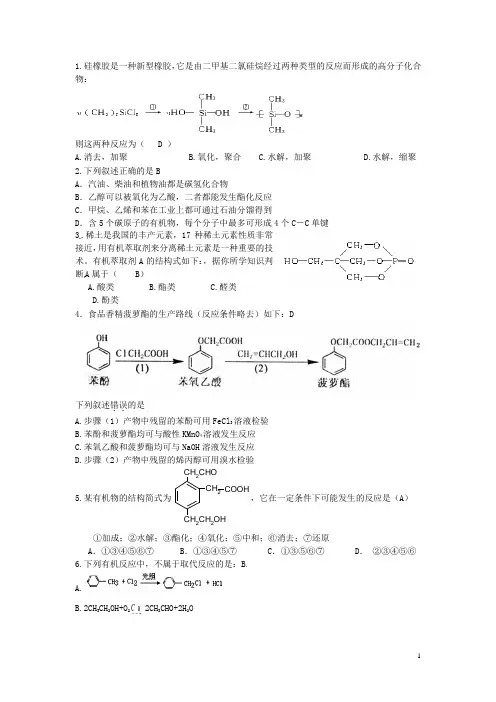
1.硅橡胶是一种新型橡胶,它是由二甲基二氯硅烷经过两种类型的反应而形成的高分子化合物:则这两种反应为( D )A.消去,加聚B.氧化,聚合C.水解,加聚D.水解,缩聚2.下列叙述正确的是BA.汽油、柴油和植物油都是碳氢化合物B.乙醇可以被氧化为乙酸,二者都能发生酯化反应C.甲烷、乙烯和苯在工业上都可通过石油分馏得到D.含5个碳原子的有机物,每个分子中最多可形成4个C-C单键3.稀土是我国的丰产元素,17种稀土元素性质非常接近,用有机萃取剂来分离稀土元素是一种重要的技术。
有机萃取剂A的结构式如下:,据你所学知识判断A属于(B)A.酸类B.酯类C.醛类D.酚类4.食品香精菠萝酯的生产路线(反应条件略去)如下:D下列叙述错误..的是A.步骤(1)产物中残留的苯酚可用FeCl3溶液检验B.苯酚和菠萝酯均可与酸性KMnO4溶液发生反应C.苯氧乙酸和菠萝酯均可与NaOH溶液发生反应D.步骤(2)产物中残留的烯丙醇可用溴水检验5.某有机物的结构简式为CH2CHOCH2COOHCH2CH2OH,它在一定条件下可能发生的反应是(A)①加成;②水解;③酯化;④氧化;⑤中和;⑥消去;⑦还原A.①③④⑤⑥⑦B.①③④⑤⑦C.①③⑤⑥⑦D.②③④⑤⑥6.下列有机反应中,不属于取代反应的是:BA.B.2CH3CH2OH+O2C u2CH3CHO+2H2OC 、ClCH 2CH=CH 2+NaOH 2H O∆−−−→HOCH 2CH=CH 2+NaCl D 、8.已知正四面体形分子E 和直线型分子G 反应,生成四面体形分子L 和直线型分子M 。
(组成E 分子的元素的原子序数小于10,组成G 分子的元素为第三周期的元素。
)如下图,则下列判断中正确的是( B )(E) (G) (L) (M)A . 常温常压下,L 是一种液态有机物B .E 中化学键是极性键C .G 有漂白性D .上述反应的类型是加成反应9.在核磁共振氢谱中出现两组峰,其氢原子数之比为3:2的化合物是:D :10.莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中。

7、9月三鹿奶粉事件调查结果显示,三鹿牌婴儿配方奶粉是被一种名为三聚氰胺的化合物所污染。
三聚氰胺简称三胺,也被人们称为“蛋白精”,其结构简式如下,下列说法不正确...的是( )A.三聚氰胺显弱碱性,能与盐酸反应B.1mol三聚氰胺可以与3mol氢气发生加成反应C.三聚氰胺所有原子一定共面D.三聚氰胺的分子式为C6N6H68、固体NH4I放入一个体积为 VL的真空密闭容器中,加热至一定温度后,恒温下发生下列反应:NH4I(s) NH3(g)+HI(g); 2HI(g) H2(g)+I2 (g)。
平衡时,测得容器中气体共为5 mol,其中HI为1.5 mol,则下列说法正确的是( )A.平衡时氨气为2.5 molB.平衡时HI的分解率为20%C.若开始时放入固体NH4I的量增大一倍,则平衡时气体共为10 molD.其它条件不变把容器的体积缩小到V/2 L,重新达到平衡时H2的浓度是原平衡的2倍9、已知2Fe3++2I-=2Fe2++ I2,当把Cl2通入FeI2溶液中时,下列离子方程式一定不正确...的是( )A. Cl2+2I-=I2+2Cl-B. 4Cl2+6I-+2Fe2+=2Fe3++3I2+8Cl-C. 3Cl2+2Fe2++4I-=2Fe3++2I2+6Cl-D. 2Cl2+2Fe2++2I-=2Fe3++I2+4Cl-10、下列溶液中,说法正确的是( )A. NaHCO3溶液中可以大量存在NO3—、[Al(OH)4]—、K+、S2-等离子B. 室温下0.1 mol/L的NaOH溶液与pH=1的某酸HA等体积混合后,溶液中C(Na+)≥C(A-)C. 1 mol/L的醋酸溶液加水稀释时,溶液中所有离子浓度均减小D. t℃时,水的离子积常数为Kw,则[c(OH-)]2=Kw的水溶液一定呈中性11、2 mol NaHCO3和一定量Na2O2固体在密闭容器中加热使其充分反应,测得150℃时,容器中仅剩余两种气体,则容器中剩余的固体( )A.只有Na2CO3B.一定为Na2CO3和NaOHC.可能有Na2O2D.可能有NaOH12、下列各项中的两个量,其比值一定为2:1的是()A.液面在“0”刻度时,50mL碱式滴定管和25mL碱式滴定管所盛液体B.在碳与浓硫酸的反应中,还原产物与氧化产物的物质的量C. 1mol Na2O2与1molNa2O中的阴离子数目D.相同温度下,0.2mol/L醋酸溶液和0.1mol/L醋酸溶液中c(H+)13、已知①2C(s)+O2(g)=2CO(g);ΔH=-221.0kJ/mol ②2H2(g)+O2(g)=2H2O(g);ΔH=-483.6kJ/mol。
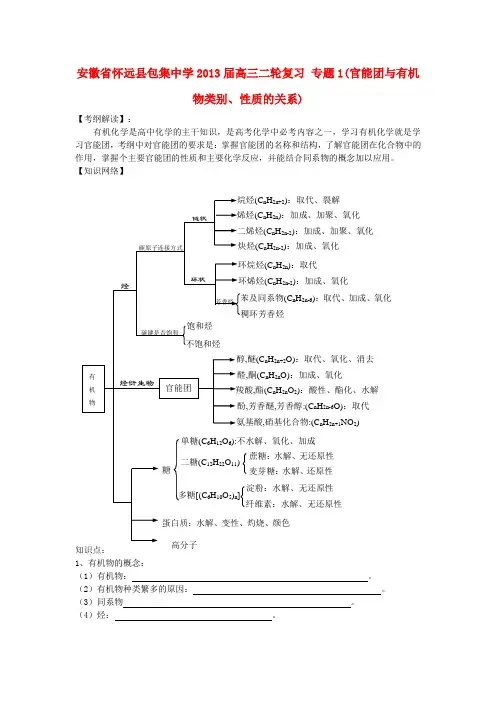
安徽省怀远县包集中学2013届高三二轮复习专题1(官能团与有机物类别、性质的关系)【考纲解读】:有机化学是高中化学的主干知识,是高考化学中必考内容之一,学习有机化学就是学习官能团,考纲中对官能团的要求是:掌握官能团的名称和结构,了解官能团在化合物中的作用,掌握个主要官能团的性质和主要化学反应,并能结合同系物的概念加以应用。
【知识网络】1、有机物的概念:(1)有机物:。
(2)有机物种类繁多的原因:。
(3)同系物。
(4)烃:。
2、官能团(1)定义:(2)常见官能团:RCOOH4.四种有机分子的空间结构5、重要有机物的物理性质归纳(1)溶解性: 有机物均能溶于有机溶剂.能溶于水的有机物为:低级的醇、醛、酸 微溶于水:①苯酚 ②苯甲酸 ③C 2H 5-O-C 2H 5注意:水溶性规律。
有机物是否溶于水与组成该有机物的原子团(包括官能团)有密切关系。
在有机物分子常见的官能团中,—OH 、—CHO 、—COC —、—COOH 、—SO 3H 等,皆为亲水基,—R 、—NO 2、—X 、—COOR —等皆为憎水基。
一般来讲,有机物分子中当亲水基占主导地位时,该有机物溶于水;当憎水基占主导地位时,则难溶于水。
由此可推知: ①烃类均难溶于水,因其分子内不含极性基团。
②含有—OH 、—CHO 、及—COOH 的各类有机物(如醇、醛、酮、羧酸),其烃基部分碳原子数小于等于3时可溶于水。
③当活泼金属原子取代有机物分子中的氢原子后所得的产物可溶于水。
如CH 3CH 2ONa 、CH 3COONa 、C 6H 5ONa 等。
(2)密度:比水轻的:①烃(含苯及其同系物、矿物油) ②酯(含油脂) ③一氯烷烃 比水重: ①溴苯 ②溴乙烷 ③四氯化碳液态 ④硝基苯 ⑤苯酚 (3)有毒的物质:苯、硝基苯、甲醇、甲醛(4)常温下呈气态: ①分子中含碳原子数小于或等于4的烃(新戊烷除外) ②CH 3Cl ③HCHO(5)有特殊气味或香味:①苯 ②甲苯 ③CH 3COOC 2H 5 ④CH 3CH 2OH6、几类重要的有机物(1)糖类:又叫碳水化合物,一般符合C n (H 2O)m 的通式,但是符合该通式的不一定就属于糖类,不符合该通式的也可以属于糖类。

安徽省怀远县包集中学高考化学第二轮复习教案:盐类水解知识及其应用教学目标知识技能:使学生掌握盐类水解的实质和规律,并能够运用水解规律及平衡知识解释、说明有关化学事实。
能力培养:创设问题情景,引导学生注重掌握知识的准确性,培养学生运用知识逻辑推理,解决新问题的能力。
科学思想:通过实验及问题讨论,加强学生对现象与本质的辩证关系的理解,使学生学会用实验方法和逻辑推理去探究物质之间的内在联系。
科学品质:通过对水解知识的拓展与迁移,激发学生的学习兴趣和求知欲,让学生自己设计实验,培养学生的创造性和严谨求实的科学品质。
科学方法:分析推理,迁移应用及科学抽象。
重点、难点水解规律的综合应用及准确的分析表述。
教学过程设计教师活动【引言】我们已经知道盐溶液不一定是中性溶液,其原因是由于盐类的水解。
本次课的内容是复习水解实质、规律及相关知识在解决实际问题中的应用。
学生活动回忆思考有关盐类水解的概念及其规律。
【投影演示】(1)少量CH3COONa固体投入盛有无水乙醇的培养皿,滴加几滴酚酞,然后再加入少量水。
(2)少量镁粉投入盛有NH4Cl水溶液的培养皿。
【提问】请结合两个实验现象,分析、解释其本质原因,并写出有关离子方程式。
观察实验,记录现象:(1)开始酚酞不变色,加水后变红色;(2)有气泡产生。
讨论分析现象得出:实验(1)CH3COO-与水电离出的H+结合生成CH3COOH,而使水的电离平衡向右移动,溶液显碱性。
因此盐类水解,水也是必要的反应物之一。
CH3COO-+H2O CH3COOH+OH-实验(2)NH4+水解,使溶液显酸性,镁与水解产生的氢离子发生置换反应生成氢气。
NH4+H2ONH3·H2O+H+Mg+2H+=Mg2++H2↑由于水解平衡的正向移动,产生的气体中除氢气可能也有氨气。
归纳小结:【板书】一、盐类水解的实质【投影】例1现有酚酞、石蕊、0.1mol/L氨水、氯化铵晶体、0.1mol/L盐酸、熟石灰和蒸馏水,若仅用上述试剂怎样用简单实验方法证明氨水是弱碱?请讨论可能的实验方案。

安徽省怀远县包集中学2013届高三二轮复习化学考试说明的解读一、选修占15%。
化学的考试范围包括两个部分。
第一部分包括必修模块“化学1”、“化学2”和选修模块“化学反应原理”(对应《考试大纲》中规定的“必考内容部分”);第二部分包括选修模块“有机化学基础”和“物质结构与性质”的部分内容,约占15%。
二、新增和强化了部分内容点。
这包括:了解科学探究的基本过程,学习运用以实验和推理为基础的科学探究方法;了解定量研究的方法是化学发展为一门科学的重要标志;了解科学、技术、社会的相互关系(如化学与生活、材料、能源、环境、生命过程、信息技术的关系等);了解在化工生产中遵循“绿色化学”思想的重要性;能用盖斯定律进行有关反应热的简单计算;了解能源是人类生存和社会发展的重要基础;了解化学在解决能源危机中的重要作用;了解催化剂在生产、生活和科学研究领域中的重大作用;了解难溶电解质的溶解平衡;常见金属元素增加了Cu;能根据实验试题要求,做到(1)设计、评价或改进实验方案,(2)了解控制实验条件的方法,(3)分析或处理实验数据,得出合理结论,(4)绘制和识别典型的实验仪器装置图;物质结构与性质模块所要求的考查点几乎是全新的,要求掌握用电子排布式表示的常见元素为1~36号。
三、部分内容被弱化。
包括:共价键的极性、分子的极性、氢键、分子间作用力等不做要求,元素化合物内容仅限于所规定的元素,不要求到族的范围,有机化合物仅限于所规定的几种常见物质,不要求掌握到这些物质的同系物,即就物质论物质,不再延伸;定量实验仅强调了溶液的配制,中和滴定实验没有提及。
四、侧重考查学生的基本科学素养。
以化学基础知识、基本能力和重要方法为考查重点,体现新课程标准对知识与技能、过程与方法、情感态度与价值观等目标要求,密切联系学生生活经验和社会实际,较原来强化了以学生生活经验和社会实际为背景考查内容点,突出强调了重要方法和探究能力的考查,注意发掘考生观察问题、发现问题和解决问题的能力,进一步重视对考生获取加工信息的能力的考查。


3、可以从石油或煤中获得的基本化工原料是(写名称),其分子式为,结构简式为,空间结构为。
4、生活中常见的有特殊香味的,能够溶解多种有机物和无机物的,能与水以混溶的有机物是,(写名称),俗名为。
其分子式为,结构简式为,它的官能团是,(写名称和结构简式)5、生活中常见的有强烈刺激性气味的无色液体是,(写名称),俗名为。
分子式为,结构简式为,它的官能团是,(写名称和结构简式)。
6、基本营养物质是,,。
7、葡糖糖和果糖的化学式是,它们属糖,它们互为体。
蔗糖和麦芽糖的化学式是,它们属糖,它们互为体。
米的主要成分是,棉花的主要成分是。
其化学式都可表示为,它们属糖,它们属于同分异构体吗?。
8、油脂包括和。
它们分别是酯和酯。
能使溴水褪色的是。
9.毛发、皮、丝、酶的主要成分是。
10、葡萄糖的结构简式是,它的特征反应是①,②。
11、蔗糖水解条件是,水解产物是12、淀粉的特征反应是。
水解条件是,水解的最终产物是。
13、蛋白质的特征反应是:①,②。
水解的最终产物是。
14、油脂在酸性条件下水解为和。
在碱性条件下水解为和。
后者水解反应也称为。
二、基本概念1、烃:仅含两种元素的有机物称为碳倾化合物,也称为烃。
例如:苯分子组成中只有两种元素,所以它属于;乙醇分子组成中有3种元素,所以它烃(填“是”或“不是”)。
2、同系物:结构,相差一个或多个原子团的物质。
例如:乙烷和丁烷都是烷烃,是烃,(填“饱和”或“不饱和”),分子中都是键,故结构相似,但C4H10-C2H6= C2H4,即分子组成相差了2个CH2原子团,所以乙烷和丁烷属于关系。
3、同分异构体:相同,不同的化合物。
例如:正丁烷CH3-CH2-CH2-CH2-CH3和异丁烷CH3-CH-CH3的分子式都是,CH3但它们的碳原子排列不同,即结构不同,所以正丁烷和异丁烷互称为说明:1、同系物分子式通式相同,结构相似,性质相似。
2、互为同分异构体的有机物不可能是同系物关系。
三、基本规律1、烃类的密度都小于水,都难溶于水。

安徽省怀远县包集中学2013届高三二轮复习高考化学全套基础知识汇总一.物质的组成、性质和分类:(一)掌握基本概念1.分子分子是能够独立存在并保持物质化学性质的一种微粒。
(1)分子同原子、离子一样是构成物质的基本微粒.(2)按组成分子的原子个数可分为:单原子分子如:He、Ne、Ar、Kr…双原子分子如:O2、H2、HCl、NO…多原子分子如:H2O、P4、C6H12O6…2.原子原子是化学变化中的最小微粒。
确切地说,在化学反应中原子核不变,只有核外电子发生变化。
(1)原子是组成某些物质(如金刚石、晶体硅、二氧化硅等原子晶体)和分子的基本微粒。
(2)原子是由原子核(中子、质子)和核外电子构成的。
3.离子离子是指带电荷的原子或原子团。
(1)离子可分为:阳离子:Li+、Na+、H+、NH4+…阴离子:Cl–、O2–、OH–、SO42–…(2)存在离子的物质:①离子化合物中:NaCl、CaCl2、Na2SO4…②电解质溶液中:盐酸、NaOH溶液…③金属晶体中:钠、铁、钾、铜…4.元素元素是具有相同核电荷数(即质子数)的同—类原子的总称。
(1)元素与物质、分子、原子的区别与联系:物质是由元素组成的(宏观看);物质是由分子、原子或离子构成的(微观看)。
(2)某些元素可以形成不同的单质(性质、结构不同)—同素异形体。
(3)各种元素在地壳中的质量分数各不相同,占前五位的依次是:O、Si、Al、Fe、Ca。
5.同位素是指同一元素不同核素之间互称同位素,即具有相同质子数,不同中子数的同一类原子互称同位素。
如H有三种同位素:11H、21H、31H(氕、氘、氚)。
6.核素核素是具有特定质量数、原子序数和核能态,而且其寿命足以被观察的一类原子。
(1)同种元素、可以有若干种不同的核素—同位素。
(2)同一种元素的各种核素尽管中子数不同,但它们的质子数和电子数相同。
核外电子排布相同,因而它们的化学性质几乎是相同的。
7.原子团原子团是指多个原子结合成的集体,在许多反应中,原子团作为一个集体参加反应。

安徽省怀远县包集中学2013届高三二轮复习 周末理综化学试题一7.下列有关说法中错误..的是( ) A .对大型船舶的外壳所进行的“牺牲阳极的阴极保护法”,是应用了电解池原理。
B .青铜是我国使用最早的合金,钢是用量最大、用途最广的合金。
C .硅的提纯与应用,促进了半导体元件与集成芯片业的发展。
D .光纤通讯是光作为信息的载体,制造光导纤维的基本原料是石英。
8.设阿伏加德罗常数为N A 。
则下列说法正确的是 ( )A .常温常压下,18.0 g 重水(D 2O)中所含的电子数为10 N AB .1cm 3铁所含的铁原子数是ρ·N A /56(ρ是铁的密度,单位为g·cm -3)C .2.24LCO 2与足量的N a 2O 2反应,Na 2O 2转移的电子总数一定为0.1N AD .常温下,2.7g 铝片投入足量的浓硫酸中,铝失去的电子数为0.3N A9.下列各组离子,一定能大量共存的是 ( )A .常温下,c(H +)/c(OH -)=1×10-12的溶液:I -、Cl -、HCO 3-、Na +B .在pH=1的溶液中:K +、Cl -、NO 3-、Fe 2+C .加入铝粉能产生氢气的溶液:NH 4+、Fe 2+ 、SO 42- 、Cl -D .由水电离出的c(H +)=1×10-12 mol•L -1溶液中:K +、Cl - 、NO 3- 、Na+ 10.化学反应N 2+3H 2 = 2NH 3的能量变化如图所示,该反应的热化学方程式是( )A .N 2(g)+3H 2(g) = 2NH 3(l)⊿H = 2(a —b —c)kJ/molB .N 2(g)+3H 2(g) = 2NH 3(g)⊿H = 2(b —a)kJ/molC .21N 2(g)+23H 2(g) = NH 3(l) ⊿H = (b +c —a)kJ/mol D .21N 2(g)+23H 2(g) =NH 3(g) ⊿H = (a +b)kJ/mol11.下列各溶液中,叙述正确的是( )A .0.1mol /L 的(NH 4)2SO 4溶液中:c(SO 42–) >c(NH 4+)>c(H +)>c(OH ˉ)B .25℃时,将pH=3的盐酸溶液和pH=11的氨水等体积混合后,溶液中离子浓度的关系: ()()()()4c c c c NH Cl OH H +--+>>> C .将0.11mol L -⋅ 醋酸溶液加大量水稀释后,溶液的pH 增大D .Na 2CO 3溶液中:()()()()223332c c c c H CO CO HCO Na --+=++12.某工厂用CaSO 4、H 2O 、NH 3、CO 2制备(NH 4)2SO 4,其工艺流程如下:CaSO 4浊液 甲 乙 滤液 (NH 4)2SO 4CaCO 3 生石灰+CO 2↑煅烧 提纯 足量NH 3 适量CO 2 过滤下列推断不合理的是( )A .往甲中通入CO 2有利于(NH 4)2SO 4的生成B .生成lmol(NH 4)2SO 4至少消耗2mol NH 3C .可采用加热蒸干的方法从滤液中提取(NH 4)2SO 4晶体D .CaCO 3煅烧所得的CO 2可以循环使用13.恒温、恒压下,1 molA 和nmolB 在一个容积可变的容器中发生如下反应: A(g)+2B(g) 2C(g)。
安徽省怀远县包集中学高三化学复习有机化学基础》回归课本提要第一章认识有机化合物(1)有机物和有机化学的定义?P1(2)有机化合物从结构上有两种分类方法?各分类方法中的子目录以及归类?P3~4(3)有机物种类繁多的原因?P7~8第二章烃和卤代烃(1)烷烃、烯烃和炔烃物理性质上的相似性和递变性?P28~29如:烷烃的熔沸点较(因为凝固后是晶体),密度较且ρρ(H2O)。
烷烃的物理性质随着分子里碳原子数的递增,呈现规律性的变化。
常温下,它们的状态由_____态变到_____态又变到_____态;它们的沸点逐渐_______,相对密度逐渐_______。
烃的支链越多,熔沸点越____。
如熔沸点:正丁烷____异丁烷。
(烯烃和炔烃相似)(2)烷烃、烯烃和炔烃结构上的差异?烯烃的顺反异构及具备顺反异构的条件?(3)烷烃、烯烃和炔烃各自所具有的化学性质以及所属有机反应的类型(4)实验室制乙炔? 图片中的仪器、试剂及对应用途?P32(5)脂肪烃的来源(可结合必修二的石油化工等内容巩固)P35~36(6)苯的特殊结构及C原子杂化方式?苯均有的化学性质?P37~38苯的同系物以及其余芳香烃结构和性质?P38~39,P39的资料卡片(7)芳香烃的来源(可结合必修二的煤的干馏等内容巩固)P39(8)卤代烃的用途、结构和性质(尤其是水解和消去)P40~42P42氟利昂的性质和用途。
P42科学视野:臭氧层的保护第三章烃的含氧衍生物(1)简单醇和酚的命名?P48(2)醇类的结构特点和主要化学性质以及所属有机反应的类型?P49~52甲醇、乙醇、丙醇等低级醇易溶于水的原因?P49实验室制乙烯? 图片中的仪器、试剂及对应用途、反应条件?P51(3)苯酚的物理性质(尤其注意颜色、水溶性知识点)?P52苯酚沾在皮肤上的危害与处理?P52(4)苯酚的化学性质和用途?P53~54(5)甲醛、乙醛等醛类的物理性质和用途?P56(6)乙醛的结构特点和主要化学性质以及所属有机反应的类型?P57~58 P58学与问注:银镜反应实验、新制Cu(OH)2悬浊液反应(7)羧酸的结构特点和分类?P60(8)乙酸的物理性质和化学性质?P60~61P60科学探究:验证乙酸、碳酸和苯酚的酸性强弱(9)常见酯类的存在和用途P62(10)酯类的物理性质和化学性质(酸性和碱性时的水解)P62?P63思考与交流:乙酸乙酯制备实验(必修二)的平衡问题思考第四章生命中的基础有机化学物质(1)六大营养素?三大营养物质?P72(2)油脂的分类、组成、结构?P74(3)油脂的物理性质和化学性质?P75~78P76科学视野:肥皂、合成洗涤剂的影响?(4)糖类的定义、结构和分类?P79P79资料卡片:糖类与糖水化合物的关系?(5)蛋白质与氨基酸的关系?氨基酸的结构和性质?P86~87(6)蛋白质的结构和性质(水解、盐析、变性、颜色反应、灼烧等)?P88~90 (7)酶与核酸的了解和认识?P91~93。
安徽省怀远县包集中学高考化学第二轮复习教案:铝铁教学目标知识技能:复习铝盐、偏铝酸盐及氢氧化铝之间的转化关系及转化时量的关系;能用离子方程式正确表达它们之间的关系;应用化学平衡原理解释氢氧化铝的两性,掌握实验室制备氢氧化铝的方法;复习铁,二价铁,三价铁三者之间的相互转化关系,并能正确写出有关的氧化还原反应的离子方程式;掌握铁离子及亚铁离子的检验方法;通过计算掌握变价金属与硝酸反应时铁的量不同,反应产物不同。
能力培养:培养学生总结概况形成规律性认识的能力;培养学生的实验能力、观察能力及综合分析问题和解决问题的能力。
科学思想:通过复习氢氧化铝的两性及铝元素在化合物中的转化关系,对学生进行量变到质变、矛盾的对立统一等辩证唯物主义观点的教育;通过对铝、铁的综合题的计算,使学生建立数、形结合思想,拓展解题思路。
科学品质:通过学习,使学生善于总结,并在总结中发现问题。
科学方法:教会学生将化学中的定量问题表格化、图象化;通过对实验的观察,了解现象与本质的关系,使学生进一步掌握用实验的方法将化学中微观的问题宏观化;抽象的问题具体化。
重点、难点重点:氢氧化铝的两式电离;铝化合物之间转化的量的关系;铁,二价铁,三价铁之间的转化关系及氢氧化亚铁转化成氢氧化铁;难点:铝化合物之间转化的图象表示;变价金属与硝酸反应的计算。
教学过程设计教师活动【引言】铝、铁是中学化学元素化合物中的重点,而其中的Al(OH)3、和“铁三角”的这两部分内容既是重点又是难点,同时又是高考的热点。
所以高三对这两部分内容的复习是非常重要的。
结合这段内容,我准备了八个问题,其中有两个问题昨天已经布置下去了,请同学们分成小组先把上节布置的内容讨论一下,然后我们再按提纲逐一讨论,最后一起归纳总结。
我们今天采用大屏幕实物投影,请同学们将讨论的结果直接写在白纸上,以便和其他的同学一起交流。
【投影】题目见右栏将学生分成5~6人一组,按问题逐一讨论。
学生活动回忆并讨论昨天布置的两题:式正确表示其关系。
选择题(每小题只有一个正确答案,每小题3分,共60分)1.下列各组物质的最简式相同的是A.乙酸和乙二酸 B.丁酸和乙酸 C.甲醛和乙酸 D.乙二酸和乙二醇2.下列说法中错误的是A.C2H6和C4H10一定是同系物B.在相同条件下,燃烧等物质的量的C2H4和乙醇,消耗O2体积相同C.相对分子质量相同的两种物质一定是同分异构体D.烯烃各同系物中碳的质量分数都相等6.下列操作达不到预期目的的是①石油分馏时把温度计插入液面以下②用溴水除去乙烯中混有的SO2气体③用乙醇与3mol·L-1的H2SO4溶液混合共热到170℃制乙烯④将苯和溴水混合后加入铁粉制溴苯⑤将饱和食盐水滴入盛有电石的烧瓶中制乙炔A.①②④ B.③⑤ C.②③④⑤ D.①②③④7.甲酸、乙酸、碳酸、苯酚的酸性由强到弱的顺序是A.碳酸、苯酚、甲酸、乙酸B.甲酸、乙酸、碳酸、苯酚C.甲酸、碳酸、苯酚、乙酸D.苯酚、碳酸、乙酸、甲酸8.下列物质属于同系物的是B.CH3CH2Cl和CH2ClCH2CH2ClC.C2H5OH和CH4O D.CH3COOH和C17H33COOH9.有5种有机物:⑤CH2=CH—CH=CH2 ,其中可用于合成高分子材料的正确组合为A.①②④ B.①②⑤ C.②④⑤ D.③④⑤10.将一定量的有机物充分燃烧后的产物通入足量的石灰水中完全吸收,经过滤得沉淀20g,滤液质量比原石灰水减少5.8g,该有机物不可能是A.乙烷 B.乙烯 C.乙醇 D.乙二醇11.用括号中的试剂除去各组物质中的少量杂质正确的是A.苯中的甲苯(溴水) B.乙酸乙酯中的乙酸(NaOH溶液)C.乙醇中的乙酸(NaOH溶液) D.乙醇中的水(新制的CaO)12.一定质量的某有机物与足量金属钠反应要得V A L气体。
相同质量的该有机物与足量的NaHCO3浓溶液反应,可得V B L气体。
已知在同温同压下V A和V B相同,则该有机物可能是HOOC—CH2—CH—CH2—COOHOHOOHO—HO—A.CH3CH(OH)COOH B.HOOC—COOHC.CH3CH2CH2OH D.13.已知化学式为C4H10O的醇有4种异构体,若在该分子中增加1个羰基,形成的C5H10O2 的羧酸可能有的结构有A.2种B.4种C.6种D.5种16.等物质的量的乙醇、乙二酸、甘油,分别与足量金属钠作用,生成等物质的量的H2,则乙醇、乙二酸、甘油物质的量之比为A.6:3:2 B.1:2:3 C.3:2:1 D.4:3:217.某有机物分子式为C3H6O2在酸性条件下水解得一元酸A与一元醇B,A与B的相对分子质量相等,则以下结论不正确的是A.A中含碳26.09% B.A具有还原性C.B经氧化也可得到一元酸且酸性比A强 D.B分子结构中有甲基18.将40mL 0.2mol/L NaOH溶液和20mL0.2mol/L的CH3COOH溶液混和,充分反应后蒸干并加强热,最终得到的固体是A.Na2CO3B.CH3COONa C.NaOH和CH3COONa的混合物D.NaOH19.中草药陈皮中含有(碳、氢原子未画出,每个折点代表一个碳原子),它具有抗菌作用。
第一课时学案一、考纲展示:1、了解常见非金属元素(H、C、N、O、Si、S、Cl等)单质及重要化合物的主要性质及应用。
2、了解常见非金属元素单质及其重要化合物对环境质量的影响。
二、考点整合(一)非金属元素活动性规律的判断方法:(1)看非金属单质与H2化合的难易程度,越易化合,则其非金属性越强。
(2)看形成气态氢化物的稳定性,稳定性越强,则其非金属性越强.(3)看非金属之间的置换能力,A能置换出B,则A的非金属属性强于B。
(4)依据元素周期表中的位置进行判断,同一周期越靠右,其非金属性越强;同一主族越靠上,其非金属性越强.(5)看最高价氧化物对应水化物的酸性强弱,一般酸性越强,则其非金属性越强。
(二)非金属单质的制备方法:(1)电解法电解水溶液:如2NaCl+2H2O Cl2↑+H2↑+2NaOH电解熔融物:如2NaCl Cl2↑+2Na(2)分解法:如2KClO3△2KCl+3O2↑;2KMnO4△K2MnO4+MnO2+O2↑(3)置换法如Cl2+2NaBr△2NaCl+Br2(4)氧化法如4HCl(浓)+MnO2△MnCl2+Cl2↑+2H2O(5)还原法如Zn+2HCl H2↑+ZnCl2;C+H2O 高温CO+H2; 2C+SiO2高温Si+2CO↑(三)重要的非金属元素及化合物的转化关系1、氯及其化合物的转化关系2、硫及其化合物的转化关系3、硅及其化合物的转化关系4、氮、磷及其化合物的转化关系三、典例解析例1、下列各组气体中,在通常情况下既能共存又能用浓硫酸干燥的是()A、CO2、H2S、Cl2B、H2、O2、SO2C、HCl、HBr、HID、NH3、HCl、CO2例2、下列说法正确的是()A、非金属单质不可能置换出金属单质B、仅由非金属元素不可能组成离子化合物C、非金属元素中,只有磷元素有不同的单质D、白烯转化为红磷是化学变化例3、下列有关因果关系的描述正确的是()A、因为盐酸的酸性强于氢硫酸,所以氯元素比硫元素非金属性强B、因为元素最高价态化合物有氧化性,所以磷酸具有强氧化性C、因为O2转化为O3是吸热反应,所以O3比O2稳定D、金刚石转变为石墨的结构发生了改变,因而是一个化学反应例4、通过化合反应不能制备的物质是()A、FeCl3B、H2SiO3C、Fe(OH)3D、NaHCO3答案:1、B 2、D 3、D 4、B四、随堂训练1、如图所示,关闭开关B,在A处通入少量SO2气体,则D中观察到现象I;打开开关B,从A处通入过量SO2,在C处观察到现象II,则I、II分别为()A、无变化;红色消失B、变为红色;无变化C、变为红色;红色褪去D、无变化;无变化2、湿润的淀粉碘化钾试纸接触某气体而显蓝色,该气体中可能有( )①Cl2②NO2③H2S ④SO2⑤HCl ⑥Br2(g)A、①③④B、①②⑤C、①②⑥D、②④⑤3、汉代器物上的颜料“汉紫”至今尚未发现其自然存在的记载。
安徽省怀远县包集中学高中化学必修二重要的有机化合物提高训练I 卷(40分)1.关于乙酸的下列说法中不正确的是()A.乙酸易溶于水和乙醇B.无水乙酸又称冰醋酸,它是纯净物C.乙酸是一种重要的有机酸,是有刺激性气味的液体D.乙酸分子里有四个氢原子,所以不是一元酸2.下列有关乙醇的物理性质的应用中不正确的是()A.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去B.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中草药的有效成分C.由于乙醇能够以任意比溶解于水,所以酒厂可以勾兑各种浓度的酒D.由于乙醇容易挥发,所以才有俗语“酒好不怕巷子深”的说法3.上海环保部门为了使城市生活垃圾得到合理利用,近年逐步实施了生活垃圾分类投放的办法。
其中塑料袋、废纸、旧橡胶制品等属于()A.无机物 B.有机物 C.盐类 D.非金属单质4.某有机化合物X,经过下列变化后可在一定条件下得到乙酸乙酯。
则有机物X是()A.C2H5OH B.C2H4C.CH3CHO D.CH3COOH5.白酒、食醋、蔗糖、淀粉等均为家庭厨房中常用的物质,利用这些物质能完成的实验是()①检验自来水中是否含氯离子②鉴别食盐和小苏打③蛋壳能否溶于酸④白酒中是否含甲醇A.①② B.①④ C.②③ D.③④6.既能发生酯化反应,又能使紫色的石蕊试液变红的物质是()A.CH3CH2OH B.H2CO3C.CH3COOH D.CH3COOC2H57.可以判断油脂皂化反应基本完成的现象是()A.反应液使红色石蕊试纸变蓝色B.反应液使蓝色石蕊试纸变红色C.反应后静置,反应液分为两层D.反应后静置,反应液不分层8.既能发生酯化反应,又能使紫色的石蕊试液变红的物质是()A.CH3CH2OH B.H2CO3C.CH3COOH D.CH3COOC2H59.可以判断油脂皂化反应基本完成的现象是()A.反应液使红色石蕊试纸变蓝色B.反应液使蓝色石蕊试纸变红色C.反应后静置,反应液分为两层D.反应后静置,反应液不分层10.辨别固体石蜡和脂肪的方法是()A.加热熔化后,滴入有酚酞的烧碱溶液共煮B.加热熔化后,加入碳酸钠溶液共煮C.加热熔化后,加入稀H2SO4共煮D.加热熔化后,滴加溴水11.有机物在反应中,常有下列原子间的共价键全部或部分断裂,如C—H、C—C、C=C、C)12.工业上为使95.6%乙醇变为100%绝对乙醇,常加入一种物质加热回流一段时间后蒸馏,得到99.5%的无水乙醇,然后再加入另一种物质加热回流一段时间后蒸馏得到绝对乙醇,这两种物质分别是()A.无水硫酸铜,生石灰 B.无水氯化钙,金属钠C.生石灰,金属镁 D.浓硫酸,金属镁13.将W1 g光亮的铜丝在空气中加热一段时间后,迅速插入下列物质中,取出干燥,如此反复几次,最后取出铜丝用蒸馏水洗涤、干燥、称得其质量为W2 g。
课标解读知识再现1.高分子化合物概述<1>几个概念:高分子化合物____________________________________________________单体____________________________________________________________链节____________________________________________________________链节数__________________________________________________________举例:合成聚乙烯的单体是_________其中链节为_________<2>高分子化合物的分类②按使用功能分类_________________________________________________③按受热时的性质分类_____________________________________________④按高分子结构特点分类___________________________________________ 2.高分子化合物的合成----聚合反响聚合反响概念____________________________________________________<1>加聚反响___________________________________________________写出以下物质合成高分子化合物的化学方程式:n CH2= CH- C l→n CH2= CH- CN→n CH2= C( CH3)COO CH3→n CH2= CH-CH=CH2→n CH2= C( CH3)- CH=CH2→小结: (按通式书写化学方程式)<2>缩聚反响_____________________________________________________写出以下物质合成高分子化合物的化学方程式:nCH3-CH-COOH→OHnCH3-CH-COOH→NH2nHO- CH2-CH2-OH+nHOOC-COOH→nHCHO+nC6H5-OH→3. 高分子化合物单体的判断<1>加聚型: [ CH CH ]n _____________ [ CH2-CH=CH-CH2 ] n_________________CH3 CH3[ CH2-CH2-CH-CH2 ] n[ CH2-CH=CH-CH2-CH-CH2 ] n________________ CH<2>缩聚型O O[O-CH-C ] n___________________ [ NH- CH2-CH-C ] n ______________C H3 CH3[O- CH2-CH2–O-C- CH2-CH2-C ] nO O规律小结:4. 高分子化学反响<1>概念:___________________________________________________________________<2>.高分子化学反响的应用①合成不能直接通过小分子物质聚合而得到的高分子化合物举例说明:___________________________________________________________②用于橡胶的硫化③广泛用于纤维素的改性(举例说明)5.合成高分子材料<1>常见高分子材料分类①:塑料:_______型热塑性塑料_________型热固性塑料②合成纤维:_______,_________,___________,__________,__________,________被称为“六大纶〞特种合成纤维③合成橡胶:通用橡胶___________,___________,____________等特种橡胶_________________________________<2>功能高分子材料(自己看书填写)分类:______________________________________________________________<3>复合材料①概念:指两种或两种以上材料组成的一种新型材料,其中一种材料为基体,另一种材料作为增强剂.②性能:具有强度高,质量轻,耐高温,耐腐蚀等优异性能,在综合性能上超过了单一材料.典题解悟夯实双基1.综合治理“白色污染〞的各种措施中,最有前景的是 ( )A.填埋或向海中倾倒处理 B.热分解或熔融再生处理C.积极寻找纸等纤维类制品替代塑料 D.开发研制降解塑料2.环境问题关系到人类的生存和开展,保护环境就是保护人类自己.从保护环境的角度出发,目前最有开展前景的一次性餐具是〔〕A.瓷器餐具B.塑料餐具C.淀粉餐具D.不锈钢餐具3. 以下物质一定不是天然高分子的是〔〕A.橡胶B.蛋白质C.尼龙D.纤维素4. 2022年“神州五号〞飞船实现了载人航天,标志着我国航天技术到达了世界先进水平,飞船应用了许多尖端的合成材料。
考点聚焦
1.合成有机高分子化合物的基本方法; 2.理解加聚反应和缩聚反应的特点,能够进行单体与聚合物结构简式的互相推断;
3.了解有机高分子化合物的结构特点和基本性质;
4.了解常见合成高分子材料的品种、性能和用途;
5.常识性了解新型高分子材料。
知识梳理
一、有机高分子化合物基础知识:
⒈定义:由 组成,M > 的有机物,又叫 或 。
⒉有关概念
⑴结构表示形式
⑵链节、聚合度、单体
⒊合成有机高分子化合物的反应类型:聚合反应
二、合成高分子材料
来源
天然有机高分子:
合成有机高分子:
单聚:一种单体加聚,烯烃、二烯烃、醛(酮)
共聚:2种或2种以上单体加聚,烯烃+烯烃、烯烃+二烯烃……
加聚反应 ⑷聚醚:
⑴酚醛缩聚: 缩聚反应 +n HCHO OH
n 催化剂
Δ
二元醇、酸缩
聚:
羟基酸缩
聚:
⑵聚酯 氨基酸缩聚: 二元酸、胺缩
聚:
⑶聚酰胺
塑料:如聚乙烯、聚丙烯、聚氯工烯等。
三塑料
大塑料:酚醛塑料
合“六大纶”:氯、涤、锦、维、丙、腈
成合成纤维
材特种纤维:芳纶纤维、碳纤维、耐辐射纤维、光导纤维
料通用橡胶:丁苯橡胶,顺丁橡胶,氯丁橡胶
合成橡胶
特种橡胶:硅橡胶、聚硫橡胶
三、功能高分子材料:
⒈功能高分子材料
⒉复合材料
【例1】橡胶属于重要的工业原料。
它是一种有机高分子化合物,具有良好的弹性,但强度较差。
为了增加某些橡胶制品的强度,加工时往往需进行硫化处理。
即将橡胶原料
与硫磺在一定条件下反应;橡胶制品硫化程度越高,强度越大,弹性越差。
下列橡
胶制品中,加工时硫化程度较高的是()
A.橡皮筋
B.汽车外胎
C.普通气球
D.医用乳胶手套
解析:橡皮筋和普通气球的弹性好,所以硫化程度小,汽车外胎与医用乳胶手套相比,前者要承受更大的压力,所以制汽车外胎的橡胶硫化程度最高。
答案:B
【例2】下列物质中,属于高分子化合物的是()
A.淀粉
B.油脂
C.棉花
D.蔗糖
解析:油脂是油和脂肪的总称,它是高级脂肪酸甘油酯,蔗糖是二糖,分子式为C12H22O11,油脂和蔗糖的相对分子质量均较小,两者均不属于高分子化合物;棉花的主要成分
是纤维素,淀粉和纤维素都是天然高分子化合物。
答案:A、C
方法要领:高分子化合物的相对分子质量应大于10000,已学的高聚物有:聚乙烯、聚氯乙烯、酚醛树酯、蛋白质、聚异戊二烯等。
且所有高分子化合物均是混合物
(n为一定范围值)
【例3】合成结构简式为[CH 2-CH=CH-CH 2-CH-CH 2]n 的高聚物,其单体是( )
C 6H 5
①苯乙烯 ②丁烯 ③丁二烯 ④丙炔 ⑤苯丙烯
A.①②
B.④⑤
C.③⑤
D.①③
解析:本题考查学生是否能运用弯箭头法求有机高聚物的单体。
从链节的一端开始,把键
收回,-CH 2-CH-CH 2-CH=CH-CH 2-,得CH=CH 2和CH 2=CH-CH=CH 2。
把单键变双
C 6H 5 C 6H 5
键,双键变单键,遇到碳超过五价,则令其断键即可。
答案:D
方法要领:根据高聚物结构简式推断其单体,可用弯箭头法。
【例4】Nomex 纤维是一种新型阻燃性纤维,它是由间苯二甲酸和间二苯胺在一定条件下
以等物质的量缩聚合成,请把Nomex 纤维结构简式写在下面的方框中。
解析:将形成肽键的知识迁移应用于形成Nomex 纤维即可。
可按以下思路进行: ⑴-COOH 与-NH 2以1:1缩合形成什么结构?(肽键:-CO -NH -)
⑵Nomex 纤维是高分子化合物,还是低分子化合物?
⑶Nomex 纤维的结构简式能否写成二分子缩合结构?
⑷间苯二甲酸两个-COOH 和间苯二胺上的两个-NH 2在缩聚相互结合的可能性是否
均等?
⑸将两个单体结构简式分别沿纸平面旋转600,其结构简式怎样写?
[ ]
⑹Nomex 纤维的结构简式怎样写?
答案:
HOOC COOH H 2N NH 2
NH 2
NH 2
(缩聚物)
COOH COOH (间苯二甲酸) (间苯二胺)
方法要领:这是由-COOH与-NH2通过脱水后形成的高
聚物。
由氨基酸缩聚为蛋白质的原理:氨基(-NH2)与羧基(-COOH)缩去-H和-OH(生成H2O),余下部分相连为缩聚物。
把此原理迁移到本题得解。
注意:(1)官能团在苯环中处于间位上;(2)由于没有弄清题意而写成二分子缩合物。
【例5】某种ABS工程树脂,由丙烯腈(CH2=CHCN,符号A)、1,3-丁二烯(CH2=CH-CH=CH2,符号B)和苯乙烯(C6H5-CH=CH2,符号S)按一定配比共聚而得。
(1)A、B和S三种单体中,碳氢比(C:H)值最小的单体是。
(2)经元素分析可知该ABS样品的组成为C a H b N c(a、b、c为正整数),则原料中A和B的物质的量之比是(用a、b、c表示)。
解析:三种单体分子式分别为A:C3H3N、B:C4H6、S:C8H8,只有丁二烯C4H6的碳氢比小于1。
设A、B、C物质的量分别为x、y、z,则:
a=3x+4y+8z
b=3x+6y+8z 解得:x=c、y=(b-a)/2.
c=x
【一题多解】只有丙烯腈含N,且其为c;A和S中C、H原子数比相等,B中H比C多2个,即ABS中H比C每多2个,含1个丁二烯分子。
故丁二烯为(b-a)/2。
答案:(1)1,3-丁二烯(写B或写结构简式也可)(2)c:(b-a)/2[或2c:(b-a)]
方法要领:善于把结构简式化为分子式,即可快速求出原子个数比。
抓住原子守恒列式
求丁二烯数目。