质量体系风险评估表范例
- 格式:xls
- 大小:115.00 KB
- 文档页数:14



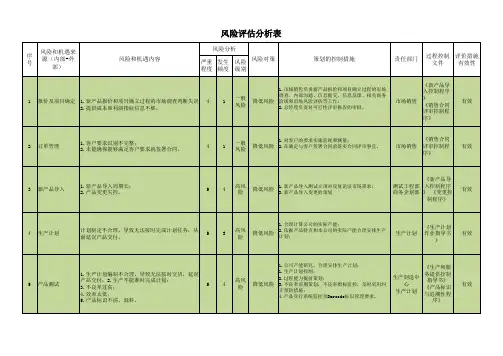


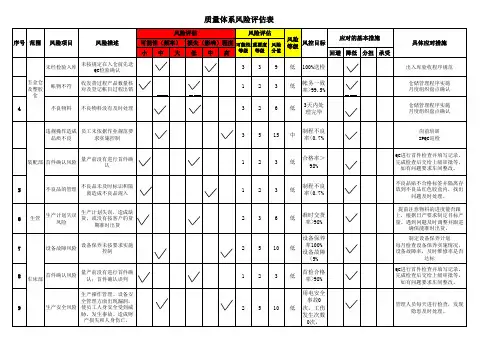
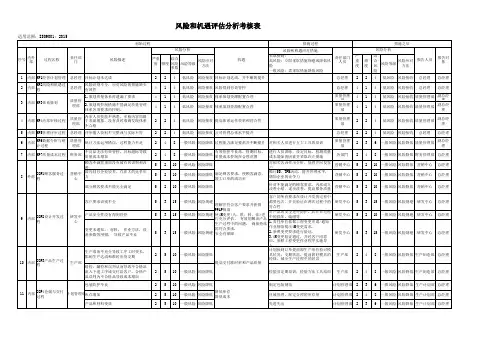


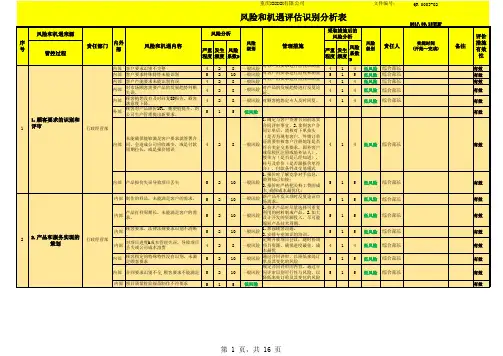
内部输入项目不全。
428一般风险 1.总经理确保每一项输入均得到评审。
2.管理评审计划内容需充分。
414低风险质量部长有效内部输出项目未能有效落实。
428一般风险1.明确责任人、完成日期。
2.评审上年度输出执行情况。
414低风险质量部长有效内部未对对现有操作更改和新设施或新产品进行的制造可行性评估。
313低风险313低风险有效内部管理评审结果未对风险和机遇所采取措施的有效性验证。
313低风险313低风险有效内部管理评审输出未对纠正措施的有效性进行验证。
414低风险414低风险有效内部制订的改善措施不符合要求。
428一般风险 1.积极主动到第一现场发现、分析问题。
2.寻求本部团队意见,内部加强培训。
3.验证改善效果,广泛推广。
4.改善后期跟进,结案。
414低风险质量部长有效内部对潜在的不合格没有识别。
428一般风险充分掌握质量体系过程,以及各个过程之间的关系,结合实际才能发现或识别潜在的不合414低风险质量部长有效内部对不合格没有采取纠正措施。
5210一般风险按《纠正和预防措施控制程序》执行515低风险质量部长有效内部对潜在的不合格没有采取预防措施。
5210一般风险充分掌握质量体系过程,以及各个过程之间的关系,并按《纠正和预防措施控制程序》执515低风险质量部长有效内部对不合格的纠正预防措施没有进行有效性检查评定。
5210一般风险按《纠正和预防措施控制程序》执行515低风险质量部长有效内部对于产品设计或过程设计有影响的纠正预防措施未纳入FMEA,不合格易重复发生。
5210一般风险按《纠正和预防措施控制程序》执行515低风险质量部长有效内部管理者代表对改进活动的策划、实施工作,没有有效评价。
428一般风险按《持续改进控制程序》执行414低风险质量部长有效内部对重大改进项目提供的资源不充分。
428一般风险按《持续改进控制程序》执行414低风险总经理有效内部没有持续改进工作计划。
313低风险313低风险有效内部改进项目没有改进的计划。
验证和确认的范围质量风险评估低可测性 高风险高可测性 低风险风险=严重性×可能性×可检测性 RPN=S ×P ×D××××制药有限公司验证和确认范围质量风险评估1.概念:1.1质量风险:指质量危害出现的可能性和严重性的结合。
2.质量风险管理的程序:启动风险管理过程风险识别风险分析 风险评价风险降低 风险接受事件评审质量风险管理程序的输出/结果风险管理工具风险沟通风险评估风险评审不接受风险控制3、风险矩阵图4风险评估方法4.1 风险识别:可能影响产品质量、产量、工艺操作或数据完整性的风险; 4.2 风险分析:本案例应用失败模式效果分析,识别潜在的失败模式,对风险发生的频率、高中危害发生的可能性(F)危害严重性(S)低中 高 高低 中 高低 低 中低中高严重性和可测量性评分。
4.3 风险判定:包括评估先前确认风险的后果,其基础建立在严重程度、可能性及可检测性上;4.3.1 严重程度(S):测定风险的潜在后果,主要针对可能危害产品质量、患者健康及数据完整性的影响。
严重程度分为四个等级:严重程度(S) 描述关键(4) 直接影响产品质量要素或工艺与质量数据的可靠性、完整性或可跟踪性。
此风险可导致产品不能使用;直接影响GMP原则,危害产品生产活动高(3) 直接影响产品质量要素或工艺与质量数据的可靠性、完整性或可跟踪性。
此风险可导致产品召回或退回;不符合GMP原则,可能引起检查或审计中产生偏差中(2) 尽管不存在对产品或数据的相关影响,但仍间接影响产品质量要素或工艺与质量数据的可靠性、完整性或可跟踪性;此风险可能造成资源的极度浪费或对企业形象产生较坏影响低(1) 尽管此类风险不对产品或数据产生最终影响,但对产品质量要素或工艺与质量数据的可靠性、完整性或可跟踪性仍产生较小影响4.3.2 可能性程度(P):测定风险产生的可能性。
根据积累的经验、工艺/操作复杂性知识或小组提供的其他目标数据,可获得可能性的数值。