实验一、三组分液-液体系相图的绘制
- 格式:ppt
- 大小:809.00 KB
- 文档页数:47

实验2 三组分液—液相图的绘制实验目的1熟悉相律,掌握由三角形坐标法表示的三组分系统相图。
2 用溶解度法作出具有一对共轭溶液的正戊醇—醋酸—水系统的相图。
基本原理三组分系统组分数K=3, 当系统处于恒温恒压条件时,根据相律, 系统的条件自由度为:φ-=*3f式中φ为系统的相数。
系统最大条件自由度为213max =-=*f , 因此,浓度变量最多只有两个, 可用平面图表示系统的状态和组成间的关系, 称三组分相图。
通常用等边三角形坐标表示,如图1所示。
等边三角形顶点分别表示纯物质A 、B 、C, AB 、BC 、CA 三条边分别表示A 和B 、B 和C 、C 和A 所组成的二系统组成, 三角形内任何一点都表示三族分系统的组成。
将三角形的每一边分为100等份, 通过三角形内任何一点O 引平行各边直线, 根据几何原理,a+b+c=AB=BC=CA=100%, 因此O 点组成可用a 、b 、c 来表示。
即O 点表示的三个组成的百分组成为B%=b, C%=c, A%=a 。
如果已知三组分中任两个百分组成,只须作两条平行线,其交点就是被测系统的组成点。
在正戊醇—醋酸—水三组分系统中, 正戊醇和水几乎完全不互溶的,而醋酸和正戊醇及醋酸和水都是互溶的, 在正戊醇和水系统中加入醋酸则可促使正戊醇和水的互溶。
由于醋酸在正戊醇层和水层中非等量分配,因此,代表两层浓度的a 、b 点的连线并不一定与底边平行(如图2) 。
设加入的醋酸后系统总组成为c, 平衡共存的两相叫共轭溶液,其组成由通过c 的连线上的a 、b 两点表示 。
图中曲线以下区为两相共存区,其余部分为单相区。
图1 图2 图3 现有一个正戊醇和水的二组分系统,其组成为k 。
于其中逐渐加入醋酸,则系统总组成沿kB 变化(正戊醇和水比例保持不变),在曲线以下区域内则存在互不混溶的两共轭相,将溶液振荡时则出现混浊状态。
继续滴加醋酸直到曲线上的d 点, 系统将由两相区进入单相区,液体将由混浊转为清澈, 继续加醋酸至e 点,液体仍为清澈的单相。

绘制正己烷-乙醇-水的三组分液系相图孟晓燕;胡小燕【摘要】The n-hexane-alcohol-water ternary liquid phase diagram was obtained through the solubility curves of the ternary determined by cloud-piont-titration method.It showed that at room temperature 10.0 ℃, in then-hexane-al-cohol-water ternary liquid phase diagram, at the isothermal consolute D point, the mass fraction of alcohol and n-hex-ane was 73.0% and 14.1%, respectively.Two conjugate ternary solutions were formed inthe binodal solubility curve BDC, and at the system point O, the mass ratio of the two conjugate solutions was mG: mH=|OH|:|OG|.%采用浊点滴定法测定各组分的溶解度曲线,绘制出了正己烷-乙醇-水的三组分液系相图.结果表明,在室温为10.0℃时,正己烷-乙醇-水的三组分液系相图中,等温会溶点D点处,乙醇、正己烷的质量分数分别为73.0%、14.1%;双结点溶解度曲线BDC内,形成了两个共轭的三组分溶液;物系点 O 时,两共轭溶液数量的比值为mG:mH=|OH|:|OG|.【期刊名称】《上饶师范学院学报》【年(卷),期】2016(036)006【总页数】4页(P74-77)【关键词】浊点滴定法;溶解度曲线;正己烷-乙醇-水;三组分液系相图【作者】孟晓燕;胡小燕【作者单位】上饶师范学院化学化工学院,江西上饶 334001;安远县塘村学校,江西赣州 342113【正文语种】中文【中图分类】O625.61在油脂工业中,溶剂浸提是最常用的有效提取油脂的过程。

Ⅰ、目的要求1.掌握用三角坐标表示三组分相图的方法;2.能正确利用溶解度方法绘制KCl-HCl-H2O三组分系统的相图;3.了解湿固相法的原理,学会确定溶液中纯固相组成点的方法。
Ⅱ、基本原理为了绘制相图就需要通过实验获得平衡时各相间的组成及二相的连接线,即先使体系达到平衡,然后把各相分离,再用化学分析法或物理方法测定达成平衡时各相的组成。
但体系达到平衡的时间,可以相差很大。
对于互溶的液体,一般平衡达到的时间很快;对于溶解度较大,但不生成化合物的水盐体系,也容易达到平衡。
对于一些难溶的盐,则需要相当长的时间,如几个昼夜。
由于结晶过程往往要比溶解过程快得多,所以通常把样品置于较高的温度下,使其较多溶解,然后将其移至温度较低的恒温槽中,使之结晶,加速达到平衡。
另外,摇动、搅拌、加大相界面也能加快各相间的扩散速度,加速达到平衡。
由于在不同温度时的溶解度不同,所以系统所处的温度应该保持不变。
湿固相法的基本原理:在等边三角形相图中凡带有饱和溶液的固相组成点,必定处于饱和溶液组成点和纯固相点的连结线上,测定一组饱和溶液和湿固相(饱和溶液所对应的固相)的组成,它们的连结延长线将交于一点,即纯固相组成点。
本实验是测定在一定温度和压力下,KCl-HCl-H2O三组分体系中各组分的质量百分组成,从而绘制出三组分相图(体系中KCl处于饱和状态,溶解的KCl与KCl固体处于平衡状态)。
由KCl、HCl、H2O组成的三组分体系,在HCl的含量不太高时,HCl完全溶于水而成盐酸溶液,与KCl有共同的负离子Cl-。
所以当饱和的KCl水溶液中加入盐酸时,由于同离子效应使KCl的溶解度降低。
本实验即是研究在不同浓度的盐酸溶液中KCl的溶解度,通过此实验熟悉盐水体系相图的构筑方法和一般性质。
为了分析平衡体系各相的成分,可以采取各相分离方法。
如对于液体可以用分液漏斗来分离。
但是对于固相,分离起来比较困难。
因为固体上总会带有一些母液,很难分离干净,而且有些固相极易风化潮解,不能离开母液而稳定存在。

实验项目一.实验名称三液系(三氯甲烷~醋酸~水)相图绘制二.实验目的(1)熟悉相律和三角形坐标表示三组分相图的方法。
(2)用溶解度法绘制具有一对共轭溶液的三组分相图。
三.实验原理在萃取时,具有一对共轭溶液的三组分相图对确定合理的萃取条件极为重要。
在定温定压下,三组分体系的状态和组分之间的关系通常可用等边三角形坐标表示,如图1所示:图1 图2等边三角形三顶点分别表示三个纯物质A,B,C。
AB,BC,CA,三边表示A和B,B和C,C和A所组成的二组分体系的组成。
三角形内任一点则表示三组分体系的组成。
如点P的组成为: A%=Cb B%=Ac C%=Ba 具有一对共轭溶液的三组分体系的相图如图2所示。
该三液系中,A和B,及A和C完全互溶,而B和C部分互溶。
曲线DEFHIJKL为溶解度曲线。
EI和DJ是连接线。
溶解度曲线外为单相区,曲线外为两相区。
物系点落在两相区内,即分为两相。
图3绘制溶解度曲线的方法有许多种,本实验采用的方法是:将将完全互溶的两组分(如氯仿和醋酸)按照一定的比例配制成均相溶液(图中N 点),再向清亮溶液中滴加另一组分(如水),则系统点沿BN线移动,到K点时系统由清变浑。
再往体系里加入醋酸,系统点则沿AK上升至N’点而变清亮。
再加入水,系统点又沿BN’由N’点移至J点而再次变浑,再滴加醋酸使之变清……如此往复,最后连接K、J、I……即可得到互溶度曲线,如图3所示。
四.仪器与药品滴定管(50ml,酸式)1支;移液管(2ml,胖度)4支;滴定管(50ml,碱式)1支;(5ml,刻度)2支;有塞锥形瓶(100ml)2只;(10ml ,刻度)1支;有塞锥形瓶(25ml)4只;分液漏斗(60ml)2只。
氯仿(AR),冰醋酸(AR),0.5mol/L标准NaOH溶液。
五.实验步骤(1)在洁净的酸式滴定管内装水,移取6ml氯仿及1ml醋酸于干燥洁净的100ml磨口锥形瓶中,然后慢慢滴入水,且不停地振摇,至溶液由。
![[新版]三相图的绘制(氯化钾、盐酸、水)](https://uimg.taocdn.com/a702e66e30b765ce0508763231126edb6f1a767b.webp)
基础化学实验实验 三相图的绘制——O H HCl KCl 2--体系Ⅰ、目的要求1.掌握用三角坐标表示三组分相图的方法;2.能正确利用溶解度方法绘制KCl-HCl-H2O三组分系统的相图;3.了解湿固相法的原理,学会确定溶液中纯固相组成点的方法。
Ⅱ、基本原理为了绘制相图就需要通过实验获得平衡时各相间的组成及二相的连接线,即先使体系达到平衡,然后把各相分离,再用化学分析法或物理方法测定达成平衡时各相的组成。
但体系达到平衡的时间,可以相差很大。
对于互溶的液体,一般平衡达到的时间很快;对于溶解度较大,但不生成化合物的水盐体系,也容易达到平衡。
对于一些难溶的盐,则需要相当长的时间,如几个昼夜。
由于结晶过程往往要比溶解过程快得多,所以通常把样品置于较高的温度下,使其较多溶解,然后将其移至温度较低的恒温槽中,使之结晶,加速达到平衡。
另外,摇动、搅拌、加大相界面也能加快各相间的扩散速度,加速达到平衡。
由于在不同温度时的溶解度不同,所以系统所处的温度应该保持不变。
湿固相法的基本原理:在等边三角形相图中凡带有饱和溶液的固相组成点,必定处于饱和溶液组成点和纯固相点的连结线上,测定一组饱和溶液和湿固相(饱和溶液所对应的固相)的组成,它们的连结延长线将交于一点,即纯固相组成点。
本实验是测定在一定温度和压力下,KCl-HCl-H2O三组分体系中各组分的质量百分组成,从而绘制出三组分相图(体系中KCl处于饱和状态,溶解的KCl与KCl固体处于平衡状态)。
由KCl、HCl、H2O组成的三组分体系,在HCl的含量不太高时,HCl完全溶于水而成盐酸溶液,与KCl有共同的负离子Cl-。
所以当饱和的KCl水溶液中加入盐酸时,由于同离子效应使KCl的溶解度降低。
本实验即是研究在不同浓度的盐酸溶液中KCl的溶解度,通过此实验熟悉盐水体系相图的构筑方法和一般性质。
为了分析平衡体系各相的成分,可以采取各相分离方法。
如对于液体可以用分液漏斗来分离。

三液系(三氯甲烷~醋酸~水)相图的绘制薛念华一.实验目的:1.熟悉相律和用三角形坐标表示三组分相图的方法。
2.用溶解度法绘制具有一对共轭溶液的三组分相图。
二.实验原理:在定温定压下,三组分体系的状态和组成之间的关系通常可用等边三角形坐标,如下图所示。
等边三角形三顶点分别表示三个纯物A、B、C。
AB、BC、CA三边分别表示A和B、B和C、C和A所组成的二组分体系的组成。
三角形内任一点则表示三组分体系的组成。
如O点的组成为A%=Cc’,B%=Aa’,C%=Bb’。
具有一对共轭溶液的三组分体系相图,在该三液系中,A和B、A和C完全互溶,而B和C只能有限度的互溶,B和C的浓度在Ba和Cd之间可以完全互溶,介于ad 之间体系分为两层,一层是B在C中的饱和溶液(d点),另一层是C在B中的饱和溶液(a点),这对溶液称为共轭溶液。
曲线abd为溶解度曲线。
曲线外是单相区,曲线内是二相区。
物系点落在两相区内即分成二相,如O点分成组成为E和F的二相,EF 线称为连结线。
绘制溶解度曲线的方法较多。
本实验是先在完全互溶的两个组分(如A和C)以一定的比例混合所成的均相溶液(如图II上的N点)中滴加入组分B,物系点则沿NB 线移动,直至溶液变浑,即为L点,然后加入A,物系点沿LA上升至N’点而变清。
如再滴加B,则物系点又沿N’B移动,当移至L’点时溶液再次变浑。
再滴加A使之变清……。
如此重复,最后连接L,L’,L’’……,即可绘出溶解度曲线。
三.仪器与药品:滴定管(50mL,酸式)×1,滴定管(50mL,碱式)×1,有塞锥形瓶(100mL)×2,有塞锥形瓶(25mL)×4,锥形瓶(100mL)×2,移液管(2mL,胖肚)×4,移液管(5mL,刻度)×2,移液管(10mL,刻度)×1,分液漏斗(60mL)×2,漏斗架×1,氯仿(分析纯),冰醋酸(分析纯),0.5mol/L标准NaOH溶液。
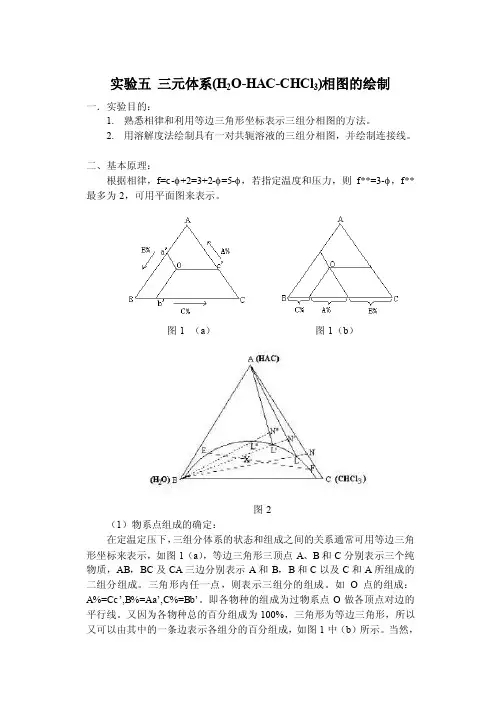
实验五三元体系(H2O-HAC-CHCl3)相图的绘制一.实验目的:1.熟悉相律和利用等边三角形坐标表示三组分相图的方法。
2.用溶解度法绘制具有一对共轭溶液的三组分相图,并绘制连接线。
二、基本原理:根据相律,f=c-φ+2=3+2-φ=5-φ,若指定温度和压力,则f**=3-φ,f**最多为2,可用平面图来表示。
图1 (a)图1(b)图2(1)物系点组成的确定:在定温定压下,三组分体系的状态和组成之间的关系通常可用等边三角形坐标来表示,如图1(a),等边三角形三顶点A、B和C分别表示三个纯物质,AB,BC及CA三边分别表示A和B,B和C以及C和A所组成的二组分组成。
三角形内任一点,则表示三组分的组成。
如O点的组成:A%=Cc’,B%=Aa’,C%=Bb’。
即各物种的组成为过物系点O做各顶点对边的平行线。
又因为各物种总的百分组成为100%,三角形为等边三角形,所以又可以由其中的一条边表示各组分的百分组成,如图1中(b)所示。
当然,给出一定组成的溶液百分比,按照上述表示方法,也应该能找出对应的物系点。
(2)溶解度曲线的绘制对于具有一对共轭溶液的三液系相图,如图2,该三液系相图中A和B,A和C为完全互溶而B和C为部分互溶,曲线abc为溶解度曲线。
曲线上方为单相区,曲线下方为二相区,物系点落在二相区内,即分为二相,如X 点则分成组成为E和F的二相,而EF线称为连接线。
对于溶解度曲线的绘制,本实验是先以完全互溶的两个组分(如A和C),以一定的比例混合所组成的均相溶液,如图2上的N点,滴加入组分B,根据平衡相图的直线规则,物系点则沿着NB移动,直至溶液变混,即为L点。
再加入A,物系点由LA上升至N’点而变清。
再加入B,此时物系点又沿着N’B由N’移动至L’而再次变混,再滴加A使变清……,如此反复,最后连接L,L’,L’’……即可画出溶解度曲线。
(3)连接线的绘制由于连接线是表示在两相区内呈平衡两相的组成(或A在两相中的分配),所以可以在两相区内配制溶液,待平衡后分析每相中的任何一种组成的含量,连接在溶解度曲线上该两含量的组成点而得出。

实验三氯甲烷—醋酸—水三液系相图的绘制一.实验目的1.掌握用三角坐标表示三组分相图的方法;2.用溶解度法绘制具有一对共轭溶液的三组分相图。
二.实验原理为了绘制相图就需要通过实验获得平衡时各相间的组成及二相的连接线,即先使体系达到平衡,然后把各相分离,再用化学分析法或者物理方法确定达成平衡时各相的组成。
但体系达到平衡的时间,可以相差很大。
对于互溶的液体,一般平衡达到的时间很快;对于溶解度较大但不生成化合物的水盐体系,也容易达到平衡。
对于一些难溶的盐,则需要相当长的时间,如几个昼夜。
由于结晶过程往往要比溶解过程快得多,所以通常把样品置于较高的温度下,使其溶解较多,然后将其移至温度较低的恒温槽中,使之结晶,加速达到平衡,另外,摇动、搅拌、加大相界面也能加快各相间的扩散速度,加速达到平衡。
水和氯仿的相互溶解度很小,而醋酸却与水、氯仿互溶。
在水和氯仿组成的两相混合物中加入醋酸,能增大水和氯仿间的互溶度,醋酸增多,互溶度越大,当加入醋酸到某一数量时,水和氯仿能完全互溶,原来由两相组成的混合体系由混变清。
在温度恒定的情况下,使两相体系变成均匀的混合物所需要的醋酸量,取决于原来混合物中水和氯仿的比例。
同样,把水加到醋酸和氯仿的均相混合物中时,当水达到一定数量,原来的均相体系变成水相和氯仿相的两相混合体系,体系由清变混。
使体系变成两相所需要的水量,取决于醋酸和氯仿的起始成分。
因此利用体系在相变化时的浑浊和清亮现象的出现。
可以判断体系中各组分间互溶度的大小。
一般由清到浊,肉眼比较容易分辨。
所以实验由均相样品中加入第三物质使变成二相的方法,测定两相间的相互溶解度。
当二相共存并达到平衡时,将二相分离,测得二相的成分,然后用直线连接这二点,即得连接线。
用等边三角形的方法表示三元相图。
等边三角形的三个定点各代表纯组分,三角形三条边AB、BC和CA分别代表A和B,B和C,C和A所组成的二组分的组成,而三角形内任意一点表示三组分的组成。

实验5 三液系相图的绘制注意事项:1.实验所用玻璃仪器的洁净度会影响相点变化,实验结束时一定要认真清洗玻璃仪器并放入指定烘箱烘干。
2.滴定时必须充分振荡3.加入液体体积大于1mL时用滴定管直接加入,准确记录每次加入液体体积4.当溶液总体积超过30mL时,转移到150mL干净锥形瓶中滴定,以便界面观察实验步骤:1.液体密度的测定取50mL干燥锥形瓶,称重,用刻度移液管移取2.00mL环己烷后再称重,计算环己烷密度,样品留待第2步用。
2.溶解度曲线的测定(1)用1.00mL刻度移液管移取0.10mL水加入步骤1中的锥形瓶中,摇匀变浑浊,然后用滴定管滴加1滴乙醇,摇匀则变浊,边滴边摇,继续滴至溶液恰好由浊变清时,记下所加乙醇的体积(毫升),得到第1组溶解度数据。
(2)用刻度移液管移取1.00mL乙醇加入上述溶液中,摇匀,用水返滴至溶液刚由清变浊,记下所用水的体积,得到第2组溶解度数据。
(3)按照数据记录表格中所规定数字继续加入水,然后再用乙醇滴定,如此反复进行实验,共测得10组溶解度数据。
3.连接线的测定(1)用5.00mL刻度移液管依次移取3.00mL环己烷、3.00mL水以及3.00mL乙醇于干燥的25mL具塞锥形瓶中,充分摇动后静置分层。
(2)取100mL锥形瓶,配制质量分数为50%的环己烷-乙醇溶液50mL。
(3)取干燥洁净的50mL具塞锥形瓶称重。
另取一支干燥洁净的1.00mL移液管用吸耳球轻轻吹气并同时插入(1)溶液的下层(即水层)取1.00mL溶液(这样可以防止上层液体进入移液管中),放入已称重的50mL具塞锥形瓶中,再称其重量,得出水层质量m G。
(4)用滴定管滴加质量分数为50%的环己烷-乙醇混合物于上述水层溶液中,边滴边摇动,至溶液由浊变清,再称其质量,得出加入的环己烷-乙醇的质量m E。
4.数据处理(1)根据表格1查得实验温度下水、乙醇的密度,将试验获得的10组溶解度数据中的体积换算成质量,求出个组分的质量分数(单位:%),填入数据记录表中。

实验八三组分体系等温相图的绘制【目的要求】1. 熟悉相律,掌握用三角形坐标表示三组分体系相图。
2. 掌握用溶解度法绘制相图的基本原理。
【实验原理】对于三组分体系,当处于恒温恒压条件时,根据相律,其自由度f*为:f*=3-Φ式中,Φ为体系的相数。
体系最大条件自由度f*max=3-1=2,因此,浓度变量最多只有两个,可用平面图表示体系状态和组成间的关系,通常是用等边三角形坐标表示,称之为三元相图。
如图2-8-1所示。
等边三角形的三个顶点分别表示纯物A、B、C,三条边AB、BC、CA分别表示A和B、B和C、C和A所组成的二组分体系的组成,三角形内任何一点都表示三组分体系的组成。
图2-8-1中,P点的组成表示如下:经P点作平行于三角形三边的直线,并交三边于a、b、c三点。
若将三边均分成100等份,则P点的A、B、C组成分别为:A%=Pa=Cb,B%=Pb=Ac,C%=Pc=Ba。
苯-醋酸-水是属于具有一对共轭溶液的三液体体系,即三组分中二对液体A和B,A和C 完全互溶,而另一对液体B和C只能有限度的混溶,其相图如图2-8-2所示。
图2-8-1 等边三角形法表示三元相图图2-8-2 共轭溶液的三元相图图2-8-2中,E、K2、K1、P、L1、L2、F点构成溶解度曲线,K1L1和K2L2是连结线。
溶解度曲线内是两相区,即一层是苯在水中的饱和溶液,另一层是水在苯中的饱和溶液。
曲线外是单相区。
因此,利用体系在相变化时出现的清浊现象,可以判断体系中各组分间互溶度的大小。
一般来说,溶液由清变浑时,肉眼较易分辨。
所以本实验是用向均相的苯-醋酸体系中滴加水使之变成二相混合物的方法,确定二相间的相互溶解度。
【仪器试剂】具塞锥形瓶(100mL,2只、25mL,4只);酸式滴定管(20mL,1支);碱式滴定管(50mL,1支);移液管(1mL,1支、2mL,1支);刻度移液管(10mL,1支、20mL,1支);锥形瓶(150mL,2第二篇基础实验2只)。

三组分液-液体系的平衡相图1、什么是平衡相图?答:研究多相系统的状态如何随温度、压力和浓度等条件的改变而发生改变,并用图形表示系统状态的变化,这种图形即平衡相图,简称相图。
2、试用相律分析一下恒温恒压条件时,三组分液-液体系单相区的条件自由度是几?两相区的条件自由度是几?答:恒温恒压条件时相律表达式为:f﹡=C-Φ,三组分体系C=3,即f*=3-Φ,当Φ=1时,f*=2;当Φ=2时,f*=1。
3、等边三角形坐标的顶点、线上的点、面上的点分别代表几组分的组成?答:三个顶点分别代表三个纯组分A、B和C,AB线代表(A+B)的两组分体系,AC线代表(A+C)的两组分体系,BC线代表(B+C)的两组分体系,面上的点(三角形内各点)是三组分体系。
4、如何确定等边三角形坐标面上的点的组成?答:通过三角形内任何一点O引平行线于各边的直线,根据几何原理,a+b+c=AB=BC=CA=100%,或者a'+b'+c'=AB=BC=CA=100%。
因此,O点的组成可由a'、b'、c'来表示,即O点所代表的三个组分的百分组成是:B%= b',C%= c',A%= a'。
5、通过任一顶点B向其对边引直线BD,则BD线上的各点所表示的组成中,A、C两个组分含量的比值如何?答:A、C两个组分的含量的比值保持不变。
6、如果有两个三组分体系D和E,将其混合之后其组成点会落在哪?答:其成分必定位于D、E两点之间的连线上。
7、对于等边三角形坐标内的任意一组成O,向其加纯B,体系的组成点会落在哪?若蒸发掉B,体系的组成点又会落在哪?答:向其中加入纯B时体系总组成点将沿直线OB向B移动,即落在OB直线上。
蒸发掉B时体系总组成点将沿直线OB的反方向移动,即落在OB的反向延长线上。
8、已知一三组分体系P的百分组成为:B%=20,C%=30,A%=50,如何在等边三角形坐标上绘制出P点?答:在B%=20处做一条顶点B对边的平行线,该线上所有点B的百分组成均为B%=20,再在C%=30在处做一条顶点C对边的平行线,该线上所有点C的百分组成均为C%=30,这两条平行线的交点即为P。
实验2三组分液—液相图的绘制实验2 三组分液—液相图的绘制实验⽬的1熟悉相律,掌握由三⾓形坐标法表⽰的三组分系统相图。
2 ⽤溶解度法作出具有⼀对共轭溶液的正戊醇—醋酸—⽔系统的相图。
基本原理三组分系统组分数K=3, 当系统处于恒温恒压条件时,根据相律, 系统的条件⾃由度为:φ-=*3f式中φ为系统的相数。
系统最⼤条件⾃由度为213max =-=*f , 因此,浓度变量最多只有两个, 可⽤平⾯图表⽰系统的状态和组成间的关系, 称三组分相图。
通常⽤等边三⾓形坐标表⽰,如图1所⽰。
等边三⾓形顶点分别表⽰纯物质A 、B 、C, AB 、BC 、CA 三条边分别表⽰A 和B 、B 和C 、C 和A 所组成的⼆系统组成, 三⾓形内任何⼀点都表⽰三族分系统的组成。
将三⾓形的每⼀边分为100等份, 通过三⾓形内任何⼀点O 引平⾏各边直线, 根据⼏何原理,a+b+c=AB=BC=CA=100%, 因此O 点组成可⽤a 、b 、c 来表⽰。
即O 点表⽰的三个组成的百分组成为B%=b, C%=c, A%=a 。
如果已知三组分中任两个百分组成,只须作两条平⾏线,其交点就是被测系统的组成点。
在正戊醇—醋酸—⽔三组分系统中, 正戊醇和⽔⼏乎完全不互溶的,⽽醋酸和正戊醇及醋酸和⽔都是互溶的, 在正戊醇和⽔系统中加⼊醋酸则可促使正戊醇和⽔的互溶。
由于醋酸在正戊醇层和⽔层中⾮等量分配,因此,代表两层浓度的a 、b 点的连线并不⼀定与底边平⾏(如图2) 。
设加⼊的醋酸后系统总组成为c, 平衡共存的两相叫共轭溶液,其组成由通过c 的连线上的a 、b 两点表⽰。
图中曲线以下区为两相共存区,其余部分为单相区。
图1 图2 图3 现有⼀个正戊醇和⽔的⼆组分系统,其组成为k 。
于其中逐渐加⼊醋酸,则系统总组成沿kB 变化(正戊醇和⽔⽐例保持不变),在曲线以下区域内则存在互不混溶的两共轭相,将溶液振荡时则出现混浊状态。
继续滴加醋酸直到曲线上的d 点, 系统将由两相区进⼊单相区,液体将由混浊转为清澈, 继续加醋酸⾄e 点,液体仍为清澈的单相。
实验三氯甲烷—醋酸—水三液系相图的绘制一.实验目的1.掌握用三角坐标表示三组分相图的方法;2.用溶解度法绘制具有一对共轭溶液的三组分相图。
三氯甲烷—醋酸—水是部分互溶三液系相图,水和氯仿的相互溶解度很小,而醋酸却与水、氯仿互溶。
将将完全互溶的两组分(如氯仿和醋酸)按照一定的比例配制成均相溶液(图中N点),再向清亮溶液中滴加另一组分(如水),则系统点沿BN线移动,到K点时系统由清变浑。
再往体系里加入醋酸,系统点则沿AK上升至N’点而变清亮。
再加入水,系统点又沿BN’由N’点移至J点而再次变浑,再滴加醋酸使之变清……如此往复,最后连接K、J、I……即可得到互溶度曲线。
三.仪器与药品四.实验步骤1.移取6ml氯仿、1ml醋酸于干燥洁净的100ml磨口锥形瓶中(标记1号),混合均匀。
然后慢慢滴入水,边滴边摇动,直至溶液由清亮变浑,即为终点,记录水的体积。
再向体系中加入2ml醋酸,系统又成均相,继续用水滴定,使体系再次由清变浑,分别记录此时系统中氯仿、醋酸及水的总毫升数。
然后依次加入3.5ml、6.5ml醋酸,同上方法用水滴定,并记录体系中各组分的含量。
最后加入40ml的水,盖紧瓶塞,每隔5min振摇一次,约30min 后将此溶液作测量连接线使用。
2.取另一100ml磨口锥形瓶(标记2号),移入1ml氯仿和3ml醋酸,用水滴定至终点。
然后再依次添加2ml、5ml、6ml醋酸,分别用水滴定至终点。
记录各次各组分的用量。
最后加入9ml氯仿和5ml醋酸,混合均匀,每隔5min振摇一次,约30min后作为测量另一根连接线使用。
五.数据记录与处理1.记录(表1、表2)2.溶解度曲线的绘制根据表一数据,在三角坐标纸上,绘制各次滴定的组成点,然后用曲线板拟合成一条光滑曲线,即为水-氯仿在醋酸存在情况下的互溶度曲线。
其中在BC边上的相点为实验温度、压力条件下,水在氯仿或氯仿在水中的溶解度。
1。