生物制品生产用原材料及辅料的质量控制规程推荐WORD范文
- 格式:docx
- 大小:99.35 KB
- 文档页数:4

生物制品管理制度范本第一章总则第一条为了加强生物制品的管理,保障人民健康和安全,维护生态环境的平衡和稳定,制定本管理制度。
第二条本管理制度适用于生物制品的生产、销售、使用、储存和运输等相关环节。
第三条生物制品管理的目标是确保生物制品的质量安全,防止生物制品的污染和滥用,保护消费者的合法权益。
第四条生物制品管理的原则是科学、公正、便捷、高效。
第五条生物制品管理的主体是生物制品生产企业、销售企业、使用单位、储存单位和运输单位等相关主体。
第六条政府部门负责对生物制品的管理和监督,依法行使监督权和处罚权。
第七条生物制品的安全监督是全社会共同参与的,舆论监督是重要的监督方式之一。
第二章生物制品生产管理第八条生物制品生产企业必须具备相应的生产资质和技术能力,按照法律法规要求进行生产。
第九条生物制品生产企业应当建立完善的质量管理体系,确保生产过程的可追溯性和生产环节的清晰明确。
第十条生物制品生产过程中应严格控制原材料的来源和质量,采取有效的控制措施,防止污染和交叉感染的风险。
第十一条生物制品生产企业应当对生产过程中的环境进行监测和控制,确保生产环境的洁净和卫生。
第十二条生物制品生产企业应定期进行设备设施的检查和维护,确保设备设施的正常运转和安全可靠。
第十三条生物制品生产企业应当确保员工的健康和安全,为员工提供必要的培训和防护措施。
第十四条生物制品生产企业应当建立完善的产品追溯制度,确保产品的质量安全和溯源可信。
第十五条生物制品生产企业应当主动接受政府监督和检查,及时报告生产过程中的重大事件和事故。
第十六条生物制品生产企业应当建立健全的质量投诉和处理机制,及时处理消费者的投诉和举报。
第三章生物制品销售管理第十七条生物制品销售企业必须具备相应的销售许可证和操作资质,按照法律法规要求进行销售。
第十八条生物制品销售企业应当建立完善的销售管理体系,确保销售过程的规范和透明。
第十九条生物制品销售企业应当对销售产品进行严格的质量检测和抽检,确保产品的质量安全。

生物制品生产用原材料及辅料的质量控制规程12生物制品是采用生物技术制备而成的具有活性的药品。
生物制品的生产工3艺复杂且易受多种因素影响,生产过程中使用的各种材料来源复杂,可能引入4外源因子或毒性化学材料;产品组成成分复杂且一般不能进行终端灭菌,产品5的质量控制仅靠成品检定难以保证其安全性和有效性。
因此,对生物制品生产6用原材料和辅料进行严格的质量控制,是降低制品中外源因子或有毒杂质污染7风险,保证生物制品安全有效的必要措施。
8本规程是对生物制品生产企业在生物制品生产过程中使用的原材料和辅料9质量控制的通用性要求。
10一、、生物制品生产用原材料11生物制品生产用原材料系指生物制品生产过程中使用的所有生物材料和化学12材料。
本规程所述原材料不包括用于生物制品生产的起始原材料(如细胞基质、13菌毒种、生产用人血浆和动物免疫血清等)。
141.分类15按照来源可将生物制品生产用原材料分为两大类,一类为生物原材料,主要16包括来源于微生物,人和动物细胞、组织、体液成分,以及采用重组技术或生17物合成技术生产的生物原材料等;另一类为化学原材料,包括无机和有机化学18材料。
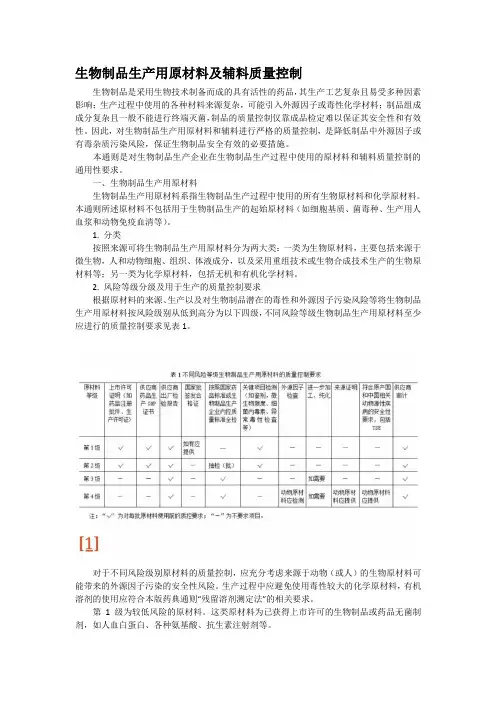
192.风险等级分级及用于生产的质量控制要求20根据原材料的来源、生产以及对生物制品潜在的毒性和外源因子污染风险等21将生物制品生产用原材料按风险级别从低到高分为以下四级,各级生物制品原22材料至少应进行的质量控制要求见附表1。
23对于不同风险级别原材料的质量控制,应充分考虑来源于动物(或人)的生24物原材料可能带来的外源因子污染的安全性风险。
生产过程中应避免使用毒性25较大的化学原材料,有机溶剂的使用应符合本版药典附录“残留溶剂检测”的26相关要求。
27第1级为较低风险的原材料。
为已获得上市许可的生物制品或药品无菌制剂。
28如人血白蛋白、各种氨基酸、抗生素注射剂等。
29第2级为低风险原材料,这类原材料为已有国家药品标准、取得国家药品批30准文号并按照我国现行药品GMP生产的用于生物制品培养基成分以及提取、纯31化、灭活等过程的化学原料药和药用级非动物来源的蛋白水解酶等。

生物制品管理制度范文1目的为加强生物制品的经营管理工作,有效的控制生物制品的购、存、销行为,确保依法经营,根据<中华人民共和国药品管理法>、<生物制品批签发管理办法>、<生物制品规程>及<____开展生物制品批签发工作相关事宜____通告>等法律、法规,制定本制度。
2适用范围适用于生物制品的采购、验收、储存养护、销售、销毁等管理工作。
3职责按此规定严格管理生物制品,保证经营安全。
4定义生物制品是应用普通的或以基因工程、细胞工程、蛋白质工程、发酵等生物技术获得的微生物、细胞及各种动物和人源的组织或液体等生物材料制备用于人类疾病预防\治疗和诊断的药品。
目前已经纳入生物制品批签发管理的药品有:人血白蛋白及疫苗类生物制品。
5内容5、1生物制品的经营5、1、1经营生物制品,必须经药品监督管理部门审核批准具有合法经营资格方可经营,否则不得从事生物制品的购销经营活动。
5、2生物制品的购进5、2、1购进生物制品,必须严格按照国家食品药品监督管理部门批准内容进行,从具有生产、经营资格的生产企业或经营企业购进。
5、2、____所购进的生物制品运输设备\记录必须符合生物制品储存运输的相关规定。
5、2、3质量管理部对供货企业的合法资格和质量保证能力进行审核,并索取加盖供货单位原印章的合法证照复印件\<药品注册证>及生物制品批签发文件复印件,进口生物制品除按照<进口药品管理制度>索取相关证照外还应提供加盖供货方原印章的原生产国或者地区药品管理机构(或者授权批签发机构)出具的批签发证明复印件5、3生物制品的验收5、3、1验收生物制品应根据供货单位原印章的同批次<生物制品批签发>复印件及检验报告进行验收,并做好验收记录,验收进口生物制品还需索取<进口药品注册证>\进口生物制品检验报告或通关单。
5、3、2生物制品应在来货运输储藏条件符合规定的前提下,在____个小时内验收完毕,并交保管员及时入库。

生物制品质量控制一、引言生物制品是指以生物材料为基础制备的药物、疫苗和诊断试剂等产品。
由于其特殊的性质,生物制品的质量控制至关重要,涉及到安全性、有效性和稳定性等方面。
本文将详细介绍生物制品质量控制的标准格式文本。
二、质量控制流程1. 原材料采购与质量评估生物制品的原材料包括生物材料、培养基、添加剂等。
在采购过程中,应确保原材料的质量符合要求。
质量评估包括检查原材料的供应商资质、原材料的物理化学性质、微生物质量等。
2. 生产工艺控制生产工艺控制是确保生物制品质量的关键环节。
包括以下方面:(1) 培养基制备:培养基的配制应符合标准操作程序,确保培养基成分准确、无菌。
(2) 发酵过程:发酵过程中,应严格控制温度、pH值、氧气供应等参数,确保菌体的生长和产物的积累。
(3) 提取和纯化:提取和纯化过程中,应采用适当的技术手段,如超滤、离心、层析等,确保产物的纯度和活性。
(4) 灭活和杀菌:对于疫苗等生物制品,灭活和杀菌是必要的步骤,应采用适当的方法,如热灭活、紫外线灭菌等。
3. 质量检测方法生物制品的质量检测方法包括物理化学检测、生物学检测和微生物检测等。
具体方法应根据产品的特性和要求选择,确保检测结果准确可靠。
(1) 物理化学检测:包括溶解度、pH值、浓度、纯度等指标的检测。
(2) 生物学检测:包括细胞毒性、细胞增殖、细胞凋亡等指标的检测。
(3) 微生物检测:包括细菌、真菌、病毒等的检测。
4. 质量控制记录质量控制记录是对质量控制过程的记录和归档,包括原材料采购记录、生产工艺记录、质量检测记录等。
记录应详细、准确,并按要求保存一定的时间。
5. 不合格品处理对于发现的不合格品,应及时进行处理。
处理方式包括返工、销毁等,应根据具体情况进行决策,并进行记录。
6. 风险评估与改进措施在生物制品质量控制过程中,应进行风险评估,识别潜在的风险因素,并采取相应的改进措施。
改进措施可以包括更新工艺流程、优化操作规程、加强培训等。

生物制品质量控制引言概述:生物制品质量控制是保证生物制品安全和有效性的关键步骤。
在生物制品的研发、生产和使用过程中,严格的质量控制措施是必不可少的。
本文将从四个方面详细阐述生物制品质量控制的重要性和具体措施。
一、原材料的质量控制1.1 选择合适的原材料:生物制品的质量受原材料的影响,因此选择合适的原材料是质量控制的第一步。
原材料应符合相关质量标准,如纯度、稳定性等。
1.2 原材料的采购管理:建立严格的原材料采购管理制度,确保供应商的可靠性和原材料的可追溯性。
采购过程中要进行严格的质量检查和评估,确保原材料的质量符合要求。
1.3 原材料的储存和处理:合理储存原材料,避免受到污染和变质。
对于需要处理的原材料,应采取适当的方法和工艺,确保其质量不受损。
二、生产过程的质量控制2.1 生产环境的控制:确保生产环境符合卫生标准,避免交叉污染和微生物污染。
定期对生产设备进行维护和清洁,保证其正常运行。
2.2 生产工艺的控制:建立规范的生产工艺流程,并进行严格的操作控制。
对每一个关键步骤进行监测和记录,确保生产过程的一致性和可追溯性。
2.3 产品质量的监测:对生产过程中的关键参数进行监测和分析,确保产品的质量符合标准。
建立有效的检测方法和质量评估体系,及时发现和纠正质量问题。
三、质量控制的文件管理3.1 建立质量管理体系:制定和完善相关的质量管理制度和标准,确保质量控制的系统性和规范性。
建立质量控制文件,包括质量手册、操作规程等,明确质量控制的要求和流程。
3.2 文件的审查和更新:对质量控制文件进行定期审查和更新,确保其与实际操作的一致性。
及时修订和发布新的质量控制文件,以适应新的技术和法规要求。
3.3 培训和培养人员:对从事质量控制工作的人员进行培训和培养,提高其质量意识和专业水平。
确保人员理解和遵守质量控制的要求,减少人为因素对质量的影响。
四、产品的质量评估和监测4.1 产品的质量评估:建立完善的质量评估体系,包括物理性质、化学性质、生物活性等方面的评估。

生物制品质量控制一、引言生物制品是指通过生物技术手段生产的药物、疫苗、血液制品等,对人类健康具有重要意义。
为了确保生物制品的安全性、有效性和一致性,需要进行严格的质量控制。
本文将详细介绍生物制品质量控制的标准格式。
二、质量控制目标1. 安全性:生物制品应符合国家相关法规和标准的要求,不得含有有害物质或微生物污染。
2. 有效性:生物制品应具有预期的治疗效果或预防效果,确保其疗效和预防效果稳定可靠。
3. 一致性:生物制品的质量应具有稳定性和一致性,不受生产批次、生产工艺和储存条件的影响。
三、质量控制内容1. 原材料控制生物制品的原材料包括细胞、培养基、培养辅助物质等。
原材料的选择应符合国家相关标准和要求,确保其质量稳定可靠。
同时,应建立原材料的供应商管理制度,对供应商进行评估和审核,确保原材料来源可靠。
2. 生产工艺控制生物制品的生产工艺应符合国家相关标准和要求。
在生产过程中,应建立严格的工艺控制点,监测和记录关键参数,确保生产过程的稳定性和一致性。
同时,应建立工艺验证制度,对新工艺进行验证,确保其可行性和稳定性。
3. 质量控制检测生物制品的质量控制检测应包括物理性状、化学性质、生物学活性、微生物限度等方面的检测。
检测方法应符合国家相关标准和要求,确保检测结果准确可靠。
同时,应建立质量控制检测记录,对检测结果进行分析和评估。
4. 稳定性研究生物制品的稳定性研究是为了评估其在储存和运输过程中的质量变化情况。
稳定性研究应包括不同储存条件下的样品稳定性测试和样品质量变化趋势分析。
稳定性研究结果应作为产品质量的参考依据,制定合理的储存和运输条件。
5. 不良事件管理生物制品在使用过程中可能出现不良事件,如药物反应、感染等。
应建立不良事件管理制度,对不良事件进行收集、分析和报告,及时采取措施进行处理和改进。
四、质量控制文件1. 质量手册:包括质量控制目标、组织架构、质量控制流程等内容。
2. 质量标准操作规程:详细描述生物制品质量控制的各个环节和操作步骤。

附件5生物制品生产工艺和质量标准通用格式和撰写指南(征求意见稿)一、治疗和预防用生物制品制造及检定规程模板二、按生物制品管理的体外诊断试剂制造及检定规程模板三、生物制品药品注册标准模板四、文本格式要求五、撰写说明和注意事项一、治疗和预防用生物制品制造及检定规程模板核准日期:XXXX年XX月XX日修订日期:XXXX年XX月XX日药品通用名称+制造及检定规程通用名汉语拼音通用名英文名称品种基本信息简介,包括:专有名称、起始材料(适用时,如血浆、生物组织、变应原等,修饰物如PEG、化学或生物毒性成分(偶联)、放射性核素)、表达体系(菌/毒种、生产用培养基/细胞基质)、主要工艺步骤、佐剂名称(若有)。
预防用生物制品格式举例:本品为×××,系用×××病毒/细菌接种××× 细胞/培养基,经培养、收获、浓缩、纯化、灭活后,加入×××佐剂制成。
含×××等辅料。
不含防腐剂和抗生素。
治疗用生物制品格式举例:本品为×××,系用×××种子(如重组工程菌、病毒、工程细胞)/原材料(如血浆、修饰物、合成物)接种××× 培养基/投料×××混均,经培养/提取/偶联/合成、收获、浓缩、纯化、灭活/处理后,加入×××制成。
含×××等辅料。
不含防腐剂和抗生素。
若适用,需提供药品的其他名称,如中英文通用名称、化学名称,化学文摘(CAS)号、国外药典收载的名称等;提供结构式、分子式、分子量等;标明糖基化位点或其他转译后修饰及相对分子量的氨基酸序列示意图。
若为生物类似药,明确本品为×××的生物类似药。

生物制品生产用原材料及辅料的质量控制规程12生物制品是采用生物技术制备而成的具有活性的药品。
生物制品的生产工3艺复杂且易受多种因素影响,生产过程中使用的各种材料来源复杂,可能引入4外源因子或毒性化学材料;产品组成成分复杂且一般不能进行终端灭菌,产品5的质量控制仅靠成品检定难以保证其安全性和有效性。
因此,对生物制品生产6用原材料和辅料进行严格的质量控制,是降低制品中外源因子或有毒杂质污染7风险,保证生物制品安全有效的必要措施。
8本规程是对生物制品生产企业在生物制品生产过程中使用的原材料和辅料9质量控制的通用性要求。
10一、、生物制品生产用原材料11生物制品生产用原材料系指生物制品生产过程中使用的所有生物材料和化学12材料。
本规程所述原材料不包括用于生物制品生产的起始原材料(如细胞基质、13菌毒种、生产用人血浆和动物免疫血清等)。
141.分类15按照来源可将生物制品生产用原材料分为两大类,一类为生物原材料,主要16包括来源于微生物,人和动物细胞、组织、体液成分,以及采用重组技术或生17物合成技术生产的生物原材料等;另一类为化学原材料,包括无机和有机化学18材料。
192.风险等级分级及用于生产的质量控制要求20根据原材料的来源、生产以及对生物制品潜在的毒性和外源因子污染风险等21将生物制品生产用原材料按风险级别从低到高分为以下四级,各级生物制品原22材料至少应进行的质量控制要求见附表1。
23对于不同风险级别原材料的质量控制,应充分考虑来源于动物(或人)的生24物原材料可能带来的外源因子污染的安全性风险。
生产过程中应避免使用毒性25较大的化学原材料,有机溶剂的使用应符合本版药典附录“残留溶剂检测”的26相关要求。
27第1级为较低风险的原材料。
为已获得上市许可的生物制品或药品无菌制剂。
28如人血白蛋白、各种氨基酸、抗生素注射剂等。
29第2级为低风险原材料,这类原材料为已有国家药品标准、取得国家药品批30准文号并按照我国现行药品GMP生产的用于生物制品培养基成分以及提取、纯31化、灭活等过程的化学原料药和药用级非动物来源的蛋白水解酶等。

生物制品质量控制一、引言生物制品是指通过生物技术手段生产的药品、疫苗、血液制品等。
由于其特殊性质和用途,对于生物制品的质量控制非常重要。
本文将详细介绍生物制品质量控制的标准格式,包括质量控制的目的、方法、流程和要求。
二、质量控制的目的生物制品质量控制的目的是确保生物制品的安全性、有效性和一致性。
通过严格的质量控制,可以保证生物制品在生产、储存和使用过程中的质量稳定性,减少潜在风险和不良反应。
三、质量控制的方法1. 原材料检验:对生物制品的原材料进行严格的检验,确保其符合质量标准和规范要求。
原材料的检验包括外观、纯度、活性等方面的测试。
2. 生产过程控制:在生物制品的生产过程中,需要对各个环节进行严格的控制。
包括生产设备的验证、生产操作的规范化、生产环境的监测等。
3. 产品检验:对生产出的生物制品进行全面的检验,确保其符合质量标准和规范要求。
产品检验包括外观、理化性质、活性、纯度、微生物检验等方面的测试。
4. 稳定性研究:对生物制品的稳定性进行研究,确定其在不同条件下的质量变化规律。
稳定性研究可以匡助确定生物制品的有效期限,并制定适当的储存和使用条件。
四、质量控制的流程1. 制定质量控制计划:根据生物制品的特性和要求,制定质量控制计划,明确质量控制的目标、方法和流程。
2. 建立质量控制体系:建立适应生物制品质量控制的组织结构和管理体系,明确各个环节的责任和职责。
3. 实施质量控制措施:按照质量控制计划和要求,对生物制品的原材料、生产过程和成品进行检验和控制。
4. 监督和审核:对质量控制的实施情况进行监督和审核,及时发现问题并采取纠正措施。
五、质量控制的要求1. 符合法规和规范:生物制品的质量控制必须符合国家和地区的法规和规范要求,包括药品管理法规、药典标准等。
2. 严格的记录和文档管理:对于生物制品的质量控制过程,必须进行详细的记录和文档管理,确保数据的准确性和可追溯性。
3. 建立有效的风险管理体系:生物制品的质量控制需要建立有效的风险管理体系,及时识别和评估潜在风险,并采取相应的控制措施。

生物制品使用管理制度范文第一章总则第一条为了规范生物制品的管理和使用,确保生物制品使用的安全性和合理性,提高生物制品使用的效率和质量,依据相关法律法规,制定本制度。
第二章生物制品管理第二条生物制品管理部门负责生物制品管理的组织、指导、监督工作。
第三条生物制品管理部门应建立健全生物制品管理档案,并定期进行更新和维护。
第四条生物制品管理部门应组织生物制品的采购、存储、调配、使用等工作,并负责生物制品的验收和报废工作。
第五条生物制品管理部门应定期对生物制品的库存情况进行盘点,并编制库存清单。
第六条生物制品的采购应根据实际需求,严格按照相关法律法规和政策规定进行采购。
第七条生物制品的存储应符合相关的规定,确保生物制品的安全性和质量。
第八条生物制品的调配应根据实际需要,合理安排生物制品的使用,并确保及时调配和更新。
第九条生物制品的使用应按照相关的规定进行,确保生物制品使用的安全性和合理性。
第三章生物制品使用第十条生物制品的使用应经过相关人员的审核和签字批准。
第十一条生物制品的使用应按照使用说明书进行,严禁超量使用或误用。
第十二条生物制品的使用场所应符合相关的规定,确保使用安全和环境卫生。
第十三条在使用过程中,如发现生物制品的异常情况或问题,应及时向生物制品管理部门汇报,停止使用,并进行相关的处理和调查。
第十四条生物制品的使用记录应独立保存,并定期进行备份和归档。
第十五条生物制品的使用应实行消耗制度,定期报废过期的生物制品。
第十六条生物制品的使用应加强相关知识的培训,提高工作人员的使用技能和操作水平。
第四章生物制品安全管理第十七条生物制品管理部门应建立健全生物制品的安全管理制度和应急预案,并定期进行演练和策划。
第十八条生物制品使用人员应严格遵守生物制品的安全操作规程,加强个人卫生防护,避免生物制品对人员和环境的危害。
第十九条对于具有较高风险的生物制品,应实行特殊管控措施,如限制使用范围、设立隔离区等。
第二十条生物制品管理部门应建立安全监测和检测机制,确保生物制品的安全性和合规性。
生物制品生产用原材料及辅料的质量控制规程12生物制品是采用生物技术制备而成的具有活性的药品。
生物制品的生产工3艺复杂且易受多种因素影响,生产过程中使用的各种材料来源复杂,可能引入4外源因子或毒性化学材料;产品组成成分复杂且一般不能进行终端灭菌,产品5的质量控制仅靠成品检定难以保证其安全性和有效性。
因此,对生物制品生产6用原材料和辅料进行严格的质量控制,是降低制品中外源因子或有毒杂质污染7风险,保证生物制品安全有效的必要措施。
8本规程是对生物制品生产企业在生物制品生产过程中使用的原材料和辅料9质量控制的通用性要求。
10一、、生物制品生产用原材料11生物制品生产用原材料系指生物制品生产过程中使用的所有生物材料和化学12材料。
本规程所述原材料不包括用于生物制品生产的起始原材料(如细胞基质、13菌毒种、生产用人血浆和动物免疫血清等)。
141.分类15按照来源可将生物制品生产用原材料分为两大类,一类为生物原材料,主要16包括来源于微生物,人和动物细胞、组织、体液成分,以及采用重组技术或生17物合成技术生产的生物原材料等;另一类为化学原材料,包括无机和有机化学18材料。
192.风险等级分级及用于生产的质量控制要求20根据原材料的来源、生产以及对生物制品潜在的毒性和外源因子污染风险等21将生物制品生产用原材料按风险级别从低到高分为以下四级,各级生物制品原22材料至少应进行的质量控制要求见附表1。
23对于不同风险级别原材料的质量控制,应充分考虑来源于动物(或人)的生24物原材料可能带来的外源因子污染的安全性风险。
生产过程中应避免使用毒性25较大的化学原材料,有机溶剂的使用应符合本版药典附录“残留溶剂检测”的26相关要求。
27第1级为较低风险的原材料。
为已获得上市许可的生物制品或药品无菌制剂。
28如人血白蛋白、各种氨基酸、抗生素注射剂等。
29第2级为低风险原材料,这类原材料为已有国家药品标准、取得国家药品批30准文号并按照我国现行药品GMP生产的用于生物制品培养基成分以及提取、纯31化、灭活等过程的化学原料药和药用级非动物来源的蛋白水解酶等。
生物制品生产用原材料及辅料质量控制规程生物制品就是采用生物技术制备而成得具有活性得药品,其生产工艺复杂且易受多种因素影响;生产过程中使用得各种材料来源复杂,可能引人外源因子或毒性化学材料;制品组成成分复杂且一般不能进行终端灭菌,制品得质量控制仅靠成品检定难以保证其安全性与有效性。
因此,对生物制品生产用原材料与辅料进行严格得质量控制,就是降低制品中外源因子或有毒杂质污染风险,保证生物制品安全有效得必要措施。
本规程就是对生物制品生产企业在生物制品生产过程中使用得原材料与辅料质量控制得通用性要求。
—、生物制品生产用原材料生物制品生产用原材料系指生物制品生产过程中使用得所有生物原材料与化学原材料。
本规程所述原材料不包括用于生物制品生产得起始原材料(如细胞基质、菌毒种、生产用人血浆与动物免疫血清等)。
1、分类按照来源可将生物制品生产用原材料分为两大类:一类为生物原材料,主要包括来源于微生物,人与动物细胞、组织、体液成分,以及采用重组技术或生物合成技术生产得生物原材料等;另一类为化学原材料,包括无机与有机化学材料。
2、风险等级分级及用于生产得质量控制要求根据原材料得来源、生产以及对生物制品潜在得毒性与外源因子污染风险等将生物制品生产用原材料按风险级别从低到高分为以下四级,各级生物制品原材料至少应进行得质量控制要求见表1。
对于不同风险级别原材料得质量控制,应充分考虑来源于动物(或人)得生物原材料可能带来得外源因子污染得安全性风险。
生产过程中应避免使用毒性较大得化学原材料,有机溶剂得使用应符合本版药典通则“残留溶剂测定法”得相关要求。
第1 级为较低风险得原材料。
这类原材料为已获得上市许可得生物制品或药品无菌制剂,如人血白蛋白、各种氨基酸、抗生素注射剂等。
第2 级为低风险得原材料。
这类原材料为已有国家药品标准、取得国家葯品批准文号并按照中国现行《药品生产质量管理规范》生产得用于生物制品培养基成分以及提取、纯化、灭活等过程得化学原料药与药用级非动物来源得蛋白水解酶等。
生物制品生产用原材料及辅料的质量控制规程第一篇:生物制品生产用原材料及辅料的质量控制规程生物制品生产用原材料及辅料的质量控制规程生物制品是采用生物技术制备而成的具有活性的药品。
生物制品的生产工艺复杂且易受多种因素影响,生产过程中使用的各种材料来源复杂,可能引入外源因子或毒性化学材料;产品组成成分复杂且一般不能进行终端灭菌,产品的质量控制仅靠成品检定难以保证其安全性和有效性。
因此,对生物制品生产用原材料和辅料进行严格的质量控制,是降低制品中外源因子或有毒杂质污染风险,保证生物制品安全有效的必要措施。
本规程是对生物制品生产企业在生物制品生产过程中使用的原材料和辅料质量控制的通用性要求。
一、生物制品生产用原材料生物制品生产用原材料系指生物制品生产过程中使用的所有生物材料和化学材料。
本规程所述原材料不包括用于生物制品生产的起始原材料(如细胞基质、菌毒种、生产用人血浆和动物免疫血清等)1.分类按照来源可将生物制品生产用原材料分为两大类,一类为生物原材料,主要包括来源于微生物,人和动物细胞、组织、体液成分,以及采用重组技术或生物合成技术生产的生物原材料等;另一类为化学原材料,包括无机和有机化学材料。
2.风险等级分级及用于生产的质量控制要求根据原材料的来源、生产以及对生物制品潜在的毒性和外源因子污染风险等,将生物制品生产用原材料按风险级别从低到高分为以下四级,各级生物制品原材料至少应进行的质量控制要求见附表1;对于不同风险级别原材料的质量控制,应充分考虑来源于动物(或人)的生物原材料可能带来的外源因子污染的安全性风险。
生产过程中应避免使用毒性较大的化学原材料,有机溶剂的使用应符合本版药典附录“残留溶剂检测”的相关要求。
第1级为较低风险的原材料,为已获得上市许可的生物制品或药品无菌制剂。
如人血白蛋白、各种氨基酸、抗生素注射剂等。
第2级为低风险原材料,这类原材料为已有国家药品标准、取得国家药品批准文号并按照我国现行药品GMP生产的用于生物制品培养基成分以及提取、纯化、灭活等过程的化学原料药和药用级非动物来源的蛋白水解酶等。
生物制品质量控制一、引言生物制品是指利用生物技术生产的具有药用价值的产品,如疫苗、血液制品、基因工程药物等。
由于生物制品的特殊性质和用途,对其质量控制要求极高。
本文将详细介绍生物制品质量控制的标准格式,包括质量控制的目的、方法、要求等。
二、质量控制的目的生物制品质量控制的目的是确保产品的安全性、有效性和一致性。
通过严格的质量控制,可以保证生物制品在生产过程中的各个环节都符合规定的标准,从而提高产品的质量和可靠性。
三、质量控制的方法1. 原材料控制:对生物制品生产所使用的原材料进行严格的筛选和检测,确保原材料的质量符合要求。
这包括对原材料的来源、纯度、稳定性等方面进行检查。
2. 生产过程控制:生物制品的生产过程需要严格控制,确保每个步骤都符合规定的标准。
这包括对生产设备、操作人员、环境条件等方面进行监测和管理。
3. 产品检测:对生产出的生物制品进行全面的检测,包括物理、化学、生物学等方面的检验。
这可以确保产品的质量符合规定的标准,并排除可能存在的安全隐患。
4. 质量记录和文档管理:对生物制品的质量记录和文档进行管理,确保其准确、完整、可追溯。
这可以为产品质量的评估和溯源提供依据。
四、质量控制的要求1. 安全性:生物制品的安全性是质量控制的首要要求。
必须确保产品不含有有害物质,并对可能存在的安全风险进行评估和控制。
2. 有效性:生物制品的有效性是质量控制的关键要求。
必须确保产品的活性成分符合规定的含量范围,并对产品的效果进行评估和验证。
3. 一致性:生物制品的一致性是质量控制的基本要求。
必须确保每个生产批次的产品质量都符合规定的标准,并对批间和批内的一致性进行评估和控制。
4. 可追溯性:生物制品的可追溯性是质量控制的重要要求。
必须建立完善的质量记录和文档管理体系,确保产品的质量可以追溯到原材料的来源和生产过程的各个环节。
五、质量控制的评估与改进为了确保生物制品质量控制的有效性,需要进行定期的评估和改进。
生物制品生产用原材料及辅料质量控制规程生物制品是采用生物技术制备而成的具有活性的药品,其生产工艺复杂且易受多种因素影响;生产过程中使用的各种材料来源复杂,可能引人外源因子或毒性化学材料;制品组成成分复杂且一般不能进行终端灭菌,制品的质量控制仅靠成品检定难以保证其安全性和有效性。
因此,对生物制品生产用原材料和辅料进行严格的质量控制,是降低制品中外源因子或有毒杂质污染风险,保证生物制品安全有效的必要措施。
本规程是对生物制品生产企业在生物制品生产过程中使用的原材料和辅料质量控制的通用性要求。
—、生物制品生产用原材料生物制品生产用原材料系指生物制品生产过程中使用的所有生物原材料和化学原材料。
本规程所述原材料不包括用于生物制品生产的起始原材料(如细胞基质、菌毒种、生产用人血浆和动物免疫血清等)。
1. 分类按照来源可将生物制品生产用原材料分为两大类:一类为生物原材料,主要包括来源于微生物,人和动物细胞、组织、体液成分,以及采用重组技术或生物合成技术生产的生物原材料等;另一类为化学原材料,包括无机和有机化学材料。
2. 风险等级分级及用于生产的质量控制要求根据原材料的来源、生产以及对生物制品潜在的毒性和外源因子污染风险等将生物制品生产用原材料按风险级别从低到高分为以下四级,各级生物制品原材料至少应进行的质量控制要求见表1。
对于不同风险级别原材料的质量控制,应充分考虑来源于动物(或人)的生物原材料可能带来的外源因子污染的安全性风险。
生产过程中应避免使用毒性较大的化学原材料,有机溶剂的使用应符合本版药典通则“残留溶剂测定法”的相关要求。
第 1 级为较低风险的原材料。
这类原材料为已获得上市许可的生物制品或药品无菌制剂,如人血白蛋白、各种氨基酸、抗生素注射剂等。
第 2 级为低风险的原材料。
这类原材料为已有国家药品标准、取得国家葯品批准文号并按照中国现行《药品生产质量管理规范》生产的用于生物制品培养基成分以及提取、纯化、灭活等过程的化学原料药和药用级非动物来源的蛋白水解酶等。
生物制品生产用原材料及辅料的质量控制规程
生物制品是采用生物技术制备而成的具有活性的药品。
生物制品的生产工艺复杂且易受多种因素影响,生产过程中使用的各种材料来源复杂,可能引入外源因子或毒性化学材料;产品组成成分复杂且一般不能进行终端灭菌,产品的质量控制仅靠成品检定难以保证其安全性和有效性。
因此,对生物制品生产用原材料和辅料进行严格的质量控制,是降低制品中外源因子或有毒杂质污染风险,保证生物制品安全有效的必要措施。
本规程是对生物制品生产企业在生物制品生产过程中使用的原材料和辅料质量控制的通用性要求。
一、生物制品生产用原材料
生物制品生产用原材料系指生物制品生产过程中使用的所有生物材料和化学材料。
本规程所述原材料不包括用于生物制品生产的起始原材料(如细胞基质、
菌毒种、生产用人血浆和动物免疫血清等)
1.分类
按照来源可将生物制品生产用原材料分为两大类,一类为生物原材料,主要包括来源于微生物,人和动物细胞、组织、体液成分,以及采用重组技术或生物合成技术生产的生物原材料等;另一类为化学原材料,包括无机和有机化学材料。
2.风险等级分级及用于生产的质量控制要求
根据原材料的来源、生产以及对生物制品潜在的毒性和外源因子污染风险等,将生物制品生产用原材料按风险级别从低到高分为以下四级,各级生物制品原
材料至少应进行的质量控制要求见附表1;对于不同风险级别原材料的质量控制,应充分考虑来源于动物(或人)的生物原材料可能带来的外源因子污染的安全性风险。
生产过程中应避免使用毒性较大的化学原材料,有机溶剂的使用应符合本版药
典附录“残留溶剂检测”的相关要求。
第1级为较低风险的原材料,为已获得上市许可的生物制品或药品无菌制剂。
如人血白蛋白、各种氨基酸、抗生素注射剂等。
第2级为低风险原材料,这类原材料为已有国家药品标准、取得国家药品批准文号并按照我国现行药品GMP生产的用于生物制品培养基成分以及提取、纯化、灭活等过程的化学原料药和药用级非动物来源的蛋白水解酶等。
第3级为中等风险等级原材料,这类原材料为非药用,包括生物制品生产用培养基成分、非动物来源蛋白水解酶、用于靶向纯化的单克隆抗体,以及用于
生物制品提取、纯化、灭活的化学试剂等。
这类生物制品原材料的质量控制要求应
高于前两个等级的原材料,为使其符合生产用原材料的要求,使用时可能需进一步加工、纯化处理或增加病毒灭活和/或去除步骤等。
第4级为高风险等级原材料。
这类材料主要包括已知具有生物作用机制的毒性化学物质,如:甲氨喋呤、霍乱毒素、金黄色葡萄菌素孔道溶血素、金黄色葡萄菌素肠毒素A和B以及中毒性休克综合征毒素;以及大部分成分复杂的动物源性组织和体液,如用于细胞培养基成分的牛血清、用于细胞消化或蛋白水解的动物来源的酶以及用于选择或去除免疫靶向性成分的腹水来源的抗体或蛋白。
这类原材料用于生物制品生产前,应进行严格的全面质量检定,或需要采取进一步的处理措施,包括(1)改进原材料的生产工艺;(2)对原材料进行处理,以灭活或去除外源因子、致病物质或特定的污染物(如动物病毒、朊蛋白等)。
对于高风险等级的原材料,应在产品研发的早期评价使用这些原材料的必要性,并寻找其他替代物或替代来源。
3、残留物的去除及限度要求
生产用原材料在生物制品中的残留物可能因其直接的毒性反应、外源因子污染或有害的免疫应答,引发受者产生不良反应或影响产品效力,应采取相应措施对这些原材料予以去除和/或灭活,去除和/或灭活工艺应进行验证。
应通过验证结果评价生产工艺对已知毒性原材料去除的一致性,或采用批放行检测,以证实所去除的毒性原材料已达到安全水平,残留有机溶剂应符合本版药典“残留溶剂测定法”的相关要求;
应尽可能采用经去除和/或灭活外源因子的生物原材料,或通过验证结果评价生产工艺去除和/或灭活原材料中可能存在的外源因子、致病物质或者与该材料相关的特定污染物的一致性,以确保产品的安全性。
三、生物制品生产用辅料
生物制品辅料系指生物制品配方中所使用的辅助材料,如佐剂、稳定剂、赋形剂等。
生物制品生产用辅料的使用应经国家药品监督管理部门批准,并符合国家相关技术要求和管理规范。
1、生物制品生产用常用辅料及分类
根据用途,生物制品常用辅料包括以下几类:
佐剂:是与一种疫苗抗原结合以增强(如加强、加快、延长和/或可能的定向)其特异性免疫反应和疫苗临床效果的一种或多种成分混合的物质。
稳定剂或保护剂:用于稳定或保护其有效成分、防止其降解或失去活性的物质。
防腐剂:用于抑制微生物生长、防止微生物污染的物质。
赋形剂:用于冻干制品中使药品成型、起支架作用的物质。
助溶剂:用于增加药品溶解性的物质
矫味剂:用于改善口服药品口感的物质。
稀释剂、缓冲剂:用于溶解、稀释制品,调整制品酸碱度的溶剂,如注射用水、氯化钠注射液、磷酸盐缓冲液(PBS)等。
2、风险等级分级及用于生产的质量控制要求
根据辅料的来源、生产以及对生物制品潜在的毒性和安全性的影响等将辅料按风险级别从低到高分为四级,各级生物制品辅料至少应进行的质量控制要求见附表2
生物制品生产企业用于生物制品注射剂生产的药用辅料,其全检的质量标准中除理化、含量/活性等检测外,应包括常规的安全性检查,如微生物限度或无菌检查、热原和/或内毒素检查、异常毒性检查等。
第1级为较低风险的辅料。
这类辅料是已获得上市许可的生物制品或药品无菌制剂。
如人血白蛋白、肝素钠和氯化钠注射液等。
第2级为低风险的辅料,这类辅料为已有国家药品标准、取得国家药品批
准文号并按照我国现行药品GMP生产的化学原料药。
如各种无机和有机化学原料药。
第3级为中等风险级别的辅料,这类辅料按照《药用辅料生产质量管理规范》规范生产,取得国家药用辅料批准文号,或按照国家备案管理的非动物源性药用辅料。
如用作稀释剂、缓冲剂配制的各种化学材料、用作保护剂/稳定剂的各种糖类、用作防腐剂的硫柳汞及软膏基质的单、双硬脂酸甘油酯等。
其质量控制要求应高于前两个等级的材料。
第4级为高风险等级辅料。
这类材料包括除上述1-3类以外的其他辅料,
如用作疫苗赋形剂的动物来源的明胶等。
非化学原料药和药用辅料用作生物制品辅料或非注射用的化学原料药或药用辅料用于生物制品注射剂生产时,应按风险等级第4级的辅料进行质量控制。
这类辅料用于生物制品生产前,应进行严格的全面质
量检定,必要时应采取进一步的处理措施,包括(1)改进辅料的生产工艺;(2)对辅料
进行处理,提高辅料纯度、灭活和/或去除外源性因子、致病物质或特定污染物(如动
物病毒、朊蛋白等)。
同时存在几种风险等级的同一种辅料,应根据生物制品产品特性和生产工艺特性选用风险级别低的辅料。
对于高风险等级的辅料,应在产品研发的早期评价使用这些辅料的必要性,并寻找其他替代物或替代来源。
3、辅料限度的控制
应根据生物制品制剂工艺和产品的安全性、有效性研究结果,以发挥有效作用的最小加量确定制剂配方中辅料的加量。
具有明确功能且可采用适宜方法进行性能测试的辅料,还应结合辅料性能测试结果综合考虑配方中辅料的加量,如防腐剂抑菌效力检查,疫苗佐剂抗原吸附效果检测等。
具有毒副作用或特定功能的辅料以及其他需要在生物制品中控制含量的辅料,应在成品检定或适宜的中间产物阶段设定辅料含量检查项并规定限度要求。