自身免疫性脑炎诊疗指南
- 格式:doc
- 大小:128.21 KB
- 文档页数:8

自身免疫性脑炎诊疗指南(2017版)一、适用对象第一诊断为自身免疫性脑炎(ICD-10:GO4.801)二、诊断依据根据《中国自身免疫性脑炎诊治专家共识》(中国医学会神经病学分会中华神经科杂志)。
三、计划住院天数为14-28天内四、计划住院总费用为10000-15000元内五、住院期间检查项目1.必需的检查项目(1)血常规、尿常规、大便常规+隐血、肝肾功能、电解质、凝血、心肌酶;(2)红细胞沉降率、甲状腺功能、风湿免疫、抗核抗体谱;(3)心电图、心脏彩超、X线胸片、胸部CT、盆腔CT和(或)超声、睾丸超声;(4)脑电图、头MRI(平扫与增强)、脑脊液检查、抗神经元抗体。
2.根据患者情况可选择的检查项目头与全身PET(必要时)、同步视频多导睡眠图六、出院标准1.一般情况良好。
2.没有需要继续住院处理的并发症和(或)合并症。
自身免疫性脑炎自身免疫性脑炎(AE)泛指一类由自身免疫机制介导的脑炎,但一般特指抗神经抗体相关的脑炎。
例如抗NMDA受体脑炎等。
AE 合并相关肿瘤者,称为副肿瘤性AE。
急性播散性脑脊髓炎、Bickerstaff 脑干脑炎等也属于广义的AE范畴。
【诊断要点】1、前驱症状:发热、头痛、单纯疱疹病毒性脑炎相关症状;2、主要症状:精神行为异常、认知障碍、近记忆力下降、癫痫发作、言语障碍、运动障碍、不自主运动,意识水平下降、自主神经功能障碍等。
3、伴随症状:睡眠障碍、CNS局灶性损害、脑干、小脑症状以及周围神经和神经肌肉接头受累等。
3、临床分为3种主要类型:①抗NMDAR脑炎,②边缘性脑炎③其他类型AE。
4、脑脊液异常:CSF白细胞增多(>5×106/L);或者脑脊液细胞学呈淋巴细胞性炎症;或者CSF寡克隆区带阳性。
5、头颅MRI:边缘系统T2或者FLAIR异常信号。
EEG异常。
【诊断标准】1.诊断条件包括临床表现、辅助检查、确诊实验与排除其他病因4个方面。
1.1 临床表现:急性或者亚急性起病(<3个月),具备以下一个或者多个神经与精神症状或者临床综合征。

自身免疫性脑炎诊疗指南概述自身免疫性脑炎(autoimmune encephalitis,AE)泛指一类由自身免疫机制介导的脑炎,但一般特指抗神经抗体相关的脑炎,例如抗NMDA受体脑炎等。
AE 合并相关肿瘤者,称为副肿瘤性AE。
急性播散性脑脊髓炎、Bickerstaff脑干脑炎等也属于广义的AE范畴。
病因和流行病学主要通过体液或者细胞免疫反应介导中枢神经系统损伤。
其中抗细胞表面蛋白抗体通常具有明确的致病性。
抗NMDAR抗体可导致神经元表面的NMDAR 可逆性的减少,并不引起神经元坏死。
肿瘤和前驱感染事件常为AE的诱因。
AE患病比例占脑炎病例的10%~20%,估算年发病率为1/10万左右。
抗NMDAR脑炎约占AE病例的80%,其他AE相关抗体包括:抗GAD、CASPR2、IgLON5、AMPAR、DPPX等。
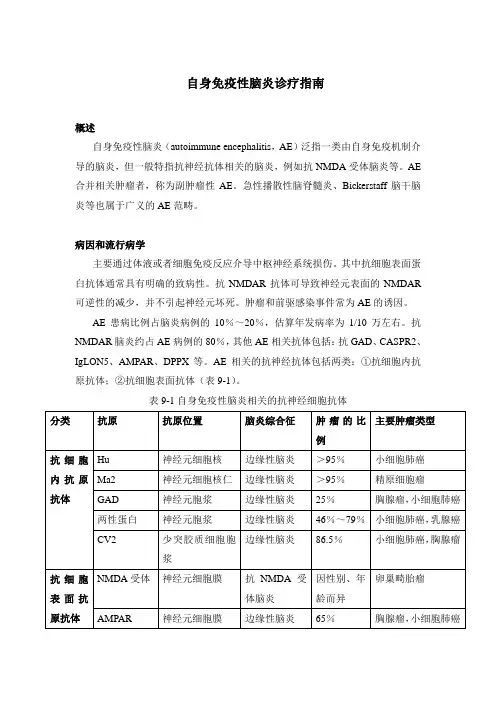
AE相关的抗神经抗体包括两类:①抗细胞内抗原抗体;②抗细胞表面抗体(表9-1)。
表9-1自身免疫性脑炎相关的抗神经细胞抗体注:部分抗体依与其他神经综合征相关,如僵人综合征、亚急性小脑变性与感觉神经元神经病等。
neurexin-3alpha.突触蛋白-3α。
GAD.glutamic acid decarboxylase,谷氨酸脱羧酶。
CASPR2.contactin associated protein 2,接触蛋白相关蛋白样蛋白2。
DPPX.dipeptidyl-peptidase-like protein-6,二肽基肽酶样蛋白-6。
Amphiphysin.两性蛋白。
NMDAR.N-methyl-D-aspartate receptor,N-甲基-D-天冬氨酸受体。
AMPAR.α-amino-3-hydroxy-5-methyl-4-isoxazole propionic acid receptor,α氨基-3-羟基-5-甲基-4-异恶唑丙酸受体。
GABA B R.γ-amino butyric acid type B receptor,γ-氨基丁酸B型受体。

临床诊治自身免疫性脑炎一例发表时间:2016-03-02T14:22:54.937Z 来源:《航空军医》2015年19期作者:刘猛饶旺福[导读] 1.江西中医药大学2013级研究生;2.江西中医药大学附属医院神经内科自身免疫性脑炎(AE)是一种中枢神经系统炎性疾病,是由机体对神经元抗原成分的异常免疫反应所致。
1.江西中医药大学2013级研究生南昌 330004;2.江西中医药大学附属医院神经内科南昌 330006 【摘要】自身免疫性脑炎(AE)是一种中枢神经系统炎性疾病,是由机体对神经元抗原成分的异常免疫反应所致。
随着神经免疫学不断发展,临床上AE患者检出率也有所增加。
在临床诊治中应尽早确诊,以采取合理有效的治疗方案,提高患者预后。
现报告1例自身免疫性脑炎病例,并复习关于AE的诊治注意事项。
【关键词】自身免疫性脑炎;临床表现及治疗。
1.病例现病史:患者青年男性,职业学生,于2015年6月11日至南昌大学第一附属医院就诊,诉数日前劳累后双下肢肢体抽搐,两眼上翻,数秒后晕厥,意识不清,持续约40分钟。
醒后不能回忆当时情景,伴明显头痛,呕吐2次,至我院就诊时上述症状共发作2次。
入院3天后患者出现持续发热,记忆力下降,头昏,精神疲惫,继而开始出现焦虑、烦躁症状,胡言乱语,目光呆滞,幻视、幻听等精神症状。
既往史:患者家属诉11年前患者曾有类似发作病史,当时诊断为病毒性脑炎,经治疗后好转,其大伯有癫痫病史。
否认手术及外伤史,否认食物、药物过敏史。
查体:入院时查体心、肺、腹无异常,神经系统检查仅见双下肢腱反射活跃,脑膜刺激征阴性。
3日后查体克氏征阳性。
影像学检查:急诊查头颅CT无异常。
颅脑磁共振及血管检查提示右侧颈内动脉眼段瘤样凸起,余无异常。
实验室检查:血清白细胞、中性粒细胞升高。
脑脊液:白细胞:30/ul,氯:119mmol/l,蛋白:557mg/l。
血清及脑脊液免疫检查:单纯疱疹病毒IgG:4.0816,抗谷氨酸抗体IgG阳性。





自身免疫性脑炎的分类及诊治刘磊1,谢竹霄1,王佳伟1, 2*(1.首都医科大学附属北京同仁医院 神经内科,北京 100730;2. 首都医科大学附属北京同仁医院 中心实验室,北京 100730)关键词:自身免疫性脑炎;发病机制;分类;治疗中图分类号:R741 文献标识码:A 文章编号:2095-8552(2021)06-0634-06doi:10.3969/j.issn.2095-8552.2021.06.002性的细胞表面蛋白。
多项动物实验发现,通过基因改造或者药物拮抗剂改变同一蛋白功能所产生的综合征和AIE 患者表现的临床综合征非常相似。
CSAab 可能致病机制包括:①抗N-甲基-D-天冬氨酸受体(N-methyl-D-aspartate receptor ,NMDAR )-IgG 使神经元表面NMDAR 交联并内化;②抗富含亮氨酸胶质瘤失活蛋白1(leucine-rich glioma-inactivated protein 1,LGI1)-IgG 阻断蛋白-蛋白间相互作用,影响电压门控钾通道,致使α氨基-3-羟基-5-甲基-4-异唑酸受体(α-amino-3-hydroxy-5-methyl-4-isoxazolepropionic acid receptor ,AMPAR )水平下降,进而影响神经元功能;③抗γ-氨基丁酸B 型受体(γ-amino butyric acid type B receptor ,GABA B R )- IgG 直接阻断受体B1亚单位。
此外,CSAab 还能促进补体沉积和自然杀伤细胞激活,从而导致细胞死亡。
SYAab 往往通过影响神经递质释放产生症状。
INAab 由于无法接触细胞内抗原,主要是通过细胞毒性T 细胞释放穿孔素和颗粒酶杀伤靶细胞而发挥致病效应,而抗体本身可能仅是一种附带效应[5]。
2 临床表现及具体分类①AIE 任何年龄均可发病,无明显性别差异,急性或亚急性起病,可有复发。

自身免疫性脑炎分型、临床表现、诊断、治疗及管理自身免疫性脑炎诊断脑炎综合征的分类包括副肿瘤性脑炎、AE、免疫(病)相关性脑炎综合征、病毒性脑炎以及特发性脑炎。
对脑炎综合征进行临床分类的目的主要是为了实施针对性治疗。
AE是一类由于免疫系统与中枢神经系统相互作用而导致的急性或亚急性炎性疾病。
临床上符合脑炎综合征的主要表现,以淋巴细胞为主的炎症细胞浸润脑实质,并在血管周围形成套袖样结构,同时具有未检出病毒抗原核酸及包涵体的神经病理学特点,需要有明确责任抗体或相信有责任抗体介导。
图 1. 脑炎综合征分类AE核心表型包括:癫痫样发作、口舌-面肌张力障碍样发作;小脑性共济失调、肢体与躯干舞蹈手足徐动、重复细微手与前臂运动、肌张力障碍与肌强直;认知障碍、睡眠障碍、重复语言等。
首先需要了解致病性抗体的概念。
根据是否致病可将自身抗体分为致病性抗体和伴随抗体。
经典的致病性自身抗体应满足如下评判指标:1)大多数患者的血清或脑脊液中应存在自身抗体,或与健康个体相比抗体滴度升高;2)运用免疫组化方法,可在病灶处观察到免疫球蛋白与靶抗原结合;3)血浆置换或特异性免疫球蛋白吸附去除血循环中的免疫球蛋白有治疗效果;4)通过注射患者血清或纯化免疫球蛋白可将疾病表型转移至实验动物;或用相应靶抗原在易感动物致敏能得到疾病表型。
责任抗体是与特定阶段临床表型具有因果关系的致病性抗体,它决定了该阶段病程神经免疫病的发生、发展和转归;并且责任抗体必须与核心表型相对应。
定位和定性是神经免疫疾病表型刻画的基础,症状、体征的特征和演变在空间与时间维度上的特定组合就构成了此类疾病的表型。
自身抗体与靶组织抗原表位结合特定部位受累,形成相对独特的核心临床表型。
责任抗体的核心在于从空间维度和时间维度与特定表型进行因果关系判断(图 3),具有因果关系的抗体即为责任抗体。
空间因果关系方面,AE 具有特定的分子基础,例如抗 GABAA 受体脑炎在颅脑磁共振上表现为大片融合型病灶及斑点型病灶,并非 GABAA 受体所有 3 个亚基均发挥作用,而主要是 GABAA 受体β3 亚基导致病灶的发生。

一种自身免疫性脑炎的治疗方法摘要:自身免疫性脑炎是一种由于自身免疫功能缺陷所引起的中枢神经性疾病,严重危害着患者的生命健康。
目前在医疗机构中治疗自身免疫性脑炎的治疗方法有很多种,本文将综述一种用糖皮质激素作为治疗药物的治疗手段。
脑炎是一种中枢神经性疾病,根据发病的原因是否由生物因素引起可以分为两种,第一种是病原性感染性脑炎,这种脑炎指的是由于病原微生物的侵入而使得脑膜等中枢神经结构遭到感染所引起的脑炎,常伴有头痛、发热等症状;另一种脑炎为非感染性脑炎,主要是由自身免疫机制所引起的,常伴有精神行为异常、认知障碍等。
糖皮质激素是目前临床治疗手段的一线免疫治疗[1]。
目前这种方法在临床应用十分广泛,本文将就这一治疗手段进行比较详细的叙述。
1.自身免疫性脑炎1.自身免疫性脑炎简介自身免疫性脑炎是一种中枢神经性疾病,这种脑炎并不是由于病原体侵犯而引起的感染,而是因为免疫系统的自我攻击引起中枢神经系统炎症。
在我国,每年都有许多患者因为自身免疫性脑炎而来医院医治,这种疾病严重威胁着患者的生命健康。
所以对于自身免疫性脑炎治疗的研究十分有意义。
1.自身免疫性脑炎的发病机制对于自身免疫性脑炎而言,其并不是完全脱离了外界因素而存在的。
自身免疫性脑炎虽然属于非感染性脑炎,但是也有可能是由于病原体的侵入而引起的。
只不过病原体侵入的部位并不一定是脑部。
一项研究结果显示,许多单状疱疹病毒感染引起的脑炎的患者在治疗结束后,还会产生继发性自身免疫性脑炎[2]。
众所周知,在治疗病原体的过程中,需要药物来治疗,而这种药物治疗的过程中,是通过药物来诱导出抗体,起到杀灭病原体的作用。
但是,在杀灭病原体以后,抗体并没有完全消失,一些抗体依然存在大脑,识别可以结合的靶点。
而且,在大脑中,有一些靶点是很容易与这些抗体结合,所以这些抗体并与这些靶点结合并进行攻击这些靶点,导致自身免疫性脑炎。
另外,肿瘤的发生也会引起自身免疫性脑炎,在某一项研究中,年轻女性抗NMDAR脑炎患者患卵巢畸胎瘤的比例高达58%[3]。
自身免疫性脑炎诊疗指南1000字自身免疫性脑炎(autoimmune encephalitis,简称AE)是一种由自身免疫反应引起的神经炎症,其特点是具有急性起病、多样的临床表现和通过血清抗体和大脑影像学证据支持的自身免疫机制。
近年来随着对该疾病的认识不断加深,AE已成为癫痫、精神科和神经科临床实践中不容忽视的疾病之一。
1. 诊断1.1 AE分类根据抗体类型的不同,AE可分为抗NMDAR自身免疫性脑炎、抗VGKC自身免疫性脑炎、抗GABA-B受体自身免疫性脑炎、抗AMPAR自身免疫性脑炎、抗GAD抗体相关自身免疫性脑炎。
临床医生应根据患者的临床表现、实验室检查以及神经成像评估,有针对性的选择合适的实验室检测指标。
1.2 临床表现AE的早期症状包括:头痛、幻觉、失眠、意识障碍、焦虑和抑郁,这些症状最初可能被误认为是神经症或精神障碍。
接着,患者可能会出现癫痫发作、运动障碍、自主神经系统紊乱、口语及记忆障碍、共济失调,甚至出现昏迷等严重表现。
AE的临床症状多样化,需要临床医生进行系统全面的评估。
1.3 实验室检测常用实验室检测指标包括:脑脊液细胞、蛋白和糖的检测,自身抗体检测(包括各类抗体如NMDAR、VGKC、GABA-B受体、AMPAR和GAD抗体)。
在自身抗体检测方面,血清和脑脊液的规范化处理和实验的正常化技术是必要的。
1.4 神经影像学检查神经影像学检查,如MRI、PET、SPECT等可协助医生了解病情。
在AE的诊断过程中,MRI应该是首选的影像学检查方法。
对于持续且体积较大的病变,MRI的灵敏度和特异度具有优势。
PET和SPECT可以提供脑功能状态的更深入的了解。
2. 治疗2.1 非药物治疗对于AE患者的治疗过程需要个化化的进行管理。
对于急性阶段的患者,亟需立即控制症状,降低并发症的发生,缓解患者的焦虑和抑郁情绪。
非药物治疗包括:心理疏导、康复与针灸等辅助治疗,可有效降低患者的焦虑抑郁程度,帮助患者逐步恢复正常的生活水平。
自身免疫性脑炎诊疗指南概述自身免疫性脑炎(autoimmune encephalitis,AE)泛指一类由自身免疫机制介导的脑炎,但一般特指抗神经抗体相关的脑炎,例如抗NMDA受体脑炎等。
AE 合并相关肿瘤者,称为副肿瘤性AE。
急性播散性脑脊髓炎、Bickerstaff脑干脑炎等也属于广义的AE范畴。
病因和流行病学主要通过体液或者细胞免疫反应介导中枢神经系统损伤。
其中抗细胞表面蛋白抗体通常具有明确的致病性。
抗NMDAR抗体可导致神经元表面的NMDAR可逆性的减少,并不引起神经元坏死。
肿瘤和前驱感染事件常为AE的诱因。
AE患病比例占脑炎病例的10%~20%,估算年发病率为1/10万左右。
抗NMDAR 脑炎约占AE病例的80%,其他AE相关抗体包括:抗GAD、CASPR2、IgLON5、AMPAR、DPPX等。
AE相关的抗神经抗体包括两类:①抗细胞内抗原抗体;②抗细胞表面抗体(表9-1)。
注:部分抗体依与其他神经综合征相关,如僵人综合征、亚急性小脑变性与感觉神经元神经病等。
neurexin-3alpha.突触蛋白-3α。
GAD.glutamic acid decarboxylase,谷氨酸脱羧酶。
CASPR2.contactin associated protein 2,接触蛋白相关蛋白样蛋白2。
DPPX.dipeptidyl-peptidase-like protein-6,二肽基肽酶样蛋白-6。
Amphiphysin.两性蛋白。
NMDAR.N-methyl-D-aspartatereceptor,N-甲基-D-天冬氨酸受体。
AMPAR.α-amino-3-hydroxy-5-methyl-4-isoxazole propionic acid receptor,α氨基-3-羟基-5-甲基-4-异恶唑丙酸受体。
GABAR.γ-amino butyric acid type B receptor,γ-氨基丁酸B型受体。
B LGI1.Leucine-rich glioma-inactivated protein 1,富含亮氨酸胶质瘤失活蛋白1。
VGKC.voltage-gated potassium channel,电压门控钾离子通道。
DPPX.Dipeptidyl-peptidase-likeprotein,二肽基肽酶样蛋白。
D2R.Dopamine2R,多巴胺2型受体。
GlyR.Glycine receptor,甘氨酸受体。
PERM.progressive encephalomyelitis with rigidity and myoclonus,伴有肌强直及阵挛的进行性脑脊髓炎。
MOG.myelin oligodendrocyte glycoprotein,髓鞘少突胶质细胞糖蛋白。
ADEM.acute disseminated encephalomyelitis,急性播散性脑脊髓炎临床表现主要症状包括精神行为异常、认知障碍、记忆力下降、癫zaozi001发作、言语障碍、运动障碍、不自主运动,意识水平下降、自主神经功能障碍等。
其他伴随症状包括睡眠障碍、CNS局灶性损害、脑干、小脑症状以及周围神经和神经肌肉接头受累等。
临床可分为3种主要类型:①抗NMDAR脑炎,抗NMDAR脑炎是AE的最主要类型,其特征性临床表现符合弥漫性脑炎。
②边缘性脑炎,以精神行为异常、颞叶癫zaozi001和近记忆力障碍为主要症状,常见的边缘性脑炎有抗LGI1抗体、抗GABAR抗体与抗AMPAR抗体相关的脑炎。
③其他类型AE,包括莫旺综合B征、抗DPPX抗体相关脑炎、抗IgLON5抗体相关脑病、自身免疫性小脑性共济失调等。
辅助检查具有以下一个或者多个的辅助检查发现,或者合并相关肿瘤。
6/L);或者脑脊液细胞学呈淋巴细胞10脑脊液异常CSF白细胞增多(>5×1.性炎症;或者CSF寡克隆区带阳性。
2.神经影像学或者电生理异常MRI边缘系统T2或者FLAIR异常信号,单侧或者双侧,或者其他区域的T2或者FLAIR异常信号(除外非特异性白质改变和卒中);或者PET边缘系统高代谢改变,或者多发的皮质和(或)基底节的高代谢;或者EEG异常:局灶性癫zaozi001或者癫zaozi001样放电(位于颞叶或者颞叶以外),或者弥漫或者多灶分布的慢波节律。
3.与AE相关的特定类型的肿瘤例如边缘性脑炎合并小细胞肺癌,抗NMDAR脑炎合并畸胎瘤等。
诊断根据《中国自身免疫性脑炎诊治专家共识》的建议,AE诊断标准如下:1.诊断条件包括临床表现、辅助检查、确诊实验与排除其他病因4个方面。
(1)临床表现:急性或者亚急性起病(<3个月),具备以下一个或者多个神经与精神症状或者临床综合征。
.1)边缘系统症状:近事记忆减退、癫zaozi001发作、精神行为异常,3个症状中的一个或者多个。
2)脑炎综合征:弥漫性或者多灶性脑损害的临床表现。
3)基底节和(或者)间脑/下丘脑受累的临床表现。
4)精神障碍,且精神心理专科认为不符合非器质性疾病。
(2)辅助检查:具有以下一个或者多个辅助检查发现,或者合并相关肿瘤。
6/L);或者脑脊液细胞学呈淋巴CSF白细胞增多(>5×10 1)脑脊液异常:细胞性炎症;或者CSF寡克隆区带阳性。
2)神经影像学或者电生理异常:MRI边缘系统T2或者FLAIR异常信号,单侧或者双侧,或者其他区域的T2或者FLAIR异常信号(除外非特异性白质改变和卒中);或者PET边缘系统高代谢改变,或者多发的皮质和(或)基底节的高代谢;或者EEG异常:局灶性癫zaozi001或者癫zaozi001样放电(位于颞叶或者颞叶以外),或者弥漫或者多灶分布的慢波节律。
3)与AE相关的特定类型的肿瘤:例如边缘性脑炎合并小细胞肺癌,抗NMDAR脑炎合并畸胎瘤等。
(3)确诊实验:抗神经元表面抗原的自身抗体阳性。
抗体检测主要采用间接免疫荧光法(indirect immunofluorescence assay,IIF)。
基于细胞底物的实验(cell based assay,CBA)具有较高的特异性和敏感性。
应尽量对患者的配对的脑脊液与血清标本进行检测,脑脊液与血清的起始稀释滴度分别为1:1与1:10。
(4)合理地排除其他病因2.诊断标准包括可能的AE与确诊的AE。
(1)可能的AE:符合A、B与D 3个条件。
(2)确诊的AE:符合A、B、C与D 4个条件。
鉴别诊断1.感染性疾病病毒性脑炎、神经梅毒、细菌等所致的中枢神经系统感染、Creutzfeldt-Jakob病等。
2.代谢性与中毒性脑病Wernicke脑病、肝性脑病、肺性脑病、肾性脑病等,青霉素类或者喹诺酮类等抗生素、化疗药物或者免疫抑制剂等引起的中毒性脑.病、放射性脑病等。
3.肿瘤性疾病颅内原发肿瘤,例如大脑胶质瘤病与原发CNS淋巴瘤等;颅内转移瘤。
4.神经系统遗传性或者变性病线粒体脑病或者线粒体脑肌病、甲基丙二酸血症、肾上腺脑白质营养不良、路易体痴呆、多系统萎缩、遗传性小脑变性等。
治疗自身免疫性脑炎的治疗包括免疫治疗、对癫zaozi001发作和精神症状的症状治疗、支持治疗、康复治疗等。
免疫治疗分为一线免疫治疗、二线免疫治疗和长程免疫治疗。
一线免疫治疗包括糖皮质激素、静脉免疫球蛋白和血浆置换。
二线免疫药物包括利妥昔单抗与静脉环磷酰胺,主要用于一线免疫治疗效果不佳的患者。
长程免疫治疗药物包括吗替麦考酚酯与硫唑嘌呤等,主要用于复发病例,也可以用于一线免疫治疗效果不佳的自身免疫性脑炎患者和肿瘤阴性的抗NMDAR脑炎患者。
抗NMDAR脑炎患者一经发现卵巢畸胎瘤,应尽快予以切除。
AE患者如果合并恶性肿瘤,应由相关专科进行手术、化疗与放疗等综合抗肿瘤治疗。
AE总体预后良好。
80%左右的抗NMDAR脑炎患者功能恢复良好,病死率2.9%~9.5%。
抗GABABR抗体相关脑炎合并小细胞肺癌者预后较差。
诊疗流程参见以下抗NMDAR脑炎。
抗NMDAR脑炎抗NMDAR脑炎是由抗NMDAR抗体介导的自身免疫性脑炎,是自身免疫脑炎的最主要类型。
临床表现1.儿童、青年多见,女性多于男性。
2.急性起病,多在2周至数周内达高峰。
病前可有发热和头痛等前驱症状。
缄默、/主要表现为精神行为异常、癫痫发作、近事记忆力下降、言语障碍3.昏迷、自主神经功能障碍等。
自主神经功能自主运动,意识水平下降/运动障碍/中枢性低通气低血压和中枢性发心动过缓、泌涎增多、障碍包括窦性心动过速、热等。
S局灶性损害的症状,例如复视、共济失调等。
辅助检查1.脑脊液检查腰穿脑脊液压力正常或者升高,超过300mmHO者少见。
脑26/L,脑脊液细胞学呈淋巴脊液白细胞数轻度升高或者正常,少数超过100×10细胞性炎症,可见浆细胞。
脑脊液蛋白轻度升高,脑脊液的寡克隆区带可呈阳性,脑脊液抗NMDAR抗体阳性。
2.头MRI多数患者头MRI无明显异常,或者仅有散在的皮质、皮质点片状FLAIR 高信号;部分患者可见边缘系统FLAIR和T2高信号,病灶分布可超出边缘系统的范围。
3.头FDG-PET/CT可见代谢异常,以双侧枕叶代谢明显减低为主要特点。
4.脑电图多呈弥漫或者多灶的慢波,偶尔可见癫痫波,异常δ刷是该病较特异性的脑电图改变,多见于重症患者。
5.肿瘤学卵巢畸胎瘤在青年女性患者中较常见。
中国女性抗NMDAR脑炎患者卵巢畸胎瘤的发生率为14.3%~47.8%。
卵巢超声和盆腔CT有助于发现卵巢畸胎瘤,卵巢微小畸胎瘤的影像学检查可以为阴性。
男性患者合并肿瘤者罕见。
诊断(图9-1)诊断标准:确诊的抗NMDAR脑炎需要符合以下3项(参考2016年Lancet Neurol标准):1.6项主要症状中的1项或者多项:①精神行为异常或认知障碍;②言语障碍;③癫zaozi001发作;④运动障碍/不自主运动;⑤意识水平下降;⑥自主神经功能障碍或中枢性低通气。
2.抗NMDAR抗体阳性建议以脑脊液CBA法抗体阳性为准。
若仅有血清标本可供检测,除了CBA结果阳性,还需要采用TBA与培养神经元进行IIF予以最终确认。
.3.合理地排除其他疾病病因。
治疗免疫治疗分为一线免疫治疗、二线免疫治疗和长程免疫治疗。
一线免疫治疗包括糖皮质激素、静脉免疫球蛋白和血浆置换。
二线免疫药物包括利妥昔单抗与静脉环磷酰胺等,主要用于一线免疫治疗效果不佳的患者。
长程免疫治疗药物包括吗替麦考酚酯与硫唑嘌呤等,主要用于复发病例,也可以用于一线免疫治疗效果不佳的患者和肿瘤阴性的抗NMDAR脑炎患者。
其他免疫治疗包括鞘内注射甲氨蝶呤与地塞米松等。
抗NMDAR脑炎患者一经发现卵巢畸胎瘤,应尽快予以切除(图9-2)。
脑炎综合征或者急性、亚急性起病的6个主症中的至少1个症状(参见诊断标准)抗体检测:转染细胞抗NMDAR()(,+脑脊液()无论血清+或者-)而脑脊液(血清(+-))血清抗体检测:大鼠海马与小脑组织+血清()-血清()脑炎NMDAR确诊抗脑炎NMDAR不能确诊抗图9-1 抗NMDAR脑炎诊疗流程图9-2 抗NMDAR抗体脑炎的免疫治疗程序抗LGI1抗体相关脑炎抗LGI1抗体相关脑炎由抗LGI1抗体介导,是自身免疫性边缘性脑炎的主要类型之一,病变以海马区受累为主,也可累及基底节区。