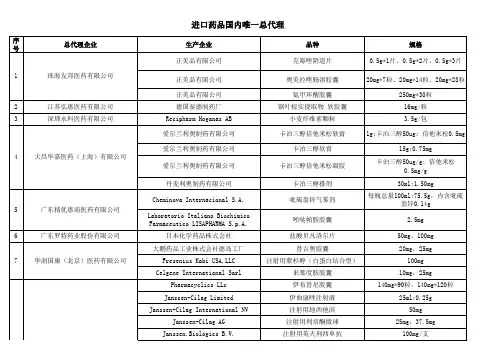
进口药品总代理名录
- 格式:xlsx
- 大小:23.86 KB
- 文档页数:12

名词定义一、采购平台:特指陕西省医疗机构药品集中采购平台,依托陕西省药械集中采购网(http:///),为全省医疗机构药品集中采购活动提供服务的综合性网络系统。
二、采购人:全省实施基本药物制度的基层医疗卫生机构,区级及区级以上人民政府、国有企业(含国有控股企业)等举办的非营利性医疗机构,和自愿参加陕西省医疗机构药品集中采购的其他医疗机构。
三、申报人:指参加药品集中采购活动的国内药品生产企业和进口药品总代理商。
国(境)外生产企业只能授权委托一家总代理,且是通关单上标明的报验单位或收货单位。
不接受以集团公司名义进行申报。
申报人只能授权一个自然人参加本次药品集中采购活动,并承担相应法律责任。
集团公司所属全资及控股子公司可共同委托一个自然人做为授权代表,其他自然人只能代表一个申报人参加本次药品集中采购活动。
四、配送企业:具务国家规定的配送资质和条件,向采购人提供药品配送及相关服务的药品经营企业。
五、入围品种目录:指通过竞价议价后,最终形成可供采购人选择的药品品种目录。
六、化合物实体专利药品:指国家食品药品监督管理总局网站药品注册相关专利信息公开公示中,可查询到的并在专利有效期的实用新型或工艺流程等专利药品。
七、实用新型或工艺流程等专利药品:指国家食品药品监督管理总局网站药品注册相关专利信息公开、公示中,可查询到的并在专利有效期的实用新型或工艺流程等专利药品。
八、国家科学技术奖药品:指2004年以来获得国家自然科学二等奖或国家科学技术进步二等奖及以上奖项的药品,不包括获得上述奖项的通用技术和其他通用研究成果的药品。
以国务院或科技部颁发的奖项证书为依据。
九、单独定价药品:指国家发展改革委或陕西省物价局公布的化学药及生物制品类单独定价药品。
十、优质优价中成药:指国家发展改革委或陕西省物价局公布的优质优价中成药。
十一、国家一类新药:指获得国家一类新药证书且国家食品药品监督管理局颁发的生产批件上注明一类新药的药品。

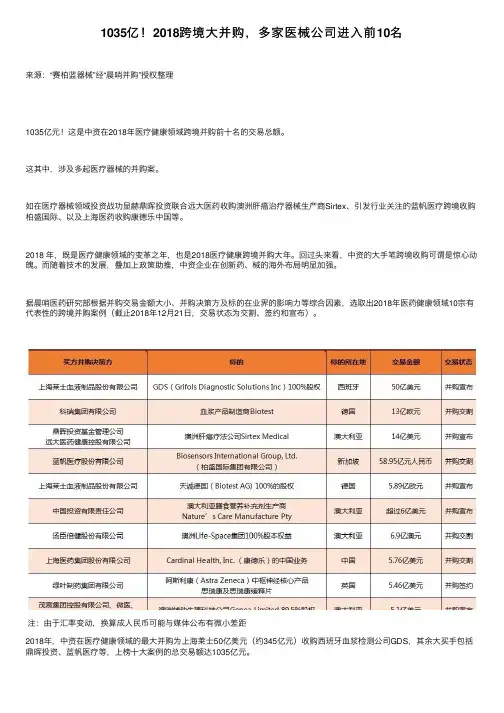
1035亿!2018跨境⼤并购,多家医械公司进⼊前10名来源:“赛柏蓝器械”经“晨哨并购”授权整理1035亿元!这是中资在2018年医疗健康领域跨境并购前⼗名的交易总额。
这其中,涉及多起医疗器械的并购案。
如在医疗器械领域投资战功显赫⿍晖投资联合远⼤医药收购澳洲肝癌治疗器械⽣产商Sirtex、引发⾏业关注的蓝帆医疗跨境收购柏盛国际、以及上海医药收购康德乐中国等。
2018 年,既是医疗健康领域的变⾰之年,也是2018医疗健康跨境并购⼤年。
回过头来看,中资的⼤⼿笔跨境收购可谓是惊⼼动魄。
⽽随着技术的发展,叠加上政策助推,中资企业在创新药、械的海外布局明显加强。
据晨哨医药研究部根据并购交易⾦额⼤⼩、并购决策⽅及标的在业界的影响⼒等综合因素,选取出2018年医药健康领域10宗有代表性的跨境并购案例(截⽌2018年12⽉21⽇,交易状态为交割、签约和宣布)。
注:由于汇率变动,换算成⼈民币可能与媒体公布有微⼩差距2018年,中资在医疗健康领域的最⼤并购为上海莱⼠50亿美元(约345亿元)收购西班⽛⾎浆检测公司GDS,其余⼤买⼿包括⿍晖投资、蓝帆医疗等,上榜⼗⼤案例的总交易额达1035亿元。
上海莱⼠ & 科瑞集团收购标的:GDS、天诚国际 & Biotest交易⾦额:391亿元 & 13亿欧元上海莱⼠(002252.SZ)在停牌近⼗个⽉后,抛出了近400亿的海外医药标的收购案,并勾勒出了⼀幅,通过⾏业整合实现⾎制品产业链全覆盖,带领中国⾎液制品⾛向世界的美好愿景。
11⽉,上海莱⼠称通过发⾏股份、⽀付现⾦或两者结合的⽅式,拟作价5.89亿欧元收购Biotest的母公司天诚德国,以及拟作价约50亿美元收购Grifols, S.A.(基⽴福)⼦公司Grifols Diagnostic Solutions Inc(GDS),两者合计价值约折为391亿元。
同时基⽴福在此次交易完成后,预计将成为上海莱⼠持股5%以上的股东,为上海莱⼠第⼆⼤股东。

精彩论坛-> 国外采购及买家信息共享-> 日本食品农产品进口商名录登录-> 注册-> 回复主题-> 发表主题fongken2006-08-25 09:01 日本综合贸易商社ALC。
INC。
地址:东京都中央区新川1-23-5SHINKAWA-EAST,1-23-5,SHINKAWA,CHUO-KU,TOKYOTel:0081-3-5541-2053 Fax:0081-3-5541-2140E-mail:*******************.jp社长:本村博志资本金:23,000万日元从业人数:175人设立:1979年1月业务内容:食品特色:消费物资输入各国(株)爱峰商会AIHOO TRADINGCO,LTD。
地址:奇玉县大宫市日进町3-493-23-493-2。
NISSHINCHO,OMIRA Tel:0081-48-668-5055 Fax:0081-48-668-1243社长:荻谷弘康复资本金:1,500万日元老派从业人数:4人设立:1983年6月业务内容:冷冻蔬菜等农业产业加工品特色:中国贸易的多年的业务经验有专业商社(株)葵源六甲AOLGEN-ROKKOCORP地址:京都府京都市南区久世高田町126Tel:0081-75-931-5525 Fax:0081-75-931-5584社长:杉山正义资本金:1000万日元老派从业人数:3人设立:1993年3月业务内容:食品青山贸易(株)http/AOYAMA TRADECO,LTD地址:兵车县姬路市青山14641464,AOYAMA,HIMEJI,HYOGOTel:0081-792-66-6035 Fax:0081-792-67—4624E-mail:aoyamaz@siluer.ocn.ne.jp社长:赵善云资本金:1000万日元从业人数:15人设立:1992年10月业务内容:化学品(株)本铺AKACHAN HONPOCO,LTD地址:大阪府大阪市中央区南本町3-3-213-3-21 MINAMI-HONMACHI,CHUO-KU,OSAKATel:0081-6-6251-0625 Fax:0081-6-6251-3340社长:小原正司资本金:19000万日元从业人数:2700人设立:1941年2月业务内容:进口生活用品及生产资料朝阳贸易(株)ASAHI TRADINGCO,LTD地址:东京都中央区八丁堀4-10-4 白铜第一HKUDODALLTLBLDG,4-10-4,HATTYOBORL,CHUO-KU,TOKYO Tel:0081-3-3351-0771 Fax:0081-3-3351-2344社长:华井满资本金:9600万日元从业人数:50人设立:1968年9月业务内容:原料羽毛,进出口食品原料及健康食品(株)亚细亚交易AJAKOEKICO,LTD地址:大分县别府市原町18-2418-24,HARA-MACHI,BEPPU,OITATel:0081-977-21-0888 Fax:0081-977-21-2048E-mail:******************.ne.jp社长:圜田展久资本金:2000万日元从业人数:3人设立:1972年5月业务内容:进口竹制品制药(株)ASGENPHARMACEUTICAL CO,LTDhttp/www.asgen.cojp地址:爱知县名古屋市东区泉2-28-22-28-2,IZUML,HLGASHI-KU,NAGOYATel:0081-52-9031-1212 Fax:0081-52-931-1331E-mail:**************.jp社长:水墅昌树资本金:1000万日元从业人数:60人设立:1968年1月业务内容:中药材,中成药,化工医药品,食品原料(株)甘栗太郎AMAGURITARO CO,LTD地址:东京都千代田区神田松永町1111,MATSUNAGACHO,KANDA,CHIYODA-KU,TOKYOTel:0081-3-3251-9021 Fax:0081-3-3251-9280社长:田中康则资本金:1280万日元从业人数:130人设立:1956年11月业务内容:天津甘栗(株)新井清太郎商店SEITARO ARAICO,LTD地址:神奈川县横浜市中区尾上町1-81-8,ONOE-CHO-NAKA-KU,YOKOHANATel:0081-45-681-6729 Fax:0081-45-662-2357社长:新井光世资本金:2000万日元从业人数:100人设立:1888年4月业务内容:香辛料,辣椒干,脱水蔬菜,植物生产品,柳腾制品,轻工品。

(株)汉药UCHIDA WAKANYAKU,LTD地址:东京都中央区日本桥本町4-2-84-2-8,HONCHO,NIHONBASHI,CHUO-KU,TOKYOTel:0081-3-3803-9656 Fax:0081-3-3806-1261社长:内田尚和资本金:18000万日元从业人数:220人设立:1952年7月业务内容:进口中国产生药,中国茶等,多种类(株)达藤商事ENDO TRADING CO,LTD地址:兵车县伊丹市山田4-7-284-7-28,YAMADA,ITAMITel:0081-727-83-6136 Fax:0081-727-77-1395社长:达藤资本金:1000万日元从业人数:9人设立:1968年10月业务内容:(进口)冷冻果菜,生鲜野菜,盐渍野菜,栗子,干柿,蜂蜜,肉缶诘及肉制品。
特色:食油食品,土畜产品,工芸品,输入业务大阪太洋物产(株)TALYO BUSSAN OSAKA CO,LTD地址:大阪府大阪市北区梅田1-2-2-1300PM 28 13F。
OSAKA EKIMAE DAINBLDG1-2-2-1300,UMEDA KITA-KU,OSAKATel:0081-6-6346-1531 Fax:0081-6-6346-0837社长:坂本良正资本金:5000万日元从业人数:15人设立:1988年4月业务内容:(进口)羊毛,食肉,野菜,食料品,缎通,石材,绵系,针织制品大西贤(株)http/www.jtr.or.jp/onishi/default.htmK.ONISHI&CO.,LTD地址:大阪府大阪市天王寺区东高津町9-279-27,HIGASHIKOZU-CHO,TENNOJI-KU,OSAKATel:0081-6-6764-5171 Fax:0081-6-6764-5181E-mail: **********************.jp社长:大西正夫资本金:3,000万日元从业人数:60人设立:1957年7月业务内容:(进口)服装,兽毛,毛皮,木制品,草柳藤制品,作业用手袋,帽子,食品,茶。

医药代理商名录1. 医药代理商的定义医药代理商是指在医药行业从事代理销售和推广的企业或个人。
他们作为中间人,连接生产厂商和医疗机构,通过销售药品、医疗器械和其他医药产品来获取利润。
2. 医药代理商的分类医药代理商可以根据其经营范围和形式进行分类。
2.1 地区代理商地区代理商是指在特定地区内代理销售和推广医药产品的企业或个人。
他们负责在特定地区内建立销售网络,招募销售代表,并与生产厂商合作,推动产品销售。
2.2 产品代理商产品代理商是指代理销售特定医药产品的企业或个人。
他们与生产厂商签订代理协议,负责销售和推广该产品,通常专注于某一领域或特定类型的产品。
2.3 进口代理商进口代理商是指代理进口医药产品的企业或个人。
他们与国外生产厂商合作,负责产品的进口、注册、销售和推广,通常具备丰富的国际贸易和药品注册经验。
2.4 特许经销商特许经销商是指代理某个品牌或特定系列产品的企业。
他们与品牌方签订特许经销协议,获得独家销售权,并负责推广和销售该品牌产品。
3. 医药代理商的重要性医药代理商在医药行业的分销链中扮演着重要角色,具有以下重要性:3.1 拓展市场医药代理商通过建立销售网络和渠道,帮助生产厂商将产品推向更广泛的市场。
他们可以在各个地区建立销售队伍,与医疗机构和药店建立合作关系,实现产品的广泛销售。
3.2 推广和营销医药代理商负责产品的推广和营销工作,通过举办学术会议、举办培训班、发布广告等方式,向医生、药店和患者介绍产品的特点和优势,从而提高产品的知名度和销量。
3.3 渠道管理医药代理商负责管理产品在各个销售渠道的供应和销售情况,确保产品能够及时供应给医疗机构和药店。
他们还负责收集市场反馈和销售数据,通过分析数据提供给生产厂商,帮助其制定销售策略和市场定位。
4. 医药代理商名录以下是一些著名的医药代理商名录:1.赛诺菲(Sanofi):赛诺菲是全球知名的医药代理商,拥有丰富的产品线,涵盖药品、疫苗和医疗器械等领域。

中药材是指药用植物、动物的药用部分,采收后经初加工形成的原料药材。
食药物质①是指传统作为食品,且列入《药典》的物质。
中药材(食药物质)进出境时,企业应当向主管海关申报预期用途,明确“药用”或者“食用”。
为便于表述,本节下文中“中药材(食药物质)”统称为“中药材”。
一、进口中药材申报为“药用”的进口中药材应为列入《药典》药材目录的物品。
进口药用的中药材由药品监督管理部门实施检验和检验监督管理。
海关依照《进出境中药材检疫监督管理办法》对进境药用的中药材实施检疫和检疫监督管理。
申报为“食用”的中药材应为法律、行政法规、规章、文件规定可用于食品的物品(即应当是已纳入《按照传统既是食品又是中药材的物质目录》②管理的物质)。
现行《按照传统既是食品又是中药材的物质目录》详见本节参考资料。
进口食药物质由海关依照进出口食品相关规定实施检验检疫和监督管理。
(一)资质要求1.准入要求:海关对进境中药材实施检疫准入制度。
2.境外生产企业注册登记海关总署对进出境中药材实施风险管理;对向境内输出中药材的境外生产、加工、存放单位(以下简称“境外生产企业”)实施注册登记管理。
海关总署根据风险分析的结果,确定需要实施境外生产、加工、存放单位注册登记的中药材品种目录。
海关总署对列入目录的中药材境外生产企业实施注册登记。
部分已注册的境外中药材生产企业可在海关总署网站查询:“新西兰输华鹿茸鹿角注册企业名单”可在海关总署动植物检疫司“企业信息”-“动物产品类”-“其他动物产品”栏目中查询;“希腊输华西红花注册企业名单”“老挝输华植物源性中药材注册企业名单”可在海关总署动植物检疫司“企业信息”-“植物产品类”-“其他植物产品”栏目中查询。
3.进境动植物检疫审批海关总署对进境中药材(动物源性中药材、植物源性中药材)实施检疫审批。
进境中药材需办理进境动植物检疫审批的,货主或者其代理人应当在签订贸易合同前,取得进境动植物检疫许可。
办理指南见本书第十三章第二节、第三节。


进口药品国内销售代理商备案规定进口药品国内销售代理商备案规定进口药品国内销售代理商是指《药品流通监督管理办法》(暂行)第五十一条所规定的直接与国外制药厂商订立进口药品国内销售代理协议的代理商,包括总代理、地区代理等。
这些代理商必须在与国外制药厂商签订国内销售代理协议2个月内办理备案手续。
办理备案手续,由进口药品国内销售代理商直接向国家药品监督管理局市场监督司提出,不得委托非本企业人员代为办理备案手续。
办理备案手续,需提交以下中文文件:⑴企业法定代表人授权经办人员办理备案的委托授权书(原件和复印件);⑵加盖本企业印章的许可证、营业执照(复印件)和进口药品注册证(原件和复印件);⑶本企业与国外制药厂商签订的进口药品国内销售委托代理协议及协议约定的进口药品名称、原产地、规格和数量(原件和复印件);⑷本企业详细通讯地址、邮政编码、电话(传真)、企业法定代表人姓名、职务。
国家药品监督局对上述文件审验后,将原件退还备案企业,复印件留存备查。
负责备案的人员,对可能涉及的企业商业保密,负有保密责任。
备案表格由国家药品监督管理局统一印制并统一编排序号。
备案登记表中的备案事项如有变更,必须在30天内办理变更手续。
办理变更手续,可由企业以加盖本企业印章的书面方式告知受理备案的部门。
进口药品国内销售代理商不履行备案手续从事进口药品国内销售代理活动的,药品监督管理部门将根据《药品流通监督管理办法》(暂行)第四十五条规定予以处罚;对备案事项中备案企业名称、代理销售药品的名称、代理销售药品的规格、协议代理销售药品的数量、代理销售药品的原产地及公司名称、进口药品注册证号、进口口岸名称这些项目的变更,不按时办理变更手续的,将根据《药品流通监督管理办法》(暂行)第四十七条规定处罚。
国家药品监督管理局确定进口药品国内销售代理商备案制度,目的是从强化国内药品市场监督管理出发,本着不增加企业负担的原则,从源头掌握和了解进口药品的情况,便于在监督工作中及时发现、及时查处进口药品中的违法行为。
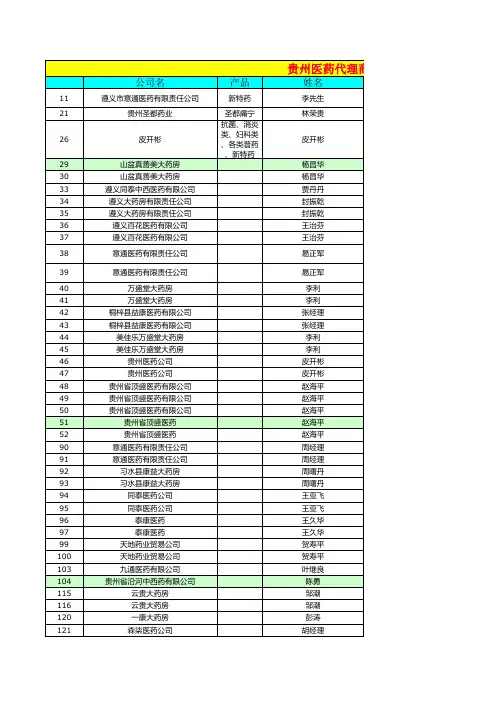
公司名称WEB奥格生物技术(上海)有限公司北海市康源生物工程有限责任公司北京艾格威科贸有限公司北京宝赛生物技术有限公司北京北方红豆杉生态科技有限责任公司北京博奥森生物技术有限公司北京博思拜生物技术有限公司北京东方红航天生物技术有限公司 北京东方瑞德生物技术有限公司北京金福腾科技有限公司北京金晔生物工程有限公司北京经科宏达生化试剂生物技术公司北京九隆升微生物资源开发有限公司北京具象科技发展有限公司北京康普递恩生物工程技术有限公司北京柯瑞生物工程有限公司北京科技桥技术开发有限公司北京六环美迪生物工程技术有限公司北京陆桥技术有限责任公司 北京迈胜普技术有限公司北京美迪科生物技术有限公司北京美联胚胎生物工程有限公司北京赛百盛生物工程公司北京三博远志生物技术有限责任公司北京桑普生物化学技术有限公司北京舒伯伟化工仪器有限责任公司北京望尔生物技术有限公司北京维通利华实验动物技术有限公司北京禹光生物科学研究中心有限公司北京中健高科研究所毕龙生物在线碧云天沧州市金箭明胶有限公司成都法玛基因科技有限公司成都拉克生物工程实业有限公司成都瑞翔生物技术有限公司大连普瑞康生物技术有限公司 大连卓尔高科技有限公司福建博特生物科技有限公司福建新大陆生物技术有限公司 广东三九生物降解塑料有限公司广东汕头市润科生物工程有限公司广州中田美生物基因工程有限公司哈尔滨三乐源生物工程集团股份有限公司海南泰利达海洋产业有限公司海南五和堂芦荟有限公司海泰克生物技术有限公司杭州桀舜生物科技有限公司杭州中肽生化有限公司 河北省阜城县京阜明胶有限公司河北省南和春熙生物工程有限责任公司河南百奥生物工程有限公司河南启明星生物技术有限公司 赫兹生物技术有限公司黑龙江强尔生物技术开发股份有限公司湖北畅响生物工程园有限公司湖北华工生化工程有限公司湖北裕峰生物工程有限公司湖南威恒生物技术有限公司湖南雅龙生物工程有限责任公司湖南尤特尔生化有限公司吉林省宏久参业科技股份有限公司吉林省蛙王生物工程有限公司济南鑫贝西生物技术有限公司 建德市华云化工有限公司 江门量子高科生物工程有限公司江苏南通康德生物制品有限公司江阴市立达海洋生物工程有限公司 金柚美洗护网昆明克别拉木生物工程有限公司昆明生宝生物技术有限公司兰州宝瑞生物技术有限公司兰州同健生物科技股份有限公司廊坊维尔康生物化工有限公司朗斯国际连锁机构洛阳市华健生物工程有限公司美国科恩国际有限公司美国科峻仪器公司美国美联科技有限公司美国普洛麦格公司北京办事处南京海泰纳米材料有限公司南京华龙生物反应器有限公司南京建成生物工程研究所南京南农高科技股份有限公司南京赛尔金生物医学有限公司南宁市世威生物工程有限责任公司南通双林生物制品有限公司 宁波市科瑞生物工程有限公司宁夏自然生物制品有限公司诺维信(中国)投资有限公司青岛海博生物技术有限公司青岛海泰生物技术有限公司青岛弘信海生生物工程有限公司青岛鹏洋科技发展有限公司驱蚊香草/北京高科中欧生物工程研究中心山东阿波罗集团有限公司 山东宝来利来生物工程股份有限公司山东黄河龙集团生物工程有限公司 山东临朐华元生物工程有限公司 山东临沂万业生物有限公司山东山松生物工程集团山东禹城环宇集团陕西百盛园生物科技信息有限公司陕西慧科植物开发有限公司陕西慧科植物开发有限公司上海百事得生物科技有限公司上海保兴生物设备工程有限公司上海博道基因技术有限公司上海博亚生物技术有限公司上海迪发酿造生物制品有限公司上海丰业生物科技发展有限公司上海复旦悦达生物技术有限公司上海复汇生物技术有限公司 上海复申科技实业有限公司上海皓嘉生物学前沿网站上海华舜生物工程有限公司 上海基康生物技术有限公司上海吉英生物科技有限公司上海交大昂立天然药物工程技术有限公司上海龙头生物技术有限公司上海天能科技有限公司上海纬群生物技术有限公司上海泽龙生物工程有限公司深圳百奥生物技术有限公司深圳慧通生物工程有限公司 深圳科润达生物工程公司深圳赛泰克生物科技有限公司深圳市津福美生物技术开发有限公司深圳市康百得生物科技有限公司深圳市赛泰克生物科技有限公司深圳市裕盛嘉实业有限公司生物试剂部深圳市中佳威生物技术有限公司沈阳昂宇高科技有限公司生物通科技有限公司石家庄市新泽兴化工有限公司四川龙蟒福生科技有限责任公司四川新客隆生物科技实业有限公司台湾基因科技股份有限公司<BIG5>台州市丰润生物化学有限公司唐山太博尔生物工程有限公司天津市生命科学应用研究所威海市海奥生物工程有限公司微芯生物基因表达谱芯片一站式解决方案温州市绿洁化学有限公司武汉(拜尔)生物技术有限公司武汉金丰生物环保制品有限公司武汉绿环生物技术有限公司(武汉成长动物营养研究所) 武汉市康欣生物科技有限责任公司武汉市银杏技术开发有限公司武汉武大天源生物工程有限公司武汉烯王生物工程有限公司西安交大开元生物科技发展有限公司 西安瑞克生物西安天行健天然生物制品有限公司西安中鑫生物技术有限公司厦门安普利生物工程有限公司协和华东干细胞基因工程有限公司 亚能生物技术(深圳)有限公司烟台市赋康苑生物工程有限公司简介新加坡奥格营养有限公司在中国设立的分公司,负责奥格营养公司所有产品在中国市场的推广。
广东省•港澳大湾区内地九市进口港澳药品医疗器械管理条例(草案修改稿征求意见稿)第一条【立法目的和依据】为了贯彻落实勺粤港澳大湾区发展规划纲要B,加强学港澳大湾区内地九市临床急需进口港澳药品侯疗器械管理,满足粤港澳大湾区居民用药用械需求,保障用药用械安全,保护和促进公众健康,根据6中华人民共和国药品管理法B《医疗器械监督管理条例》等有关法律、行政法规,结合本省实际,制定本条例。
第二条【适用范围】本条例适用于在粤港澳大湾区内地九市行政区域内临床急需进口港澳药品医疗器械的申请、采购、进口、配送、使用及其监督管理等活动。
本条例所称购港澳大湾区内地九市是指广州市、深圳市、珠海市、佛山市、惠州市、东莞市、中山市、江门市、肇庆市。
本条例所称临床急需进口港澳药品医疗器械(以下简称急需港澳药械)是指%港澳大湾区内地九市指定医疗机构使用临床急需、已在港澳上市的药品,以及使用临床急需、港澳公立医院已采购使用、具有临床应用先进性的医疗器械。
急需港澳药械的申请、采购、进口、配送、使用以及监督管理除应当遵守本条例规定外,还应当遵守药品、医疗器械管理其他相关法律法规的规定。
第三条【政府职责】省和粤港澳大湾区内地九市人民政府对本行政区域内急需港澳药械监督管理工作负贡,统一领导、组织、协调本行政区域内的急需港澳药械监督管理工作以及突发事件应对工作,建立健全省、市人民政府及有关部门密切协作的监督管理工作机制和信息共享机制。
第四条【部门职责】省和粤港澳大湾区内地九市人民政府药品监督管理部门负责本行政区域内的急需港测药械监督管理工作.省和明港澳大湾区内地九市人民政府R生健康主管部门负在本行政区域内的急需港澳药械使用行为监督管理工作。
省和粤港澳大湾区内地九市人民政府医疗保障部门负责本行政区域内的急需港澳药械医疗服务价格项目监督管理工作。
省和粤港澳大湾区内地九市人民政府发展改革、财政、商务、市场监督管理、中医药以及海关等有关部门在各自职贵范困内做好急需港澳药械监督管理相关工作。