化工原理-蒸馏
- 格式:ppt
- 大小:541.52 KB
- 文档页数:75


化工原理蒸馏
蒸馏是一种重要的化工分离方法,利用物质的不同挥发性使其分离纯化。
蒸馏过程中,液体组分根据其挥发性差异在加热的条件下先蒸发,然后再经过冷凝回收成液体。
在蒸馏过程中,会产生不同的馏分,从而实现物质的分离和纯化。
在蒸馏中,首先将混合物加热至使其中的较易挥发组分蒸发并进入冷凝器,然后通过冷却将其转化为液体并收集。
而不易挥发的组分则在蒸馏瓶中富集,进一步提高纯度。
这样通过连续蒸发和冷凝,直到从混合物中逐渐分离出所需的纯组分。
蒸馏技术在石油、化工、制药等领域具有广泛的应用。
例如在石油炼制过程中,原油经过初次蒸馏分离得到不同沸点范围的馏分,例如天然气、汽油、柴油、液化石油气等。
而在制药过程中,蒸馏被用来纯化药物原料以去除杂质。
蒸馏的效率取决于诸多因素,包括温度、压力、液体性质和设备设计等。
不同的物质对于温度和压力的要求也不同,因此需要根据实际情况进行调整。
同时,蒸馏设备的设计也会影响蒸馏效率,例如塔板和填料的选择。
总之,蒸馏是一种重要的化工分离技术,能够实现混合物中的组分分离和纯化。
它在石油、化工、制药等领域具有广泛应用,并且可以根据具体情况进行调整以达到最佳效果。


第六章蒸馏蒸馏定义:蒸馏分类:易挥发组分难挥发组分有回流蒸馏(精馏)无回流蒸馏:简单蒸馏(间歇操作)平衡蒸馏(连续操作)特殊蒸馏:萃取蒸馏、恒沸蒸馏按操作压力可分为加压、常压和减压蒸馏两组分精馏和多组分精馏第一节双组分溶液的气液相平衡一、溶液的蒸汽压与拉乌尔定律纯组分的蒸汽压与温度的关系:拉乌尔定律:在一定温度下,理想溶液上方气相中任意组分的分压等于纯组分在该温度下的饱和蒸气压与它在溶液中的摩尔分数的乘积。
p=p A0x AA(6-2)p=p B0x B=p B0(1-Bx) (6-3)A式中p A、p B——溶液上方A,B组分的平衡分压,Pa;p0——在溶液温度下纯组成的饱和蒸汽压,随温度而变,其值可用安托尼(Antoine)公式计算或由相关手册查得,Pa;x、x B——溶液中A,B组分的摩尔分数。
A二、理想溶液气液平衡(一)t-y-x图1.沸点-组成图(t- x- y图)(1)结构以常压下苯-甲苯混合液t- x- y图为例,纵坐标为温度t,横坐标为液相组成x A和汽相组成y A(x,y均指易挥发组分的摩尔分数)。
下曲线表示平衡时液相组成与温度的关系,称为液相线,上曲线表示平衡时汽相组成与温度的关系,称为汽相线。
两条曲线将整个t- x- y图分成三个区域,液相线以下称为液相区。
汽相线以上代表过热蒸汽区。
被两曲线包围的部分为汽液共存区。
t- x- y图数据通常由实验测得。
对于理想溶液,可用露点、泡点方程计算。
(2)应用在恒定总压下,组成为x,温度为t1(图中的点A)的混合液升温至t2(点J)时,溶液开始沸腾,产生第一个汽泡,相应的温度t2称为泡点,产生的第一个气泡组成为y1(点C)。
同样,组成为y、温度为t4(点B)的过热蒸汽冷却至温度t3(点H)时,混合气体开始冷凝产生第一滴液滴,相应的温度t3称为露点,凝结出第一个液滴的组成为x1(点Q)。
F、E两点为纯苯和纯甲苯的沸点。
图苯-甲苯物系的t- x- y图图苯-甲苯物系的y- x图应用t- x- y图,可以求取任一沸点的气液相平衡组成。

化工原理6蒸馏1. 简介蒸馏是一种常用的分离技术,特别适用于液体混合物的分离。
在化工工业中,蒸馏被广泛应用于石油炼制、化学品生产、药品制造等领域。
本文将介绍蒸馏的原理、工艺和常见设备。
2. 蒸馏的原理蒸馏的原理基于不同物质的沸点不同。
蒸馏过程中,液体混合物被加热至其中物质的沸点,使其蒸发,并在蒸馏塔内上升。
然后,蒸汽与冷凝器中的冷却介质接触,将蒸汽重新变为液体,实现分离。
较挥发性的物质将优先蒸发,而较不挥发性的物质较晚蒸发。
3. 蒸馏的工艺蒸馏的工艺包括以下几个步骤:3.1 加热液体混合物首先,将液体混合物加热至其中物质的沸点。
加热可以使用多种方式,如蒸汽加热、火焰加热或电加热。
3.2 蒸发当液体混合物被加热至其中物质的沸点时,液体开始蒸发,生成蒸汽。
蒸汽随后在蒸馏塔内上升。
3.3 冷凝蒸汽在蒸馏塔顶部进入冷凝器,与冷凝介质接触,冷凝成液体。
冷凝过程中,将产生副产物和所需产品。
3.4 分离通过不同组分的沸点差异,液体混合物在冷凝过程中实现分离。
较挥发性的物质先冷凝,较不挥发性的物质则较晚冷凝。
3.5 收集产品经过分离后,所需产品被收集。
副产物通常会单独收集和处理。
4. 蒸馏设备蒸馏设备是实现蒸馏过程的关键。
常见的蒸馏设备包括以下几种:4.1 蒸馏塔蒸馏塔是蒸馏过程中最重要的设备之一。
它通常由一个筒体和多个板或填料组成。
液体混合物从塔底部进入,通过逐个板或填料的交替进行蒸发和冷凝。
这种连续的蒸发和冷凝过程最终实现了分离。
4.2 冷凝器冷凝器用于将蒸汽冷凝为液体。
它通常由管道和冷却介质组成,如水或空气。
冷凝器可以采用不同的结构,如冷却管、换热器或冷凝室。
4.3 加热器加热器用于加热液体混合物,将其加热至其中物质的沸点。
加热器可以采用不同的形式,如蒸汽加热器、电加热器或火焰加热器。
4.4 分离精馏塔分离精馏塔是一种特殊的蒸馏设备,用于实现高效的分离。
它通常由多个塔板或填料层组成,可以通过不同的蒸馏段和冷凝器段实现精馏。
第六章 蒸 馏1、质量分数与摩尔分数的相互换算:(1) 甲醇-水溶液中,甲醇(CH 3OH )的摩尔分数为0.45,试求其质量分数。
(2) 苯-甲苯混合液中,苯的质量分数为0.21,试求其摩尔分数。
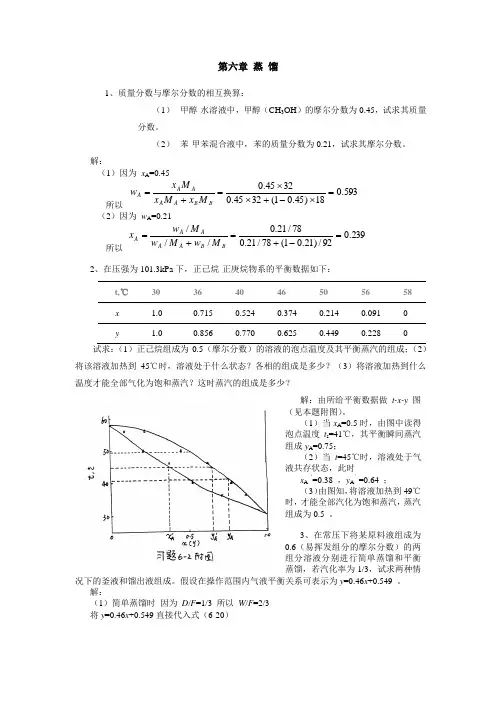
解:(1)因为 x A =0.45所以(2)因为 w A =0.21所以2、在压强为101.3kPa 下,正己烷-正庚烷物系的平衡数据如下:t,℃ 30 36 40 46 50 56 58 x 1.0 0.715 0.524 0.374 0.214 0.091 0 y1.00.8560.7700.6250.4490.228试求:(1)正己烷组成为0.5(摩尔分数)的溶液的泡点温度及其平衡蒸汽的组成;(2)将该溶液加热到45℃时,溶液处于什么状态?各相的组成是多少?(3)将溶液加热到什么温度才能全部气化为饱和蒸汽?这时蒸汽的组成是多少?解:由所给平衡数据做t-x-y 图(见本题附图)。
(1)当x A =0.5时,由图中读得泡点温度t s =41℃,其平衡瞬间蒸汽组成y A =0.75;(2)当t =45℃时,溶液处于气液共存状态,此时x A ‘=0.38 ,y A ’=0.64 ; (3)由图知,将溶液加热到49℃时,才能全部汽化为饱和蒸汽,蒸汽组成为0.5 。
3、在常压下将某原料液组成为0.6(易挥发组分的摩尔分数)的两组分溶液分别进行简单蒸馏和平衡蒸馏,若汽化率为1/3,试求两种情况下的釜液和馏出液组成。
假设在操作范围内气液平衡关系可表示为y =0.46x +0.549 。
解:(1)简单蒸馏时 因为 D /F =1/3 所以 W /F =2/3 将y =0.46x +0.549直接代入式(6-20)593.018)45.01(3245.03245.0=⨯-+⨯⨯=+=B B A A AA A Mx Mx M x w 239.092/)21.01(78/21.078/21.0///=-+=+=B B A A A A A M w M w M wx解之x w =0.498由式(6-22)其中所以 (2)平衡蒸馏时 由Fx F =Dy +Wx得与y =0.46x +0.549 联立求解,得到x =0.509 ,y =0.7834、在连续精馏塔中分离由二硫化碳和四氯化碳所组成的混合液。



化工原理蒸馏
蒸馏是一种常用的分离技术,在化工工艺中广泛应用。
它通过利用液体混合物的不同沸点差异,将液体混合物分离成组成相对纯净的组分。
蒸馏过程中,液体混合物首先被加热至使得其中组分开始蒸发。
蒸气进入蒸馏塔,通过与冷凝在塔顶的冷却介质接触,发生冷凝,而后与塔内回流液体混合物进行质量和热量的交换。
这种热量和质量的交换使得高沸点组分向下方下降,而低沸点组分则向上升腾。
在蒸馏塔的上部,收集到的冷凝液体称为顶产物,中间的蒸馏液称为塔底产物。
通过逐步加热混合物,我们可以连续地收集不同沸点组分,并达到分离的目的。
在进行蒸馏操作时,需要考虑几个重要因素。
首先是选择适当的塔设计。
蒸馏塔的设计取决于混合物的性质和所需分离的组分。
其次是控制好供热的方式和力度,以确保达到适当的沸点差,使得分离过程更为高效。
此外,在实际操作过程中,还需要对蒸馏塔进行不断的操作和参数调整,以达到最佳的分离效果。
蒸馏作为一种常用的分离技术,在石油、化工等行业得到广泛应用。
通过蒸馏可以分离出石油中的汽油、柴油等燃料,也可以分离出化学反应中产生的不同组分。
不仅如此,蒸馏还可用于酒精的提取、水的纯化等领域。
总之,蒸馏是一种重要的分离技术,通过利用液体混合物的沸点差异,实现组分的有效分离。
在化工工艺中的广泛应用使得蒸馏具有重要的实际意义和理论价值。


化工原理学–蒸馏引言蒸馏是化工过程中常用的一种分离技术,通过对混合物进行加热使其产生蒸汽,再将蒸汽冷凝得到纯净物质的方法。
在化工领域,蒸馏广泛应用于石油和化学工业中,用于分离液体混合物中的组分。
蒸馏原理蒸馏是基于物质的不同沸点而进行的分离技术。
在一种混合物中,不同成分具有不同的沸点,通过加热可以将低沸点成分转变为蒸汽,然后再通过冷凝将蒸汽转变为液体,从而实现纯度较高的分离。
在蒸馏过程中,需要一个蒸馏塔来进行操作。
蒸馏塔通常由一个加热器、塔板和冷凝器组成。
混合物首先被加热,在塔板上产生蒸汽。
蒸汽在塔板上与冷凝液进行接触,使其冷凝并收集。
这样,高沸点成分留在塔板上,而低沸点成分则以蒸汽的形式进入上层。
通过逐层重复这个过程,可以实现对混合物中各成分的分离。
蒸馏的分类蒸馏可以根据不同的条件和原理进行分类。
常见的蒸馏方法包括常压蒸馏、减压蒸馏、真空蒸馏等。
1.常压蒸馏:常压蒸馏是在常压条件下进行的蒸馏过程。
常压蒸馏适用于沸点较低的液体混合物,其中低沸点成分可以轻松转化为蒸汽。
2.减压蒸馏:减压蒸馏是在降低环境压力的条件下进行的蒸馏过程。
通过降低环境压力,可以使高沸点成分在较低温度下转化为蒸汽,从而减少热量的需求。
3.真空蒸馏:真空蒸馏是在低于大气压的条件下进行的蒸馏过程。
真空蒸馏适用于高沸点液体或易分解的物质,可以避免在较高温度下进行加热,从而减少热敏感成分的损失。
蒸馏的应用蒸馏作为一种常用的分离技术,广泛应用于石油炼制、化学工业、食品工业等领域。
1.石油炼制:蒸馏在石油炼制过程中起到了至关重要的作用。
通过蒸馏,可以将原油中的各种成分分离出来,例如汽油、柴油、润滑油和残渣等。
这种蒸馏过程被称为石油精馏。
2.化学工业:在化学工业中,蒸馏被广泛用于分离和纯化化学品。
例如,通过蒸馏可以从反应产物中分离出目标产品,并去除杂质。
3.食品工业:蒸馏也在食品工业中得到应用。
例如,酿酒过程中的蒸馏可以用于分离酒精和水,从而提高酒精的浓度。
第六章蒸馏蒸馏定义:蒸馏分类:易挥发组分难挥发组分有回流蒸馏(精馏)无回流蒸馏:简单蒸馏(间歇操作)平衡蒸馏(连续操作)特殊蒸馏:萃取蒸馏、恒沸蒸馏按操作压力可分为加压、常压和减压蒸馏两组分精馏和多组分精馏第一节双组分溶液的气液相平衡一、溶液的蒸汽压与拉乌尔定律纯组分的蒸汽压与温度的关系:拉乌尔定律:在一定温度下,理想溶液上方气相中任意组分的分压等于纯组分在该温度下的饱和蒸气压与它在溶液中的摩尔分数的乘积。
pA=p A0x A(6-2)pB=p B0x B=p B0(1-xA) (6-3)式中p A、p B——溶液上方A,B组分的平衡分压,Pa;p0——在溶液温度下纯组成的饱和蒸汽压,随温度而变,其值可用安托尼(Antoine)公式计算或由相关手册查得,Pa;xA、x B——溶液中A,B组分的摩尔分数。
二、理想溶液气液平衡(一)t-y-x图1.沸点-组成图(t- x- y图)(1)结构以常压下苯-甲苯混合液t- x- y图为例,纵坐标为温度t,横坐标为液相组成x A和汽相组成y A(x,y均指易挥发组分的摩尔分数)。
下曲线表示平衡时液相组成与温度的关系,称为液相线,上曲线表示平衡时汽相组成与温度的关系,称为汽相线。
两条曲线将整个t- x- y图分成三个区域,液相线以下称为液相区。
汽相线以上代表过热蒸汽区。
被两曲线包围的部分为汽液共存区。
t- x- y图数据通常由实验测得。
对于理想溶液,可用露点、泡点方程计算。
(2)应用在恒定总压下,组成为x,温度为t1(图中的点A)的混合液升温至t2(点J)时,溶液开始沸腾,产生第一个汽泡,相应的温度t2称为泡点,产生的第一个气泡组成为y1(点C)。
同样,组成为y、温度为t4(点B)的过热蒸汽冷却至温度t3(点H)时,混合气体开始冷凝产生第一滴液滴,相应的温度t3称为露点,凝结出第一个液滴的组成为x 1(点Q)。
F 、E 两点为纯苯和纯甲苯的沸点。
图 苯-甲苯物系的t - x - y 图 图 苯-甲苯物系的y - x 图应用t - x - y 图,可以求取任一沸点的气液相平衡组成。