[化学]诱导效应理论突破
- 格式:doc
- 大小:17.00 KB
- 文档页数:2


![[化学]诱导效应理论突破](https://uimg.taocdn.com/5d81b54b312b3169a451a469.webp)
中公教育·给人改变未来的力量公考资讯早知道、 公考咨询交流、 公考资料获取, 尽在河南中公网站 为了帮助大家更好的备战河南教师招聘学科知识与教学能力,河南教师招聘考试网讲师整理了河南教师招聘各学科知识的备考资料,希望对大家备考河南教师招聘学科知识科目有所帮助诱导效应理论突破诱导效应理论在有机化学中是一个非常重要的理论,它在研究有机化合物的结构、有机反应机理和有机合成中起很重要的作用。
1.概念诱导效应是指在有机分子中引入一原子或原子团后,可使分子中成键电子云密度分布发生变化,这种变化不仅发生在直接相连的部分,而且沿着分子链影响整个分子的电子云密度分布。
这种因某一原子或原子团的电负性,而引起分子中σ键电子云分布发生变化,进而引起分子性质发生变化的效应叫做诱导效应。
2.特点电子云偏移沿着σ键传递,并随着碳链的增长而减弱或消失。
例如,CH3CH2CH2COOH 是弱酸,该分子中的α-碳原子上引入一个电负性比氢强的氯原子后,能使整个分子的电子云向氯原子偏移,结果增强了羟基中氢原子的质子化,使一氯醋酸成为强酸。
但是,在Y 原子引入一个氯原子后,对-COOH 的影响就可以忽略不计了。
3.规律比较各种原子或原子团的诱导效应时,常以氢原子为标准。
吸引电子能力(电负性较大)比氢原子强的原子或原子团(如—X 、—OH 、—NO2、—CN 等)有吸电子的诱导效应,整个分子的电子云偏向取代基。
吸引电子的能力比氢原子弱的原子或原子团(如烷基)具有给电子的诱导效应,整个分子的电子云偏离取代基。
在诱导效应中,一般用箭头“→”表示电子移动的方向,表示电子云的分布发生了变化。
诱导效应是一种短程的电子效应,一般隔三个化学键影响就很小了。
诱导效应只改变键内电子云密度分布,而不改变键的本性。
在分子中各相邻的共价键上以静电诱导方式引起的各价电子对的偏移(σ键电子的偏移)。
具有吸电子的诱导效应原子或原子团的相对强度如下: 对同族元素:-F>-Cl>-Br>-I中公教育·给人改变未来的力量公考资讯早知道、 公考咨询交流、 公考资料获取, 尽在河南中公网站对同周期元素:-F>-OR>-NR2具有给电子的诱导效应的原子团主要是烷基,其相对强度如下:【参考答案】1.按照给电子诱导效应的大小排列为(3)>(1)>(4)>(2)。

诱导效应目录[隐藏]概述简史诱导效应的产生诱导效应的递降率诱导效应指数番茄叶挥发性物质诱导效应[编辑本段]概述诱导效应是指在有机分子中引入一原子或基团后,使分子中成键电子云密度分布发生变化,从而使化学键发生极化的现象,称为诱导效应(Inductive Effects)。
在有机化合物分子中,由于电负性不同的取代基(原子或原子团)的影响,使整个分子中的成键电子云密度向某一方向偏移,使分子发生极化的效应,叫诱导效应。
诱导效应的特征是电子云偏移沿着ζ键传递,并随着碳链的增长而减弱或消失。
例如,醋酸是弱酸(pKi=4.76),醋酸分子中的α-碳原子上引入一个电负性比氢强的氯原子后,能使整个分子的电子云向氯原子偏移,结果增强了羟基中氢原子的质子化,使一氯醋酸成为强酸(pKi=2.86,酸性比醋酸强)。
比较各种原子或原子团的诱导效应时,常以氢原子为标准。
吸引电子能力(电负性较大)比氢原子强的原子或原子团(如—X、—OH、—NO2、—CN等)有吸电子的诱导效应(负的诱导效应),用-I表示,整个分子的电子云偏向取代基。
吸引电子的能力比氢原子弱的原子或原子团(如烷基)具有给电子的诱导效应(正的诱导效应),用I表示,整个分子的电子云偏离取代基。
在诱导效应中,一般用箭头“→”表示电子移动的方向,表示电子云的分布发生了变化。
诱导效应是一种短程的电子效应,一般隔三个化学键影响就很小了。
诱导效应只改变键内电子云密度分布,而不改变键的本性。
在分子中各相邻的共价键上以静电诱导方式引起的各价电子对的偏移(ζ 键电子的偏移)。
诱导效应在有机化学中是一个非常重要的理论,它在研究有机化合物的结构、有机反应机理和有机合成中起很重要的作用。
[编辑本段]简史1923年G.N.路易斯首先提出取代基团吸引或释放电子的作用可以在整个分子中的各键上引起价电子对移动的概念。
C.K.英戈尔德等将常见的基团和原子排列成一个诱导效应强弱的定性序列。
还有不少科学工作者根据化合物的物理化学性质、反应平衡常数和速率常数等方面的大量实验结果,提出了各种基团特性常数,以定量或半定量地表达基团的诱导效应强弱。

⾼中化学竞赛-电⼦效应⾼中化学奥林匹克竞赛辅导元素电负性表电⼦效应电⼦效应分为诱导效应、共轭效应、超共轭效应、场效应。
⼀、诱导效应诱导效应是电⼦效应的⼀种,是由路易斯⾸先提出的。
诱导效应是指在有机化合物分⼦中由于原⼦的电负性差异,导致σ键电⼦的移动,使分⼦中的电⼦云密度分布发⽣变化。
这种因分⼦中原⼦或基团的极性(电负性)不同⽽引起成键电⼦对向电负性⼤的⽅向移动的现象称为诱导效应,其特点是能沿分⼦链传递且迅速减弱。
如氯丁烷分⼦中,取代在碳原⼦上的氯原⼦的电负性较强,C-Cl键产⽣偶极,使与氯原⼦连接的第⼀个碳原⼦(α–C)产⽣部分正电荷(δ+),也使第⼆个碳原⼦(β-C)带有部分正电荷,第三个碳原⼦(γ-C)带有部分更少的正电荷,依次影响下去。
这种影响的特征是沿着碳链传递,随着碳链的增长⽽迅速减弱,⼀般传递到第三个碳原⼦这种影响就忽略不计了。
(其中δ表⽰微⼩,δδ表⽰更微⼩,依次类推)诱导效应是⼀种静电作⽤,共⽤电⼦并不能完全转移到另⼀原⼦上,只是电⼦云密度分布发⽣变化,即键的极性发⽣变化。
由极性键所表现出的诱导效应称作静态诱导效应( Is),⽽在化学反应过程中由于外电场(如溶剂、试剂)的影响⽽产⽣键的极化称作动态诱导效应(Id)。
实验测得原⼦或基团的吸电⼦能⼒顺序为:1.吸电⼦诱导效应(–I)和给电⼦诱导效应(+I)静态诱导效应通常采⽤烷烃H-CR3上的氢作为⽐较标准,规定其为0。
如果⽤电负性较碳原⼦⼩的Y取代了H-CR3上的氢原⼦,化合物Y-CR3中-CR3部分的电⼦云密度⽐H-CR3中⼤,Y 叫做给电⼦基团。
由给电⼦基团引起的诱导效应叫做给电⼦诱导效应(+I)。
如果⽤电负性较碳原⼦⼤的X取代了H-CR3上的氢原⼦后,化合物X-CR3中-CR3部分的电⼦云密度⽐在H-CR3中的⼩,X叫做吸电⼦基团。
由吸电⼦基团引起的诱导效应叫做吸电⼦诱导效应(–I)。
2.吸电⼦诱导效应(–I)和给电⼦诱导效应(+I)的相对强度静态诱导效应的强弱与取代基或原⼦的电负性强弱相关。
![[转载]关于基团在诱导效应和共轭效应中的给电子或吸电子效应](https://uimg.taocdn.com/a491d4fcf9c75fbfc77da26925c52cc58bd690f1.webp)
[转载]关于基团在诱导效应和共轭效应中的给电⼦或吸电
⼦效应
原⽂地址:关于基团在诱导效应和共轭效应中的给电⼦或吸电⼦效应作者:有机化学
1、诱导效应中针对基团或原⼦与C连接时电负性的⼤⼩、电⼦的转移⽅向,可分为吸电⼦诱导和给电⼦诱导。
⼀般情况下,烷基及环烷烃基团表现出给电⼦的诱导效应,H的诱导规定为零,其余基团基本上都表现为吸电⼦的诱导效应。
2、在共轭效应中,也可根据共轭体系内电⼦的转移⽅向分为给电⼦共轭和吸电⼦共轭。
⼀般情况下,表现为邻对位定位的基团主要体现了给电⼦的共轭效应,⽽间位定位基则主要都表现出了吸电⼦的共轭效应。
3、对于某些基团来说,其共轭与诱导的给与吸是⼀致的。
⽐如+I的烷基与环烷基,其共轭也为+C,表现为—I的间位定位基,其共轭效应也为—C。
4、⽽对于另外⼀些基团⽽⾔,其诱导与共轭对电⼦的推移⽅向刚好相反。
如除+I的基团外,其余的第⼀类定位基,都表现为—I,但他们的共轭却为+C。
并且除卤素基团外,都是+C效应⼤于—I。

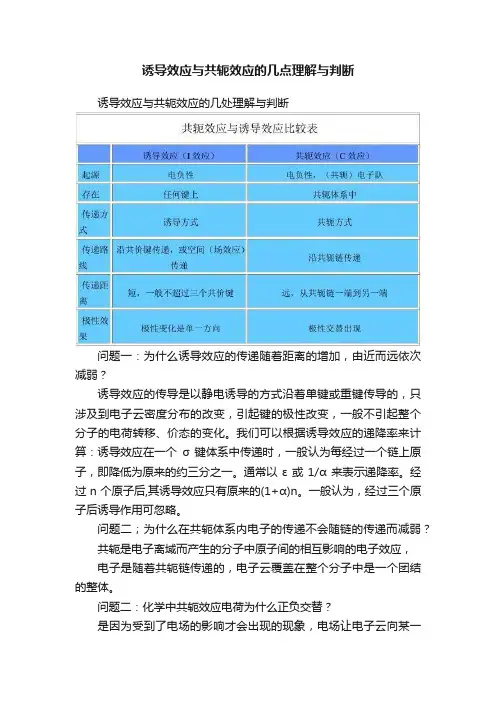
诱导效应与共轭效应的几点理解与判断诱导效应与共轭效应的几处理解与判断问题一:为什么诱导效应的传递随着距离的增加,由近而远依次减弱?诱导效应的传导是以静电诱导的方式沿着单键或重键传导的,只涉及到电子云密度分布的改变,引起键的极性改变,一般不引起整个分子的电荷转移、价态的变化。
我们可以根据诱导效应的递降率来计算:诱导效应在一个σ 键体系中传递时,一般认为每经过一个链上原子,即降低为原来的约三分之一。
通常以ε或1/α来表示递降率。
经过n个原子后,其诱导效应只有原来的(1+α)n。
一般认为,经过三个原子后诱导作用可忽略。
问题二;为什么在共轭体系内电子的传递不会随链的传递而减弱?共轭是电子离域而产生的分子中原子间的相互影响的电子效应,电子是随着共轭链传递的,电子云覆盖在整个分子中是一个团结的整体。
问题二:化学中共轭效应电荷为什么正负交替?是因为受到了电场的影响才会出现的现象,电场让电子云向某一方向偏移,那么就会产生一边显正电荷一边显负电荷的现象。
问题三:在有机化学反应中如何区分和比较出诱导效应与共轭效应?首先要明确在一个共轭体系中,一般情况下诱导和共轭是同时存在的。
共轭是指由于原子间电负性不同,引起分子中电子密度分布的不均衡,通过共轭π键传递,而且不论距离远近,其作用贯穿整个共轭体系中,这样所产生的电子效应。
诱导是由于原子或基团电负性的影响沿着分子中的键传导,引起分子中电子云按一定方向转移或键的极性通过键链依次诱导传递的效应。
它们的区别是共轭效应起因于电子的离域,而不仅是极性或极化的效应。
共轭效应只存在于共轭体系中,不象诱导效应那样存在于一切键中。
诱导效应是由于键的极性或极化性沿σ键传导,而共轭效应则是通过π电子的转移沿共轭链传递,是靠电子离域传递;共轭效应的传导可以一直沿着共轭键传递而不会明显削弱,不象诱导效应削弱得那么快,取代基相对距离的影响不明显,而且共轭链愈长,通常电子离域愈充分,体系能量愈低愈稳定,键长平均化的趋势也愈大。

诱导效应和共轭效应的异同点诱导效应和共轭效应是有机化学中两个重要的概念。
它们都涉及到分子的极性和电荷分布。
在本文中,我们将探讨这两种效应的异同点。
异同点之一:定义诱导效应是一个原子或基团中的电子云受到相邻原子或基团的极性影响而发生的电荷重分布。
这种电荷分布可以使分子的极性增强或减弱。
共轭效应是与分子中的共轭键有关的一种电子重分布效应。
共轭键之间的电子云可以通过共轭效应的作用而增强或减弱。
异同点之二:原理诱导效应可以通过分子中的原子或基团之间的极性相互作用来解释。
当一个原子或基团中的电子云被一个邻近原子或基团的极性所影响时,它会偏向那个极性,导致电荷分布的不均匀。
共轭效应涉及到分子中的共轭键,这些键中的电子云可以相互作用并重分布,形成一种共轭体系。
这种重分布可以通过一系列的化学反应来解释。
异同点之三:影响诱导效应可以影响分子的物理性质和化学反应性。
这种效应可以增加或减少分子的极性,从而影响分子的溶解度和反应速率。
共轭效应可以增强或减弱共轭键中的双键性质。
这种效应可以影响分子的化学反应性、光学性质和电子结构。
异同点之四:实际应用诱导效应和共轭效应在有机合成和分析化学中有着广泛的应用。
许多化学反应中都涉及到这些效应,因此了解这些效应对于理解和预测反应机理是非常重要的。
在有机合成中,这些效应可以用来控制反应中的化学反应性和选择性。
在分析化学中,这些效应可以用来确定分子的结构和检测分子中的化学反应性。
综上所述,诱导效应和共轭效应是有机化学中的两个重要概念。
它们在定义、原理、影响和实际应用方面都有所不同,但都对有机化学的研究和应用产生了深远的影响。


共轭效应是指两个以上双键(或三键)以单键相联结时所发生的电子的离位作用。
英戈尔德,C.K.称这种效应为仲介效应,并且认为,共轭体系中这种电子的位移是由有关各原子的电负性和p 轨道的大小(或主量子数)决定的。
据此若在简单的正常共轭体系中发生以下的电子离位作用:(例如:CH2 CH—CH CH2、CH2 CH—CH O)。
Y 原子的电负性和它的p 轨道半径愈大,则它吸引电子的能力也愈大,愈有利於基团—X Y从基准双键A B—吸引电子的共轭效应(如同右边的箭头所示)。
与此相反,如果A原子的电负性和它的p 轨道半径愈大,则它释放电子使其向Y 原子移动的能力愈小,愈不利於向—X Y基团方向给电子的共轭效应。
中间原子B 和X 的特性也与共轭效应直接相关。
诱导效应是指在有机分子中引入一原子或基团后,使分子中成键电子云密度分布发生变化,从而使化学键发生极化的现象,称为诱导效应。
诱导效应在有机化合物分子中,由于电负性不同的取代基(原子或原子团)的影响,使整个分子中的成键电子云密度向某一方向偏移,这种效应叫诱导效应。
诱导效应的特征是电子云偏移沿着σ键传递,并随着碳链的增长而减弱或消失。
例如,醋酸是弱酸(pKi=4.76),醋酸分子中的α-碳原子上引入一个电负性比氢强的氯原子后,能使整个分子的电子云向氯原子偏移,结果增强了羟基中氢原子的质子化,使一氯醋酸成为强酸(pKi=2.86,酸性比醋酸强)。
比较各种原子或原子团的诱导效应时,常以氢原子为标准。
吸引电子能力(电负性较大)比氢原子强的原子或原子团(如—X、—OH、—NO2、—CN等)有吸电子的诱导效应(负的诱导效应),用-I表示,整个分子的电子云偏向取代基。
吸引电子的能力比氢原子弱的原子或原子团(如烷基)具有给电子的诱导效应(正的诱导效应),用I表示,整个分子的电子云偏离取代基。
在诱导效应中,一般用箭头“→”表示电子移动的方向,表示电子云的分布发生了变化。
诱导效应是电子共轭是原子间成键的一种的方式吧,具体:1单双键交替出现的体系称为共轭体系。
诱导效应和共轭效应的基团1.引言1.1 概述概述诱导效应和共轭效应是有机化学中重要的概念,它们描述了基团对分子性质和化学反应的影响。
这些效应可以通过基团中电子的分布和能级重新排布来解释。
在有机化学中,分子的性质和化学反应往往受到其结构中基团的影响。
基团是分子中与主要化学反应有关的部分,它们通过共享或吸引电子的方式参与到反应过程中。
诱导效应和共轭效应描述了基团通过电子的重新分布来影响分子的性质和反应性。
诱导效应是指一个基团通过共享电子对另一个基团施加一定的电子密度或电荷的效应。
通过共享电子,基团可以增加或减少某个区域的电子密度,进而影响分子的极性和电荷分布。
这种效应可以通过电子云的极性和取向来实现。
例如,一个含有引入电子密度的基团可以通过共享电子而使周围区域的电子密度增加,从而增强其亲电性。
相反,一个含有吸引电子的基团可以通过共享电子而减少周围区域的电子密度,从而降低其亲电性。
共轭效应是指存在共轭结构的基团通过重新排布电子能级来影响分子的性质。
共轭结构是指分子中存在两个或多个相互共享电子的不饱和中心。
这些共轭结构可以具有特定的能级分布,使得分子的π电子在共轭系统中流动。
由于共轭结构的存在,分子的共振能级发生变化,导致分子的电子分布和性质发生改变。
共轭效应可以影响分子的化学稳定性、光学性质以及反应性。
本文将详细介绍诱导效应和共轭效应的基本概念、定义和解释,并通过一些实例加以说明。
同时,还将讨论它们在有机化学反应中的应用,并探讨它们对分子性质的重要影响。
最后,我们将总结这两种效应的特点和应用,并展望它们在未来有机化学研究中的潜在价值。
在接下来的章节中,我们将详细讨论诱导效应和共轭效应的定义、机制和实际应用。
我们希望本文能够帮助读者更好地理解这些基团效应,并将其应用于有机合成和反应设计中。
1.2 文章结构文章结构部分的内容可以按照以下方式来编写:文章结构本文将按照以下结构进行讨论。
首先,在引言部分(章节1)中,我们将简要介绍诱导效应和共轭效应的概念,并明确本文的目的。
诱导效应1简介诱导效应的特征是电子云偏移沿着ζ键传递,并随着碳链的增长而减弱或消失。
例如,醋酸是弱酸(pKa=4.76),醋酸分子中的α-碳原子上引入一个电负性比氢强的氯原子后,能使整个分子的电子云向氯原子偏移,结果增强了羟基中氢原子的质子化,使一氯醋酸成为强酸(pKa=2.86,酸性比醋酸强)。
2简史1923年G.N.路易斯首先提出取代基团吸引或释放电子的作用可以在整个分子中的各键上引起价电子对移动的概念。
C.K.英戈尔德等将常见的基团和原子排列成一个诱导效应强弱的定性序列。
还有不少科学工作者根据化合物的物理化学性质、反应平衡常数和速率常数等方面的大量实验结果,提出了各种基团特性常数,以定量或半定量地表达基团的诱导效应强弱。
其中最著名的是L.P.哈米特的取代常数ζ(见哈米特方程)和R.W.塔夫脱的极性取代常数ζ*。
1962年蒋明谦和戴萃辰认为诱导效应不仅与成键原子的电负性有关,还与键长有关,并根据原子的电负性及其共价半径,提出用诱导效应指数来定量地表示基团的诱导效应强弱。
3比较标准比较各种原子或原子团的诱导效应时,常以氢原子为标准。
吸引电子能力(电负性较大)比氢原子强的原子或原子团(如—X、—OH、—NO2、—CN等)有吸电子的诱导效应(负的诱导效应),用-I表示,整个分子的电子云偏向取代基。
吸引电子的能力比氢原子弱的原子或原子团具有给电子的诱导效应(正的诱导效应),用+I表示,整个分子的电子云偏离取代基。
在诱导效应中,一般用箭头“→”表示电子移动的方向,表示电子云的分布发生了变化。
诱导效应是一种短程的电子效应,一般隔三个化学键影响就很小了。
诱导效应只改变键内电子云密度分布,而不改变键的本性。
在分子中各相邻的共价键上以静电诱导方式引起的各价电子对的偏移(ζ 键电子的偏移)。
4产生诱导效应是由于一个共价键的价电子对在两原子间的不对称状态(键的极性状态),或由于一个成键原子带有电荷所引起。
一个共价键价电子对的不对称共用状态是由这两个成键原子的电负性不同引起的。
有机化学中的电子效应电子效应是影响有机化合物反应活性和反应规律的重要因素之一,深入理解有机化学中的电子效应,可以对有机化学的认识由感性向理性方向发展。
电子效应包括诱导效应、共轭效应和超共轭效应;有时三种效应同时存在,表现共同作用的综合结果。
一、诱导效应〔Inductive effect 〕诱导效应是电子效应的一种,是由路易斯〔Lewis 〕首先提出。
路易斯认为,对于有机化合物,诱导效应是由一个电负性较强的原子X 取代了碳原子上的氢原子后,在C -X 键上产生一个极性分布,这个极性分布通过电性诱导作用,在分子中其它键上引起一系列的极性变化,结果在整个分子中产生一个向着X 原子方向的较大范围的电子运动,这种电子运动称为诱导效应:δ-电负性比碳弱的元素原子也可以在分子中引起一系列的极性变化,只是所产生的诱导效应的方向刚好相反。
诱导效应是指在有机化合物分子中引入一个基团或原子后,由于原子的电负性差异,导致σ键电子的移动,使分子中的电子云密度分布发生变化,而这种变化不但发生在直接相连的部分,也可以影响到不直接相连的部分。
这种因某一原子或基团的极性而引起电子沿碳链向某一方向移动的效应,称为诱导效应。
如氯丙烷分子中,取代在碳上的氯原子的电负性较强, C -Cl 键产生偶极,使与氯原子连接的第一个碳原子〔α-碳原子〕产生部分正电荷〔δ+〕,也使第二个碳原子带有部分正电荷,第三个碳原子带有更少的正电荷,依次影响下去。
这种影响的特征是沿着碳链传递,并随着碳链的增长而迅速减弱或消失,一般传递到第三个碳原子就可忽略不计。
诱导效应是一种静电作用,共用电子并不能完全转移到另一原子,只是电子云密度分布发生变化,亦即键的极性发生变化。
δ+ δ+ δ+ δ- CH 3—CH 2—CH 2→Cl1.静态诱导效应〔I s 〕诱导效应分为静态诱导效应和动态诱导效应。
静态诱导效应是由分子本身结构决定的,是分子本身所固有的极化效应,与由极性溶剂或反应试剂等产生的外电场无关。
水的诱导效应1. 引言水是地球上最重要的物质之一,它在自然界中起着至关重要的作用。
除了满足人类的生活需求外,水还扮演着许多其他角色,其中之一就是诱导效应。
水的诱导效应是指水分子在特定条件下通过电荷分布和氢键形成而产生的特殊性质。
本文将深入探讨水的诱导效应及其在化学、生物学和环境科学等领域中的应用。
2. 水的电荷分布和氢键形成水分子由一个氧原子和两个氢原子组成,氧原子带有部分负电荷,而氢原子则带有部分正电荷。
这种不均匀的电荷分布使得水分子具有极性。
当多个水分子靠近时,它们会通过氢键相互连接。
氢键是一种强烈吸引力作用力,可以在不同分子之间或同一分子内部形成。
3. 水的诱导极化当一个非极性物质(如脂肪)与水接触时,由于水分子具有极性,它们会诱导非极性物质中的电子重新分布。
这种重新分布使得非极性物质在水中表现出极性特征,称为水的诱导极化。
诱导极化可以改变物质的溶解性、反应活性和其他性质。
4. 水的诱导效应在化学中的应用水的诱导效应在化学反应中起着重要作用。
它可以促进离子间的相互作用,加速反应速率。
此外,水的诱导效应还可以改变溶液中分子之间的距离和角度,从而影响分子之间的相互作用力。
这对于研究溶液中的化学平衡以及配位化合物的形成具有重要意义。
5. 水的诱导效应在生物学中的应用水是生命存在和运行所必需的。
它在细胞膜、蛋白质结构和酶催化等过程中起着关键作用。
水分子通过诱导效应能够调节生物大分子(如蛋白质和核酸)之间的相互作用,并影响其结构和功能。
此外,水还通过调控细胞内外环境、维持体温和运输营养物质等方式参与生物体的正常功能。
6. 水的诱导效应在环境科学中的应用水的诱导效应对环境科学研究也具有重要意义。
例如,在水污染治理中,研究水的诱导效应可以帮助我们理解污染物在水中的迁移和转化过程。
此外,水的诱导效应还可以影响土壤湿度、植物生长和农作物产量等环境因素。
7. 结论水的诱导效应是由于其特殊的电荷分布和氢键形成而产生的。
有机化学诱导效应赤字诱导效应使分子发生极化的反应在有机化合物分子中,由于电负性不同的取代基(原子或原子团)的影响,使整个分子中的成键电子云密度向某一方向偏移,使分子发生极化的效应,叫诱导效应。
由极性键所表现出的诱导效应称做静态诱导效应,而在化反应过程中由于外电场(如试剂、溶剂)的影响所产生的极化键所表现出的诱导效应称做动态诱导效应。
诱导效应只改变键内电子云密度分布,而不改变键的本性。
且与共轭效应相比,无极性交替现象。
基本性质编辑诱导效应的特征是电子云偏移沿着σ键传递,并随着碳链的增长而减弱,最终消失。
诱导效应是一种短程力,传递到第三个碳时已经很弱,传到第五个碳时几乎完全消失。
诱导效应是一种静电作用,是永久性的,属于电子效应的一种。
表示方法在诱导效应中,一般用箭头“→”表示电子移动的方向,表示电子云的分布发生了变化。
例如,氯原子取代了烷烃碳上的氢原子后,如下图:由于氯的电负性较大,吸引电子的能力较强,电子向氯偏移,使氯带部分负电荷(δ)、碳带部分正电荷(δ)。
带部分正电荷的碳又吸引相邻碳上的电子,使其发生偏移。
类型静态诱导效应:由于分子内极性共价键的存在(内在电场)而导致的,使静态分子固有的性质。
对化合物反应活性的影响具有两面性,在一定条件下可增加反应活性,也可能会降低反应活性。
动态诱导效应:是发生在化学反应时,由于外界电场的出现而发生的。
通常只是在进行化学反应的瞬间才表现出来,所起的作用大都是加速反应的进行。
诱导效应指数化学活性的定量尺度。
发展简史1923年G.N.路易斯首先提出取代基团吸引或释放电子的作用可以在整个分子中的各键上引起价电子对移动的概念。
C.K.英戈尔德等将常见的基团和原子排列成一个诱导效应强弱的定性序列。
科学工作者根据化合物的物理化学性质、反应平衡常数和速率常数等方面的大量实验结果,提出了各种基团特性常数,以定量或半定量地表达基团的诱导效应强弱。
其中最著名的是L.P.哈米特的取代常数σ(见哈米特方程)和R.W.塔夫脱的极性取代常数1962年蒋明谦和戴萃辰认为诱导效应不仅与成键原子的电负性有关,还与键长有关,并根据原子的电负性及其共价半径,提出用诱导效应指数来定量地表示基团的诱导效应强弱。
为了帮助大家更好的备战河南教师招聘学科知识与教学能力,河南教师招聘考试网讲师整理了河南教师招聘各学科知识的备考资料,希望对大家备考河南教师招聘学科知识科目有所帮助
诱导效应理论突破
诱导效应理论在有机化学中是一个非常重要的理论,它在研究有机化合物的结构、有机反应机理和有机合成中起很重要的作用。
1.概念
诱导效应是指在有机分子中引入一原子或原子团后,可使分子中成键电子云密度分布发生变化,这种变化不仅发生在直接相连的部分,而且沿着分子链影响整个分子的电子云密度分布。
这种因某一原子或原子团的电负性,而引起分子中σ键电子云分布发生变化,进而引起分子性质发生变化的效应叫做诱导效应。
2.特点
电子云偏移沿着σ键传递,并随着碳链的增长而减弱或消失。
例如,CH3CH2CH2COOH是弱酸,该分子中的α-碳原子上引入一个电负性比氢强的氯原子后,能使整个分子的电子云向氯原子偏移,结果增强了羟基中氢原子的质子化,使一氯醋酸成为强酸。
但是,在Y原子引入一个氯原子后,对-COOH的影响就可以忽略不计了。
3.规律
比较各种原子或原子团的诱导效应时,常以氢原子为标准。
吸引电子能力(电负性较大)比氢原子强的原子或原子团(如—X、—OH、—NO2、—CN等)有吸电子的诱导效应,整个分子的电子云偏向取代基。
吸引电子的能力比氢原子弱的原子或原子团(如烷基)具有给电子的诱导效应,整个分子的电子云偏离取代基。
在诱导效应中,一般用箭头“→”表示电子移动的方向,表示电子云的分布发生了变化。
诱导效应是一种短程的电子效应,一般隔三个化学键影响就很小了。
诱导效应只改变键内电子云密度分布,而不改变键的本性。
在分子中各相邻的共价键上以静电诱导方式引起的各价电子对的偏移(σ键电子的偏移)。
具有吸电子的诱导效应原子或原子团的相对强度如下:对同族元素:-F>-Cl>-Br>-I
对同周期元素:-F>-OR>-NR2
具有给电子的诱导效应的原子团主要是烷基,其相对强度如下:
【参考答案】
1.按照给电子诱导效应的大小排列为(3)>(1)>(4)>(2)。
2.当氯原子取代乙酸的α-H后,生成氯乙酸,由于氯的吸电子作用通过碳链传递,使羟基中O-H键极性增大,氢更易以质子形式解离下去,从而酸性增强。
即:
中公讲师杨梅解析注:本文章用于访问者个人学习、研究或欣赏,版权为“中公教师考试网”所有,未经本网授权不得转载或摘编。
已经本网授权使用作品的,应在授权范围内使用,并注明"来源:中公教师考试网"。
违反上述声明者,本网将追究其相关法律责任。
热门推荐:学科知识与能力学科知识与教学能力
更多精彩内容请访问:河南教师招聘考试网河南教师资格证考试
更多考试信息欢迎访问河南教师招聘河南人事考试网。