抗体药物偶联物的制备研究 PPT
- 格式:ppt
- 大小:510.00 KB
- 文档页数:27


抗体药物偶联制备
抗体药物偶联制备是一种将抗体与药物分子结合在一起,以提高药物的靶向性和有效性的技术。
以下是一般的抗体药物偶联制备步骤:
1. 选择合适的抗体和药物:根据疾病目标和药物特性,选择合适的抗体和药物分子。
2. 修饰抗体:利用化学方法将抗体表面引入偶联官能团。
常用的修饰方法包括活性酯化、N-羟基琥珀酰亚胺(NHS)酯化、巯基化等。
3. 链接药物:将修饰后的抗体与药物分子进行偶联。
常用的偶联方法包括亲核取代反应、酰胺形成反应、酯化反应等。
4. 纯化和检测:对偶联后的抗体药物进行纯化,以去除未反应的杂质。
常用的纯化方法包括凝胶过滤层析、负离子交换层析等。
同时,对偶联后的抗体药物进行质量检测,确保偶联效率和药物的活性。
5. 评估抗体药物的效价和稳定性:通过体外和体内实验,评估抗体药物的靶向性、抗体依赖性细胞毒性(ADCC)和药物释
放性能等。
需要注意的是,抗体药物偶联制备是一个复杂的过程,需要充分考虑抗体和药物的特性、偶联方法的选择、纯化和检测等因
素。
同时,制备过程中需要注意控制修饰和偶联的条件,以确保药物的活性和抗体的稳定性。


科研实验中的抗体偶联药物结合物:...抗体(antibody)毒素(drug)连接物(linker)构建ADC-抗体药物偶连物ADCs的组成包括肿瘤抗原特异性mAb,稳定的可裂解或不可裂解的linker,以及有效的细胞毒性载荷。
rug)、连接物(linker)构建ADC-抗体药物偶连物ADCs的组成包括肿瘤抗原特异性mAb,稳定的可裂解或不可裂解的linker,以及有效的细胞毒性载荷。
ADC由以下三部分组成:抗体(antibody):其作用是特异性识别靶细胞毒素(drug):起到损伤细胞的作用连接物(linker):连接抗体与毒素相关资料:DBCO-PEG4-vc-PAB-MMAEDBCO-PEG4-MMAFDBCO-PEG4-Ahx-DM1DBCO-PEG4-vc-PAB-Duocarmycin SADBCO-PEG4-vc-PAB-(PEG2)-Duocarmycin SADBCO-PEG4-VA-PBDDBCO-PEG4-vc-PAB-MMAFDBCO-PEG4-vc-PAB-MMADDBCO-PEG4-vc-PAB-Duocarmycin TMDBCO-PEG4-vc-PAB-(PEG2)-Duocarmycin TMDBCO-PEG4-vc-PAB-Duocarmycin DMDBCO-PEG4-vc-PAB-(PEG2)-Duocarmycin DMDBCO-PEG4-VC-PAB-DMAE-PNU159682DBCO-PEG4-DMAE-PNU159682DBCO-PEG4-GGFG-DX8951DBCO-PEG4-vc-PAB-Ahx-DM1DBCO-PEG8-VA-PAB-SG3199Gly3-vc-PAB-MMAEGly3-MMAFGly5-Ahx-DM1PNU159682-EDA-Gly3ADC pre-screening kit AProtein A-DM1Protein A-MMAEProtein A-MMAFProtein A-DuocarmycinProtein A-CalicheamicinProtein A-PBDADC pre-screening kit GProtein G-DM1Protein G-MMAEProtein G-MMAFProtein G-DuocarmycinProtein G-AmanitinProtein G-AmanitinRabbit Anti-vc-PAB-MMAE pAbMouse Anti-vc-PAB-MMAE mAb (B11F11) Rabbit Anti-MMAF pAbMouse Anti-MMAF mAb (F3B11) Mouse Anti-MMAE / F mAb (B12A2) Mouse Anti-MMAE /F mAb (C12A1) Rabbit Anti-DM1/4 pAbMouse Anti-DM1/4 mAb (F1D5)Mouse Anti-DM1/4 mAb (G2F3)Rabbit Anti-Calicheamicin pAbMouse Anti-Calicheamicin mAb (B1G9)Mouse Anti-Calicheamicin mAb (C1F12)Rabbit Anti-Duocarmycin pAbMouse Anti-Duocarmycin mAb (E11A1)Mouse Anti-Duocarmycin mAb (H7A9)Mouse Anti-Duocarmycin mAb (E6B3)Rabbit Anti-PNU-159682 pAbMouse Anti-PNU-159682 mAb (F7F2)Mouse Anti-PNU-159682 mAb (C1E3)Mouse Anti-PNU-159682 mAb (D12H11)Rabbit Anti-Amanitin pAbMouse Anti-Amanitin mAb (H3E1)Mouse Anti-Amanitin mAb (H12D6)Mouse Anti-Amanitin mAb (C2C4)Rabbit Anti-SN38 pAbMouse Anti-SN38 mAb (10F11A9D6)Mouse Anti-SN38 mAb (8E10F12F3)Mouse Anti-SN38 mAb (8E10A4A1)Rabbit Anti-PBD SG3199 pAbMouse Anti-PBD SG3199 (7H6H9A6) mAbMouse Anti-PBD SG3199 (8G2H12A9) mAbMouse Anti-PBD SG3199 (8B3D12G1) mAb资料仅供科研参考,其他合成技术疑问欢迎探讨(2021.4.lrx )。
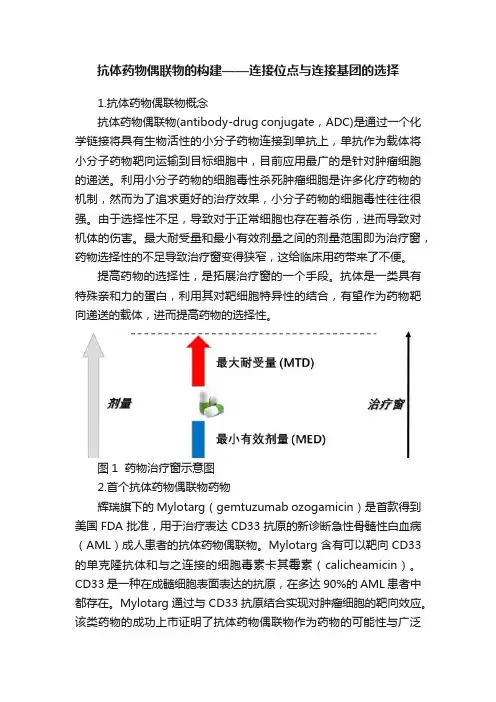
抗体药物偶联物的构建——连接位点与连接基团的选择1.抗体药物偶联物概念抗体药物偶联物(antibody-drug conjugate,ADC)是通过一个化学链接将具有生物活性的小分子药物连接到单抗上,单抗作为载体将小分子药物靶向运输到目标细胞中,目前应用最广的是针对肿瘤细胞的递送。
利用小分子药物的细胞毒性杀死肿瘤细胞是许多化疗药物的机制,然而为了追求更好的治疗效果,小分子药物的细胞毒性往往很强。
由于选择性不足,导致对于正常细胞也存在着杀伤,进而导致对机体的伤害。
最大耐受量和最小有效剂量之间的剂量范围即为治疗窗,药物选择性的不足导致治疗窗变得狭窄,这给临床用药带来了不便。
提高药物的选择性,是拓展治疗窗的一个手段。
抗体是一类具有特殊亲和力的蛋白,利用其对靶细胞特异性的结合,有望作为药物靶向递送的载体,进而提高药物的选择性。
图1 药物治疗窗示意图2.首个抗体药物偶联物药物辉瑞旗下的Mylotarg(gemtuzumab ozogamicin)是首款得到美国FDA批准,用于治疗表达CD33抗原的新诊断急性骨髓性白血病(AML)成人患者的抗体药物偶联物。
Mylotarg含有可以靶向CD33的单克隆抗体和与之连接的细胞毒素卡其霉素(calicheamicin)。
CD33是一种在成髓细胞表面表达的抗原,在多达90%的AML患者中都存在。
Mylotarg通过与CD33抗原结合实现对肿瘤细胞的靶向效应。
该类药物的成功上市证明了抗体药物偶联物作为药物的可能性与广泛应用前景。
图2 Mylotarg结构式(来源:)3.抗体与药物连接位点的选择对抗体进行药物偶联时,往往使用带有特殊侧链的氨基酸作为反应位点。
其中以半胱氨酸和赖氨酸为最多。
半胱氨酸在抗体中以二硫键的形式存在,因此需要对其进行还原为自由巯基进行下一步反应。
其中在抗体(IgG)链间有4对二硫键,比较容易被还原。
而在抗体链内,有12对二硫键,较难被还原。
赖氨酸则广泛分布于抗体结构域,大约有86个赖氨酸残基,其中有大约20个赖氨酸残基可作为连接位点。

抗体adc偶联工艺
抗体均为蛋白质分子,可以结合到特定的抗原上。
ADC(Antibody-Drug Conjugate,抗体
药物偶联物)是一种通过将特定的药物与抗体结合来增强治疗效果的药物传递系统。
抗体ADC的偶联工艺通常包括以下步骤:
1. 选择适当的抗体:选择具有高亲和力且特异结合于靶向肿瘤细胞的抗体。
通常选择单克隆抗体,以确保高度专一性。
2. 修饰抗体:在抗体分子上引入化学修饰,以提供药物偶联的位置。
最常用的修饰是通过基于酶的反应,如Sortase A,将药物结合位点引入抗体分子中。
3. 药物偶联:将药物与修饰后的抗体结合。
药物通常是细胞毒性化合物,如化疗药物。
偶联的方法包括使用特定的化学反应(如酰胺反应)、交联剂(如SMCC)或特定酶的使用(如Lys-C)。
4. 纯化和表征:纯化ADC以去除未偶联的抗体和未偶联的药物。
然后,对ADC进行各种表征,如浓度测定、电泳分析和质谱分析。
5. ADC稳定性评估:对ADC的稳定性进行评估,包括在不同的温度、pH和储存条件下的稳
定性检测。
抗体ADC的偶联工艺可以根据具体的药物和抗体的要求进行修改和改进。
这种技术可以增强
药物的特异性,减少对正常细胞的毒性,提高治疗效果,并降低治疗剂量和副作用。

抗体药物偶联物的研究进展抗体药物偶联物(antibody-drug conjugates,ADCs)是一种由单克隆抗体与化学药物通过共价键结合而成的生物分子复合物。
ADCs在肿瘤治疗上具有广阔的应用前景,其能够实现药物的靶向性、增加药物在肿瘤部位的稳态浓度,并最终导致肿瘤的死亡。
ADCs主要由三部分组成,即载体抗体、毒性药物和结合二者的连接剂。
其中,抗体的选择决定了ADCs的药物靶向性,而药物和连结剂的选择则决定了ADCs的药物毒性。
ADCs的制备关键在于要实现药物与抗体之间的扩散过程,这不仅要求化学药物的稳定性、连结剂的活性,还要考虑抗体活性和整个结构的稳定性。
因此,ADCs的制备需要耗费较大的精力和费用。
在临床应用层面上,ADCs主要用于治疗肿瘤类疾病,如乳腺癌、黑色素瘤等。
其中不乏一些ADCs已经进入临床阶段,如Ado-trastuzumab emtansine(Kadcyla,T-DM1)和Brentuximab vedotin(Adcetris)等。
这些药物在肿瘤治疗上已经获得了很好的临床疗效,但是ADCs仍面临着一些制约因素,例如药物选型、药物的物理化学性质、药物分配和代谢、抗体地位等诸多问题亟需解决。
总体而言,ADCs的研究进展是与多学科的交叉融合相伴随的。
在此背景下,药物学、化学、细胞生物学、分子生物学等领域均为ADCs的研究做出了巨大的贡献。
未来,ADCs的发展会趋于多样化与个性化,从中发现动态的疗效和药物安全性之间的关联。
ADCs的优化将依赖于新的生物标志物和建立“药物-靶标结构-功能-疗效”的整合策略。
此外,由于ADCs对于肿瘤细胞生长、侵袭、细胞凋亡等生物学特征的影响深远,因此ADCs具有避免多药耐药性的潜力,并可能实现“从新药开发到真正的治疗解决方案”的转型。
目前,ADCs的研究是具有广阔发展前景的,将有望成为未来抗癌治疗的重要方向之一。

抗体偶联药物(antibody-drug conjugates, ADC) 因其良好的靶向性及抗癌活性目前已成为抗肿瘤抗体药物研发的新热点和重要趋势,受到越来越多的关注 。
ADC 药物由单克隆抗体 、 高效应的细胞毒性物质以及连接臂三部分组成, 它将抗体的靶向性与细胞毒性药物的抗肿瘤作用相结合, 可以降低细胞毒性抗肿瘤药物的不良反应 , 提高肿瘤治疗的选择性, 还能更好地应对靶向单抗的耐药性问题.
有以下几个问题,需要思考:1) 靶标与抗体的选择 2)接头与偶联技术 3)负载药物 4)ADC药物的质量属性分析
重点说一下偶联技术:
非特定位点:通常药物与抗体的偶联是通过抗体上赖氨酸残基或链间二硫键还原产生的半胱氨酸残基实现的 。
这两种方式所获得的抗体药物偶联物中单个抗体上偶联的药物个数为 0个到 8 个不等, 具有较大的异质性,这对抗体偶联药物的批间一致性提出 了巨大的挑战 。
位点特异性偶联的方法还包括使用非天然氨基酸、 硒代半胱氨酸和酶解偶联法。
简单介绍一下一个在研的ADC项目:
构成:Herceptin+linker+MMAF/MMAE,通过在Herceptin碳端(重链或轻链)引入额外序列CAAX,进而采用特定的酶反应使linker+drug部分能偶联在特定位点。
采用在血浆中稳定的而在靶向部位易裂解的linker,保证了ADC药物的安全性以及有效性。
临床前数据表明,此药物与Herceptin具有相同的体外结合亲和力以及相同的PK特性;在HER2
阳性细胞株上,展现出良好的体外细胞毒性;在体内异种乳腺癌细胞株BT-474以及胃癌细胞株NCI-N87试验中,表现出强的抑制肿瘤效果。
{对ADC项目或此项目有兴趣的,可以交流一下}。

抗体偶联药物(ADCs)分析抗体偶联药物(Antibody-Drug Conjugates,ADCs)是一类由单克隆抗体和具有强效细胞毒性的小分子药物通过生物活性连接子偶联而成的新型生物药物。
其药物作用机理为通过单克隆抗体特异导向靶标癌细胞,再由偶联的小分子药物杀死癌细胞。
因此,ADC兼具了单克隆抗体药物高度特异性和靶向性的特点,以及小分子药物清除癌细胞的高效性,能协同发挥抗体药物和化学药物各自的优点,能够降低对生物系统的伤害。
常用的抗体偶联药物的制备是通过两步偶联反应,先将抗体与偶联剂(linker)结合形成中间体(抗体-linker),然后中间体再与小分子药物连接生成抗体偶联药物,如下图所示。
抗体偶联药物ADCs两步反应。
在反应过程中可能会出现以下几个问题:1, 部分抗体和小分子药物不能成功偶联;2, 抗体中存在多个结合位点(Cys, Lys 残基等),结合部位以及结合数量的不同会导致不均一性;3, 由于小分子药物的疏水性更高,与单抗结合数量的不同可能导致ADC药物的疏水性发生变化等问题。
这些未偶联的裸抗和具有细胞毒性的小分子以及偶联药物的不均一性可能会对ADC药物的药效、安全性产生影响。
相比单克隆抗体,ADCs药物的生产工艺更为复杂,因此为了保证ADCs药物的安全性和有效性,需对ADCs药物的质量进行监控。
药物抗体比(drug to antibody ratio,以下简称DAR)是评价ADCs药物的生产工艺和产品质量的重要参数之一。
因此,在ADC申报前对于ADC药物结构、DAR、药效、安全性的全面评估是至关重要的。
百泰派克拥有多种先进色谱质谱分析仪器,结合专业生物信息学分析团队,能快速、准确的为您提供专业系统的抗体偶联药物分析评定服务。
检测平台• MALDI-TOF质谱。
• ESI-TOF质谱。
• UV/VIS光谱。
• UV-MALDI质谱。
• 反相高效液相色谱 (RP-HPLC)。
• 亲水相互作用色谱 (HILIC)。


抗体药物偶联物(Antibody-drug conjugates,ADCs)是一种将抗体与药物通过化学连接结合在一起的分子复合物,用于靶向癌细胞等病变细胞。
这种结构通常包括三个主要组件:抗体、链接器和药物负载。
抗体:ADCs的核心是单克隆抗体,通常是针对癌细胞表面特异性抗原的抗体。
这个抗体负责与癌细胞表面的特定抗原结合,以实现靶向性。
链接器(Linker):链接器是将抗体与药物连接起来的化学结构。
链接器有两种主要类型:可裂解的链接器和不可裂解的链接器。
可裂解的链接器(Cleavable Linker):这种链接器在抗体与药物到达目标细胞后能够被细胞内部的特定酶或条件性因素降解。
这导致释放药物负载到目标细胞内,实现局部释放。
这种设计有助于减少非特异性的药物释放。
不可裂解的链接器(Non-cleavable Linker):这种链接器在抗体与药物到达目标细胞后不发生降解。
药物通过内吞作用释放到细胞内。
这种设计可能更适合一些情况。
药物负载:药物负载是通过链接器与抗体连接的药物分子。
这些药物通常是细胞毒性的,可以杀死或阻止癌细胞的生长。
整个结构可以简化为以下模式:
抗体
−
链接器
−
药物负载
抗体−链接器−药物负载
抗体药物偶联物的设计旨在提高药物的靶向性,减少对正常细胞的损伤,从而改善治疗效果和减少副作用。
不同的ADCs可能采用不同的抗体、链接器和药物组合,以满足特定治疗需求。
这是一个不断发展的领域,有许多公司和研究机构致力于开发新的ADCs以及改进已有的技术。
抗体药物偶联物 (ADC) 概述
抗体-药物偶联物 (ADC)由所需的单克隆抗体、活性药物和适当的接头组成。
抗体和药物之间适当的连接体维持ADC的稳定性并提供特定的桥梁,从而帮助抗体选择性地将药物递送至肿瘤细胞并在肿瘤部位准确地释放药物。
ADC PEG 连接体的选择是靶标依赖性的,基于对所使用的活性药物(包括细胞毒素)、抗体-靶标抗原复合物的内化和降解以及缀合物的临床前体外和体内活性比较的了解。
单分散聚乙二醇 PEG是靶向治疗中应用广泛的一种连接子。
PEG连接体具有高利用率、靶向性、调节PH值等特点。
PEG连接体具有多种官能团选择,可以与不同的抗体和药物缀合,形成不同的连接体,如pH敏感连接体、二硫键连接体、β-葡萄糖醛酸连接基...
单分散胺-PEG-羧基作为小分子连接基,含有亲水基团,可以溶解在大多数溶剂中,因此胺基也广泛用于ADC设计中。
此外,与匹配的抗体或药物连接的胺基可以作为pH敏感的连接体。