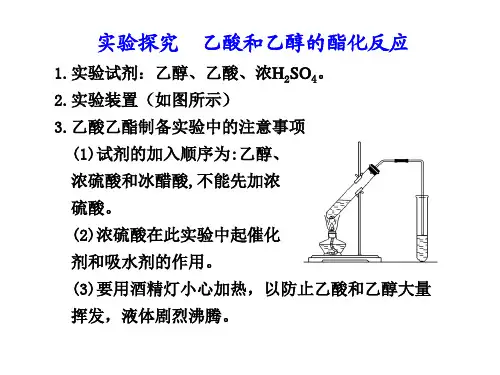
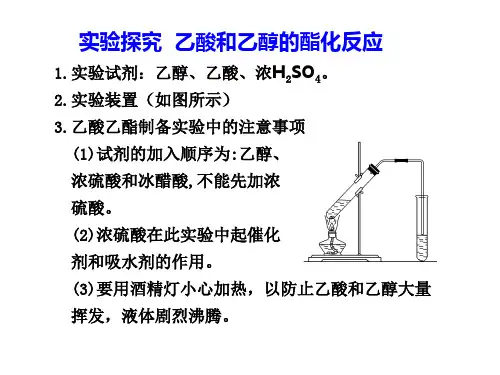
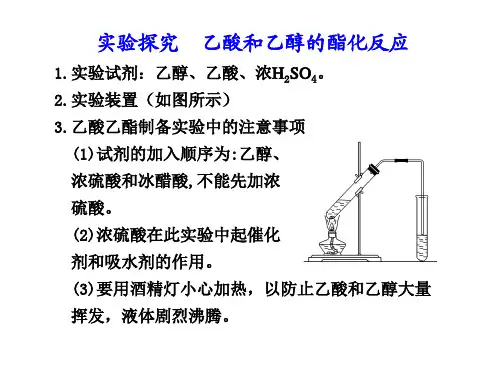
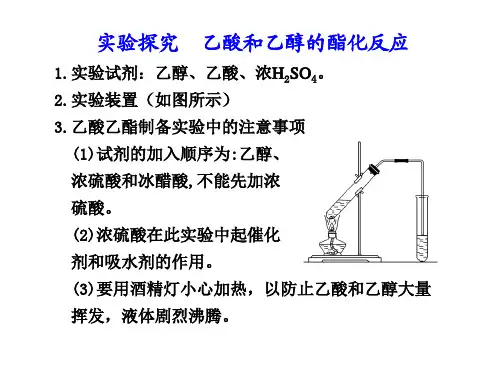
答案 (1)在一支30 mL的大试管(A)中注入4 mL乙 醇,缓慢加入1 mL的浓硫酸,边加边振荡试管,待冷 却至室温时,再加入4 mL乙酸并摇匀 CH3COOH+HOCH2CH3浓△硫酸 CH3COOC2H5+H2O (2)BC
(3)根据各物质的沸点数据可知,乙酸(117.9℃)、 乙醇(78.0℃)的沸点都比较低,且与乙酸乙酯的沸 点(77.5℃)比较接近,若用大火加热,反应物容易随 生成物(乙酸乙酯)一起蒸出来,导致原料的大量损 失;另一个方面,温度太高,
随生成物(乙酸乙酯)一起蒸出来,导致原料的大 量损失;另一个方面,温度太高,可能发生其他副 反应。 (4)在步骤③中的主要现象是:试管B中的液体分成 上下两层,上层油状液体无色(可以闻到水果香味), 下层液体(浅)红色,振荡后下层液体的红色变浅。 分离出来的是粗产品乙酸乙酯,乙酸乙酯粗产品的 提纯步骤为:①向粗产品中加入碳酸钠粉末(目的 是除去粗产品中的乙酸);②向其中加入饱和食盐 水与饱和氯化钙溶液,振荡、静置、分液(目的是 除去粗产品中的碳酸钠、乙醇);③向其中加入无 水硫酸钠(目的是除去粗产品中的水);④最后将
返回
畅想网络
Imagination Network
感谢观看!
文章内容来源于网络,如有侵权请联系我们删除。
3
为30 mL,那么所盛溶液不超过10 mL,按体积比1:4:4 的比例配浓硫酸、乙酸和乙醇的混合溶液,由此可 知,对应的浓硫酸、乙酸和乙醇的体积为1 mL、 4 mL、4 mL。既然在题中已经给定的是30 mL的大 试管,那就不能用其他规格的试管,在答题时要特别
注意。配制混合溶液的主要操作步骤可叙述为:在 一支30 mL的大试管(A)中注入4 mL乙醇,缓慢加入 1 mL的浓硫酸,边加边振荡试管,待冷却至室温时, 再加入4 mL乙酸并摇匀。其反应的化学方程式为: CH3COOH+HOCH2CH浓3 硫△酸 CH3COOC2H5+H2O。 (2)饱和碳酸钠溶液的作用主要有3个:①使混入乙 酸乙酯中的乙酸与Na2CO3反应而除去;②使混入的 乙醇溶解;③使乙酸乙酯的溶解度减小,减少其损 耗及有利于它的分层和提纯。故选B、C项。 (3)根据各物质的沸点数据可知,乙酸(117.9℃)、 乙醇(78.0℃)的沸点都比较低,且与乙酸乙酯的沸 点(77.5℃)比较接近,若用大火加热,反应物容易
![实验探究 乙酸和乙醇的酯化反应[优质PPT]](https://uimg.taocdn.com/b39cb91287c24028915fc347.webp)