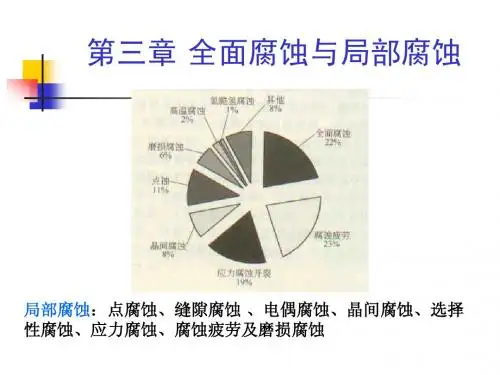
第3章 影响腐蚀的结构因素
- 格式:ppt
- 大小:1.34 MB
- 文档页数:63


第一章绪论腐蚀:由于材料与其介质相互作用(化学与电化学)而导致的变质和破坏。
腐蚀控制的方法:1)、改换材料 2)、表面涂漆/覆盖层3)、改变腐蚀介质和环境 4)、合理的结构设计5)、电化学保护均匀腐蚀速率的评定方法:失重法和增重法;深度法;容量法(析氢腐蚀);电流密度;机械性能(晶间腐蚀);电阻性.第二章电化学腐蚀热力学热力学第零定律状态函数(温度)热力学第一定律(能量守恒定律) 状态函数(内能)热力学第二定律状态函数(熵)热力学第三定律绝对零度不可能达到2.1、腐蚀的倾向性的热力学原理腐蚀反应自发性及倾向性的判据:∆G:反应自发进行<∆G:反应达到平衡=∆G:反应不能自发进行>注:ΔG的负值的绝对值越大,该腐蚀的自发倾向性越大.热力学上不稳定金属,也有许多在适当条件下能发生钝化而变得耐蚀.2.2、腐蚀电池2.2.1、电化学腐蚀现象与腐蚀电池电化学腐蚀:即金属材料与电解质接触时,由于腐蚀电池作用而引起金属材料腐蚀破坏.腐蚀电池(或腐蚀原电池):即只能导致金属材料破坏而不能对外做工的短路原电池.注:1)、通过直接接触也能形成原电池而不一定要有导线的连接;2)、一块金属不与其他金属接触,在电解质溶液中也会产生腐蚀电池.丹尼尔电池:(只要有电势差存在)a)、电极反应具有热力学上的可逆性;b)、电极反应在无限接近电化学平衡条件下进行;c)、电池中进行的其它过程也必须是可逆的.电极电势略高者为阴极电极电势略低者为阳极电化学不均匀性微观阴、阳极微观、亚微观腐蚀电池均匀腐蚀2.2.2、金属腐蚀的电化学历程腐蚀电池:四个部分:阴极、阳极、电解质溶液、连接两极的电子导体(即电路)三个环节:阴极过程、阳极过程、电荷转移过程(即电子流动)1)、阳极过程氧化反应++-M nM→ne金属变为金属离子进入电解液,电子通过电路向阴极转移.2)、阴极过程还原反应[]--⋅DDne+ne→电解液中能接受电子的物质捕获电子生成新物质.(即去极化剂)3)、金属的腐蚀将集中出现在阳极区,阴极区不发生可察觉的金属损失,只起到了传递电荷的作用金属电化学腐蚀能够持续进行的条件是溶液中存在可使金属氧化的去极化剂,而且这些去极化剂的阳极还原反应的电极电位比金属阴极氧化反应的电位高2.2.3、电化学腐蚀的次生过程难溶性产物称二次产物或次生物质由于扩散作用形成,且形成于一次产物相遇的地方阳极——[]+n M(金属阳离子浓度)(形成致密对金属起保护作用) 阴极——pH高2.3、腐蚀电池类型宏观腐蚀电池、微观腐蚀电池、超微观腐蚀电池2.3.1、宏观腐蚀电池特点:a)、阴、阳极用肉眼可看到;b)、阴、阳极区能长时间保持稳定;c)、产生明显的局部腐蚀1)、异金属(电偶)腐蚀电池——保护电位低的阴极区域2)浓差电池由于同一金属的不同部位所接触的介质浓度不同所致a、氧浓差电池——与富氧溶液接触的金属表面电位高而成为阳极区eg:水线腐蚀——靠近水线的下部区域极易腐蚀b、盐浓差电池——稀溶液中的金属电位低成为阴极区c、温差电池——不同材料在不同温度下电位不同eg:碳钢——高温阳极低温阴极铜——高温阴极低温阳极2.3.2、微观腐蚀电池特点:a)、电极尺寸与晶粒尺寸相近(0.1mm-0.1μm);b)、阴、阳极区能长时间保持稳定;c)、引起微观局部腐蚀(如孔蚀、晶间腐蚀)原因:a)、化学成分的不均匀性;b)、金属组织结构的不均匀性;多项合金不同相的电位不同c)、金属物理状态的不均匀性——应变、内应力不均匀;d)、金属表面膜(涂层)的不完整性.由于以上原因而形成的微观电池并不是金属发生电化学腐蚀的充分条件,还应在溶液中具有去极化剂才可发生2.3.3、超微观腐蚀电池特点:a)、电极用肉眼和普通显微镜难以分辨(100-1000nm);b)、阴、阳极区随时间不断变化;c)、引起均匀腐蚀2.4、电极电位与电化学腐蚀倾向性的判断2.4.1、电极和电极电位电极:指电子导体和离子导体组成的体系,常以金属/溶液表示注:腐蚀中的电极只指电子导体电极电位的表示:1)、金属浸入溶液中经水化作用而形成双电层 负点性金属水化后金属阳离子进入溶液——水化能 > 金属键能难溶性金属水化后从溶液中吸附阳离子——水化能 < 金属键能2)、形成气体电极——极难溶金属(Pt)和非金属导体(石墨)特点:电极导体本身不参与反应,仅起导电和反应载体作用2.4.2、平衡电极电位和非平衡电极电位平衡电极电位:水合与脱水达到动态平衡时的电极电位能斯特方程:⎪⎪⎭⎫ ⎝⎛+=R a a nF RT e e 0ln θ其中:e θ为标准电极电位; F 为法拉第常数;R aa 0为氧化态物质与还原态物质的活化比 注:浓度对电极电位有影响对于非平衡电极电位,其电极反应是不可逆的,因为电极过程中,即使阴极与阳极过程反应速率相等,达到了电子交换的平衡,但物质交换达不到平衡. 非平衡电极电位可以是稳定的也可以是不稳定的.电荷转移速率相等时即为稳定点位,也称开路电位或自腐蚀电位,即外电流为零时的电位.非平衡电极电位不服从能斯特方程,只能实验测得.2.4.3、电化学腐蚀倾向性的判断和电动序∵nFE G P T -=∆, e A e C E E E -=其中:F 为法拉第常数,F =96500 C/mol ; n 为参与反应的电子数;e C E 、e A E 分别为阴、阳极反应的平衡电位e A e C E E <:电位为e A E 的金属不会发生腐蚀 ∴电极电位判据 e A e C E E =:平衡状态e A e C E E >:电位为e A E 的金属自发进行腐蚀电动序:按金属在标准电极电位值E e 由低(负)值到高(正)值逐渐增大的次序排 列,得到的次序表称电动序.标准氢电极电位为零,电位比其低的为负电性金属,比其高的为正点性金属. 金属负电性越强,其在酸性溶液中越易发生析氢腐蚀.在可自发发生的反应中,电极电位较负的反应是氧化反应,较正的反应是还原反应.电偶序:金属或合金在一定电解质溶液中测得的稳定电位的相对大小排列而成的 次序表.电偶序比电动序更能反映金属实际腐蚀的性质.2.5、电位-pH 图及其应用2.5.1、水的E-pH 图要素:两条直线三个区域:a ---氢电极反应平衡电位-pH 关系的直线;b ---氧电极反应平衡电位-pH 关系的直线.b 线以上: 水被阳极电解为氧气;a 线以下: 水被阴极电解为氢气;a 、b 线之间: 水稳定区.2.5.2、电位-pH 图的绘制A 、列出可能发生的反应方程;B 、列出每个反应相应的Nernst 公式;C 、在水的电位-pH 图上绘制平衡关系。

第三章压力容器破坏形式压力容器常会由于设计结构不合理,制造质量差,使用维护不当或其他原因而发生破裂,并且破裂事故的形式多样,且很多是在使用限期内发生。
发生事故时,往往不仅容器本身遭到破坏,而且还会危及周围设施和职工的生命与健康,因此我们必须从各方面采取积极可靠的措施来保证安全运行,防止事故的发生。
第一节延性破裂延性破裂是压力容器在内部压力作用下,器壁上产生的应力达到器壁材料的强度极限,从而发生断裂的一种形式。
这种形式属韧性破裂,因此,该形式的破坏也称韧性破坏。
(一)机理压力容器的金属材料在外力作用下引起变形和破坏分为三个阶段(1)弹性变形阶段指当对材料施加的外力不超过材料固有的弹性极限值时,一旦外力消失,材料仍能回复到原来的状态而不产生明显的残余变形。
(2)弹塑性变形指对材料施加的外力超过材料固有的弹性极限值,材料将产生很大的塑性变形,外载荷消失后材料不再恢复原状,塑性变形仍将保留。
(3)断裂阶段指材料发生塑性变形后,如施加外力继续增加,当应力超过了材料的强度极限后,材料将发生断裂。
(二)特点及预防发生延性破裂的容器,其承受的压力、变形程度、断口特点及破裂具有以下特点:压力容器发生延性破裂是在较高的应力下发生的,即容器内的压力先后超过最高工作压力、设计压力而达到了容器的爆破压力值,容器破裂时的实际爆破压力往往接近于计算的爆破压力值。
若观察发生破裂的容器可知,由于容器在爆破前发生了明显变形,直径增大,破裂处的器壁显著减薄。
发生延性破裂的容器一般无碎片飞出,只是裂开一个口,口的大小与容器爆破时所释放的能量有关。
对于在液压试验中出现的延性破裂,由于液体的可压缩性极小,因此容器的裂口也比较窄,最大也不会超过半径。
但容器由于内部气体压力急骤升高而引起的破裂,裂口就比较宽。
既然容器发生延性破裂是由于超压而引起的,那么容器在试压和使用过程中就应该严禁超压,要严格按照有关规定进行压力试验与操作。
同时,也应按规定安装合适的安全泄压装置,并保证其灵敏可靠;与此同时,也要加强对容器的维护与检查,发生器壁腐蚀,减薄、变形应立即停止使用。





铜及其合金的腐蚀问题材研1001 杜伟 602080502038第一章绪论一研究铜及铜合金腐蚀的意义铜及铜合金色泽美观,性能优异,广泛应用于机械、化学、电子等众多工业领域。
铜的化学性质较为活泼,长时间暴露于空气或水中,尤其是在有腐蚀介质存在的环境中很容易发生腐蚀。
因此铜的腐蚀与防护问题是腐蚀学领域一个亟待解决的重要问题。
在有色金属的生产中,铜的产量仅次于铝,居第二位。
在电化学顺序中,铜具有比氢更高的正电位(+0.35 VSHE),故铜有较高的热力学稳定性,不会发生氢的去极化作用,被列为耐腐蚀金属之一。
但是在湿度较高、腐蚀性介质(如含二氧化硫的空气、含氧的水、氧化性酸以及在含有CN-、NH4+等能与铜形成络合离子的液体)中,铜则发生较为严重的腐蚀。
铜合金表现出比纯铜更高的耐腐蚀性,如:黄铜(Cu Zn合金)耐冲击腐蚀性好;铜镍合金具有耐酸耐碱、耐海水的性能以及抗应力腐蚀开裂的特性;锡青铜合金可耐各种腐蚀;硅青铜合金机械强度高、耐应力腐蚀开裂性能好。
铜会发生腐蚀早已为人们所知,可以说人类一开始使用铜就发现了这一现象。
虽然金属腐蚀现象极其广泛和常见,但作为一门科学对其进行研究却还是近百年的事。
在现代科学中,金属腐蚀的定义是:“金属在环境介质的作用下,由于化学反应、电化学反应或物理作用而产生的破坏”[1,2]。
由此定义可见,金属腐蚀的发生必须有包括金属材料和环境介质在内的相界面上的作用体系,金属发生腐蚀需要外部环境。
腐蚀是对金属材料的一种破坏,这种破坏使许多金属设备的使用寿命大为缩短甚至报废,带来巨大的经济损失,它会使生产停顿、物质流失、资源耗损、产品质量降低、环境受到污染、影响新技术的发展。
二铜的腐蚀环境铜的腐蚀按铜的使用环境可分为气相腐蚀和液相腐蚀,而液相腐蚀可按酸碱度进一步分为酸性液体、中性液体和碱性液体中的腐蚀。
在过去的数十年里,人们对铜在酸性溶液中、碱性溶液中和中性盐类溶液中以及自来水供水系统中的腐蚀进行了深入广泛的研究。


第一章几何结晶学基础1-1. 晶体,晶胞的定义;空间格子构造的特点;晶体的基本性质. 1-2. 参网页上的模型,运用对称要素组合定律,写出四方柱,六方柱,四方四面体,斜方双锥,六八面体,三方柱,复三方三角面体,四六面体的点群符号, 并写出其所属的晶系和晶族. 1-3. 参阅网页上的模型,请确定单型中的六八面体,复三方偏三角面体,复六方双锥,和聚型中2,3,4 号模型在晶体定向中,各晶体的晶轴分别与哪些对称轴重或晶棱方向平行? 1-4. 请写出单型三方柱,四方柱,四方双锥,六方柱,菱面体,斜方双锥各晶面的主要晶面符号. 1-5. 请写出下列聚型模型各晶面的晶面符号:1,2,3,4.两个对称面相互成1)60°,2)90°,3)45°,4)30°,可组合成什么点群? 1-6. 由两根相交的二次轴互成1)90°,2)60°,3)45°,4)30°,可以组合成什么点群? 1-7. 试在面心立方格子中画出菱面体格子一晶面在X,Y,Z 轴分别截得2,4,6 个轴单位,请写出此晶面符号. 1-8. 作图表示立方晶体的(123),(012),(421)晶面. 1-9. 在六方晶体中标出晶面(0001),(2110),(1010),(1120),(1210) 的位置. 1. 答:晶体最本质的特点是其内部的原子,离子,或原子集团在三维空间以一定周期性重复排列而成, 晶体的空间格子构造有如下特点: 结点空间格子中的点,在实际晶体中它们可以代表同种质点占有的位置,因此也称为晶体结构中的等同点位置. 行列结点在一维方向上的排列 . 空间格子中任意两个结点连接的方向就是一个行列方向.面网结点在平面上的分布构成面网.空间格子中,不在同一行列上的任意三个结点就可联成一个面网.平行六面体空间格子中的最小单位.它由六个两两平行且大小相等的面组成. 晶体的基本性质是指一切晶体所共有的性质, 这些性质完全来源于晶体的空间格子构造.晶体的基本性质主要包括以下五点: 1 ) . 自限性(自范性),指晶体在适当条件下自发形成封闭几何多面体的性质. 晶体的的多面体形态是其格子构造在外形上的反映. 暴露在空间的晶体外表, 如晶面,晶棱与角顶分别对应其晶体空间格子中的某一个面网,行列和结点. 2 ) . 结晶均一性,指同一晶体的各个不同部分具有相同的性质.因为以晶体的格子构造特点衡量,晶体不同部分质点分布规律相同,决定了晶体的均一性. 3 ) . 对称性,指晶体中的相同部分在不同方向上或不同位置上可以有规律地重复出现.这些相同部位可以是晶面,晶棱或角顶.晶体宏观上的对称性反映了其微观格子构造的几何特征. 4 ) . 各向异性,指晶体的性质因方向不同而具有差异.如云母的层状结构显示了在不同方向上的结合强度不同.从微观结构角度考虑,代表云母晶体的空间格子在不同方向上结点位置的排列不同.5 ) . 稳定性(最小内能),指在相同的热力学条件下,具有相同化学组成的晶体与气相,液相,非晶态相比,晶体具有最小内能,因此也是稳定的结构. 2. 答: 点群运用组合定律晶系晶族四方柱L 4 4L 2 5PC 1,2,3 四方中级六方中级六方柱L6 6L 2 7PC 1.2.3 四方四面体Li 4 2L 2 2P 4,5 四方中级斜方双锥3L 2 3PC 1,2,3 正交低级六八面体3L 4 4L 3 6L 25 等轴高级9PC 三方中级复三方三角面L 3 3L 2 3PC 1,2,3 体四六面体3L 4 4L 3 6L 25 等轴高级9PC 六方中级三方柱Li 6 3L 2 3P 4 3 答:略4. 答: 三方柱晶面1(2110) 晶面2( 1210) 晶面3(1120) 晶面4(0001) 晶面5(0001) 四方柱晶面1(100) 晶面2(010) 晶面3(100) 晶面4(010) 晶面5(001) 晶面6(001) 四方双锥晶面1(h0l) 晶面2(0kl) 晶面3(h0l) 晶面4(0kl) 晶面5(h0l) 晶面6(0kl) 晶面7(h0l) 晶面8(0kl) 六方柱晶面1(10l0) 晶面2(01l0) 晶面3(l100) 晶面4(l010) 晶面5(0l01) 晶面6(1l00) 晶面7(0001) 晶面8(000l) 菱面体晶面1(h00l) 晶面2(0k0l) 晶面3(h00l) 晶面4(0l0l) 晶面5(00il) 晶面6(00il) 斜方双锥晶面1(hkl) 晶面2(hkl) 晶面3(hkl) 晶面4(hkl) 晶面5(hk l ) 晶面6(hk l ) 晶面7 (hkl) 晶面8(hkl) 5. 答: 60°L33P 90°L22P 45°L44P 30°L66P 6. 答: 90°3L 2 60°L33L2 45°L 4L 30°L 6L 6 4 2 2 7. 答:略.(632) 8. 答:略9. 答:略第二章晶体化学基础和无机化合物晶体结构1-1. 晶格能与哪些因素有关?已知MgO 晶体具有氯化钠的结构型, 其晶格常数 a 为0.42nm,试计算MgO 的晶格能. 1-2. 计算具有简单立方(SC)和体心立方(BCC)结构金属(单质)晶胞的堆积密度(空间利用率). 1-3. 金属钼具有BCC 结构,其晶格常数 a 为0.3146nm,试计算钼原子的半径. 金属铬的晶格常数 a 为0.2884nm,密度为7.19g/cm3,通过计算确定铬是简单立方,体心立方还是面心立方结构.(Cr 52.00) 1-4. 在氧离子面心立方紧密堆积中,画出适合正离子填充的空隙形状和位置, 并分析八面体空隙和四面体空隙数分别与氧离子数有什么关系? 1-5. 比较面心立方最紧密堆积和六方最紧密堆积的异同点. 1-6. ThO2 具有萤石结构:Th4+离子半径为0.100nm,O2-离子半径为0.140nm,试问1)实际结构中的Th4+正离子配位数与预计配位数是否一致?2)结构是否满足鲍林规则. 1-7. 从负离子的立方密堆积出发,说明以下情况各产生什么结构类型:1)正离子填满所有四面体空隙位置;2)正离子填满一半四面体空隙位置;3)正离子填满所有八面体空隙位置. 1-8. 在萤石晶体中Ca2+半径为0.112nm,F-半径为0.131nm,求萤石晶体的堆积密度?萤石晶体a=0.547nm,求萤石的密度. 1-9. 根据教材中的萤石结构图,画出萤石晶胞的投影图,并注明Ca2+离子和F离子的标高. 1-10. 下列硅酸盐矿结构各属何种结构类型?(有Al3+离子的要说明其在结构中所处的位置): CaMg[Si2O6] Ca2Al[AlSiO7] Mg[Si4O10](OH)2 K[AlSi3O8] 1.答:因素为(1)离子的电子结构(2)离子的晶体结构类型(3)正负离子平衡距离.MgO 的晶格能为3955.5 KJ mol . 2.答:SC 堆积密度为52.36%,BCC 堆积密度为68.02%. 3.答:钼原子半径为0.1362nm.铬是体心立方BCC 结构. 4.答:四面体数:氧离子数=2:1,八面体数:氧离子数=1:1. 5.答:略. 6.答: (1)半径计算得出Th4+应为六配位,由于ThO2 为萤石结构,故不一致. (2) 不满足多面体规则,电价规则可满足. 7.答:1)反萤石结构.2)闪锌矿结构.3)NaCl 型结构. 8.答:堆积密度为60.41%,萤石的密度为 3.17g cm3. 9.答:图略. 10. 答:CaMg[Si2O6] 单链状. Ca2Al[AlSiO7] 组群状,双四面体.Al3+离子一部分位于氧八面体空隙, 另一部分位于四面体空隙. Mg[Si4O10](OH)2 层状. K[AlSi3O8] 架状.Al3+离子位于氧四面体空隙.第三章晶体的结构缺陷.3-1 方镁石(MgO)的密度是 3.58g/cm3,其晶格常数是0.42nm,计算MgO 中每个晶胞中肖特基缺陷的数目. 3-2 1)在CaF2 晶体中,弗兰克尔缺陷形成能为2.8eV,肖特基缺陷的生成能为 5.5eV, 计算在25℃和1600℃时热缺陷的浓度? 2)如果CaF2 晶体中,含有百万分之一的YF3 杂质,则在1600℃时,CaF2 晶体中是热缺陷占优势还是杂质缺陷占优势?请说明原因. 3-3 在下述晶体中,你认为何类缺陷占优势?1)用MgCl2 掺杂的NaCl;2)用Y2O3 掺杂的ZrO2;3)用YF3 掺杂的CaF2;4)在一种还原性气氛中加热的WO3. 3-4 试写出下列缺陷方程: 1) 3) 2) 4) 3-5 当ZrO2 添加到Y2O3 中,为保持结构的电中性,在形成置换型固溶体的同时, 还产生正离子空位,写出其缺陷反应方程式. 3-6 高温结构材料Al2O3 可以用ZrO2 来实现增韧,也可以用MgO 来促进Al2O3 的烧结:1)如加入0.2mol%ZrO2,试写出缺陷反应式和固溶体分子式;2)如加入0.3mol%ZrO2 和Xmol%MgO 对Al2O3 进行复合取代,试写出缺陷反应式,固溶体分子式,并求出X 值. 3-7 ZnO 属六方晶系,a=0.3242nm,c=0.5195nm,每个晶胞中含有2 个ZnO 分3 子,测得晶体密度分别为5.74,5.606g/cm ,求两种情况下各产生什么型式的固溶体? 3-8 非化学计量化合物FexO 中,Fe3+/Fe2+=0.1,求FexO 中空位浓度及x 值. 1.答:平均每个晶胞0.0082 对肖特基缺陷. 2.答:⑴T1=298K,弗兰克缺陷浓度2.21×10-24 ,肖特基缺陷浓度为1.374×10-31;T2=1873K, 弗兰克缺陷浓度 1.72×10-4,肖特基缺陷浓度为 1.4×10-5;⑵T=1600℃,热缺陷1.72×10-4,杂质缺陷1×10-6,热缺陷占优势3.答: 4.答:略5. 答: 6.答:①Al1.997Zr0.002O3 ②Zr0.003Mg0.003Al1.994O3 7.答:略8.答:Fe0.957O,空位浓度[ ]=0.0435第四章非晶态固体4-1 试分析影响熔体粘度的因素有哪些? 4-2 名词解释:晶子学说和无规则网络学说,单键强度,网络形成剂和网络变性剂4-3 玻璃的组成是13mol%Na2O,13mol%CaO,74mol%SiO2,计算非桥氧分数. 有两种不同配比的玻璃,其组成如下: 序号1 2 Na2O( mol%) 8 12 CaO( mol%) 12 8 SiO2( mol%) 80 80 试用玻璃结构参数说明两种玻璃高温下粘度的大小. 4-4 有一组二元硅酸盐熔体,其R 志变化规律如下,写出熔体一系列性质的变化规律:R = 2 , 2.5, 3, 3.5, 4 游离碱含量的变化; O/Si 比的变化; 低聚物数量; 熔体粘度; 形成玻璃的能力; 析晶能力. 4-5 什么是硼反常现象?为什么会产生硼反常现象. 1. 答:溶体组成,质点活化能,温度等. 2. 答:略. 3. 答:R 值为2.35.X 值为0.7.非桥氧分数为17.5%.两种玻璃结构参数相同,但(1)的钙含量高,所以(1)粘度大. 4.答:游离碱含量的变化增大; O/Si 比的变化增大; 低聚物数量增多; 熔体粘度递减; 形成玻璃的能力递减; 析晶能力递增. 5.答:略.第五章固体的表面与界面行为5-1 名词解释: 表面能,表面张力,吸附,接触角,晶界结构,润湿角. 5-2 试说明晶界能总小于两个相邻晶粒的表面能之和的原因. 5-3 MgO-Al2O3-SiO2 系统的低共熔物放在Si3N4 陶瓷片上,在低共熔温度下, 液相的表面张力为900×10-3N/m,而液体与固体的界面能为600×10- 3 N/m,测得接触角为70.52°. (1) (2) 求Si3N4 的表面张力; 把Si3N4 在低共熔温度下进行热处理,测试其热腐蚀的槽角为60°,求Si3N4 的晶界能. 5-4 生产氧化铅瓷件过程中需要镀银,已知1000℃时γAl2O3 s=1.0×10-3N/m, γAg L=0.92×10-3N/m,γAg L/Al2O3 s=1.77×10-3N/m,问液态银能否润湿氧化铅瓷件表面?可以用什么方法改善它们之间的润湿性? 5-5 5-6 5-7 5-8 影响润湿效果的主要因素有哪些? 大块状的石英材料经煅烧后易于破碎,这是为什么? 试说明晶粒之间的晶界应力大小对晶体性能的影响. 在真空中和在空气中将云母片剥落后再合上,会出现什么现象?说明理由? 5-9 5-10 什么是粘附功?粘附性越好是否就意味着粘附功越小,为什么? 1 克石英当它粉碎(在湿空气中)成每颗粒半径为1μm 的粉末时质量增加至 1.02 克,它的吸附水膜厚度为多少?(石英密度是2.65g/cm3) 1. 3. 答:略2. 答:略答:⑴900×10-3N/M ⑵1559×10-3N/M 4. 答:θ=147°>90°,液态银不能润湿氧化铅表面,可以通过以下方法改善它们之间的润湿性:增大瓷件表面粗糙度;设法除去表面吸附膜等. 5. 略6. 略7. 略8. 略9. 略10. 答:膜厚度为0.0177um第六章相图及其相平衡6-1 名词解释: 凝聚系统;介稳平衡;无变量点;低共熔点;双升点;双降点;液相独立析晶. 6-2 简述SiO2 的多晶转变现象,说明为什么在硅酸盐产品中SiO2 经常是以介稳状态存在. 6-3 具有不一致熔融二元化合物的二元相图(图6-11 所示),在低共熔点E 发生如下析晶过程: .已知 E 点 B 含量为20%,化合物AmBn 的 B 含量为64%.现有C1 和C2 二种配合料,已知C1 中的 B 含量为C2 中 B 含量的 1.5 倍,且在高温熔融冷却析晶时,从该二配合料中析出的初相(即到达低共熔温度前析出的第一种晶体)含量相等.试计算C1 和C2 配合料的组成. 6-4 今通过实验测得如图所示的各相图,试判断这些实验结果的正确性,若有错误,予以修正,并说明理由. 6-5 已知 A 和 B 两组份构成具有低共熔点的有限固溶体二元系统(图6-17). 试根据下列实验数据绘制概略相图: 的熔点为1000℃, 的熔点为700℃. A B 含B25%的试样在500℃完全凝固, 其中含73.3.%初相SA(B)和26.7%SA(B)+SB(A) 共生体.含B50%的试样在同一温度下凝固完毕,其中含40%初相SA(B) 和60%SA(B)+SB(A) 共生体,而SA(B)相总量占晶相总量的50%,实验数据均在达到平衡状态时测定. 6-6 试完成下图中的配料点1,2,3 的结晶路程(表明液,固相组成点的变化及其结晶过程各阶段系统中发生的相变化). 6-7 下图所示为一个三元化合物的三元相图. (1) (2) (3) (4) 判断三元化合物N 的性质; 标出边界曲线的降温方向(转熔界线用双箭头); 指出无变点K,L,M 的性质分析点1,2 的结晶路程(表明液固相组成的变化及各阶段的相变化) 6-8 如图6-43,配合料P 的液相在无变点K 发生独立析晶,最终在低共熔点 F 结束结晶.试问此时所获得的C3S,C2S,C3A 和C12A7 四种晶相的含量各为多少?,如果在F 点仍未达到平衡,残留液相能否离开F 点向其它无变点继续转移?为什么? 6-9 如图6-43,今取配合料成分恰好如无变点h 的组成,在充分平衡条件下, 问: (1) (2) (3) 加热该配合料,什么温度开始出现液相? 要使物料全部熔融,至少要加热到多高温度? 写出配合料加热到开始出现液相时和全部熔融时的反应过程. 6-10 如图6-43,若原始液相组成位于配合料圈内,并恰好在CaO 和C3S 初相区的边界曲线上: (1) (2) 说明此液相的结晶路程在缓慢冷却到无变点K 的温度1455℃时急剧冷却到室温,则最终获得哪些相? 各相含量如何? 1.答:名词解释略. 2.答:略,提示从动力学角度说明. 3.答:C1 配料组成为 A 74.1%,B 25.9%;C2 配料组成为 A 82.7%,B 17.3%. 4.答:(A)B 的熔点温度只有一个,两点应该重合.(B)液相组成不应该存在范围.(C)低共熔温度不应该是一条倾斜的直线,应该是水平的.(D)(E)均为二元系统,P 最大为3,不应该出现四相点和四相区域. 5.答:图略,提示低共熔温度线上三点的B%分别为5%,80%,95%. 6.答:略. 7.答:(1)N 为不一致熔融三元化合物.(2)略.(3)L 点位于△BNC 内部,为低共熔点, 点位于△ANB 交叉位, K 为双升点, 点位于△ANC 内部, M 为低共熔点. (4)略. 8.答:C3S,C2S,C3A 和C12A7 四种晶相的含量略,残留液相不能离开F 向其它无变量点转移,因为三元系统最多存在四相,在F 点已有四相. 9.答:(1)加热该配合料,1335 度开始出现液相.(2)要使物料全部熔融,至少要加热到2570 度.(3)略. 10. 答:最终获得C3S,C2S,玻璃相.第七章扩散与固相反应7-1 名词解释: 无序扩散,晶界扩散,表面扩散,本征扩散,非本征扩散,自扩散,互扩散,稳定扩散,不稳定扩散,扩散活化能,扩散通量. 7-2 已知CaO 的肖特基缺陷生成能为6ev,欲使Ca2+在CaO 中的扩散直至CaO 的熔点(2600 ℃)都是非本征扩散,要求三价杂质离子的浓度是多少? 7-3 设有一条内径为30mm 的厚壁管道,被厚度为0.1mm 的铁膜隔开.通过管子的一端向管内输送氮气,以保持膜片一侧氮气浓度为1 200mol/m ,而另一侧的氮气浓度为100 mol/m3.如在700℃下测得通过管道的氮气流量为 2.8×10-8mol/s,求此时氮气在铁中的扩散系数. 7-4 在二根金晶体圆棒的端点涂上示踪原子Au,并把棒的两端如图所示连接. 在920℃下加热100 小时,Au 示踪原子的扩散分布如图所示,并满足下列关系: 3 M 为实验中示踪原子总量,求此时金的自扩散系数. 7-5 试定性地分析和讨论从室温到熔融温度范围内,氯化锌添加剂(10-4mol%) 对氯化纳单晶中所有离子(Zn,Na,Cl)的扩散能力的影响. 7-6 试从扩散介质的结构,性质,晶粒尺寸,扩散物浓度,杂质等方面分析影响扩散的主要因素. 7-7 根据ZnS 烧结的数据测定了扩散系数,在450℃和563℃时,分别测得扩散系数为1.0 ×10 cm /s 和3.0×10 cm /s.(1)确定激活能和D0;(2)根据你对结构的了解, 试从运动的观点和缺陷的产生来推断激活能的含义;(3)根据ZnS 和ZnO 相互类似的特点,预测D 随硫的分压而变化的关系. 7-8 试分析碳原子在面心立方和体心立方铁八面体空隙间跳跃情况并以D=λ Pг形式写出其扩散系数(设点阵常数为a).式中λ为跃迁自由程,P 为跃迁几率,而г为跃迁频率. 7-9 指出以下概念中的错误: (1) (2) (3) 如果固体中不存在扩散流,则说明原子没有扩散; 因固体原子每次跳动方向是随机的,所以在任何情况下扩散流量为零; 晶界上原子排列混乱,不存在空位,所以以空位机制扩散的原子在晶界处无法扩散; -4 2 -4 2 (4) 间隙固溶体中溶质浓度较高,则溶质所占据的间隙越多,供扩散的空余间隙越少,即Z 值越小,越容易导致扩散系数的降低. 7-10 以空位机制进行扩散时,原子每次跳动一次就相当于空位反向跳动一次, 并未形成新的空位,而扩散活化能中却包含着空位形成能,此说法正确吗?请给出说明. 1. 2. 3. 4. 答:略答:1.1×10-5mol/m3 答:D=3.6×10 m /s 答:根据表中数据,以-ln ,求D 为2.33×10-7m2/s 对x2 作图,得一直线,求斜率K,t=360000s,D= -12 2 5. 答:低温时,以杂质扩散为主,ZnCl2 的加入对Na 离子的扩散能力有扩散作用, 而对氯离子的扩散能力影响不大,在高温条件下,本征扩散为主要形式, ZnCl2 的加入影响可忽略. 6. 略7. 答:①Q=48.9kJ,D0=0.39cm2/s ②质点处于其他质点作用的三位势阱中作周期性振动,若要摆脱其他质点的束缚,必须具有克服势阱作用的能量,这部分能量称为激活能,激活能包括迁移能和缺陷形成能. ③D∝PS2-1/4,硫分压越小,D 越大,硫分压增大,D 减小. 8. 9. 答:面心立方(fcc), = ,P= ,D= ,体心立方(bcc),D= 答:①扩散流的产生需要一个推动力,但在宏观上不存在扩散流,只要有一定温度,原子之间存在杂乱无章的自扩散. ②当有外力作用,如处于电场中,扩散流量不为零,只有在平衡状态下,扩散流量为零. ③晶界上原子所受束缚力低,其能量/振动频率搞,迁移能力强,其原子迁移到内部相党羽空位的反向扩散,不仅存在扩散,其扩散能力还比内部强. ④对扩散系数的影响可以忽略. 10.答:不正确.扩散系数是宏观值不是单个原子跳动机理的简单叠加.第八章固相反应8-1 MgO 和SiO2 固相反应生成Mg 2SiO4,反应时扩散离子是什么?写出界面反应方程. 8-2 MoO3 和CaCO3 反应时, 反应机理受到CaCO3 颗粒大小的影响. MoO3 : 当CaCO3 =1:1,MoO3 的粒径r1 为0.036mm,CaCO3 的粒径r2 为0.13mm 时,反应是扩散控制的;而当CaCO3 :MoO3=15:1,r2<0.03 时,反应由升华控制, 试解释这种现象. 8-3 试比较杨德方程和金斯特林格方程的优缺点及其适用条件. 8-4 当测量氧化铝-水化物的分解速率时,发现在等温试验期间,质量损失随时间线性增加到50%左右,超过50%时,质量损失的速率就小于线性规律.线性等温速率随温度指数地增加,温度从451℃增大到493℃时速率增大10 倍,试计算激活能,并说明这是一个扩散控制的反应?还是一般反应或是界面控制的反应. 8-5 1 平均粒径为1μm 的MgO 粉料与Al2O3 粉料以1: 摩尔比配料并均匀混合. 将原料在1300℃恒温3600h 后,有0.3mol 的粉料发生反应生成Mg Al2O4, 该固相反应为扩散控制的反应.试求在300h 后,反应完成的摩尔分数以及反应全部完成所需的时间. 答:扩散离子是Mg2+和Si4+,界面反应方程为: g 2+ +SiO4 Mg2SiO4+Si4+ Si4++4MgO Mg2SiO4+2 Mg2+ 2.答:当MoO3 的粒径r1 为0.036mm,CaCO3 的粒径r2 为0.13mm 时, CaCO3 颗粒大于MoO3,反应由扩散控制,反应速率随着CaCO3 颗粒度减小而加速,当r2<r1 时存在过量CaCO3,由于产物层变薄,扩散阻力减小,反应由MoO3 粒径升华控制, 并随着MoO3 粒径减小而加剧. 3.答:略. 4.答:1):. 由阿累尼乌斯公式: K=Aexp(-Q/RT)得: Q=R In k2/k1 (T1T2/T2-T1)=In10 *R*776*724/(493-451)=257.189KJ/mol R 故反应激活能为257.189kJ/mol 2):此反应为热分解反应,反应是在反应物与产物层的界面处进行的.由题中所述,反应进行到一定程度后质量损失速率小于线性规律,由此可推测该反应由扩散控制, 即后期由于反应物表层已被先前生成的大量产物层所包裹,导致新产生的气体无法扩散到外界去,从而减缓反应进行. 5.答:由于该固相反应为扩散控制反应,且粉料可视为均状大小球形,故用金斯特林格方程得: 1-2/3G-(1-G) 2/3 =kt G1=0.3/(1+1)=0.15 代入得K=7.45×10 -7 由题中所给条件;t1=3600h 所以当t2=300h 时,G2=0.045 令G=1,则T=1/3k=4.47×10 h 5第九章相变9-1 名词解释: 一级相变,二级相变,玻璃析晶,玻璃分相,均态成核,非均态成核,马氏体相变,亚稳分解,不稳分解. 9-2 为什么成核生长机理的相变过程需要有一定的过冷或过热, 相变才能发生, 在什么情况下需要过冷, 什么情况下需要过热?一般物质具有的最大成核速率的过冷度应该如何求得? 9-3 当一个球形晶核在液态中形成时,其自由能的变化△G=4πr2γ+ 4/3 r3△GV.式中r 为球形晶核的半径;γ为液态中晶核的表面能;△GV 为单位体积晶核形成时释放的体积自由能,求临界半径rk 和临界核化自由能△Gk. 8-4 如果液态中形成一个边长为a 的立方体晶核时, 其自由能△G 将写出什么形式?求出此时晶核的临界立方体边长ak 和临界核化自由能△Gk, 并比较球状晶核时,哪一种形状的△G 值更大,为什么? 9-5由 A 向 B 转变的相变过程中, 单位体积能变化△GV 在1000℃时为-419J/cm3, 在900℃时为-2093J/cm3,设A-B 间界面能为5×10-5J/ cm3,求: (1) (2) 在900℃和1000℃时的临界半径; 在1000℃进行相变时所需的能量. 9-6 试从热力学,动力学和形貌等方面比较亚稳分解和不稳分解这两种分相过程的特点. 9-9 某物质从熔体析晶,当时间分别为1s 和5s 时,测得晶相的体积分数分别为0.1%与11.8%,试用Vβ/V=1-exp(-Ktn)式计算Avrami 指数及其速率常数K. 9-10 如果直径为20μm 的液滴,测得成核速率IV=10 S cm ,如果锗能够过冷227℃,试计算锗的晶-液界面能?(TM=1231K,△H=34.8kJ/mol,ρ =5.35g/cm ) 9-11 举例说明相变理论在科学研究和生产实际中的应用. 1. 2. 答:略答: ,当,过热,过冷度为扩散活化能. 3. 4. 答: 答: , , ,显然立方体晶核形成, ,球形晶核较大. ,过冷;当, 3 -1 -1 -3 5. 答:900℃, ×10-17J =4.778, 1000℃, =2.387nm, 6. 9. 10. 11. 答:略答:n=3,K=10-3 答: 答:略第十章烧结过程10-1 名词解释: 熔融温度,烧结温度,烧结,烧成,液相烧结,固相烧结,晶粒生长,二次再结晶,晶粒极限尺寸,晶粒平均尺寸. 10-2 烧结的模型主要有哪几种?各适用于哪些典型的传质过程? 10-3 若固-气界面能为0.1J/m ,如果用直径为1μm 的粒子组成压块的体积为1cm ,试计算由烧结推动力而产生的能量是多少? 10-4 设有粉料粒度为5μm,若经2h 烧结后,x/r=0.1.如果不考虑晶粒的生长,若烧结至x/r=0.2.并分别通过蒸发-凝聚;体积扩散;粘性流动; 溶解-沉淀传质,则各需要多少时间?若烧结8h,则各传质过程的颈部增长x/r 又是多少? 10-5 如上题粉料的粒度改为16μm,烧结至x/r=0.2,各传质需要多少时间? 若烧结时间为8h,各个过程的x/r 又是多少?从两题计算的结果,讨论粒度与烧结时间对四种传质过程的影响程度? 10-6 下列过程中, 哪些能使烧结强度增加, 而不产生致密化过程?试说明理由.(1) 蒸发-凝聚(2)体积扩散(3)粘性流动(4)晶界扩散(5)表面扩散(6)溶解-沉淀. 10-7 制造透明Al2O3 材料时, 原始粉料粒度为2μm, 烧结至最高温度保温0.5h, 测得晶粒尺寸10μm,试问若保温时间为2h,晶粒尺寸多大?为抑制晶粒生长加入0.1%MgO,此时若保温时间为2h,晶粒尺寸又有多大? 10-8 晶界遇到夹杂物时会出现几种情况,从实现致密化目的考虑,晶界应该如何移动?怎样控制? 10-9 在烧结时,晶粒生长能够促进坯体致密化吗?晶粒生长会影响烧结速率吗?试说明之. 10-10 影响烧结的因素有哪些?最易控制的因素是哪几个? 1.答:名词解释略. 2.答:略. 3.答:烧结推动力而产生的能量是0.6J.提示,先算出粒子个数,再算出气固界面消失的面积. 4.答:根据查得各传质方式公式可得: 时间分别为16h,64h,8h,128h,若只烧结8h,则X/R 分别为0.1×41/3,0.1×4 1/5,0.2,0.1×41/6. 5.答:略6.答:略. 7.答:略3 2。
腐蚀的原理腐蚀是指金属或合金在特定环境中受到化学或电化学作用而逐渐失去其原有性能的过程。
腐蚀是一种不可逆的过程,会导致材料的损坏和性能下降,因此对腐蚀的原理进行深入了解对于材料保护和延长使用寿命具有重要意义。
腐蚀的原理主要包括化学腐蚀和电化学腐蚀两种类型。
化学腐蚀是指金属在化学环境中与其他物质发生化学反应而导致腐蚀,例如金属与氧气发生氧化反应形成金属氧化物。
而电化学腐蚀是指金属在电解质溶液中发生的电化学反应,产生阳极和阴极两种区域,从而引发腐蚀。
化学腐蚀的原理是金属与其他物质发生化学反应,形成金属的氧化物、硫化物、氯化物等化合物,这些化合物会导致金属表面的腐蚀和破坏。
例如,铁与氧气发生氧化反应生成铁氧化物,即铁锈,导致铁制品的腐蚀。
另外,金属与酸、碱等化学物质也会发生化学反应导致腐蚀。
电化学腐蚀的原理是在电解质溶液中,金属表面会形成阳极和阴极两种区域,阳极区域发生氧化反应,而阴极区域则发生还原反应,从而引发金属表面的腐蚀。
电化学腐蚀的速度与电解质的浓度、温度、金属的组成和结构等因素密切相关。
腐蚀的原理不仅涉及化学和物理方面的知识,还与材料的结构、组织、表面状态等密切相关。
例如,金属的晶粒大小、晶界、缺陷等都会影响金属的腐蚀行为。
此外,环境因素如温度、湿度、氧气浓度等也会对腐蚀的发生和发展产生重要影响。
为了防止腐蚀的发生,可以采取一系列的防腐措施,包括表面涂层、阴极保护、合金设计、材料选择等。
通过了解腐蚀的原理,可以有针对性地选择合适的防腐措施,从而保护金属材料,延长其使用寿命。
总之,腐蚀的原理是一个复杂的过程,涉及多方面的知识。
深入了解腐蚀的原理对于材料保护和应用具有重要意义,也为我们提供了有效的防腐方法和措施。
希望通过对腐蚀原理的深入研究,能够为材料科学和工程技术的发展提供有益的参考。
摘要在许多化工生产中都要用到盐酸,或含氯化合物在适当的条件下也会生成盐酸,因此盐酸对化工设备引起的腐蚀是严重的、常见的。
阻止金属腐蚀的方法有很多种,但有机缓蚀剂在抑制金属腐蚀上具有经济、高效、环保等优点,被广泛应用于化学清洗、工业用水、机械设备等工业领域,并成为工业生产中不可缺少的防腐蚀材料。
大多数有机缓蚀剂为吸附型缓蚀剂,它们会在金属表面吸附时会形成保护膜,可阻碍腐蚀介质与金属表面的接触,从而达到减缓金属腐蚀的目的。
然而,有关缓蚀剂的缓蚀机理仍需深入研究,以期为设计开发新型缓蚀剂提供理论指导。
本论文以油酸咪唑啉为缓蚀剂,盐酸为腐蚀剂,研究碳钢在不同条件下制备的油酸咪唑啉中的腐蚀效果。
同样的钢片在缓蚀剂中,改变条件,诸如:反应温度、缓蚀剂浓度、腐蚀剂浓度等,可以测出缓蚀剂能发挥出更好的缓蚀效果的条件,以帮助工业生产节约更多的缓蚀剂购买费用以及设备保养、维修费用。
经实验测定,合成咪唑啉缓蚀剂的最佳操作条件为反应温度150℃,反应时间2.5小时,胺酸比1.2:1。
测定咪唑啉缓蚀剂缓蚀效果的条件为在pH值为6的水中,缓蚀剂加入量20mg/L,最大缓蚀率可达91.86%。
在柴油中添加油溶性咪唑啉20mg/L时,最大缓蚀率为94.78%。
关键词:咪唑啉;腐蚀速度;缓蚀率IAbstractHydrochloric acid was used in many chemical productions. Or chlorine- containing compound under the properly conditions will generate hydrochloric acid. So, the corrosion of chemical equipment caused by hydrochloric acid is serious, common. There are many ways to prevent metal from corrosion, but as an economic and effective technique to inhibit corrosion, organic corrosion inhibitor has been widely applied in various industrial departments, such as chemical cleaning, industrial water, mechanical equipment, which has become an indispensable industrial anti- corrosion material. Most organic corrosion can adsorb onto the metal surface and form a protective film, which block corrosive medium diffusion to metal surface, and thus slow down corrosion rate. However, the inhibition mechanism of inhibitor is still need to further research in order to guide designing newly-type inhibitor.In this paper, Oleic acid imidazoline is used to as a corrosion inhibitor and hydrochloric acid as etchant to make a study of carbon steel in oleic imidazoline corrosion the corrosion effectiveness which is prepared under the different conditions. At the same time, change the reaction conditions, such as: reaction temperature, concentration of the inhibitor, concentration of the etchant, and so on. This will help measure the inhibitors under which conditions can play a better inhibition effectiveness. In order to help industrial production to save more puechase costs of the inhibitor and the maintenance, maintenance costs of the equipment.The result shows that the best operating conditions of prepared imidazoline are the ratio of amic amine to oleic acid is 1.2:1, the reaction temperature is 150℃, the reaction time is 2.5h from the experiment. Determination of the inhibition efficiency for imidazoline corrosion inhibitors at pH 6 in water, corrosion inhibitor dosage 20mg/ L, the maximum inhibition efficiency can be achieved 91.86%. Added to the diesel oil-soluble imidazoline 20mg/L, the maximum inhibition efficiency can be achieved 94.78%.Keywords: Imidazoline; Corrosion velocity; Inhibition efficiencyII目录摘要 (I)ABSTRACT ................................................................................................................. I I 目录 ......................................................................................................................... I II 第1章引言 .. (1)1.1盐酸腐蚀简介 (1)1.1.1盐酸的腐蚀机理 (1)1.1.2盐酸腐蚀影响因素 (1)1.2缓蚀剂 (2)1.2.1缓蚀剂的概念及分类 (2)1.2.2缓蚀剂的发展历程 (4)1.2.3国内外研究现状 (4)1.2.4缓蚀剂的发展趋势 (6)1.3咪唑啉类缓蚀剂 (6)1.3.1咪唑啉类缓蚀剂的结构及特性 (6)1.3.2咪唑啉类缓蚀剂的分类 (7)1.3.3 咪唑啉及其衍生物的合成 (7)1.3.4咪唑啉及其衍生物的作用机理 (8)1.3.5分子结构因素影响 (10)1.3.6咪唑啉及其衍生物在合成过程中需要注意的问题 (13)第2章实验部分 (15)2.1实验原理 (15)2.2实验原料及仪器设备 (15)2.2.1实验原料及试剂 (15)2.2.2实验仪器及设备 (16)2.3实验操作步骤 (18)2.3.1实验方案 (18)2.3.2实验具体操作过程 (18)2.4分析方法 (19)III2.5产品收率与缓蚀率的计算 (19)第3章实验数据及讨论 (21)3.1咪唑啉缓蚀剂的合成 (21)3.1.1反应温度的影响 (22)3.1.2胺酸摩尔比的影响 (22)3.1.3反应时间的影响 (23)3.1.4带水剂的影响 (24)3.2咪唑啉缓蚀剂缓蚀曲线分析 (25)第4章结论 (29)参考文献 (30)致谢 (32)IV第1章引言1.1盐酸腐蚀简介盐酸在现代化工生产中应用十分广泛,用于如:稀有金属的湿法冶金、有机合成、漂染工业、金属加工、食品工业、无机药品及有机药品的生产等。