实验报告5
- 格式:doc
- 大小:76.50 KB
- 文档页数:5

篇一:实验报告范文心理学实验报告2009-09-14 11:09短时记忆的信息提取2006年12月28日星期四 10:34摘要本次实验通过测定男女两名被试对不同长度识记数字的检查项目的再认,重复sternberg著名的短时记忆信息提取实验,了解短时记忆信息的提取方式。
结果发现,两名被试的反应时并没有随着记忆项目长度的增加而随着增加,也就是说,本次实验没有验证实验假设,本次实验是不成功的。
关键词:系列扫描短时记忆加因素法1 前言1900年ge.muller和a.pilzecker提出两类记忆,直到半个世纪后才引起人们的注意,现在已经确认存有短时记忆和长时记忆。
一般认为,短时记忆是指对信息保持几秒钟直至一分钟左右的记忆。
在20 世纪,sternberg发展了唐德斯的减数法反应时间,提出了加法法则,称之为加因素法。
这种实验并不是对减数法反应时间的否定,而是减数法的发展和延伸。
加因素法反应时间实验认为完成一个作业所需的时间是一系列信息加工阶段分别需要的时间的总和,如果发现可以影响完成作业所需时间的一些因素,那么单独地或成对地应用这些因素进行实验,就可以观察到完成作业时间的变化。
加因素法反应时间实验的逻辑是:如果两个因素的效应是互相制约的,那么这两个因素只作用于同一个信息加工阶段;如果两个因素的效应是分别独立的,即可以相加,那么这两个因素各自作用于不同的加工阶段。
这样,通过单变量和多变量的实验,从完成作业的时间变化来确定这一信息加工过程的各个阶段。
因此,重要的不是区分出每个阶段的加工时间,而是辨别认知加工的顺序,并证实不同加工阶段的存在。
加因素法假定,当两个实验因素影响两个不同的阶段时,它们将对总反应时间产生独立的效应,即不管一个因素的水平变化如何,另一个因素对反应时间的影响是恒定的。
这样称两个因素的影响效应是相加的。
加因素法的基本手段是探索有相加效应的因素,以区分不同的加工阶段。
使用加因素法分析心理过程的一个典型实验是sternberg的“短时记忆信息提取任务”。

实验报告总结5篇实验报告总结 (1) 时间像流水般一去不复返,我的物流工作实习也一去不复返。
从学校踏入社会,从学生转换成工作者,我学到了很多很实际的东西。
工作的规则,复杂的人际关系都需要我们慢慢去适应。
我从事的是物流工作的实习,这是一门服务的行业,始终坚持顾客是上帝。
但并非我说学的专业,刚开始我不怎么感兴趣,心想既来了就好好做着。
无论什么样的事情都可以锻炼自己,可以学到你想要的。
我的职位是一名接送货员,主要的工作是从客户那里安全的把货物送回来。
在别人看来,这也许是一份很简单的工作,但是要把它做好还要花点心思。
因为你去接货时,要跟客户鉴定一份合同,关于货物安全的,所以你不有丝毫的大意,一个很小的失误都会带来很多的问题。
这些问题都关系到公司的信誉问题,所以要非常的细心。
这些对我来说,还是没什么问题的。
其实更让我感到吃力的事是复杂的人际关系,我每天要面对不同的客户,他们的性格各异。
这不免让我感到有点措手不及,尤其对于刚出校门的我们来说。
特别是对于内向性格的我,实在有点难以应付。
但我并没有灰心,我的毅力没那么弱,别人做好的,我也能做好。
相信困难只是暂时的,通过领导的耐心指点,同事的帮助,以及自己的努力,这些问题都解决了,我进步了。
我认为心态很重要,因为这是良心剂。
同时我还要处理好跟同事之间的关系,争吵,争论,是家常便饭,但更重要的是相互之间的理解,沟通与支持。
有了他们我不在孤单,温暖的画面一幕一幕,感到常在。
但是在物流工作实习中我还是发现了自己在很多方面还不足,还没什么经验,毕竟刚出校门。
所以我要不段的学习,不断的提高自己,便更好的适应这个社会。
在工作中要严格要求自己,要有一颗宽容的心,向身边的人学习。
一切要从全局出发,重团结,讲诚信。
无论在什么岗位我始终以饱满的热情对待自己的工作,勤勤恳恳,尽职尽责,踏踏实实的完成自己的本职工作。
同时还应具有较强的应变和适应能力。
几个月来,我十分注意对现实的了解和掌握。
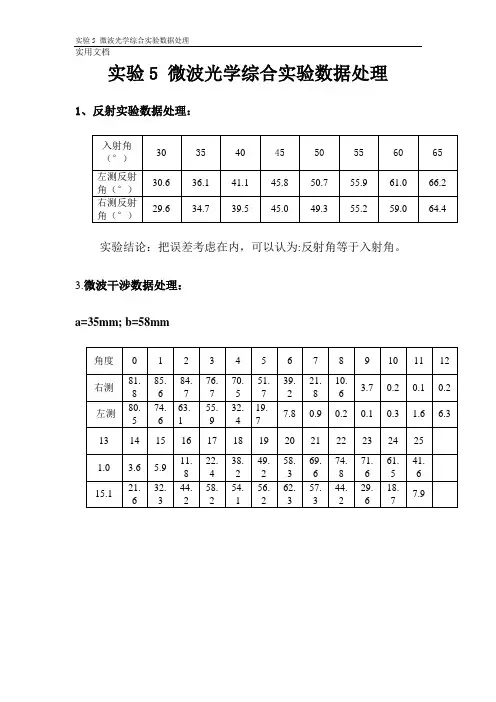
实验5 微波光学综合实验数据处理1、反射实验数据处理:
实验结论:把误差考虑在内,可以认为:反射角等于入射角。
3.微波干涉数据处理:
a=35mm; b=58mm
由公式求得的理论值:第一级加强点ϕ=21.0°第一级减弱点不在所测得范围内。
由实验数据求得的值:第一级加强点ϕ值在20°~22°之间,与理论值近似相等
4、微波的偏振数据处理:
实验结论:把误差考虑在内,可以认为得到的实验数据基本和理论值相等。
5、微波的迈克尔逊干涉
实验数据:读数为极小值时的刻度(mm ):4.170;19.762;35.170;53.736;69.337
读数为极大值时的刻度(mm ):11.596;27.929;42.821;
61.353
数据处理:由读数极小值测得的波长:λ=(69.337-4.170)
⨯2/4=32.58nm
由读数极大值测得的波长:λ=(61.353-11.596)
⨯2/3=33.17nm
求均值:λ=32.88nm 理论值; λ=33.3nm
相对误差:=
σ%100⨯-理
实
理λλλ=1.26%
6、微波的布拉格衍射数据处理:
根据实验数据测得的衍射角曲线:如图
下图为理论测得的衍射角曲线:如图
实验结果:
经对比可知:实验所测得的衍射角曲线和理论测得的衍射角曲线可以近似看作相等(把误差考虑在内),实验测得100面第一级加强点的衍射角为θ=68.1°
第二级加强点的衍射角为θ=37.8°
测得110面第一级加强点的衍射角为θ=56.4°。


虚拟仪器实验报告实验五一、实验目的本次虚拟仪器实验的目的是深入了解和掌握虚拟仪器在数据采集、处理与分析方面的应用,通过实际操作和实验,提高对虚拟仪器技术的理解和运用能力。
二、实验设备与环境1、计算机:配置满足虚拟仪器软件运行要求。
2、虚拟仪器软件:如 LabVIEW 等。
3、数据采集卡:用于采集外部物理量信号。
三、实验原理虚拟仪器是基于计算机的仪器系统,它将计算机硬件资源与仪器测量、控制功能结合在一起。
通过软件编程,实现对数据的采集、处理、分析和显示。
在本次实验中,主要利用数据采集卡采集外部信号,然后在虚拟仪器软件中进行处理和分析。
四、实验步骤1、硬件连接将数据采集卡正确安装到计算机上,并连接外部传感器或信号源,确保连接稳定可靠。
2、软件设置打开虚拟仪器软件,进行数据采集卡的配置,包括采样频率、通道选择、量程设置等。
3、程序编写使用图形化编程语言,编写数据采集、处理和分析的程序。
例如,实现数据的实时采集、滤波处理、频谱分析等功能。
4、运行程序编译并运行编写好的程序,观察采集到的数据和处理结果。
5、数据分析对采集到的数据进行分析,评估数据的准确性和可靠性,查找可能存在的问题。
五、实验结果与分析1、数据采集结果成功采集到了外部信号,数据的幅度、频率等特征与预期相符。
2、滤波处理效果通过低通、高通或带通滤波,有效地去除了噪声和干扰,使信号更加清晰。
3、频谱分析结果对采集到的周期性信号进行频谱分析,准确地得到了信号的频率成分和幅值分布。
分析实验结果时,发现了一些问题。
例如,在某些情况下,采集到的数据存在一定的误差,可能是由于传感器精度、信号干扰或采样频率设置不当等原因引起的。
针对这些问题,进行了进一步的调试和改进。
六、实验中遇到的问题及解决方法1、数据采集不稳定解决方法:检查硬件连接,确保接触良好;调整采样频率和缓冲区大小。
2、程序运行出错解决方法:仔细检查程序代码,查找语法错误和逻辑错误;参考软件的帮助文档和示例程序。

实验报告5 循环结构1. 实验目的本次实验主要通过编写程序练习循环结构的使用,包括for循环和while循环,并掌握循环结构在解决问题中的应用。
2. 实验内容2.1 for循环2.1.1 基本语法for循环一般的基本语法如下:pythonfor 变量in 可迭代对象:循环体其中,变量为循环控制变量,可迭代对象为需要遍历的对象,循环体为要执行的操作。
2.1.2 实验步骤本次实验选择使用for循环来实现如下功能:1. 计算1到100之间所有正整数的和。
2. 输出一个400行的矩形,每行有20个星号。
python计算1到100之间所有正整数的和sum = 0for i in range(1, 101):sum += iprint("1到100之间所有正整数的和为:", sum)输出一个400行的矩形,每行有20个星号for i in range(1, 401):print("*", end="")if i % 20 == 0:print()2.2 while循环2.2.1 基本语法while循环的基本语法如下:pythonwhile 循环条件:循环体其中,循环条件为判断条件,当循环条件为True时,执行循环体中的操作。
2.2.2 实验步骤本次实验选择使用while循环来实现如下功能:1. 计算1到100之间所有偶数的和。
2. 输出1到100之间所有的质数。
python计算1到100之间所有偶数的和sum = 0i = 1while i <= 100:if i % 2 == 0:sum += ii += 1print("1到100之间所有偶数的和为:", sum)输出1到100之间所有的质数num = 2while num <= 100:prime = Truefor i in range(2, int(num 0.5) + 1):if num % i == 0:prime = Falsebreakif prime:print(num, end=" ")num += 13. 实验结果运行以上代码,可以得到以下结果:1到100之间所有正整数的和为: 5050...1到100之间所有偶数的和为: 25502 3 5 7 11 13 17 19 23 29 31 37 41 43 47 53 59 61 67 71 73 79 83 89 97 4. 实验总结通过本次实验,我学会了使用循环结构来解决问题。

初中科学实验报告范文5篇实验报告1:溶胶与胶体的制备与性质实验目的观察溶胶与胶体的制备过程,了解它们的性质和特点。
实验材料- 玻璃杯- 漏斗- 过滤纸- 海藻酸钠- 酒精- 显微镜实验步骤1. 在玻璃杯中加入适量的海藻酸钠。
2. 慢慢加入少量的酒精,并用玻璃杯轻轻搅拌。
3. 观察溶胶与胶体的形成和变化。
4. 用过滤纸过滤溶胶与胶体,观察过滤后的物质。
实验结果溶胶与胶体都呈现悬浮状态,但溶胶颗粒更小,无法被肉眼观察到。
胶体颗粒较大,可以在显微镜下观察到。
实验结论溶胶与胶体都是由固体颗粒在液体中悬浮而成的,但它们的颗粒大小不同。
溶胶颗粒比胶体颗粒更小,所以无法被肉眼观察到。
实验报告2:水的蒸发与沸腾实验目的观察水的蒸发和沸腾过程,了解它们的特点。
实验材料- 水- 烧杯- 温度计- 燃烧器实验步骤1. 将水倒入烧杯中。
2. 在水的表面插入温度计。
3. 用燃烧器加热水,观察水的蒸发和沸腾过程。
4. 记录水的温度随时间的变化。
实验结果水的蒸发和沸腾都是水分子由液态转变为气态的过程。
蒸发发生在水表面,而沸腾则发生在整个液体内部。
实验结论从实验结果可以看出,水的蒸发和沸腾是由于水分子的热运动变得剧烈。
蒸发和沸腾都是水的气态转变过程,只是发生的位置不同。
实验报告3:色彩与光的反射实验目的观察不同颜色的物体对光的反射情况,了解色彩与光的关系。
实验材料- 红色、绿色、蓝色的物体各一个- 手电筒实验步骤1. 打开手电筒,照射红色物体,观察反射光的颜色。
2. 重复上述步骤,分别照射绿色和蓝色物体,观察反射光的颜色。
3. 总结不同颜色物体的反射情况。
实验结果红色物体反射的光为红光,绿色物体反射的光为绿光,蓝色物体反射的光为蓝光。
实验结论不同颜色的物体对光的反射情况不同,它们会选择性地吸收某些颜色的光,而反射其他颜色的光。
实验报告4:磁铁与铁砂的吸引作用实验目的观察磁铁与铁砂之间的吸引作用,了解磁铁的性质。
实验材料- 磁铁- 铁砂实验步骤1. 将磁铁放在铁砂上方,并轻轻晃动磁铁。

化学实验报告范文5篇1.化学实验报告范文实验步骤(1)在试管中加入5mL5%的过氧化氢溶液,把带火星的木条伸入试管。
(2)加热实验(1)的试管,把带火星的木条伸入试管。
(3)在另一支试管中加入5mL5%的过氧化氢溶液,并加入2g二氧化锰,把带火星的木条伸入试管。
(4)待实验(3)的试管内液体不再有现象发生时,重新加热3mL5%的过氧化氢溶液,把带火星的木条伸入试管。
(该步骤实验可以反复多次)(5)实验后将二氧化锰回收、干燥、称量。
实验现象及现象解释:(1)木条不复燃(2)木条不复燃H2O2分解O2速度太慢没足够的O2试木条复燃(3)3H2O2产生大量气泡木条复燃MnO2使H2O2加速分解O2,O2使木条复然(4)新加入的H2O2产生大量气泡因为MnO2继续作为催化挤的作用!H2O2继续分解(5)5MnO2的质量不变因为MnO2是催化剂所以只是改变化学反应速度,不改变其化学性质和质量2.化学实验报告范文实验名称探究化学反应的限度实验目的1.通过对FeCl3溶液与KI溶液的反应的探究,认识化学反应有一定的限度。
2.通过实验使学生树立尊重事实,实事求是的观念,并能作出合理的解释。
实验仪器和试剂试管、滴管、0.1mol/L氯化铁溶液、0.1mol/LKI溶液、CCl4、KSCN溶液。
实验过程1.实验步骤。
(1)取一支小试管,向其中加入5mL0.1mol/LKI溶液,再滴加0.1mol/L氯化铁溶液5~6滴。
(2)向试管中继续加入适量CCl4,充分振荡后静置。
(3)取试管中上层清液,放入另一支小试管中,再向其中滴加3~4滴KSCN溶液。
2.实验结论。
问题讨论1.实验步骤(2)和实验步骤(3)即I2的检验与Fe的检验顺序可否交换?为什么?2.若本实验步骤(1)采用5mL0.1mol/LKI溶液与5mL0.1mol/L氯化铁溶液充分混合反应,推测反应后溶液中可能存在的微粒?为什么?3.化学实验报告范文实验名称用实验证明我们吸入的空气和呼出的气体中的氧气含量有什么不同实验目的氧气可以使带火星的木条复燃,木条燃烧越旺,说明氧气含量越高一、实验器材:药品水槽、集气瓶(250ml)两个、玻片两片、饮料管(或玻璃管)、酒精灯、火柴、小木条、水,盛放废弃物的大烧杯。

实验报告6篇实验报告 (1) 利用混合物中各组分在某种溶剂中的溶解度不同,而使它们相互分离;一般过程:1、选择适宜的溶剂:①不与被提纯物起化学反应;②温度高时,化合物在溶剂中的溶解度大,室温或低温时溶解度很小;而杂质的溶解度应该非常大或非常小;③溶剂沸点较低,易挥发,易与被提纯物分离;④价格便宜,毒性小,回收容易,操作安全;2、将粗产品溶于适宜的热溶剂中,制成饱和溶液:如溶质过多则会成过饱和溶液,会有结晶出现;如溶剂过多则会成不饱和溶液,会要蒸发掉一部分溶剂;3、趁热过滤除去不溶性杂质,如溶液颜色深,则应先用活性炭脱色,再进行过滤;4、冷却溶液或蒸发溶液,使之慢慢析出结晶,而杂质留在母液中或杂质析出,而提纯的化合物则留在溶液中;5、过滤:分离出结晶和杂质;6、洗涤:除去附着在晶体表面的母液;7、干燥结晶:若产品不吸水,可以放在空气中使溶剂自然挥发;不容易挥发的溶剂,可根据产品的性质采用红外灯烘干或真空恒温干燥器干燥,特别是在制备标准样品和分析样品以及产品易吸水时,需将产品放入真空恒温干燥器中干燥;实验报告 (2)例一定量分析实验报告格式(以草酸中h2c2o4含量的测定为例)实验题目:草酸中h2c2o4含量的测定实验目的:学习naoh标准溶液的配制、标定及有关仪器的使用;学习碱式滴定管的使用,练习滴定操作。
实验原理:h2c2o4为有机弱酸,其ka1=5.9×10-2,ka2=6.4×10-5。
常量组分分析时cka1>10-8,cka2>10-8,ka1/ka2<105,可在水溶液中一次性滴定其两步离解的h+:h2c2o4+2naoh===na2c2o4+2h2o计量点ph值8.4左右,可用酚酞为指示剂。
naoh标准溶液采用间接配制法获得,以邻苯二甲酸氢钾标定:-cook-cooh+naoh===-cook-coona+h2o此反应计量点ph值9.1左右,同样可用酚酞为指示剂。
实验方法:一、naoh标准溶液的配制与标定用台式天平称取naoh1g于100ml烧杯中,加50ml蒸馏水,搅拌使其溶解。

实验5 气体绝热指数测量。
【预习提示】1、 熟悉气体的定压比热容、定容比热容、绝热指数、热力学过程等基本概念。
2、 理解热力学第一定律和理想气体的状态方程。
3、 了解绝热膨胀法测量空气的绝热指数的基本原理和方法。
4、 了解用传感器精确测量气体压强和温度的基本原理和方法。
【实验目的】1、 学习绝热膨胀法测量气体绝热指数的原理和方法。
2、 观察和分析热力学系统的状态和过程特征,掌握实现等值过程的方法。
3、 初步了解半导体气体压力传感器和电流型集成温度传感器的工作原理和使用方法。
【实验原理】1、 测量绝热指数的原理根据热力学第一定律,A E Q +∆=,系统自外界吸收的热量Q 等于系统内能的增加E ∆和对外界所做的功A 之和。
压强、温度、体积是研究气体状态的三个基本参量。
设想一储气瓶,上面有充气阀、放气阀,用打气球向瓶内打气,瓶内空气被压缩,也强增大,温度升高。
等瓶内气体稳定后,空气分子分布均匀,瓶内气体温度与室温相同,此时气体状态记录为(011T ,V ,p );迅速打开放气阀,使瓶,内气体与大气相通,则瓶内气体将有喷出,当压强降为大气压0p 时,关闭放气阀,根据热力学第一定律,气体对外界做功,内能减少,气体温度下降为T 1,,由于放气较快,瓶内保留气体可视作为未与外界进行热量交换,视为绝热膨胀过程;瓶内气体低于外界温度,气体将会从外界吸热直到达到室温为止,压强也会增加为P 2,这个过程视作为等容吸热过程。
将绝热膨胀后瓶内剩余气体作为一定质量的热力学系统来研究。
剩余气体放气前处于状态I ()011,,T V P ,经过绝热膨胀后气体由状态I 变为状态II ()120,,T V P 。
1V 是瓶内剩余气体在状态I 的体积,2V 是储气瓶的体积。
再经过等容吸热的过程由状态II ()120,,T V P 变为状态III ()022,,T V P 。
气体的状态变化过程如图所示。
由于状态I 和状态III 的温度均为0T ,因此,由状态I 到状态III 可视为等温过程。

【导语】进⾏科学实验的时候,⼀般需要写科学实验报告,以便⾃⼰记录相关的信息,找出不⾜的地⽅并改正。
以下是整理的科学实验报告模板,欢迎阅读!1.科学实验报告模板 ⼀、实验内容 1、实验⽬的:掌握⼀元线性回归⽅程的建⽴和基本的经济检验和统计检验。
2、实验要求:(1)对原始指标变量数据作价格因⼦的剔除处理;(2)对回归模型做出经济上的解释;(3)独⽴完成实验建模和实验报告。
⼆、实验报告 1、问题的提出 居民的消费在社会经济发展中具有重要的作⽤,合理适度的消费可以有利的促进经济的平稳健康的增长。
要充分发挥消费对经济的拉动作⽤,关键问题是如何保证居民的消费⽔平。
根据宏观经济学理论,⼀国的GDP扣除掉折旧和税收就是居民的可⽀配的收⼊了,⽽居民的收⼊主要⽤于两个⽅⾯:⼀是储蓄,⼆是消费。
如果⼈均GDP增加,那么居民的可⽀配收⼊也会增加,这样居民⽤于消费的应该也会增加。
本次实验通过运⽤中国年⼈均消费与经济⽔平(⽤⼈均GDP这个指标来表⽰)数据,建⽴模型研究⼈均消费和经济⽔平之间的关系。
西⽅消费经济学者们认为,收⼊是影响消费者消费的主要因素,消费是需求的函数。
消费经济学有关收⼊与消费的关系即消费函数理论有:(1)凯恩斯的绝对收⼊理论。
该理论认为消费主要取决于消费者的净收⼊,边际消费倾向⼩于平均消费倾向。
并且进⼀步假定,⼈们的现期消费,取决于他们现期收⼊的绝对量。
(2)杜森贝利的相对收⼊消费理论。
该理论认为消费者会受⾃⼰过去的消费习惯以及周围消费⽔准来决定消费,从⽽消费是相对的决定的。
这些理论都强调了收⼊对消费的影响。
除此之外,还有其他⼀些因素也会对消费⾏为产⽣影响。
(1)利率。
⼀般情况下,提⾼利率会刺激储蓄,从⽽减少消费。
但在现实中利率对储蓄的影响要视其对储蓄的替代效应和收⼊效应⽽定,具体问题具体分析。
(2)价格指数。
价格的变动可以使得实际收⼊发⽣变化,从⽽改变消费。
(3)⽣活环境,⽣活理念。
有些⼈受传统消费观念的影响,对现在流⾏的超前消费很不赞同,习惯于把钱存⼊银⾏,这样势必会影响⼀个地区的消费⽔平。
实验5溶液酸碱性的检验实验报告一、实验目的1.学习并熟悉常见的酸碱指示剂;2.通过纸浸法和滴定法,检测溶液的酸碱性。
二、实验原理酸碱指示剂是一种能够根据溶液的酸碱性质而改变颜色的物质。
常用的指示剂有酚酞、酸性紫、甲基橙、溴酚蓝等。
纸浸法是通过将指示纸浸入待检液体中,根据所见的颜色变化来判断溶液的酸碱性。
酸性溶液下,酸碱指示剂会呈现红色或橙色;碱性溶液下,指示剂呈现黄色或绿色。
滴定法是通过逐滴加入酸碱指示剂到待检液体中,根据颜色的变化来判断酸碱中和点的位置。
颜色的改变通常发生在酸碱中和点附近。
三、实验步骤1.准备酸碱指示剂:将酚酞、酸性紫、甲基橙、溴酚蓝分别加入小量的水溶液中,制备指示液;2.准备待检溶液:分别取一定量的醋酸、硫酸、氨水、氢氧化钠溶液;3.纸浸法:将指示纸分别浸入各种待检溶液中,观察颜色变化并记录下来;4.滴定法:将待检溶液倒入试管中,加入少量的酸碱指示剂,然后逐滴加入酸或碱,同时搅拌,直到初次颜色变化,记录下来滴加的体积。
四、实验数据记录1.酚酞指示剂:a.醋酸:红色b.硫酸:红色c.氨水:黄色d.氢氧化钠:黄色2.酸性紫指示剂:a.醋酸:红色b.硫酸:红色c.氨水:蓝色d.氢氧化钠:蓝色3.甲基橙指示剂:a.醋酸:橙色b.硫酸:红色c.氨水:橙色d.氢氧化钠:黄色4.溴酚蓝指示剂:a.醋酸:黄色b.硫酸:黄色c.氨水:蓝色d.氢氧化钠:蓝色五、实验结果分析通过纸浸法和滴定法,我们可以判断待检溶液的酸碱性质。
从实验数据可以看出:1.酚酞和酸性紫指示剂在酸性溶液中会呈现红色,而在碱性溶液中会呈现黄色或绿色;2.甲基橙指示剂在酸性溶液中会呈现红色,而在碱性溶液中会呈现黄色;3.溴酚蓝指示剂在酸性溶液中会呈现黄色,在碱性溶液中会呈现蓝色。
六、实验讨论通过本实验,我们可以很容易地区分溶液的酸碱性质。
在纸浸法中,待检液体会与指示纸上的指示剂发生染色反应,而在滴定法中,我们可以通过颜色的变化来找到酸碱中和点。
化学实验报告5篇化学实验报告模板1实验步骤(1)在试管中加入5mL5%的过氧化氢溶液,把带火星的木条伸入试管;(2)加热实验(1)的试管,把带火星的木条伸入试管;(3)在另一支试管中加入5mL5%的过氧化氢溶液,并加入2g二氧化锰,把带火星的木条伸入试管;(4)待实验(3)的试管内液体不再有现象发生时,重新加热3mL5%的过氧化氢溶液,把带火星的木条伸入试管;(该步骤实验可以反复多次) (5)实验后将二氧化锰回收、干燥、称量。
实验现象及现象解释:实验编号实验现象现象解释(1)木条不复燃(2)木条不复燃H2O2分解O2速度太慢没足够的O2试木条复燃.(3) 3H2O2产生大量气泡木条复燃MnO2使H2O2加速分解O2,O2使木条复然(4)新加入的H2O2产生大量气泡因为MnO2继续作为催化挤的作用!H2O2继续分解(5) 5MnO2的质量不变因为MnO2是催化剂所以只是改变化学反应速度,不改变其化学性质和质量化学实验报告模板2[实验目的]1、掌握常用量器的洗涤、使用及加热、溶解等操作。
2、掌握台秤、煤气灯、酒精喷灯的使用。
3、学会液体剂、固体试剂的取用。
[实验用品]仪器:仪器、烧杯、量筒、酒精灯、玻璃棒、胶头滴管、表面皿、蒸发皿、试管刷、试管夹、药匙、石棉网、托盘天平、酒精喷灯、煤气灯。
药品:硫酸铜晶体。
其他:火柴、去污粉、洗衣粉[实验步骤](一)玻璃仪器的洗涤和干燥1、洗涤方法一般先用自来水冲洗,再用试管刷刷洗。
若洗不干净,可用毛刷蘸少量去污粉或洗衣粉刷洗,若仍洗不干净可用重络酸加洗液浸泡处理(浸泡后将洗液小心倒回原瓶中供重复使用),然后依次用自来水和蒸馏水淋洗。
2、干燥方法洗净后不急用的玻璃仪器倒置在实验柜内或仪器架上晾干。
急用仪器,可放在电烘箱内烘干,放进去之前应尽量把水倒尽。
烧杯和蒸发皿可放在石棉网上用小火烘干。
操作时,试管口向下,来回移动,烤到不见水珠时,使管口向上,以便赶尽水气。
也可用电吹风把仪器吹干。
化学实验报告范例5篇化学实验报告范例11.准备工作(1) 清洗容量瓶,移液官及需用的玻璃器皿。
(2) 配制铁标溶液和其他辅助试剂。
(3) 开机并试至工作状态,操作步骤见附录。
(4) 检查仪器波长的正确性和吸收他的配套性。
2. 铁标溶液的配制准确称取0.3417g铁盐NH4Fe(SO4)·12H2O 置于烧杯中,加入10mlHCL加少量水。
溶解入500ml容量瓶中加水稀释到容量瓶刻度。
3 .绘制吸收曲线选择测量波长取两支50ml干净容量瓶,移取100μ g m l-1铁标准溶液2.50ml 容量瓶中,然后在两个容量瓶中各加入0.5ml盐酸羟胺溶液,摇匀,放置2min后各加入1.0ml邻二氮菲溶液,2.5ml醋酸钠溶液,用蒸馏水稀释至刻度线摇匀,用2cm吸收池,试剂空白为参比,在440——540nm间,每隔10nm测量一次吸光度,以波长为横坐标,吸光度为纵坐标,确定最大吸收波长4.工作曲线的绘制取50ml的容量瓶7个,各加入100.00μɡ ml-1铁标准0.00,0.20,0.40,0.60,0.80,1.00,1.20ml,然后分别加入0.5ml邻二氮菲溶液,2.5ml醋酸钠溶液,用蒸馏水稀释至刻度线摇匀,用2cm 吸收池,以试剂空白为参比溶液,在选定波长下测定并记录各溶液光度,记当格式参考下表:5.铁含量的测定取1支洁净的50ml容量瓶,加人2.5ml含铁未知试液,按步骤(6 )显色,测量吸光度并记录.K=268.1 B= -2.205 R*R=0.9945 CONC. =K *ABS+B C = 44.55mol ml-16.结束工作测量完毕,关闭电源插头,取出吸收池, 清洗晾干后人盆保存.清理工作台,罩上一仪器防尘罩,填写仪器使用记录.清洗容量瓶和其他所用的玻璃仪器并放回原处.化学实验报告范例2723型操作步骤1、插上插座,按后面开关开机2、机器自检吸光度和波长,至显示500。
3、按OTO键,输入测定波长数值按回车键。
初中科学实验报告范文精选5篇-电流研究性报告范文实验报告1:电流的发现及性质研究实验目的:通过实验观察和探究电流的发现及其性质。
实验器材:- 干电池- 电灯泡- 导线- 电流表实验步骤:1. 将干电池的正极和电灯泡的一端用导线连接起来。
2. 将电流表串联在电灯泡和负极之间。
3. 将干电池的负极与电灯泡的另一端用导线连接起来。
实验结果:当电路连通后,电流表指针偏转,显示有电流通过。
同时,电灯泡也亮起来。
如果断开电路,电流表指针归零,电灯泡熄灭。
实验结论:通过实验我们发现,当电路连通后,电流从正极流向负极,并且在电路中产生了辐射热和光热,导致电灯泡发光。
当电路断开时,电流停止流动,电灯泡熄灭。
实验报告2:电流的方向与强弱关系研究实验目的:通过实验观察和探究电流的方向与强弱关系。
实验器材:- 干电池- 电灯泡- 导线- 电流表实验步骤:1. 将干电池的正极和电灯泡的一端用导线连接起来。
2. 将电流表串联在电灯泡和负极之间。
3. 将干电池的负极与电灯泡的另一端用导线连接起来。
实验结果:将电流表接在正极和电灯泡之间,电流表指针指向正方向,表示电流从正极流向负极。
将电流表接在负极和电灯泡之间,电流表指针指向负方向,表示电流从负极流向正极。
实验结论:通过实验我们发现,电流的流动方向与电流表的指示方向相反。
当电流强度增大时,电流表的指针偏转角度增大;当电流强度减小时,电流表的指针偏转角度减小。
实验报告3:电流与电阻关系研究实验目的:通过实验观察和探究电流与电阻的关系。
实验器材:- 干电池- 电灯泡- 导线- 电流表- 变阻器实验步骤:1. 将干电池的正极和电灯泡的一端用导线连接起来。
2. 将电流表串联在电灯泡和负极之间。
3. 将干电池的负极与电灯泡的另一端用导线连接起来。
4. 连接变阻器在电路的一部分。
实验结果:改变变阻器的电阻大小,我们观察到当电阻增大时,电流减小;当电阻减小时,电流增大。
实验结论:通过实验我们发现,电流与电阻呈反比关系。
学生实验报告(5篇)(经典版)编制人:__________________审核人:__________________审批人:__________________编制单位:__________________编制时间:____年____月____日序言下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!并且,本店铺为大家提供各种类型的经典范文,如报告总结、合同协议、心得体会、演讲致辞、策划方案、职场文书、党团资料、教案资料、作文大全、其他范文等等,想了解不同范文格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!Moreover, our store provides various types of classic sample essays, such as report summaries, contract agreements, insights, speeches, planning plans, workplace documents, party and youth organization materials, lesson plans, essay compilations, and other sample essays. If you would like to learn about different sample formats and writing methods, please stay tuned!学生实验报告(5篇)报告,汉语词语,公文的一种格式,是指对上级有所陈请或汇报时所作的口头或书面的陈述。