磷酸锂中铁含量的测定
- 格式:pdf
- 大小:76.32 KB
- 文档页数:2

磷酸铁锂化学分析方法范围本标准规定了磷酸铁锂中磷、铁、锂以及碳的分析方法.本标准适用于磷酸铁锂产品、半成品及磷铁矿的分析.1.0 引用标准1.1 GB/T601-88 化学试剂滴定分析(容量分析)用标准溶液的制备;1.2 GB/T4701.7-1994 《磷铁的化学分析方法》;1.3 GB/T 3885.4-1983 锂辉.锂云母精矿化学方法火焰原子吸收光度法测定锂量.2.0 铁量的测定2.1 方法提要在盐酸溶液中,用二氯化锡将铁(Ⅲ)还原成铁(Ⅱ),然后加入氯化高汞以氧化过量的二氯化锡,用二苯胺磺酸钠为指示剂,以重铬酸钾标准溶液滴定,其反应式如下:2Fe3++Sn2++6Cl- →SnCl62-+2Fe2+4Cl-+Sn2++2HgCl2 →SnCl62-+Hg2Cl22Fe2++Cr2O72-+14H+ →6Fe3++2Cr3++7H2O2.2试剂2.2.1盐酸:(1+1);2.2.2 硫酸—磷酸混酸:将150ml硫酸慢慢地加入500ml水中,冷却后加入150ml磷酸,用水稀释至1L,混匀;2.2.3 二氯化锡溶液(100g/L ):称取10g氯化锡溶于10ml(1+1)盐酸中,用水稀释至100ml (若溶液浑浊则需过滤);2.2.4 二苯胺磺酸钠指示剂(0.5%):2.2.5 氯化高汞饱和溶液【C(1/6K2Cr2O7)=0.0500mol/L】溶液:称取2.4518g预先在150度烘干1h的重铬酸钾(基准试剂)于250ml烧杯中,以少量水溶解后移入1L容量瓶中,用水定容。
2.3 分析步骤称取0.2000g试样于250ml三角瓶中,加入10ml盐酸溶液,置于低温电炉上加热至完全溶解,取下稍冷,加入30ml水,加热至沸,趁热滴加二氯化锡溶液至黄色消失后再过量1~2滴,流水冷却至室温,加入10ml氯化高汞饱和溶液,混匀,静置2min后,用水稀释至80ml,加入20ml硫磷混酸溶液,4~5滴二苯胺磺酸钠指示剂,用重铬酸钾标准溶液滴定,溶液由绿色转变成蓝紫色为终点。


目录一.铁含量的检测2二.火焰原子吸收分光光度法测定锂、镍、锰、钴、钙、镁、铜、锌4三.差减重量法测定水份8四.磷酸铁锂样品PH值的检测9五.磷含量的检测10六.碳含量的检测12七.振实密度的检测13八.粒度的检测14九.比表面积的检测16磷酸铁锂化学分析方法适用范围:磷酸铁锂的主元素铁含量,杂质项目,水分,PH值,磷含量和碳含量的检测。
一.铁含量的检测1.方法提要试样以酸分解,在热溶液中以SnCl2还原大部分Fe3+,以CuSO4-靛红指示剂,滴加TiCl3还原剩余的Fe3+,过量的Ti3+在微量Cu的催化下短时间内氧化成四价,然后以二苯胺磺酸钠为指示剂,用K2Cr2O7标准溶液滴定至紫红色为终点。
2.试剂2.1 盐酸:1+1(GR)。
2.2 SnCl2 5%:称取SnCl2 5g以20ml(1+1)HCl加热溶解后用水稀至100ml。
2.3 TiCl3溶液:量取30ml 15%的TiCl3加30ml(1+1)HCl,以水稀至100ml,加几粒锌粒。
2.4 CuSO4-靛红指示剂:0.5g靛红指示剂溶于0.1%的100ml CuSO4溶液中,再加(1+4)H2SO40.5ml。
2.5 二苯胺磺酸钠:0.5%的水溶液。
2.6H2SO4-H3PO4混酸:15%。
2.7K2Cr2O7标准溶液0.05mol/L:称取 1.2258g150℃-160℃烘2小时的K2Cr2O7溶于水,定容至500ml。
3.分析步骤准确称取LiFePO4样品1.0000g于250ml烧杯中,用水润湿,加9mlHClO4,加热分解至高氯酸冒浓烟,待烟冒至少许,剩余高氯酸体积约3-5ml,取下冷却用水冲洗表面皿,转入100ml容量瓶中用水定容,摇匀沉清,分取20.00ml清液于250ml锥形瓶中,加(1+1)盐酸20ml,加热至沸腾煮沸半分钟。
加SnCl2至溶液呈淡黄色,滴加2滴CuSO4-靛红指示剂变绿色,滴加TiCl3至绿色消失,过量半滴,放置溶液变为蓝色,冷却至室温,加15ml硫磷混酸,以二苯胺磺酸钠为指示剂,用K 2Cr 2O 7标准溶液滴至紫红色为终点。
![一种测定磷酸铁锂中元素含量的荧光分析方法[发明专利]](https://uimg.taocdn.com/4e1a7f1e7275a417866fb84ae45c3b3567ecdd31.webp)
(19)中华人民共和国国家知识产权局(12)发明专利申请(10)申请公布号 (43)申请公布日 (21)申请号 201610168627.7(22)申请日 2016.03.23(71)申请人 合肥国轩高科动力能源有限公司地址 230011 安徽省合肥市新站区岱河路599号(72)发明人 方婷婷 夏劲 (74)专利代理机构 合肥天明专利事务所 34115代理人 汪贵艳(51)Int.Cl.G01N 23/223(2006.01)(54)发明名称一种测定磷酸铁锂中元素含量的荧光分析方法(57)摘要本发明公开了一种用于测定磷酸铁锂中磷铁元素含量的荧光分析方法,包括将磷酸铁锂样品平分为三份;采用盐酸处理第一份磷酸铁锂样品,过滤后用重铬酸钾标准溶液滴定,测得铁元素含量;采用盐酸处理第二份磷酸铁锂样品,过滤后用磷钼酸铵容量法测得磷元素含量;将第三份磷酸铁锂样品配制成含量不同的六个标准样品;再分别压制成片状,再通过X射线荧光光谱法测得各片状标准样品中铁、磷元素的荧光强度;绘出XRF标准曲线;将待测的磷酸铁锂样品压制成片状中,测其荧光强度;通过XRF标准曲线,即得出铁、磷元素含量。
本发明先利用湿化学法和X 荧光光谱法相结合的方法快捷高速,且操作简单、误差小,消耗时间长,对环境污染环保。
权利要求书1页 说明书5页CN 105842266 A 2016.08.10C N 105842266A1.一种用于测定磷酸铁锂中磷铁元素含量的荧光分析方法,其特征在于:包括以下步骤:(1)取同一批次磷酸铁锂样品,并将其平分为三份;(2)采用盐酸处理第一份磷酸铁锂样品,过滤未反应的碳后,形成待测样品溶液;用重铬酸钾标准溶液对其进行滴定,测得待测样品溶液中铁元素的含量;(3)采用盐酸处理第二份磷酸铁锂样品,过滤未反应的碳后,形成待测样品溶液;用磷钼酸铵容量法测得待测样品溶液中磷元素的含量;(4)将第三份磷酸铁锂样品均分为至少六份,分别加入不同含量的碳酸钙基准物质,配制成含量不同的标准样品;再采用粉末压片法将各个标准样品分别压制成片状,然后通过X 射线荧光光谱法测得各片状标准样品中铁、磷元素的荧光强度;(5)将步骤(4)中通过X射线荧光光谱法所测得的磷酸铁锂样品中铁、磷元素的荧光强度,与通过步骤(2)、(3)所测得的磷酸铁锂样品中铁、磷元素的含量进行关联,形成以荧光强度为纵坐标、以铁、磷元素的含量为横坐标的XRF标准曲线;(6)采用与步骤(4)中相同的粉末压片法将待测的磷酸铁锂样品压制成片状,得到待测样品,通过X射线荧光光谱法测得待测样品中各元素的荧光强度;通过步骤(5)所得的XRF标准曲线,即可得出待测样品中铁、磷元素的含量。

锂含量的测定1 原理试样用盐酸-硝酸溶解,在硝酸介质中,使用空气—乙炔火焰,于原子吸收分光光度计波长670.78nm处测定锂的吸光度。
2 试剂及仪器硝酸:浓硝酸;盐酸:1+1体积比;高纯碳酸锂;氯化钾(10%)锂标准贮存溶液(1mg/mL):称取碳酸锂0.5324 g于100 mL烧杯中,用少量水润湿,滴加10mL(1:1)硝酸至全部溶解,加热煮沸2min,冷却后,转入100mL 容量瓶中,用蒸馏水稀释至刻度。
锂标准溶液(100ug/mL),取10mL的上述溶液,加入100 mL的容量瓶中,用蒸馏水稀释至刻度。
分别移取0、1.00、2.00、3.00、4.00、5.00 mL锂标准溶液(100ug/mL)于一组100mL容量瓶中,加入2mL硝酸(1+1),加1mL氯化钾溶液,稀释至刻度,摇匀。
与试样同时同条件下于原子吸收光谱波长670.78nm处测量其吸光度,以锂浓度为横坐标,吸光度为纵坐标;绘制工作曲线。
3 分析步骤3.1 测定称取试样0.5000 g置于250 mL烧杯中,加少量水润湿试样,加入25 mL盐酸(1+1),盖上表面皿,加热溶解,待试样分解后,取下稍冷,加入10mL硝酸继续加热溶解,蒸发至体积5 mL左右,取下稍冷,加入20 mL水,煮沸,取下冷却,用蒸馏水冲洗表面皿,移入250 mL容量瓶中,以水稀释至刻度,摇匀。
移取4.00 mL试液于100 mL容量瓶中,加1mL氯化钾溶液,以水稀释至刻度,摇匀,与标准溶液同时同条件下,于原子吸收光谱670.78nm处测量其吸光度,在工作曲线上查出锂的浓度。
3.2 回收率测定(准确度测定)取4 mL试样溶液,取2 mL锂标准溶液,加入100 mL容量瓶中,加1mL氯化钾溶液,以水稀释至刻度,摇匀,与标准溶液同时同条件下,于原子吸收光谱670.78nm处测量其吸光度,在工作曲线上查出锂的浓度,据此计算回收率,回收率范围95%~105%正常。
3.3 精密度测定平行至少测三次样品的锂含量,求平均值和平均相对偏差。

磷酸铁锂化学分析方法第1部分总铁的测定重铬酸钾滴定法讨论稿编制说明一、工作简况(包括任务来源、协作单位、主要工作过程)1.1 任务来源根据工业和信息化部《关于印发2012年第二批行业标准制修订计划的通知》(工信厅科【2012】119号)文件及全国有色金属标准化技术委员会“关于转发2012年有色金属国家、行业标准制(修)订项目计划的通知”,“磷酸铁锂化学分析方法(5部分)”行业标准制订项目(项目号:2012-0637T-YS、2012-0638T-YS、2012-0639T-YS、2012-0640T-YS、2012-0641T-YS)由佛山市邦普循环科技有限公司(现更名为广东邦普循环科技股份有限公司)牵头起草,计划完成年限2013年。
1.2 起草单位情况邦普,创立于2005年。
企业总部(广东邦普循环科技股份有限公司)位于广东南海新材料产业基地核心区,总注册资本7645万元人民币;循环基地(湖南邦普循环科技有限公司)位于湖南长沙国家节能环保新材料产业基地,总注册资本6000万元人民币。
邦普,是全球专业的废旧电池及报废汽车资源化回收处理和高端电池材料生产的国家级高新技术企业。
通过几年的快速发展,邦普已形成“电池循环、载体循环和循环服务”三大产业板块,专业从事数码电池(手机和笔记本电脑等数码电子产品用充电电池)和动力电池(电动汽车用动力电池)回收处理、梯度储能利用;传统报废汽车回收拆解、关键零部件再制造;以及高端电池材料和汽车功能瓶颈材料的工业生产、商业化循环服务解决方案的提供。
其中,邦普年处理废旧电池总量超过6000吨、年生产镍钴锰氢氧化物4500吨,总收率超过98.58%,回收处理规模和资源循环产能已跃居亚洲首位。
邦普通过独创的“逆向产品定位设计”技术,在全球废旧电池回收领域率先破解“废料还原”的行业性难题,并成功开发和掌握了废料与原料对接的“定向循环”核心技术,一举成为回收行业为数不多的新材料企业。
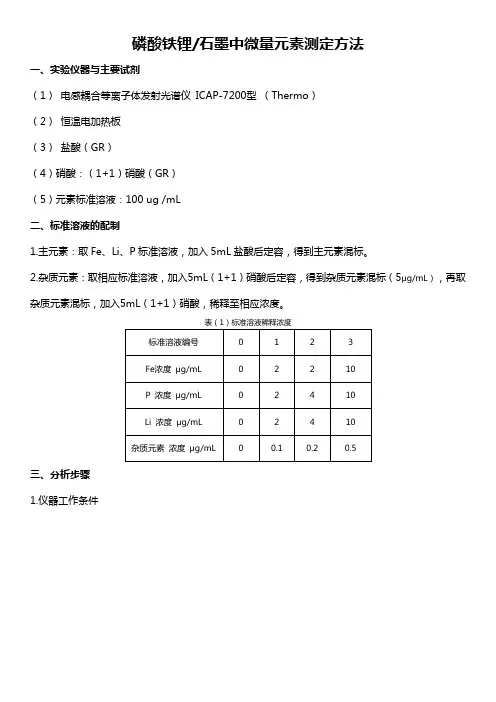
磷酸铁锂/石墨中微量元素测定方法一、实验仪器与主要试剂(1)电感耦合等离子体发射光谱仪ICAP-7200型(Thermo)(2)恒温电加热板(3)盐酸(GR)(4)硝酸:(1+1)硝酸(GR)(5)元素标准溶液:100 ug /mL二、标准溶液的配制1.主元素:取Fe、Li、P标准溶液,加入5mL盐酸后定容,得到主元素混标。
2.杂质元素:取相应标准溶液,加入5mL(1+1)硝酸后定容,得到杂质元素混标(5μg/mL),再取杂质元素混标,加入5mL(1+1)硝酸,稀释至相应浓度。
三、分析步骤1.仪器工作条件表(2)元素测试波长2. 试样溶液配制2.1 称取0.5000g (精确至0.0001g)LiFePO4试样于100mL 烧杯中,加少量水润湿试样,加入30mL 硝酸(1+1),盖上玻璃表面皿在加热器上加热至微沸(180-220℃),保持30min,取下冷却,过滤,将滤液转移至100mL 容量瓶中,以水稀释至刻度,摇匀,用来测试杂质元素。
2.2 取1.00mL上述溶液于250mL 容量瓶中,加20mL 盐酸(GR)用水稀释至刻度,摇匀,用来测试主元素。
3. 上机测试3.1 分析参数设置:样品重复测试2次样品冲洗时间10S3.2 等离子源设置:功率1150W辅助气流量0.5 L/min雾化器气体流量0.7 L/min3.3 标准溶液浓度设置3.4 按照表(2)的工作条件新建测试方法,先用标准溶液绘制工作曲线,然后测试试样溶液谱线强度,在标准曲线上得到溶液中各元素的浓度,输入样品的重量、体积、稀释倍数,结果计算机自动给出。
4. 检出限测试4.1配置试样溶液时,同时配置试剂空白,上机测试时,连续测试空白溶液10次,得到相对标准偏差。
4.2以10次基体空白溶液的3倍标准偏差做为该基体条件下的检出限,其中方法定量限采用3倍检出限乘以稀释因子。
表(3)元素检出限四、注意事项1.Na和Ca元素性质不稳定,标准溶液保存时间不易过长,有条件可单独配置这两种元素的混合标准溶液。

锂电池正极材料中锂磷铁含量的测试方法一、原子吸收光谱法(Atomic Absorption Spectroscopy, AAS)原理:原子吸收光谱法基于原子或离子在特定波长下对吸收光的选择性吸收现象。
样品溶液经过雾化和干燥后进入火焰或炉体中,吸收特定波长的光线后,通过检测系统测量光强的变化,进而计算出待测元素的浓度。
步骤:1.先将锂电池正极材料样品悉数溶解于酸性溶液中,并配制成待测元素的标准溶液系列。
2.将样品及其标准溶液系列分别进入原子吸收光谱仪中进行测试。
根据样品的吸光度与标准曲线之间的关系,可以计算出锂、磷、铁的含量。
应用范围:原子吸收光谱法在锂电池领域得到广泛应用,可用于锂电池正极材料中锂、磷、铁含量的测定。
二、原子荧光光谱法(Atomic Fluorescence Spectroscopy, AFS)原理:原子荧光光谱法通过对原子或离子激发和荧光辐射的研究,实现对元素含量的分析。
样品原子经过电子冲击激发而产生的荧光辐射强度与元素含量成正比,通过测定样品荧光光谱强度,可以计算出待测元素的浓度。
步骤:1.将锂电池正极材料样品制备成适当浓度的溶液,并添加荧光剂,使样品中待测元素形成荧光化合物。
2.将样品溶液进入原子荧光光谱仪中,通过激发源对样品进行激发,并测量荧光辐射强度。
3.根据样品荧光光谱强度与标准曲线之间的关系,可以计算出锂、磷、铁的含量。
应用范围:原子荧光光谱法可用于锂电池正极材料中锂、磷、铁含量的测试,具有非常高的敏感度和选择性。
三、电感耦合等离子体发射光谱法(Inductively Coupled Plasma - Atomic Emission Spectroscopy, ICP-AES)原理:电感耦合等离子体发射光谱法是利用感应耦合等离子体将样品中的元素转化为带电离子,并通过电磁场的作用使离子激发发射特征的光线。
不同元素的发射光线通过光谱仪进行检测和分析,从而实现对元素含量的测定。

目录磷酸铁锂化学分析方法适用范围:磷酸铁锂的主元素铁含量,杂质项目,水分,PH值,磷含量和碳含量的检测。
一.铁含量的检测1.方法提要试样以酸分解,在热溶液中以SnCl2还原大部分Fe3+,以CuSO4-靛红指示剂,滴加TiCl3还原剩余的Fe3+,过量的Ti3+在微量Cu的催化下短时间内氧化成四价,然后以二苯胺磺酸钠为指示剂,用K 2Cr2O7标准溶液滴定至紫红色为终点。
2.试剂2.1盐酸:1+1(GR)。
2.2SnCl25%:称取SnCl25g以20ml(1+1)HCl加热溶解后用水稀至100ml。
2.3TiCl3溶液:量取30ml15%的TiCl3加30ml(1+1)HCl,以水稀至100ml,加几粒锌粒。
2.4CuSO4-靛红指示剂:0.5g靛红指示剂溶于0.1%的100mlCuSO4溶液中,再加(1+4)H2SO40.5ml。
2.5二苯胺磺酸钠:0.5%的水溶液。
2.6H2SO4-H3PO4混酸:15%。
2.7K2Cr2O7标准溶液0.05mol/L:称取1.2258g150℃-160℃烘2小时的K2Cr2O7溶于水,定容至500ml。
3.分析步骤准确称取LiFePO4样品1.0000g于250ml烧杯中,用水润湿,加9mlHClO4,加热分解至高氯酸冒浓烟,待烟冒至少许,剩余高氯酸体积约3-5ml,取下冷却用水冲洗表面皿,转入100ml容量瓶中用水定容,摇匀沉清,分取20.00ml清液于250ml锥形瓶中,加(1+1)盐酸20ml,加热至沸腾煮沸半分钟。
加SnCl2至溶液呈淡黄色,滴加2滴CuSO4-靛红指示剂变绿色,滴加TiCl3至绿色消失,过量半滴,放置溶液变为蓝色,冷却至室温,加15ml硫磷混酸,以二苯胺磺酸钠为指示剂,用K2Cr2O7标准溶液滴至紫红色为终点。
4.分析结果计算式中:C--K2Cr2O7标准溶液的浓度,单位mol/L;V——K2Cr2O7的体积,单位为ml;m——磷酸铁锂的质量,单位为g;55.85——Fe的摩尔质量,单位为g/mol。

磷酸铁锂化学分析方法范围本标准规定了磷酸铁锂中磷、铁、锂以及碳的分析方法.本标准适用于磷酸铁锂产品、半成品及磷铁矿的分析.1.0 引用标准1.1 GB/T601-88 化学试剂滴定分析(容量分析)用标准溶液的制备;1.2 GB/T4701.7-1994 《磷铁的化学分析方法》;1.3 GB/T 3885.4-1983 锂辉.锂云母精矿化学方法火焰原子吸收光度法测定锂量.2.0 铁量的测定2.1 方法提要在盐酸溶液中,用二氯化锡将铁(Ⅲ)还原成铁(Ⅱ),然后加入氯化高汞以氧化过量的二氯化锡,用二苯胺磺酸钠为指示剂,以重铬酸钾标准溶液滴定,其反应式如下:2Fe3++Sn2++6Cl- →SnCl62-+2Fe2+4Cl-+Sn2++2HgCl2 →SnCl62-+Hg2Cl22Fe2++Cr2O72-+14H+ →6Fe3++2Cr3++7H2O2.2试剂2.2.1盐酸:(1+1);2.2.2 硫酸—磷酸混酸:将150ml硫酸慢慢地加入500ml水中,冷却后加入150ml磷酸,用水稀释至1L,混匀;2.2.3 二氯化锡溶液(100g/L ):称取10g氯化锡溶于10ml(1+1)盐酸中,用水稀释至100ml (若溶液浑浊则需过滤);2.2.4 二苯胺磺酸钠指示剂(0.5%):2.2.5 氯化高汞饱和溶液【C(1/6K2Cr2O7)=0.0500mol/L】溶液:称取2.4518g预先在150度烘干1h的重铬酸钾(基准试剂)于250ml烧杯中,以少量水溶解后移入1L容量瓶中,用水定容。
2.3 分析步骤称取0.2000g试样于250ml三角瓶中,加入10ml盐酸溶液,置于低温电炉上加热至完全溶解,取下稍冷,加入30ml水,加热至沸,趁热滴加二氯化锡溶液至黄色消失后再过量1~2滴,流水冷却至室温,加入10ml氯化高汞饱和溶液,混匀,静置2min后,用水稀释至80ml,加入20ml硫磷混酸溶液,4~5滴二苯胺磺酸钠指示剂,用重铬酸钾标准溶液滴定,溶液由绿色转变成蓝紫色为终点。

重铬酸钾滴定法测定碳包覆磷酸铁锂中全铁谢英豪;余海军;黎俊茂;欧彦楠;李长东【摘要】实际磷酸铁锂样品颗粒表面常包覆一层碳,碳的存在可能对酸溶解样品有一定的影响.通过试验确定试样经盐酸加热10 min溶解后,过滤除碳,在酸性条件下以TiCl3为还原剂将少量的Fe3+还原,然后加入15 mL硫磷混酸,滴加3~4滴5 g/L二苯胺磺酸钠溶液后,采用重铬酸钾滴定法测定碳包覆磷酸铁锂中全铁含量.实际磷酸铁锂样品通常掺杂的金属元素对测定没有干扰.采用实验方法对实际样品的全铁含量进行测定,相对标准偏差(RSD)小于0.2%,加标回收率为99.7%~100.3%,适合于实际生产和科研中碳包覆磷酸铁锂中全铁含量的测定.【期刊名称】《冶金分析》【年(卷),期】2014(034)004【总页数】5页(P51-55)【关键词】滴定法;碳包覆磷酸铁锂;重铬酸钾;全铁【作者】谢英豪;余海军;黎俊茂;欧彦楠;李长东【作者单位】广东邦普循环科技有限公司,广东佛山528244;广东邦普循环科技有限公司,广东佛山528244;广东动力电池和电动汽车循环利用研究院士工作站,广东佛山528244;广东邦普循环科技有限公司,广东佛山528244;广东邦普循环科技有限公司,广东佛山528244;广东邦普循环科技有限公司,广东佛山528244;广东动力电池和电动汽车循环利用研究院士工作站,广东佛山528244【正文语种】中文【中图分类】O655.23磷酸铁锂由于原料来源广、成本低、无环境污染、循环性好、热稳定性好等突出优点,现广泛作为动力型锂离子电池的正极材料[1]。
然而磷酸铁锂自身的Li+扩散系数和电子电导率较小,通常需要在其颗粒表面包覆碳[2]及掺杂金属离子以改善其高倍率充放电性能。
碳的包覆导致测定样品溶解时无法判断铁元素是否能够完全溶出。
全铁含量对碳包覆磷酸铁锂性能发挥影响较大,在科研、生产和质量控制中均需要进行测定。
通常,可采用氧化还原滴定法[3-4]、电位滴定法[5-6]、X 射线荧光光谱法[7]和分光光度法[8]等手段检测样品中全铁含量。
目录一.铁含量的检测2二.火焰原子吸收分光光度法测定锂、镍、锰、钴、钙、镁、铜、锌4三.差减重量法测定水份8四.磷酸铁锂样品PH值的检测9五.磷含量的检测10六.碳含量的检测12七.振实密度的检测13八.粒度的检测14九.比表面积的检测16磷酸铁锂化学分析方法适用范围:磷酸铁锂的主元素铁含量,杂质项目,水分,PH值,磷含量和碳含量的检测。
一.铁含量的检测1.方法提要试样以酸分解,在热溶液中以SnCl2还原大部分Fe3+,以CuSO4-靛红指示剂,滴加TiCl3还原剩余的Fe3+,过量的Ti3+在微量Cu的催化下短时间内氧化成四价,然后以二苯胺磺酸钠为指示剂,用K2Cr2O7标准溶液滴定至紫红色为终点。
2.试剂2.1 盐酸:1+1(GR)。
2.2 SnCl2 5%:称取SnCl2 5g以20ml(1+1)HCl加热溶解后用水稀至100ml。
2.3 TiCl3溶液:量取30ml 15%的TiCl3加30ml(1+1)HCl,以水稀至100ml,加几粒锌粒。
2.4 CuSO4-靛红指示剂:0.5g靛红指示剂溶于0.1%的100ml CuSO4溶液中,再加(1+4)H2SO40.5ml。
2.5 二苯胺磺酸钠:0.5%的水溶液。
2.6H2SO4-H3PO4混酸:15%。
2.7K2Cr2O7标准溶液0.05mol/L:称取 1.2258g150℃-160℃烘2小时的K2Cr2O7溶于水,定容至500ml。
3.分析步骤准确称取LiFePO4样品1.0000g于250ml烧杯中,用水润湿,加9mlHClO4,加热分解至高氯酸冒浓烟,待烟冒至少许,剩余高氯酸体积约3-5ml,取下冷却用水冲洗表面皿,转入100ml容量瓶中用水定容,摇匀沉清,分取20.00ml清液于250ml锥形瓶中,加(1+1)盐酸20ml,加热至沸腾煮沸半分钟。
加SnCl2至溶液呈淡黄色,滴加2滴CuSO4-靛红指示剂变绿色,滴加TiCl3至绿色消失,过量半滴,放置溶液变为蓝色,冷却至室温,加15ml硫磷混酸,以二苯胺磺酸钠为指示剂,用K 2Cr 2O 7标准溶液滴至紫红色为终点。
磷酸铁锂电池铁含量的检测方法
磷酸铁锂电池是目前应用广泛的一种电池,其中铁含量的检测是非常重要的一个指标。
本文介绍了一种简单、快速、准确的磷酸铁锂电池铁含量检测方法。
首先,将待测样品溶解于1mol/L HCl中,加入适量的酸性钾铬
酸钾溶液作为指示剂,然后用0.1mol/L 氨水滴定至溶液转变为深绿色,记录氨水用量。
其次,用同样的方法制备铁离子的标准溶液,使用0.1mol/L 氨水滴定至溶液转变为深绿色,记录氨水用量。
最后,将待测样品铁含量的计算公式为:铁含量(mg/g)=(标
准溶液氨水用量-待测溶液氨水用量)×0.5585×1000÷样品质量(g)。
该方法简单易行,所需试剂易得,且检测结果准确、可靠,适用于磷酸铁锂电池铁含量的检测。
- 1 -。
产品中磷、铁、锂、碳的检测方法1.0范围本标准规定了磷酸铁锂中磷、铁、锂以及碳的分析方法。
本标准适用于磷酸铁锂产品、半成品及原材料的分析。
2.0 引用标准2.1 GB/T601-88 化学试剂滴定分析(容量分析)用标准溶液的制备;2.2 GB/T4701.7-1994 《磷铁的化学分析方法》;2.3 GB/T 3885.4-1983 锂辉.锂云母精矿化学方法火焰原子吸收光度法测定锂量。
3.0 铁量的测定3.1 方法提要在盐酸溶液中,用二氯化锡将铁(Ⅲ)还原成铁(Ⅱ),然后加入氯化高汞以氧化过量的二氯化锡,用二苯胺磺酸钠为指示剂,以重铬酸钾标准溶液滴定,其反应式如下:2Fe3++Sn2++6Cl-→SnCl62-+2Fe2+4Cl-+Sn2++2HgCl2 →SnCl62-+Hg2Cl26Fe2++Cr2O72-+14H+→ 6Fe3++2Cr3++7H2O3.2试剂3.2.1盐酸:(1+1);3.2.2 硫酸—磷酸混酸:将150ml硫酸慢慢地加入500ml水中,冷却后加入150ml 磷酸,用水稀释至1L,混匀;3.2.3 二氯化锡溶液(100g/L ):称取10g氯化锡溶于10ml(1+1)盐酸中,用水稀释至100ml(若溶液浑浊则需过滤);3.2.4 二苯胺磺酸钠指示剂(0.5%):3.2.5 氯化高汞饱和溶液[C(1/6K2Cr2O7)=0.0500mol/L]溶液:称取2.4518g预先在150度烘干1h的重铬酸钾(基准试剂)于250ml烧杯中,以少量水溶解后移入1L容量瓶中,用水定容。
3.3 分析步骤称取0.2000g试样于250ml三角瓶中,加入10ml盐酸溶液,置于低温电炉上加热至完全溶解,取下稍冷,加入30ml水,加热至沸,趁热滴加二氯化锡溶液至黄色消失后再过量1~2滴,流水冷却至室温,加入10ml氯化高汞饱和溶液,混匀,静置2min后,用水稀释至80ml,加入20ml硫磷混酸溶液,4~5滴二苯胺磺酸钠指示剂,用重铬酸钾标准溶液滴定,溶液由绿色转变成蓝紫色为终点。