Ch4多组分系统热力学及其在溶液中的应用.ppt
- 格式:ppt
- 大小:3.52 MB
- 文档页数:138

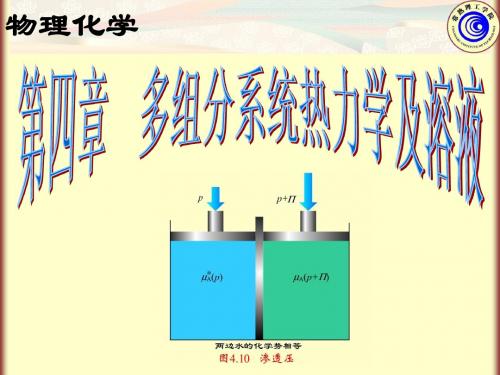


第四章多组分系统热力学及其在溶液中的应用教材分析:本章介绍了溶液组成的表示方法,讲述了化学势和偏摩尔量两个重要概念,将多组分系统的热力学理论应用于溶液中各组分的化学势的表示,从而为研究溶液的各种性质奠定了基础,在此基础上,讨论了稀溶液的最基本的性质——依数性。
它是热力学理论对于溶液系统的应用。
教学目的和要求:通过本章的教学使学生了解和掌握溶液的浓度的各种表示方法,拉乌尔定律及亨利定律,稀溶液、理想溶液的意义;实际溶液与理想溶液的区别;活度的概念及意义,标准态的选用。
化学势及偏摩尔量的定义及相关公式。
掌握稀溶液与理想溶液、非理想溶液三者的区别、关系及各自性质。
加深对拉乌尔定律及亨利定律的理解并熟悉其应用。
活度的概念及标准态的选用及溶液中各组分化学势的表示,是本章的一个难点,必须使学生理解这些概念及其意义。
重点和难点:拉乌尔定律和亨利定律;偏摩尔量和化学势概念;由两个经验定律导出溶液中各组分的化学势的过程和思路;稀溶液、理想溶液的意义;活度的概念与意义;标准态的选用。
教学内容与过程:溶液组成的表示法,偏摩尔量和化学势的概念,溶液的基本性质和两个经验定律,混合气体中各组分的化学势,稀溶液(组分的化学势与标准态,依数性),理想溶液(理想溶液的定义,化学势,通性等)。
思考题、作业:1.课后全部复习题2.作业题:6,8,10,11,12,15,17,18,20,23,25,26,27。
参考资料:1.胡英主编,《物理化学》2.天津大学主编,《物理化学》3.万洪文主编,《物理化学》4.各种习题解题辅导书5.课后所列各种参考读物。
第三节 多组分系统中物质的偏摩尔量与化学势在这以前人们所讨论的热力学体系都是纯组分的体系或者是组分不变的单相体系。
因此,所有的热力学函数U m 、H m 、S m 、G m 、F m 在体系的T 、p 一定的条件下有确定值。
即在这种情况下,要描述体系的状态只要两个状态性质(如T 、p )就行了。

第四章 多组分系统热力学及其在溶液中的应用1.在298K 时,有0.10kg 质量分数为0.0947的硫酸H 2SO 4水溶液,试分别用(1)质量摩尔浓度B m ;(2)物质的量浓度和B c (3)摩尔分数B x 来表示硫酸的含量。
已知在该条件下,硫酸溶液的密度为331.060310kg m -⨯⋅ ,纯水的浓度为3997.1kg m -⋅ 。
解:质量摩尔浓度:()2410.19.47%/1009.47%0.1981.067mol H SO B n m W kg -⨯==-⨯=⋅水物质量浓度:()24331009.47%0.10.19.47%/98997.11.02310mol H SO B n c V m --⨯⨯===⨯g 水 摩尔分数:242420.0189H SO B H SO H On x n n ==+2、在K 298和大气压力下,含甲醇()B 的摩尔分数B x 为0.458的水溶液密度为30.8946kg dm -⋅,甲醇的偏摩尔体积313()39.80V CH OH cm mol -=⋅,试求该水溶液中水的摩尔体积2()V H O 。
解:3322CH OH CH OH H O H O V n V n V =+3322CH OH CH OHH O H OV n V V n -=以1mol 甲醇水溶液为基准,则330.45832(10.458)180.027290.894610m V dm ρ⨯+-⨯===⨯ ∴23310.027290.45839.801016.7210.458H OV cm mol ---⨯⨯==⋅-3.在298K 和大气压下,某酒窖中存在酒10.0m3,其中含乙醇的质量分数为0.96。
今欲加水调制含乙醇的质量分数为0.56的酒,试计算(1)应加入水的体积;(2)加水后,能得到含乙醇的质量分数为0.56的酒的体积已知该条件下,纯水的密度为3997.1kg m -⋅,水和乙醇的偏摩尔体积为()25C H OH ω()()6312/10V H O m mol --⋅ ()()63125/10V C H OH m mol --⋅0.96 14.61 58.0 0.5617.11 56.58解:设加入水的物质的量为O H n 2',根据题意,未加水时,2520.9610.96::9.3914618C H OH H O n n -== 2525221C H O H C H O H H O H OV n V n V =⋅+⋅ 即 661001.581061.1410522--⨯⨯+⨯⨯=O H H C O H n n 解出:25167882C H OH n mol =217877H O n mol = 加入水后,25220.5610.56:():0.4984618C H O HH O H On n n -'+== 20.5610.56167882:(17877):0.4984618H O n -'+== 2'317887H O n mol = 加入水的物质的体积为23331788718105.727()999.1H O V m -⨯⨯'== 2525222252'26'6()56.5810(17877)17.1110C H OH C H OH H O H OH OC H OH H OV n V n n V n n--=++=⨯⨯++⨯⨯329.4984495 5.76753115.266V m =+=4.在K 298和kPa 100下,甲醇)(B 的摩尔分数B x 为30.0的水溶液中,水)(A 和甲醇)(B 的偏摩尔体积分别为:132765.17)(-⋅=mol cm O H V ,133632.38)(-⋅=mol cm OH CH V 。
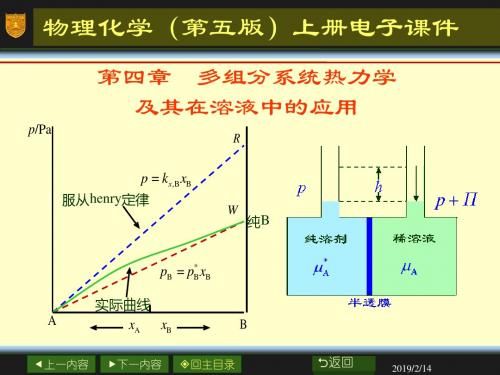
多组分系统热力学及其在溶液中的应用2在前面的讨论中,我们所涉及到的系统均为纯物质系统或组成恒定的系统。
但在实际上常见的却是多组分系统或变速成系统。
本章将就多组分系统的热力学问题进行讨论。
在正式讨论之前,先将多组分系统进行分类:①按研究的方法分:多组分系统可有单相和多相之分。
本章将讨论多组分系统单相系统。
多组分单相系统由两种或两种以上的物质以分子大小相互均匀混合而成的均匀系统当对均匀系统中各组分现用相同的标准和同样方法研究时,称之为混合物;当对均匀系统中各组分加以区别,选用不同的标准和不同的方法(例如:将系统中的组分分为溶剂(A)和溶质(B))研究时,称之为溶液。
②按聚集状态分:分为气态溶液或混合物、液态溶液或混合物、固态溶液或混合物本章讨论的对象主要是液态系统,包括液态溶液和液态混合物。
③按导电性能分:对于溶液中溶质,按其导电性能可分为电解质溶液和非电解质溶液,本能力讨论非电解质溶液。
④按规律性分:理想混合物理想稀溶液混合物{溶液{真实混合物真实溶液本章讨论的主要对象为混合物和稀溶液,适当介绍一些真实溶液。
1.物质B的物质的量分数(物质B的摩尔分数):某BnB某B=────∑B某B=1∑BnB2.物质B的物质的质量分数:WBmBWB=────∑BWB=1∑BmB3.物质B的量浓度:CB/mol·m-3nBcB=───V4.物质B的质量摩尔浓度:mB/mol·kg-1nBmB=───W剂1.拉乌尔定律在一定温度下,纯液体A有一定的蒸汽压p某A,若向液体A加入溶质B,实验表明这是溶剂A的蒸汽压会下降。
法国化学家拉乌尔归纳多次的实验结果得出如下结论:“定温下稀溶液内溶剂的蒸汽压等于同温度下纯溶剂的蒸汽压乘它在溶液内的摩尔分数”。
即pA=p某A某A推导:设溶液由二个组分构成:A-溶剂B-溶质向溶剂A加入溶质B由实验知pA<p某A即Δp=(p某A-pA)>0且某B↑→Δp↑所以Δp∝某B由于构成稀溶液,加入的溶质较少,溶剂A分子电动势受力环境没有什么改变,只是单位体积溶液中A分子的数量减少了,使气相中ρA下降,而导致pA亦下降,也就是说加入B的数量越多,ρA下降越多,pA的下降也越大,这样,Δp仅与加入溶质B的数量有关,而与其本性无关了。