高考化学 第十二章 第3讲 晶体结构与性质复习
- 格式:ppt
- 大小:6.38 MB
- 文档页数:185

课时3 晶体结构与性质(时间:45分钟分值:100分)一、选择题(本题共7个小题,每题6分,共42分,每个小题只有一个选项符合题意。
) 1.下列性质适合于某种原子晶体的是 ( )。
A.熔点1 070 ℃,易溶于水,水溶液导电B.熔点10.32 ℃,液态不导电,水溶液导电C.能溶于CS2,熔点112 ℃,沸点444.6 ℃D.熔点3 550 ℃,很硬,不溶于水,不导电解析由原子晶体所具有的一般特点,熔沸点高,硬度大,不溶于水等性质,可以推断D应该是原子晶体。
答案 D2.下列叙述正确的是 ( )。
A.原子晶体中只存在非极性共价键B.干冰升华时,分子内共价键会发生断裂C.由原子构成的晶体可以是原子晶体,也可以是分子晶体D.只要含有金属阳离子的晶体就一定是离子晶体解析原子晶体如SiO2、SiC等含有极性共价键;干冰升华时,破坏的是分子间作用力,分子间共价键没有破坏;原子也可以构成分子晶体,如固态稀有气体晶体,C正确;金属晶体中也含有金属阳离子,D不正确。
答案 C3.下面的排序不正确的是 ( )。
A.晶体熔点由低到高:CF4<CCl4<CBr4<CI4B.硬度由大到小:金刚石>碳化硅>晶体硅C.熔点由高到低:Na>Mg>AlD.晶格能由大到小:NaF>NaCl>NaBr>NaI解析选项A中晶体熔点与分子间作用力有关,相对分子质量大,分子间作用力大,熔点越高,正确;选项B中,由于碳原子半径小于硅原子半径,则键长l C-C<l C-Si<l Si-Si,所以硬度大小顺序为:金刚石>碳化硅>晶体硅,正确;选项C 中,Na 、Mg 、Al 三种金属原子半径逐渐减小,离子所带电荷逐渐增多,则金属键逐渐增强,故熔点逐渐升高,错误;选项D 中,r F -<r Cl -<r Br -<r I -,所以晶格能大小顺序NaF>NaCl>NaBr>NaI ,正确。
答案 C4.钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用。



1.有关晶体的下列说法中正确的是( )A.晶体中分子间作用力越大,分子越稳定B.原子晶体中共价键越强,熔点越高C.冰熔化时水分子中共价键发生断裂D.氯化钠熔化时离子键未被破坏解析:选B。
晶体中分子间作用力越大,其熔、沸点越高;分子内化学键的键能越大,分子越稳定,A错;原子晶体中共价键越强,其熔点越高,B正确;冰熔化时分子间作用力受到破坏,水分子中共价键未发生断裂,C错;氯化钠晶体熔化时离子键被破坏,D错。
2.下列关于晶体的说法,一定正确的是( )CaTiO3的晶体结构模型(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶点) A.分子晶体中都存在共价键B.如上图,CaTiO3晶体中每个Ti4+和12个O2-相紧邻C.SiO2晶体中每个硅原子与两个氧原子以共价键相结合D.金属晶体的熔点都比分子晶体的熔点高解析:选B。
稀有气体为单原子分子,晶体中不存在共价键。
据图可知CaTiO3晶体中,Ti4+位于晶胞的顶点,O2-位于晶胞的面心,故Ti4+的O2-配位数为12。
SiO2晶体中每个硅原子与四个氧原子相连。
汞常温下为液态,其熔点比一般分子晶体还低。
3.下列关于晶格能的说法中正确的是( )A.晶格能指形成1 mol离子键所放出的能量B.晶格能指破坏1 mol离子键所吸收的能量C.晶格能指1 mol离子化合物中的阴、阳离子由相互远离的气态离子结合成离子晶体时所放出的能量D.晶格能的大小与晶体的熔点、硬度都无关解析:选C。
晶格能指1 mol离子化合物中阴、阳离子由相互远离的气态离子结合成离子晶体时放出的能量。
4.下列各项所述的数字不是6的是( )A.在NaCl晶体中,与一个Na+最近的且距离相等的Cl-的个数B.在金刚石晶体中,最小的环上的碳原子个数C.在二氧化硅晶体中,最小的环上的原子个数D.在石墨晶体的片层结构中,最小的环上的碳原子个数解析:选C。
在二氧化硅晶体中,最小的环上有6个硅原子、6个氧原子。


高中化学选修3之知识讲解 - 《晶体结构与性质》全章复习与巩固 -《晶体结构与性质》全章复习与巩固(提高)【学习目标】1、从晶体的一般性认识出发,了解晶体与非晶体的本质区别;2、知道晶胞的概念,了解晶胞与晶体的关系,学会通过分析晶胞得出晶体的组成;3、了解分子晶体和原子晶体的特征,能以典型的物质为例描述分子晶体和原子晶体的结构与性质的关系;4、从组成微粒和微粒间相互作用的不同,认识金属晶体和离子晶体的结构及其性质特点;5、能列举金属晶体的基本规程模型――简单立方堆积、钾型、镁型和铜型。
【知识网络】【要点梳理】要点一、用均摊法分析晶体并确定晶体的组成均摊法:是指每个晶胞平均拥有的粒子数目。
如:某个粒子为n个晶胞所共有,则该粒子有胞。
(1)长方体(正方体)形晶胞中不同位置的粒子对晶胞的贡献。
1属于一个晶n1。
81 ②处于棱上的粒子,同时为4个晶胞共有,每个粒子对晶胞的贡献为。
41 ③处于面上的粒子,同时为2个晶胞共有,每个粒子对晶胞的贡献为。
2 ①处于顶点的粒子,同时为8个晶胞共有,每个粒子对晶胞的贡献为④处于体心的粒子,则完全属于该晶胞,对晶胞的贡献为1。
(2)非长方体(正方体)形晶胞中粒子对晶胞的贡献视具体情况而定。
如石墨晶胞每一层内碳原子排成六边形,其顶点的1个碳原子对六边形的贡献为1。
3要点诠释:①晶胞的组成和晶体的组成含义不同。
如NaCl晶体的组成为NaCl(化学式),晶胞的组成则表示为Na4Cl4。
②晶胞的确定方法:晶胞是晶体中周期性重复的最小结构单元,通过平移结构单元看其是否发生重合来确定其是否为晶胞。
要点二、四种晶体的类型和性质比较晶体粒子离子晶体阴、阳离子原子晶体原子分子晶体分子金属晶体金属阳离子和自由电子粒子间作用离子键共价键分子间作用力(范德华力)硬度熔点、沸点、挥发性略硬而脆硬度高硬度小低熔点、低沸点、高挥发性一般较高一般熔点和沸点较高,但有部分低熔点金属(如Ga、Hg等)导热性导电性热的不良导体固态不导电,熔化后可导电,有的溶于水能导电机械加工性物质(实例)不良大部分盐类、碱类、低不良金刚石、晶体硅、热的不良导体非导体热的不良导体非导体,具有极性键的物质,溶于水后能导电不良良热的良导体良导体金属键熔点相对较高,沸点高,熔点和沸点高,无一般无挥发性挥发性 X2、O2、S、N2、P4、各种金属(除汞外)CO2、SO2,气态氢化物、有机物、酸类与合金价金属氧化物(如NaCl、二氧化硅、碳化硅NaOH、Na2O等)要点诠释:判断晶体类型的依据与方法①依据组成晶体的微粒和微粒间的作用判断。
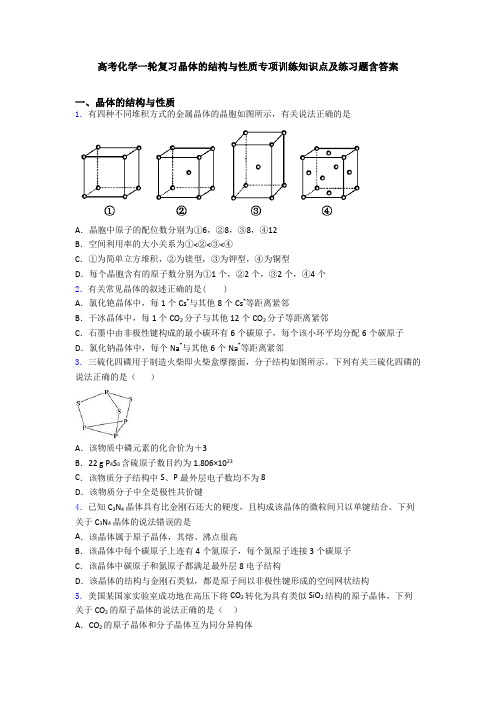
高考化学一轮复习晶体的结构与性质专项训练知识点及练习题含答案一、晶体的结构与性质1.有四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是A.晶胞中原子的配位数分别为①6,②8,③8,④12B.空间利用率的大小关系为①<②<③<④C.①为简单立方堆积,②为镁型,③为钾型,④为铜型D.每个晶胞含有的原子数分别为①1个,②2个,③2个,④4个2.有关常见晶体的叙述正确的是( )A.氯化铯晶体中,每1个Cs+与其他8个Cs+等距离紧邻B.干冰晶体中,每1个CO2分子与其他12个CO2分子等距离紧邻C.石墨中由非极性键构成的最小碳环有6个碳原子,每个该小环平均分配6个碳原子D.氯化钠晶体中,每个Na+与其他6个Na+等距离紧邻3.三硫化四磷用于制造火柴即火柴盒摩擦面,分子结构如图所示。
下列有关三硫化四磷的说法正确的是()A.该物质中磷元素的化合价为+3B.22 g P4S3含硫原子数目约为1.806×1023C.该物质分子结构中S、P最外层电子数均不为8D.该物质分子中全是极性共价键4.已知C3N4晶体具有比金刚石还大的硬度,且构成该晶体的微粒间只以单键结合。
下列关于C3N4晶体的说法错误的是A.该晶体属于原子晶体,其熔、沸点很高B.该晶体中每个碳原子上连有4个氮原子,每个氮原子连接3个碳原子C.该晶体中碳原子和氮原子都满足最外层8电子结构D.该晶体的结构与金刚石类似,都是原子间以非极性键形成的空间网状结构5.美国某国家实验室成功地在高压下将CO2转化为具有类似SiO2结构的原子晶体,下列关于CO2的原子晶体的说法正确的是()A.CO2的原子晶体和分子晶体互为同分异构体B.在一定条件下,CO2的原子晶体转化为分子晶体是物理变化C.CO2的原子晶体和分子晶体具有相同的物理性质D.在CO2的原子晶体中,每个C原子周围结合4个O原子,每个O原子与2个碳原子结合6.下列叙述正确的是A.离子晶体中,只存在离子健,不可能存在其它化学键B.可燃冰中甲烷分子与水分子之间存在氢键C.Na2O2、NaHSO4晶体中的阴、阳离子个数比均为12D.晶体熔点:金刚石>食盐>冰>干冰7.氟在自然界中常以CaF2的形式存在。


第38讲晶体结构与性质1.晶体和晶胞(1)晶体与非晶体(2)获得晶体的三条途径①熔融态物质凝固。
②气态物质冷却不经液态直接凝固(凝华)。
③溶质从溶液中析出。
(3)晶胞①概念:描述晶体结构的□11基本单元。
②晶体与晶胞的关系:数量巨大的晶胞“□12无隙并置”构成晶体。
③晶胞中粒子数目的计算——均摊法:如某个粒子为n个晶胞所共有,则该粒子有□131n属于这个晶胞。
2.四种类型晶体的比较3.离子晶体的晶格能(1)定义:气态离子形成1摩尔离子晶体释放的能量,通常取正值,单位:□31kJ·mol -1。
(2)影响因素①离子所带电荷数:离子所带电荷数越□32多,晶格能越□33大。
②离子的半径:离子的半径越□34小,晶格能越□35大。
(3)与离子晶体性质的关系晶格能越大,形成的离子晶体越□36稳定,且熔点越□37高,硬度越□38大。
1.判断正误,正确的画“√”,错误的画“×”,并指明错因。
(1)具有规则几何外形的固体一定是晶体。
(×)错因:自发地呈现多面体外形的才是晶体,人为制造出的具有规则几何外形的固体如玻璃、木材、陶瓷等均不是晶体。
(2)冰中包含的作用力有范德华力、氢键和共价键。
(√)错因:__________________________________________________________(3)区分晶体和非晶体最可靠的方法是测定其有无固定熔点。
(×)错因:区分晶体和非晶体最可靠的科学方法是对固体进行X-射线衍射实验。
(4)1 mol金刚石和SiO2中含有的共价键数目均为4N A。
(×)错因:1_mol金刚石含有的共价键数目为2N A。
(5)金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子。
(√)错因:__________________________________________________________(6)分子晶体的熔点一定比金属晶体的低。

高考化学复习第三讲晶体结构与性质1.理解离子键的形成,能根据离子化合物的结构特征解释其物理性质。
2.了解晶体的类型,了解不同类型晶体中结构微粒、微粒间作用力的区别。
3.了解晶格能的概念,了解晶格能对离子晶体性质的影响。
4.了解分子晶体结构与性质的关系。
5.了解原子晶体的特征,能描述金刚石、二氧化硅等原子晶体的结构与性质的关系。
6.理解金属键的含义,能用金属键理论解释金属的一些物理性质。
了解金属晶体常见的堆积方式。
7.了解晶胞的概念,能根据晶胞确定晶体的组成并进行相关的计算。
2016,卷甲37T(3)(4);2016,卷乙37T(6);2016,卷丙37T(4)(5);2015,卷Ⅰ 37T(4)(5);2015,卷Ⅱ 37T(2)(5);2014,卷Ⅰ 37T(1)(3)(4);2014,卷Ⅱ 37T(4)(5)晶体晶体的结构与性质[学生用书P270][知识梳理]一、晶体1.晶体与非晶体晶体非晶体结构特征结构微粒周期性有序排列结构微粒无序排列性质特征自范性有无熔点固定不固定2.得到晶体的途径(1)熔融态物质凝固。
(2)气态物质冷却不经液态直接凝固(凝华)。
(3)溶质从溶液中析出。
3.晶胞(1)概念:描述晶体结构的基本单元。
(2)晶体中晶胞的排列——无隙并置①无隙:相邻晶胞之间没有任何间隙。
②并置:所有晶胞都是平行排列、取向相同。
4.晶格能(1)定义:气态离子形成1摩离子晶体释放的能量,通常取正值,单位:kJ·mol-1。
(2)影响因素①离子所带电荷数:离子所带电荷数越多,晶格能越大。
②离子的半径:离子的半径越小,晶格能越大。
二、四种晶体类型的比较三、晶体熔、沸点的比较1.不同类型晶体熔、沸点的比较(1)不同类型晶体的熔、沸点高低的一般规律:原子晶体>离子晶体>分子晶体。
(2)金属晶体的熔、沸点差别很大,如钨、铂等熔、沸点很高,汞、铯等熔、沸点很低。
2.同种晶体类型熔、沸点的比较(1)原子晶体原子半径越小―→键长越短―→键能越大―→熔、沸点越高。

第3讲晶体结构与性质命题一晶体类型的判断及熔、沸点高低的比较1.(1)(2018年全国Ⅲ卷,35节选)ZnF2具有较高的熔点(872 ℃),其化学键类型是,ZnF2不溶于有机溶剂而ZnCl2、ZnBr2、ZnI2能够溶于乙醇、乙醚等有机溶剂,原因是。
(2)(2017年全国Ⅰ卷,35节选)K和Cr属于同一周期,且核外最外层电子构型相同,但金属K 的熔点、沸点等都比金属Cr低,原因是。
(1)ZnF2的熔点较高,故为离子晶体。
离子晶体难溶于乙醇等有机溶剂,分子晶体可以溶于乙醇等有机溶剂。
(2)金属键的强弱与半径成反比,与所带的电荷成正比。
(1)离子键;ZnF2为离子化合物,ZnCl2、ZnBr2、ZnI2的化学键以共价键为主,极性较小(2)K原子半径较大且价电子数较少,金属键较弱2.(2016年全国Ⅰ卷,37节选)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因: 。
GeCl4GeBr4GeI4熔点/℃-49.5 26 146沸点/℃83.1 186 约400GeCl4、GeBr4、GeI4熔沸点依次升高;原因是分子结构相似,相对分子质量依次增大,分子间相互作用力逐渐增强3.(2016年全国Ⅱ卷,37节选)单质铜及镍都是由键形成的晶体。
金属4.(2016年全国Ⅲ卷,37节选)GaF3的熔点高于1000 ℃,GaCl3的熔点为77.9 ℃,其原因是。
GaF3是离子晶体,GaCl3是分子晶体,离子晶体GaF3的熔沸点更高5.(2015年全国Ⅰ卷,37节选)CO能与金属Fe形成Fe(CO)5,该化合物的熔点为253 K,沸点为376 K,其固体属于晶体。
分子6.(2014年全国Ⅰ卷,37节选)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过方法区分晶体、准晶体和非晶体。
X-射线衍射命题二晶胞分析及计算7.(1)(2018年全国Ⅰ卷,35节选)Li2O是离子晶体,其晶格能可通过图(a)的Born-Haber循环计算得到。

12-41[A层基础练]1.(2018·武汉模拟)下列有关晶体的说法中,不正确的是()A.晶体中一定存在化学键B.已知晶胞的组成就可推知晶体的组成C.分子晶体在晶体态或熔融态下均不导电D.原子晶体中只存在共价键,不可能存在其他类型的化学键【解析】稀有气体形成的晶体中只存在范德华力没有化学键,A错误;晶胞是描述晶体结构的基本单元,因此已知晶胞的组成就可推知晶体的组成,B正确;分子晶体在晶体态或熔融态下均不能电离出离子,不导电,C正确;原子间通过共价键形成的空间网状结构的晶体是原子晶体,因此原子晶体中只存在共价键,不可能存在其他类型的化学键,D正确.【答案】A2.(2018·邯郸模拟)关于晶体的下列说法正确的是()A.任何晶体中,若含有阳离子就一定有阴离子B.原子晶体中只含有共价键C.原子晶体的熔点一定比金属晶体的高D.离子晶体中只含有离子键,不含有共价键【解析】金属晶体是由金属阳离子和自由电子构成的,所以有阳离子不一定有阴离子,A错误;原子晶体中原子间以共价键相结合,B正确;金属晶体有的熔点很高如钨,所以原子晶体的熔点不一定比金属晶体的高,C错误;离子晶体中也可能含有共价键,如NaOH属于离子晶体,既含有离子键,又含有共价键,D错误。
【答案】B3.(2018·贵阳模拟)金属晶体中金属原子有三种常见的堆积方式,六方堆积(镁型)、面心立方堆积(铜型)和体心立方堆积(钾型),图(a)、(b)、(c)分别代表这三种晶胞的结构,其晶胞内金属原子个数比为()A.11∶8∶4 B.3∶2∶1C.9∶8∶4 D.21∶14∶9【解析】a中原子个数=12×错误!+2×错误!+3=6,b中原子个数=8×错误!+6×错误!=4,c中原子个数=1+8×错误!=2,所以其原子个数比是6∶4∶2=3∶2∶1。
【答案】B4.(2018·仙桃模拟)下面有关晶体的叙述中,错误的是() A.白磷晶体中,分子之间通过共价键结合B.金刚石的网状结构中,由共价键形成的最小碳环上有6个碳原子C.在NaCl晶体中每个Na+(或Cl-)周围都紧邻6个Cl-(或Na+)D.离子晶体在熔化时,离子键被破坏,而分子晶体熔化时,化学键不被破坏【解析】A项,白磷晶体为分子晶体,分子之间通过范德华力结合,错误;B项,金刚石的网状结构中,由共价键形成的最小碳环上有6个碳原子,正确;C项,在NaCl晶体中每个Na+(或Cl-)周围都紧邻6个Cl-(或Na+),正确;D项,离子晶体在熔化时,离子键被破坏,而分子晶体熔化时,分子间作用力被破坏,化学键不被破坏,正确。


达标作业36晶体结构与性质[基础题] 1.下列晶体分类中正确的一组是()选项离子晶体原子晶体分子晶体A NaOH Ar SO2B H2SO4石墨SC CH3COONa水晶D Ba(OH)2金刚石玻璃解析:A项中固态Ar为分子晶体;B项中H2SO4为分子晶体、石墨是混合型晶体;D项中玻璃是非晶体。
答案:C2.离子晶体熔点的高低取决于晶体中晶格能的大小。
判断KCl、NaCl、CaO、BaO四种晶体熔点的高低顺序是()A.KCl>NaCl>BaO>CaOB.NaCl>KCl>CaO>BaOC.CaO>BaO>NaCl>KClD.CaO>BaO>KCl>NaCl解析:离子晶体中,晶格能越大,晶体熔、沸点越高;离子所带电荷总数越多,半径越小,晶格能越大。
答案:C3.关于晶体的叙述中,正确的是()A.原子晶体中,共价键的键能越大,熔、沸点越高B.分子晶体中,分子间的作用力越大,该分子越稳定C.分子晶体中,共价键的键能越大,熔、沸点越高D.某晶体溶于水后,可电离出自由移动的离子,该晶体一定是离子晶体解析:B项,分子的稳定性取决于分子内部的共价键强弱,与分子间作用力无关;C项,分子晶体熔、沸点高低,取决于分子间作用力的大小;D项,也可能是分子晶体,如HCl。
答案:A4.现有四种晶体,其离子排列方式如图所示,其中化学式正确的是()解析:A.A 离子个数是1,B 离子个数=1/8×8=1,所以其化学式为AB ,故A 错误;B.E 离子个数=1/8×4=1/2,F 离子个数=1/8×4=1/2,E 、F 离子个数比为1:1,所以其化学式为EF ,故B 错误;C.X 离子个数是1,Y 离子个数=1/2×6=3,Z 离子个数=1/8×8=1,所以其化学式为XY 3Z ,故C 正确;D.A 离子个数=1/8×8+1/2×6=4,B 离子个数=12×1/4+1=4,A 、B 离子个数比1:1,所以其化学式为AB ,故D 错误。

第3讲晶体结构与性质一、单项选择题1.二茂铁[(C5H5)2Fe]的发现是有机金属化合物研究中具有里程碑意义的事件,它开辟了有机金属化合物研究的新领域。
已知二茂铁熔点是173 ℃(在100 ℃时开始升华),沸点是249 ℃,不溶于水,易溶于苯、乙醚等非极性溶剂。
下列说法不正确的是( )A.二茂铁属于分子晶体B.在二茂铁结构中,C5H5-与Fe2+之间形成的化学键类型是离子键C.已知:环戊二烯的结构式为,则其中仅有1个碳原子采取sp3杂化D.C5H5-中一定含π键答案 B 碳原子提供孤电子对,铁原子提供空轨道,两者形成配位键,B项错误。
2.下列有关晶体的叙述中,不正确...的是( )A.氯化钠和氯化铯晶体中,阳离子的配位数均为6B.金刚石为空间网状结构C.金属钠晶体采用体心立方堆积,每个晶胞含2个原子,配位数为8D.干冰晶体中,每个CO2分子周围紧邻12个CO2分子答案 A NaCl和CsCl晶体中,阳离子的配位数分别为6和8,A项错误;金刚石为空间网状结构,B项正确;金属钠的晶体采用体心立方堆积,每个晶胞含(1+8×1)个原子,配位数为8,C项正确;干冰晶体中,每2个CO2分子周围紧邻12个CO2分子,D项正确。
二、非选择题3.(2018淮阴中学高三上检测)金属钛性能优越,被誉为继Fe 、Al 后应用广泛的“第三金属”。
(1)Ti 基态原子的核外电子排布式为 。
(2)钛能与B 、C 、N 、O 等非金属元素形成稳定的化合物。
第一电离能:N (填“>”或“<”)O。
(3)月球上的岩石——玄武岩的主要成分为钛酸亚铁(FeTiO 3)。
FeTiO 3与80%的硫酸反应可生成TiOSO 4。
S O 42-的空间构型为 形,其中硫原子采取 杂化,写出S O 42-的一种等电子体的化学式: 。
(4)Ti 的氧化物和CaO 相互作用能形成钛酸盐CaTiO 3,CaTiO 3的晶体结构如图所示(Ti 原子位于立方体的顶点)。