《仪器分析》华中师范第三版下册课后答案
- 格式:pdf
- 大小:195.89 KB
- 文档页数:12

《仪器分析》课后习题答案参考第一章电位分析法1~4 略5.(1)pMg x=5.4(2)3.65×10-6– 4.98×10-66. -17%7. 4.27×10-4%8.(1)=5.4×10-4lg=-2.31=5.0×10-3(2) Cl- =1.0×10-2 mol/L9. pH x ==5.74R入=1011Ω10. Cx=8.03×10-4 mol/L第二章电重量分析和库仑分析法1. 1.64 V2. -1.342,0.2383. 1.08 V,0.4V,7333 s4. Co先析出,阴极电位应维持在-0.313 – -0.795V之间阴极电位应维持在-0.455 – -0.795V之间5 Bi:0.283-0.190V(vs.SHE);-0.005 - -0.098(vs. Ag/AgCl)Cu:0.310-0.159V(vs.SHE);0.022 - -0.129(vs. Ag/AgCl)Ag:0.739-0.444V(vs.SHE);0.451 – 0.156(vs. Ag/AgCl)控制阴极电位大于0.310V(vs.SHE),可以使Ag分离,Cu2+和BiO+不能分离。
6 ,7 , ,89.10. t= 4472s11 6.1×10-4 mol/Lpt阴极产生OH-,改变pH使副反应发生,故pt阴极应用玻璃砂芯套管隔离第三章 伏安法和极谱分析法1~3 略4. 当pH=7时,当pH=5时,5. (1) 线性回归方程: y =6.0733x + 0.3652(2)0.536 mmol/L6. M C x 41023.2-⨯=7. 22.7 μA8. 0.0879. 1.75 ×10-3mol/L10. -0.626 V11. 5.9×10-3第四章气相色谱法1~14 略15. 8.5%,20.6%,60.9%16. 2.15%,3.09%,2.75%,6.18%,85.84%17. (1)4.5, (2)48mL,(3)5.4min,(4)103,(5)1866,(6)1.07nm18. (1)8.6,(2)1.4419. (1)n有效(A) = 636.59n有效(B) = 676(2) 2 m20.(1)0.45 ,(2)7111121.(1)4,(2)4,(3),22. (1)3236,2898,2820,3261,(2)3054(3)0.33m第五章高效液相色谱法1~16 略17. 26.24%,27.26%18. 1600,6.7,7.3,1.1,0.8,7 m19. 0.63,2.38,2.65,4.034021,3099,2818,3394,595,1535,1486,217820. 5.1%21. 0.47%第六章原子发射光谱仪1~8 略9. 2.57 eV10. 0.573%。

第一章 绪论2. 对试样中某一成分进行5次测量,所得测定结果(单位μg·mL -1)分别为0.36,0.38,0.35,0.37,0.39。
(1)计算测定结果的相对标准偏差;(2)如果试样中该成分的真实含量是0.38 μg·mL -1,计算测定结果的相对误差。
解:(1)x =539.037.035.038.036.0++++ = 0.37 μg·mL -1s =1)(12--∑=n x x ni i =15)37.039.0()38.036.0()37.036.0(222--++-+-= 0.016 μg·mL -1 s r =xs × 100 % = 37.0016.0× 100 % = 4.3 %(2)E r =μμ-x × 100 % =38.038.037.0-× 100 % = -2.6 %第二章 光学分析法导论3. 计算:(1)670.7nm 锂线的频率;(2)3300cm -1谱线的波长; (3)钠588.99nm 共振线的激发电位。
解:(1)ν === 4.470 ×1014 s -1(2)λ === 3030 nm(3)E = h= 4.136×10-15= 2.105 eV第三章 紫外-可见吸收光谱法2.何谓生色团及助色团?试举例说明。
解:含有π键的不饱和基团叫做生色团.例如C =C ;C =O ;C =N ;—N =N —有一些含有n 电子的基团,它们本身没有生色功能,但当它们与生色团相连时,就会发生n —π共轭作用,增强生色团的生色能力(吸收波长向长波方向移动,且吸收强度增加),这样的基团称为助色团。
如—OH 、—OR 、—NH 2、—NHR 、—X 等。
3.作为苯环的取代基,―NH 3+不具有助色作用,―NH 2却具有助色作用;―OH 的助色作用明显小于―O-。
试说明原因。


第二章气相色谱分析习题答案1.简要说明气相色谱分析的基本原理借助两相间分配原理而使混合物中各组分分离。
气相色谱就是根据组分与固定相与流动相的亲和力不同而实现分离。
组分在固定相与流动相之间不断进行溶解、挥发(气液色谱),或吸附、解吸过程而相互分离,然后进入检测器进行检测。
2.气相色谱仪的基本设备包括哪几部分?各有什么作用?载气系统:包括气源、气化净化和气体流速控制部件。
除去水、氧等有害物质,使流量按设定值恒定输出。
进样系统:包括进样器、气化室。
作用时将液体或固体试样,在进入色谱柱前瞬间气化。
色谱柱和柱箱:包括温度控制装置。
作用是分离样品中的各组分。
检测系统:包括检测器、放大器、检测器的电源控温装置。
从色谱柱流出的各组分,通过检测器把浓度信号转变为电信号,经过放大器放大后送到数据处理装置得到色谱图。
记录及数据处理系统:将检测到的电信号经处理后,并显示。
3.当下列参数改变时:(1)柱长缩短,(2)固定相改变(3)流动相流速增加,(4)相比减少,是否会引起分配系数的改变?为什么?答:固定相改变会引起分配系数的改变,因为分配系数只与组分的性质及固定相与流动相的性质有关。
所以:(1)柱长缩短不会引起分配系数改变(2)固定相改变会引起分配系数改变(3)流动相流速增加不会引起分配系数改变(4)相比减少不会引起分配系数改变4.当下列参数改变时:(1)柱长增加,(2)固定相量增加,(3)流动相流速减小,(4)相比增大,是否会引起分配比的变化?为什么?答:k=K/β,而β=V M/V S,分配比除了与组分,两相的性质,柱温,柱压有关外,还与相比有关,而与流动相流速,柱长无关.故:(1)不变化,(2)增加,(3)不改变,(4)减小5.试以塔板高度H做指标,讨论气相色谱操作条件的选择解:提示:主要从速率理论(vanDeemerequation)来解释,同时考虑流速的影响,选择最佳载气流速.P13-24。
(1)选择流动相最佳流速。

分析化学仪器分析第三版答案【篇一:仪器分析第五版习题及答案】/p> 1、主要区别:(1)化学分析是利用物质的化学性质进行分析;仪器分析是利用物质的物理或物理化学性质进行分析;(2)化学分析不需要特殊的仪器设备;仪器分析需要特殊的仪器设备;(3)化学分析只能用于组分的定量或定性分析;仪器分析还能用于组分的结构分析;(3)化学分析灵敏度低、选择性差,但测量准确度高,适合于常量组分分析;仪器分析灵敏度高、选择性好,但测量准确度稍差,适合于微量、痕量及超痕量组分的分析。
2、共同点:都是进行组分测量的手段,是分析化学的组成部分。
1-5分析仪器与仪器分析的区别:分析仪器是实现仪器分析的一种技术设备,是一种装置;仪器分析是利用仪器设备进行组分分析的一种技术手段。
分析仪器与仪器分析的联系:仪器分析需要分析仪器才能达到量测的目的,分析仪器是仪器分析的工具。
仪器分析与分析仪器的发展相互促进。
1-7因为仪器分析直接测量的是物质的各种物理信号而不是其浓度或质量数,而信号与浓度或质量数之间只有在一定的范围内才某种确定的关系,且这种关系还受仪器、方法及样品基体等的影响。
因此要进行组分的定量分析,并消除仪器、方法及样品基体等对测量的影响,必须首先建立特定测量条件下信号与浓度或质量数之间的关系,即进行定量分析校正。
第二章光谱分析法导论2-1光谱仪的一般组成包括:光源、单色器、样品引入系统、检测器、信号处理与输出装置。
各部件的主要作用为:光源:提供能量使待测组分产生吸收包括激发到高能态;单色器:将复合光分解为单色光并采集特定波长的光入射样品或检测器;样品引入系统:将样品以合适的方式引入光路中并可以充当样品容器的作用;检测器:将光信号转化为可量化输出的信号。
信号处理与输出装置:对信号进行放大、转化、数学处理、滤除噪音,然后以合适的方式输出。
2-2:单色器的组成包括:入射狭缝、透镜、单色元件、聚焦透镜、出射狭缝。
各部件的主要作用为:入射狭缝:采集来自光源或样品池的复合光;透镜:将入射狭缝采集的复合光分解为平行光;单色元件:将复合光色散为单色光(即将光按波长排列)聚焦透镜:将单色元件色散后的具有相同波长的光在单色器的出口曲面上成像;出射狭缝:采集色散后具有特定波长的光入射样品或检测器2-3棱镜的分光原理是光的折射。

仪器分析课后习题答案第二章光学分析法导论(书后习题参考答案)1. 已知1电子伏特=1. 602×10-19J ,试计算下列辐射波长的频率(以兆赫为单位),波数(以cm -1为单位)及每个光子的能量(以电子伏特为单位):(1)波长为900pm 的单色X 射线;(2)589.0nm 的钠D 线;(3)12.6μm 的红外吸收峰;(4)波长为200cm 的微波辐射。
解:已知1eV=1.602×10-19J, h =6.626×10-34J·s, c =3.0×108m·s -1 ①λ=900pm 的X 射线1712810333.310900100.3?=??==-λcv Hz ,即3.333×1011MHz 71010111.11090011?=?==-λσcm -11617341008.210333.310626.6--?===hv E J用eV 表示,则319161910378.110602.11008.210602.1?=??=?=---hv E eV②589.0nm 的钠D 线149810093.5100.589100.3?=??==-λcv Hz ,即5.093×108MHz 4710698.1100.58911?=?==-λσcm -119143410375.310093.510626.6--?===hv E J用eV 表示,则107.210602.11075.310602.1191919=??=?=---hv E eV③12.6μm 的红外吸收峰136810381.2106.12100.3?=??==-λcv Hz ,即2.381×107MHz 2410937.7106.1211?=?==-λσcm -120133410578.110381.210626.6--?===hv E J用eV 表示,则219201910850.910602.110578.110602.1----?=??=?=hv E eV④波长为200cm 的微波辐射8281050.110200100.3?=??==-λcv Hz ,即1.50×102MHz 31000.520011-?===λσcm -12683410939.91050.110626.6--?===hv E J用eV 表示,则719261910204.610602.110939.910602.1----?=??=?=hv E eV2. 一个体系包含三个能级,如果这三个能级的统计权重相同,体系在300K温度下达到平衡时,试计算在各能级上的相对分布(N i /N ).能级的相对能量如下。

第一章 绪论2. 对试样中某一成分进行5次测量,所得测定结果(单位μg·mL -1)分别为0.36,0.38,0.35,0.37,0.39。
(1)计算测定结果的相对标准偏差;(2)如果试样中该成分的真实含量是0.38 μg·mL -1,计算测定结果的相对误差。
解:(1)x = 539.037.035.038.036.0++++ = 0.37 μg·mL -1s =1)(12--∑=n x x ni i =15)37.039.0()38.036.0()37.036.0(222--++-+-= 0.016 μg·mL -1 s r =xs× 100 % = 37.0016.0× 100 % = 4.3 %(2)E r =μμ-x × 100 % =38.038.037.0-× 100 % = -2.6 %第二章 光学分析法导论3. 计算:(1)670.7nm 锂线的频率;(2)3300cm -1谱线的波长; (3)钠588.99nm 共振线的激发电位。
解:(1)ν = λc= cm scm 710107.670/1099792.2-⨯⨯ = 4.470 ×1014 s -1(2)λ = σ1= 133001-cm = 3030 nm(3)E = h λc= 4.136×10-15eV·s×cm scm 7101099.588/1099792.2-⨯⨯= 2.105 eV第三章 紫外-可见吸收光谱法2.何谓生色团及助色团?试举例说明。
解:含有π键的不饱和基团叫做生色团.例如C =C ;C =O ;C =N ;—N =N — 有一些含有n 电子的基团,它们本身没有生色功能,但当它们与生色团相连时,就会发生n —π共轭作用,增强生色团的生色能力(吸收波长向长波方向移动,且吸收强度增加),这样的基团称为助色团。

仪器分析课后习题答案仪器分析课后习题答案在仪器分析课程中,习题是帮助学生巩固所学知识的重要方式之一。
通过解答习题,学生可以加深对仪器分析原理和应用的理解,提高自己的分析能力。
然而,有时候习题的难度较大,学生可能会遇到一些困惑,不知道如何解答。
因此,在这篇文章中,我将为大家提供一些仪器分析课后习题的答案,并解释一些解题思路和方法。
1. 习题:某仪器的检测极限为10 ng/mL,如果样品的浓度为8 ng/mL,该仪器能否检测到?答案:根据题目中给出的检测极限为10 ng/mL,我们可以得出结论,该仪器能够检测到大于等于10 ng/mL的样品浓度。
因此,对于样品浓度为8 ng/mL的情况,该仪器无法检测到。
解题思路:检测极限是指仪器能够可靠检测到的最低浓度。
在本题中,检测极限为10 ng/mL,意味着仪器只能检测到大于等于10 ng/mL的样品浓度。
如果样品浓度低于检测极限,仪器将无法检测到。
2. 习题:某仪器的分析误差为±2%,如果测得样品A的浓度为50 mg/L,那么实际浓度的范围是多少?答案:根据题目中给出的分析误差为±2%,我们可以得出结论,测得的样品浓度的实际范围是在测量值的基础上加减2%。
对于样品A的浓度为50 mg/L的情况,实际浓度的范围是50 mg/L ± 2% = 50 mg/L ± 1 mg/L。
解题思路:分析误差是指测量结果与真实值之间的差异。
在本题中,分析误差为±2%,意味着测得的样品浓度的实际范围是在测量值的基础上加减2%。
因此,对于样品A的浓度为50 mg/L的情况,实际浓度的范围是50 mg/L ± 2% = 50 mg/L ± 1 mg/L。
3. 习题:某仪器的线性范围为10-100 mg/L,如果测得样品B的浓度为120 mg/L,该仪器的测量结果是否准确?答案:根据题目中给出的线性范围为10-100 mg/L,我们可以得出结论,该仪器只能准确测量在10-100 mg/L范围内的样品浓度。

仪器分析第三版课后题答案1. 电位滴定法中,以E-V作图绘制滴定曲线,滴定终点为() [单选题] *曲线的拐点(正确答案)曲线的最高点曲线的最低点ΔE/ΔV为零时点2. 若使用永停滴定法滴定至化学计量点时电流降至最低点且不变化,则说明()[单选题] *滴定剂和被测物均为不可逆电对滴定剂和被测物均为可逆电对滴定剂为不可逆电对,被测物为可逆电对(正确答案)滴定剂为可逆电对,被测物为不可逆电对3. pH玻璃电极产生的不对称电位来源于() [单选题] *内外玻璃膜表面特性不同(正确答案)内外溶液中H+浓度不同内外溶液中H+活度系数不同内外参比电极不一样4. 测定溶液pH时,常用()作为指示电极 [单选题] *金属-金属离子电极玻璃电极(正确答案)饱和甘汞电极惰性金属电极5. pH值测定时,酸差是指当溶液pH<1时,() [单选题] * pH测<pH真pH测=pH真pH测>pH真(正确答案)无法确定6. 紫外-可见分光光度法是由()的跃迁产生的。
[单选题] *分子中电子能级(正确答案)振动能级转动能级转动和转动能级7. 下列分析方法中哪个不属于吸收分光光度法() [单选题] *红外分光光度法荧光分析(正确答案)紫外分光光度法原子吸收分光光度法8. 以下不是分子中电子跃迁方式的为() [单选题] *σ→σ*n → n*(正确答案)π→π*n→π*9. 比尔-朗伯定律的表达式为() [单选题] *E=AlCC =AlEl=AECA=ElC(正确答案)10. 偏离比尔定律的主要因素为() [单选题] *非单色光、非稀溶液(正确答案)单色光、稀溶液非单色光、稀溶液单色光、非稀溶液11. 紫外-可见分光光度法中紫外光区的光源为() [单选题] *卤钨灯钨灯氙灯氘灯(正确答案)12. 以下哪个不是荧光光谱的特点() [单选题] *荧光波长总是大于激发光波长荧光发射光谱的形状与激发波长无关荧光光谱与激发光谱呈对称镜像关系激发光波长总是大于荧光波长(正确答案)13. 关于荧光分析法,下列叙述错误的是() [单选题] *能发射荧光的物质要能吸收紫外光-可见光能发射荧光的物质应有一定的荧光量子效率分子的刚性和共平面性越小,荧光效率会增大(正确答案)共轭体系越长,荧光效率将越大项14. 测定荧光强度时,要在与入射光成直角的方向上进行测定,原因是() [单选题] *荧光波长比入射光的波长长只有与入射光成直角的方向上才有荧光荧光是向多方向发射的,为了减少透射光的影响(正确答案)荧光强度比透射光强度大15. 红外光谱中, 分子间氢键的形成使伸缩振动频率( ) [单选题] *升高降低(正确答案)不变无法确定16. 红外光谱中,下列哪种基团的振动频率最小?() [单选题] *υC≡CυC=CυC-C(正确答案)υC-H17. 红外光谱中特征区是指以下哪个波数范围() [单选题] *4000~1250 cm-1(正确答案)400~1250 cm-1400~4000 cm-14000~1500 cm-118. H2O分子的振动自由度是() [单选题] *23(正确答案)4519. 以下哪个不是红外分光光度法中基频峰数小于振动自由度的原因() [单选题] *简并红外非活性振动仪器分辨率低红外活性振动(正确答案)20. FI-IR采用的单色器为() [单选题] *迈克逊干涉仪(正确答案)光栅棱镜真空热电偶21. 当样品基体影响较大又没有纯净的基体空白,或测定纯物质中极微量元素时,可采用()。

第一章 绪 论 1. 解释下列名词:(1)仪器分析和化学分析;(2)标准曲线与线性范围;(3)灵敏度、精密度、准确度和检出限。
答:(1)仪器分析和化学分析:以物质的物理性质和物理化学性质(光、电、热、磁等)为基础的分析方法,这类方法一般需要特殊的仪器,又称为仪器分析法;化学分析是以物质化学反应为基础的分析方法。
(2)标准曲线与线性范围:标准曲线是被测物质的浓度或含量与仪器响应信号的关系曲线;标准曲线的直线部分所对应的被测物质浓度(或含量)的范围称为该方法的线性范围。
(3)灵敏度、精密度、准确度和检出限:物质单位浓度或单位质量的变化引起响应信号值变化的程度,称为方法的灵敏度;精密度是指使用同一方法,对同一试样进行多次测定所得测定结果的一致程度;试样含量的测定值与试样含量的真实值(或标准值)相符合的程度称为准确度;某一方法在给定的置信水平上可以检出被测物质的最小浓度或最小质量,称为这种方法对该物质的检出限。
2. 对试样中某一成分进行5次测定,所得测定结果(单位μg ⋅mL -1)分别为 0.36,0.38,0.35,0.37,0.39。
(1) 计算测定结果的相对标准偏差;(2) 如果试样中该成分的真实含量是0.38 μg ⋅mL -1,试计算测定结果的相对误差。
解:(1)测定结果的平均值37.0539.037.035.038.036.0=++++=x μg ⋅mL -1标准偏差122222120158.015)37.039.0()37.037.0()37.035.0()37.038.0()37.036.0(1)(-=⋅=--+-+-+-+-=--=∑mL g n x x s ni iμ相对标准偏差 %27.4%10037.00158.0%100=⨯=⨯=x s s r(2)相对误差 %63.2%10038.038.037.0%100-=⨯-=⨯-=μμx E r 。
3. 用次甲基蓝-二氯乙烷光度法测定试样中硼时,为制作标准曲线,配制一系列质量浓度ρB (单位mg ⋅L -1)分别为0.5,1.0,2.0,3.0,4.0,5.0的标准溶液,测得吸光度A 分别为0.140,0.160,0.280,0.380,0.410,0.540。
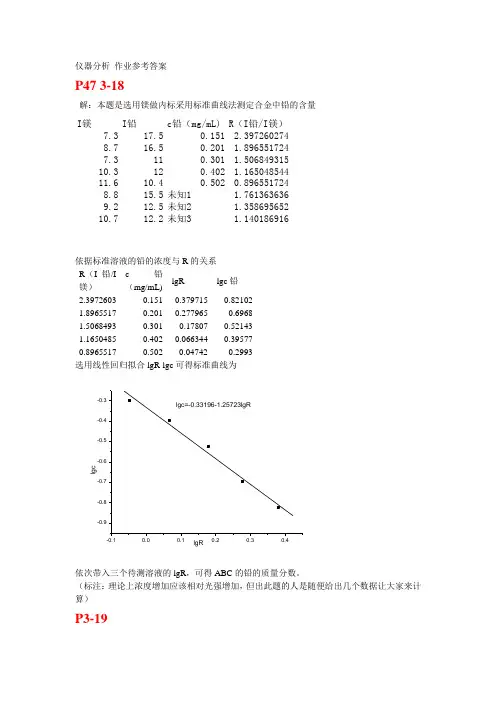
仪器分析 作业参考答案P47 3-18解:本题是选用镁做内标采用标准曲线法测定合金中铅的含量I镁I铅c铅(mg/mL)R(I铅/I镁)7.317.50.151 2.3972602748.716.50.201 1.8965517247.3110.301 1.50684931510.3120.402 1.16504854411.610.40.5020.8965517248.815.5未知1 1.7613636369.212.5未知2 1.35869565210.712.2未知3 1.140186916依据标准溶液的铅的浓度与R 的关系 R (I 铅/I 镁) c 铅(mg/mL) lgR lgc 铅2.3972603 0.151 0.379715 -0.82102 1.8965517 0.201 0.277965 -0.6968 1.5068493 0.301 0.17807 -0.52143 1.1650485 0.402 0.066344 -0.39577 0.8965517 0.502 -0.04742 -0.2993 选用线性回归拟合lgR-lgc 可得标准曲线为-0.9-0.8-0.7-0.6-0.5-0.4-0.3l g clgR依次带入三个待测溶液的lgR ,可得ABC 的铅的质量分数。
(标注:理论上浓度增加应该相对光强增加,但出此题的人是随便给出几个数据让大家来计算)P3-19解:(计算时用不到波长具体的数值、钼的质量浓度和溶液体积)镁的质量浓度 (ng/mL)I 镁 I 钼 R lgR lgc 1.05 0.67 1.8 0.372222 -0.4292 0.021189 10.5 3.4 1.6 2.1250.327359 1.021189 105 18 1.5 121.0791812.021189 1050 115 1.7 67.64706 1.8302493.021189 10500739 1.9 388.9474 2.589891 4.021189 未知 2.51.81.3888890.142668根据lgR-lgc 成线性关系拟合lgRlgc-0.4292 0.021189 0.327359 1.021189 1.079181 2.021189 1.830249 3.021189 2.5898914.0211891234l g c可得标准曲线为lgc=0.58971+1.32607lgR将lgR=0.142668带入lgc=0.58971+1.32607lgR 可得lgc,进而得c 。
WORD格式可编辑分析化学(仪器分析部分)(第三版)部分答案主编:曾泳淮高等教育出版社专业知识整理分享WORD 格式 可编辑专业知识整理分享目录第2章光学分析法导论 ................................................................................................................... 3 第3章原子发射光谱法 ................................................................................................................... 7 第4章原子吸收光谱法 ................................................................................................................. 10 第5章紫外-可见吸收光谱法 ....................................................................................................... 18 第6章红外光谱法 ......................................................................................................................... 22 第7章分子发光分析法 ................................................................................................................. 26 第8章核磁共振波谱法 ................................................................................................................. 30 第9章电分析化学法导论 ............................................................................................................. 34 第10章电位分析法 ....................................................................................................................... 37 第11章电解与库仑分析法 ........................................................................................................... 41 第12章伏安法与极谱法 ............................................................................................................... 45 第13章电分析化学的新进展 ....................................................................................................... 48 第14章色谱分析法导论 ............................................................................................................... 49 第15章气相色谱法 ....................................................................................................................... 56 第16章高效液相色谱法 ............................................................................................................... 59 第17章质谱法 ............................................................................................................................... 66 第18章其他仪器分析法 (70)C ontentWORD格式可编辑第2章光学分析法导论【2-1】解释下列名词。